回答下列问题:
(1)基态硅原子的电子排布式为____ ;基态铬原子的价电子排布图不能写成 形式,其原因是违背了
形式,其原因是违背了____ 。
(2)NaAlSi2O6中四种元素第一电离能由大到小的顺序为____ (填元素符号),灼烧硅酸铝钠时,当钠元素的价电子由____ (填“激发态”或“基态”)跃迁到另一状态时产生黄色火焰。
(3)1mol[Co(NH3)6]Cl2中含有σ键的数目为_____ NA,中心原子Co所在分区为_____ 区,价电子排布图为____ ;配体是分子_____ (填“极性”、“非极性”)。
(4)基态S原子电子占据最高能级的电子云轮廓图为____ 形,CS2的空间构型为_____ ,C2H5SH的沸点比C2H5OH低的原因____ 。
(5)Cu与O形成的一种化合物的立方晶胞如图所示:
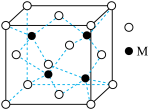
①M元素为____ ,该化合物的化学式为____ 。
②若该晶胞的边长为2nm,求该晶胞的密度____ g•cm-3。
(1)基态硅原子的电子排布式为
 形式,其原因是违背了
形式,其原因是违背了(2)NaAlSi2O6中四种元素第一电离能由大到小的顺序为
(3)1mol[Co(NH3)6]Cl2中含有σ键的数目为
(4)基态S原子电子占据最高能级的电子云轮廓图为
(5)Cu与O形成的一种化合物的立方晶胞如图所示:

①M元素为
②若该晶胞的边长为2nm,求该晶胞的密度
更新时间:2022-09-24 20:25:51
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
真题
名校
【推荐1】M、R、X、Y为原子序数依次增大的短周期主族元素,Z是一种过渡元素。M基态原子L层中p轨道电子数是s轨道电子数的2倍,R是同周期元素中最活泼的金属元素,X和M形成的一种化合物是引起酸雨的主要大气污染物,Z的基态原子4s和3d轨道半充满。请回答下列问题:
(1)R基态原子的电子排布式是_____ ,X和Y中电负性较大的是__ (填元素符号)。
(2)X的氢化物的沸点低于与其组成相似的M的氢化物,其原因是___________ 。
(3)X与M形成的XM3分子的空间构型是__________ 。
(4)M和R所形成的一种离子化合物R2M晶体的晶胞如图所示,则图中黑球代表的离子是_________ (填离子符号)。
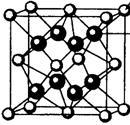
(5)在稀硫酸中,Z的最高价含氧酸的钾盐(橙色)氧化M的一种氢化物,Z被还原为+3价,该反应的化学方程式是____________ 。
(1)R基态原子的电子排布式是
(2)X的氢化物的沸点低于与其组成相似的M的氢化物,其原因是
(3)X与M形成的XM3分子的空间构型是
(4)M和R所形成的一种离子化合物R2M晶体的晶胞如图所示,则图中黑球代表的离子是

(5)在稀硫酸中,Z的最高价含氧酸的钾盐(橙色)氧化M的一种氢化物,Z被还原为+3价,该反应的化学方程式是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】前四周期A、B、C、D、E、F、G原子序数依次增大,A元素的质子数和质量数相等,B元素具有三个能级且所排电子数相同,D元素2p能级上电子数是2s能级的两倍;D和E相邻且同主族。F是第四周期未成对电子最多的原子,G是目前使用量最多的金属。
请回答下列问题:(用推出的元素符号或者化学式作答)
(1)F的价电子排布式为__________ ,B、C、D三种元素的第一电离能从大到小的顺序为_____________ 。
(2)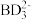 中B原子的杂化方式为
中B原子的杂化方式为__________ ,该离子的空间构型为________
(3)写出一种由A、C、D组成且既含离子键又含共价键的物质的化学式___________ ,化合物ABC中σ键和π键数目之比为___________ ,C的气态氢化物在一定的压强下,测得的密度比该压强下理论密度略大,请解释原因___________________ 。
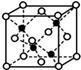
(4)E和G形成的某种晶胞如下图所示:其中白球表示E,黑球表示G。则该物质的化学式为___________________ ,假设该晶胞的密度为ρ g/cm3,用NA表示阿伏加德罗常数,则该晶胞中距离最近的G原子之间的距离为___________ cm 。
请回答下列问题:(用推出的元素符号或者化学式作答)
(1)F的价电子排布式为
(2)
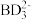 中B原子的杂化方式为
中B原子的杂化方式为(3)写出一种由A、C、D组成且既含离子键又含共价键的物质的化学式

(4)E和G形成的某种晶胞如下图所示:其中白球表示E,黑球表示G。则该物质的化学式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】已知:A、B、C、D、E、F六种元素核电荷数依次增大,属元素周期表中前四周期的元素。其中A原子核外有三个未成对电子;B和E可形成离子化合物B2E,E原子核外的M层中只有两对成对电子;C元素是地壳中含量最高的金属元素;D单质的熔点在同周期元素形成的单质中是最高的;F原子核外最外层电子数与B相同,其余各层均充满。请根据以上信息,回答下列问题:
(1)A、B、C、D的第一电离能由小到大的顺序为____ (用元素符号表示)。
(2)E与D的同族短周期元素可形成一种化合物X,X是常见的有机溶剂,X分子的空间构型是___ 。
(3)F原子的价层电子排布式是____ ,请写出一种与A的氧化物A2O互为等电子体的分子或离子_______ 。
(1)A、B、C、D的第一电离能由小到大的顺序为
(2)E与D的同族短周期元素可形成一种化合物X,X是常见的有机溶剂,X分子的空间构型是
(3)F原子的价层电子排布式是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】(1)以下列出的是一些原子的2p能级和3d能级中电子排布的情况,试判断哪些违反了泡利原理___________ ,哪些违反了洪特规则___________ 。
(2)在H-S、H-Cl两种共价键中,键的极性较强的是___________ (填“H-Cl”或“H-S”), 与
与 的结构相似,和过渡金属更容易形成配合物的是
的结构相似,和过渡金属更容易形成配合物的是___________ (填“ ”或“
”或“ ”)。
”)。
①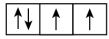 ②
②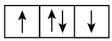 ③
③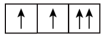 ④
④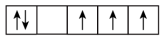 ⑤
⑤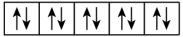 ⑥
⑥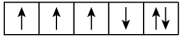
(2)在H-S、H-Cl两种共价键中,键的极性较强的是
 与
与 的结构相似,和过渡金属更容易形成配合物的是
的结构相似,和过渡金属更容易形成配合物的是 ”或“
”或“ ”)。
”)。①
 ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】铁及其化合物具有广泛的应用。回答下列问题:
(1)铁元素在元素周期表中的位置为___________ ,其形成的离子常见的有Fe2+和Fe3+,基态Fe2+的价电子的排布式为___________ ,相同条件下,Fe3+比Fe2+稳定,原因是___________ 。
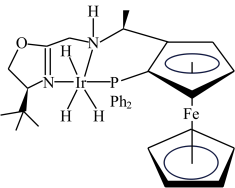
(2)一种二茂铁为骨架的新型手性膦氮配合物结构示意图如下,其中Ph为苯基,Ir为铱元素。该结构中电负性最大的元素为___________ (填元素符号,下同),分子中第二周期元素的第一电离能由大到小的顺序为___________ 。P原子的杂化方式为___________ ,分子中不含有的化学键类型是___________ (填标号)。
A.离子键 B.配位键 C.极性共价键 D.非极性共价键 E. 键 F.
键 F. 键
键
(3)铁酸钇是一种典型的单相多铁性材料其正交相晶胞结构如图所示。
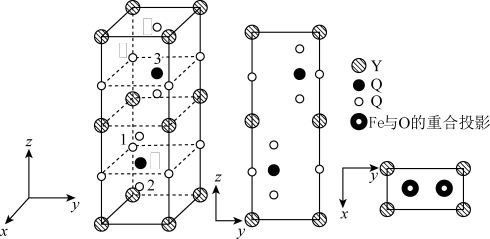
其中铁酸钇的化学式为___________ ,已知1号O原子空间坐标为(0,0, ),2号O原子空间坐标为(
),2号O原子空间坐标为( ,
, -m,
-m, -n),则3号Fe原子的空间坐标为
-n),则3号Fe原子的空间坐标为___________ ,若晶胞参数分别为a pm、b pm和c pm,阿伏加德罗常数的值用 表示,则该晶体的密度为
表示,则该晶体的密度为___________  (列出表达式)
(列出表达式)
(1)铁元素在元素周期表中的位置为
(2)一种二茂铁为骨架的新型手性膦氮配合物结构示意图如下,其中Ph为苯基,Ir为铱元素。该结构中电负性最大的元素为

A.离子键 B.配位键 C.极性共价键 D.非极性共价键 E.
 键 F.
键 F. 键
键(3)铁酸钇是一种典型的单相多铁性材料其正交相晶胞结构如图所示。

其中铁酸钇的化学式为
 ),2号O原子空间坐标为(
),2号O原子空间坐标为( ,
, -m,
-m, -n),则3号Fe原子的空间坐标为
-n),则3号Fe原子的空间坐标为 表示,则该晶体的密度为
表示,则该晶体的密度为 (列出表达式)
(列出表达式)
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】根据已学知识,请回答下列问题:
(1)基态N原子中,核外电子占据的最高能层的符号是_______ ,占据该能层电子的原子轨道形状为_______ 。
(2)写出3p轨道上有2个未成对电子的元素的符号:_______ 。
(3)某元素被科学家称之为人体微量元素中的“防癌之王”,其原子的价层电子排布式为4s24p4,该元素的名称是_______ 。
(4)已知铁是26号元素,写出基态Fe的价层电子排布式:_______ ;在元素周期表中,该元素在_______ (填“s”“p”“d”“f”或“ds”)区。
(5)NaAlO2在水溶液中实际上都是以Na[Al(OH)4]形式存在。其中[Al(OH)4]-为配离子,写出A1原子的杂化方式_______ ,该阴离子中存在的化学键有_______ (填字母代号)
A.离子键 B.极性键 C.非极性键
D.金属键 E.配位键 F.氢键
(1)基态N原子中,核外电子占据的最高能层的符号是
(2)写出3p轨道上有2个未成对电子的元素的符号:
(3)某元素被科学家称之为人体微量元素中的“防癌之王”,其原子的价层电子排布式为4s24p4,该元素的名称是
(4)已知铁是26号元素,写出基态Fe的价层电子排布式:
(5)NaAlO2在水溶液中实际上都是以Na[Al(OH)4]形式存在。其中[Al(OH)4]-为配离子,写出A1原子的杂化方式
A.离子键 B.极性键 C.非极性键
D.金属键 E.配位键 F.氢键
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】X、Y、Z、W、R、Q为前30号元素,且原子序数依次增大。X是元素周期表中原子半径最小的元素;Y元素基态原子有三个能级上有电子,且每个能级上的电子数相等;Z元素基态原子的单电子数在同周期元素基态原子中最多;W与Z同周期,第一电离能比Z的低;R与Y同主族;Q的最外层只有一个电子,其他电子层均有 个电子(n表示电子层序数)。请回答下列问题:
个电子(n表示电子层序数)。请回答下列问题:
(1)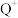 的核外电子排布式为
的核外电子排布式为______ 。
(2)化合物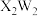 中W的杂化方式为
中W的杂化方式为______ ;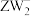 的空间结构为
的空间结构为______ 。
(3)Y、R的最高价氧化物中沸点较高的是______ (填化学式),原因是__________________ 。
(4)Y有多种同素异形体,其中一种同素异形体的晶胞结构如图所示,该晶体的晶胞中所含Y原子的个数为______ ;若晶胞的边长为 ,晶体的密度为
,晶体的密度为 ,则阿伏加德罗常数的值
,则阿伏加德罗常数的值 为
为______ (用含a和ρ的代数式表示)。
 个电子(n表示电子层序数)。请回答下列问题:
个电子(n表示电子层序数)。请回答下列问题:(1)
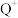 的核外电子排布式为
的核外电子排布式为(2)化合物
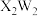 中W的杂化方式为
中W的杂化方式为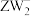 的空间结构为
的空间结构为(3)Y、R的最高价氧化物中沸点较高的是
(4)Y有多种同素异形体,其中一种同素异形体的晶胞结构如图所示,该晶体的晶胞中所含Y原子的个数为
 ,晶体的密度为
,晶体的密度为 ,则阿伏加德罗常数的值
,则阿伏加德罗常数的值 为
为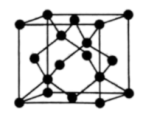
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】氧化镓是一种新型超宽窄带半导体材料,由于自身的优异性能,在紫外探测、高频功率器件等领域吸引了越来越多的关注和研究,中国科技部将其列入“十四五研发计划”,让第四代半导体获得更广泛的关注。回答下列问题:
(1)基态 原子最外层电子排布式为
原子最外层电子排布式为_______ 。
(2)①氧化镓的熔点为1740℃,氧化钙的熔点为2613℃,但有的离子晶体如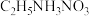 (硝酸乙基铵)的熔点只有12℃。
(硝酸乙基铵)的熔点只有12℃。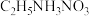 中N原子的杂化轨道类型是
中N原子的杂化轨道类型是_______ , 离子的空间结构为
离子的空间结构为_______ ,该物质中所含化学键类型:_______ (填字母)。
A.金属键 B.离子键 C.共价键 D.范德华力 E.σ键
②第一电离能:Al_______ Mg(填“>”或“<”),其原因是_______ 。
(3)锑化物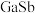 是一种超窄禁带半导体材料,可用于红外探测其晶胞结构如图所示。若该晶体的密度为
是一种超窄禁带半导体材料,可用于红外探测其晶胞结构如图所示。若该晶体的密度为 ,设Ga和Sb的原子半径分别为
,设Ga和Sb的原子半径分别为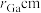 和
和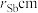 ,则原子的空间占有率为
,则原子的空间占有率为_______  (列出计算表达式,
(列出计算表达式,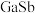 的摩尔质量为
的摩尔质量为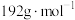 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 )。
)。

(1)基态
 原子最外层电子排布式为
原子最外层电子排布式为(2)①氧化镓的熔点为1740℃,氧化钙的熔点为2613℃,但有的离子晶体如
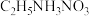 (硝酸乙基铵)的熔点只有12℃。
(硝酸乙基铵)的熔点只有12℃。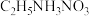 中N原子的杂化轨道类型是
中N原子的杂化轨道类型是 离子的空间结构为
离子的空间结构为A.金属键 B.离子键 C.共价键 D.范德华力 E.σ键
②第一电离能:Al
(3)锑化物
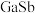 是一种超窄禁带半导体材料,可用于红外探测其晶胞结构如图所示。若该晶体的密度为
是一种超窄禁带半导体材料,可用于红外探测其晶胞结构如图所示。若该晶体的密度为 ,设Ga和Sb的原子半径分别为
,设Ga和Sb的原子半径分别为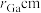 和
和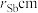 ,则原子的空间占有率为
,则原子的空间占有率为 (列出计算表达式,
(列出计算表达式,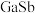 的摩尔质量为
的摩尔质量为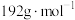 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 )。
)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】前四周期元素及其化合物在生产、生活中应用广泛。回答下列问题:
(1)下列状态的N原子或离子在跃迁时;用光谱仪可捕捉到发射光谱的是______ 。
a. b.
b.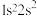 c.
c. d.
d.
(2)基态铜原子的价电子排布式为________ 。
(3) 的几何构型为
的几何构型为_______ 。
(4)已知下图均与第三周期的主族元素有关。
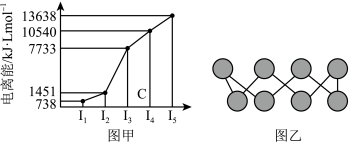
①图甲表示第一至第五电离能数据,则该元素的原子有___ 种不同运动状态的电子。
②图乙中为某单质的一种同素异形体,分子中的各原子最外层均达到8电子稳定结构,则该元素的原子的杂化轨道类型为_____ ,其易溶于 的原因是
的原因是_______ 。
(5)氨气极易溶于水,溶于水的氨分子大部分与水分子形成氢键,生成一水合氨,关于一水合氨的结构有如下两种可能,正确的是b,理由是_________ 。

(1)下列状态的N原子或离子在跃迁时;用光谱仪可捕捉到发射光谱的是
a.
 b.
b.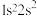 c.
c. d.
d.
(2)基态铜原子的价电子排布式为
(3)
 的几何构型为
的几何构型为(4)已知下图均与第三周期的主族元素有关。

①图甲表示第一至第五电离能数据,则该元素的原子有
②图乙中为某单质的一种同素异形体,分子中的各原子最外层均达到8电子稳定结构,则该元素的原子的杂化轨道类型为
 的原因是
的原因是(5)氨气极易溶于水,溶于水的氨分子大部分与水分子形成氢键,生成一水合氨,关于一水合氨的结构有如下两种可能,正确的是b,理由是

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】北京时间2017年10月4日,地球发生一次小行星撞击事件,撞击地点为我国云南香格里拉县城西北40公里处,爆炸当量相当于540t TNT。很可能有未燃尽的陨石落到地面。全世界已收集到4万多块陨石样品,它们大致可分为三大类:石陨石(主要成分是硅酸盐)、铁陨石(铁镍合金)、和石铁陨石(铁和硅酸盐混合物)。

回答下列问题:
(1)基态铁原子简化的电子排布式为[Ar]_______ 。
(2)TNT的结构简式如图所示。

①TNT分子中碳原子杂化类型是____ 。
②TNT的熔点比硝基苯的熔点__ (填“高”或“低”),理由是___ 。
(3)石陨石中硅酸盐之一是Ca2SiO4。
SiO44-的立体构型是_____ 。电负性:Si___ (填“>”“<”或“=”)O。
(4)K3[Fe(CN)6](铁氰化钾)溶液可以检验铁陨石中铁元素价态。
①铁氰化钾中不存在的作用力有__ (填字母)。
a.离子键 b.极性键 c.非极性键 d.π键 e.配位键 f.氢键
②1mol [Fe(CN)6]3含σ键数目为_____ 。
③CN-能与多种离子形成配合物,碳原子提供孤电子对,而不是氮原子,其原因是___ 。
(5)铁、氮组成磁材料M,其晶胞如图所示。该晶体中氮、铁原子个数之比为____ 。

(6)镍晶体的堆积方式为面心立方最密堆积。已知镍晶体密度为ρ g·cm-3,NA代表阿伏加 德罗常数的值。用含ρ和NA的代数式表示在镍晶胞中最近的两个镍原子之间的核间距D=__ nm。

回答下列问题:
(1)基态铁原子简化的电子排布式为[Ar]
(2)TNT的结构简式如图所示。

①TNT分子中碳原子杂化类型是
②TNT的熔点比硝基苯的熔点
(3)石陨石中硅酸盐之一是Ca2SiO4。
SiO44-的立体构型是
(4)K3[Fe(CN)6](铁氰化钾)溶液可以检验铁陨石中铁元素价态。
①铁氰化钾中不存在的作用力有
a.离子键 b.极性键 c.非极性键 d.π键 e.配位键 f.氢键
②1mol [Fe(CN)6]3含σ键数目为
③CN-能与多种离子形成配合物,碳原子提供孤电子对,而不是氮原子,其原因是
(5)铁、氮组成磁材料M,其晶胞如图所示。该晶体中氮、铁原子个数之比为

(6)镍晶体的堆积方式为面心立方最密堆积。已知镍晶体密度为ρ g·cm-3,NA代表阿伏加 德罗常数的值。用含ρ和NA的代数式表示在镍晶胞中最近的两个镍原子之间的核间距D=
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】微量元素指的是在人体中含量低于人体质量0.005%~0.01%的元素,包括Fe、I、Zn、Se、F、Cu、Co、Si等。
(1)F元素的基态原子核外有___ 个未成对电子,基态Fe原子的价电子排布式为____ 。
(2) 为四面体结构,其中Si原子采取的杂化类型为
为四面体结构,其中Si原子采取的杂化类型为_______ 。与 不同,
不同, 的立体构型为
的立体构型为_______ 。
(3)第一电离能Cu小于Zn,理由是_______ 。
(4)Co3+的一种配离子[Co(N3)(NH3)5]2+中,Co3+的配位数是_______ 。CoO的熔点是1935℃,CoS的熔点是1135℃,试分析CoO熔点较高的原因:_______ 。
(5)ZnO晶体存在多种结构,其中某种常见的晶胞结构(如图)。其晶胞边长为anm,阿伏加德罗常数的值为NA,则晶胞密度为_______ (列出计算式)g·cm-3

(1)F元素的基态原子核外有
(2)
 为四面体结构,其中Si原子采取的杂化类型为
为四面体结构,其中Si原子采取的杂化类型为 不同,
不同, 的立体构型为
的立体构型为(3)第一电离能Cu小于Zn,理由是
(4)Co3+的一种配离子[Co(N3)(NH3)5]2+中,Co3+的配位数是
(5)ZnO晶体存在多种结构,其中某种常见的晶胞结构(如图)。其晶胞边长为anm,阿伏加德罗常数的值为NA,则晶胞密度为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】VA族元素及其化合物在生产、生活中用途广泛。
(1)P4S3常用于制造火柴,P和S的第一电离能较大的是____ (填元素符号)。
(2)As4S4俗称雄黄,其中基态As原子的价电子排布式为____ ,有____ 个未成对电子。
(3)研究发现固态PCl5和PBr5均为离子晶体,但其结构不同,分别为[PCl4]+[PCl6]-和[PBr4]+Br-,分析PCl5和PBr5结构存在差异的主要原因是____ 。
(4)汽车尾气催化剂可将NO2还原为无毒害的气体,防止HNO3型酸雨的形成,NO2的空间构型为____ ,从结构的角度说明HNO3的酸性强于HNO2的原因:____ 。
(5)CrCl3能与H2O、NH3形成配位数为6的配合物,且相应两种配体的物质的量之比为2∶1,lmol该配合物溶于水,加入足量的硝酸银溶液,可得430.5g白色沉淀,则该配合物的化学式为____ 。(Cr的相对原子质量为52)
(6)贵金属磷化物Rh2P(化学式式量为237)可用作电解水的高效催化剂,其立方晶胞如图所示。已知晶胞边长为apm,晶体中与P距离最近的Rh的数目为____ ,晶体的密度为____ g·cm-3(列出计算式)。

(1)P4S3常用于制造火柴,P和S的第一电离能较大的是
(2)As4S4俗称雄黄,其中基态As原子的价电子排布式为
(3)研究发现固态PCl5和PBr5均为离子晶体,但其结构不同,分别为[PCl4]+[PCl6]-和[PBr4]+Br-,分析PCl5和PBr5结构存在差异的主要原因是
(4)汽车尾气催化剂可将NO2还原为无毒害的气体,防止HNO3型酸雨的形成,NO2的空间构型为
(5)CrCl3能与H2O、NH3形成配位数为6的配合物,且相应两种配体的物质的量之比为2∶1,lmol该配合物溶于水,加入足量的硝酸银溶液,可得430.5g白色沉淀,则该配合物的化学式为
(6)贵金属磷化物Rh2P(化学式式量为237)可用作电解水的高效催化剂,其立方晶胞如图所示。已知晶胞边长为apm,晶体中与P距离最近的Rh的数目为

您最近一年使用:0次



