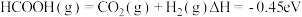下列关于反应方向、速率和平衡的说法正确的是
| A.凡是放热反应均是自发进行的反应,吸热反应都是非自发的 |
| B.化学平衡状态指的是反应物和生成物浓度相等时的状态 |
| C.一般使用催化剂可以降低反应的活化能,增大活化分子百分数,从而提高反应物的转化率 |
| D.反应NH3(g)+HCl(g)=NH4Cl(s)在常温下能自发进行,说明该反应的ΔH<0 |
更新时间:2022-11-13 12:21:15
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】中国科学院研究员团队开发了一种基于钯修饰二氧化钛的串联光热催化氮气氧化制备硝酸的新反应体系,实现了高选择性制备单一氧化产物硝酸(过程如图所示)。下列有关说法错误的是
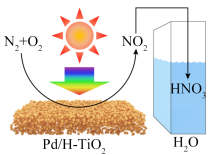

| A.该过程实现了太阳能向化学能转化 |
| B.反应N2(g)+2O2(g)=2NO2(g)的ΔH<0 |
| C.Pd/H-TiO2起到提高反应速率的作用 |
| D.生成HNO3的反应中NO2表现出还原性 |
您最近一年使用:0次
【推荐2】科学研究人员结合实验与计算机模拟结果,研究了在Pt/SiO2催化剂表面上CO2与H2的反应历程,前三步历程如图所示,其中吸附在Pt/SiO2催化剂表面上的物种用“·“标注,Ts表示过渡态。

下列有关叙述正确的是

下列有关叙述正确的是
| A.前三步总反应的反应热大于零,总反应的化学反应速率由第三步反应决定 |
| B.·HOCO转化为·CO和·OH为吸热过程 |
| C.催化剂通过参与化学反应,降低反应的活化能,减小反应的ΔH,提高反应物的转化率 |
| D.历程中活化能(能垒)最小的反应方程式为·CO+·OH+·H+3H2(g)=·CO+3H2(g)+H2O(g) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】对于可逆反应4NH3+5O2 4NO+6H2O(g),下列叙述不正确的是
4NO+6H2O(g),下列叙述不正确的是
 4NO+6H2O(g),下列叙述不正确的是
4NO+6H2O(g),下列叙述不正确的是 | A.达到平衡时,4v(O2)正=5v(NO)逆 |
| B.达到平衡状态后,NH3、O2、NO 、H2O(g)的物质的量保持不变 |
| C.达到平衡状态时,若增加容器体积,则反应速率增大 |
| D.若单位时间生成xmolNO的同时,生成xmolNH3,则反应达到平衡状态 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】已知可逆反应:AsO +2I-+2H+
+2I-+2H+ AsO
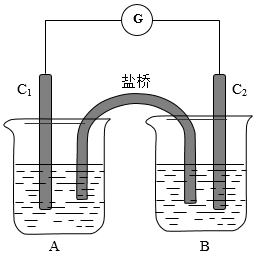
AsO +I2+H2O。据此设计出如图所示的实验装置,其中C1、C2均为铂电极,A烧杯中为KI溶液,B烧杯中为Na3AsO4溶液。以下关于该装置的说法错误的是
+I2+H2O。据此设计出如图所示的实验装置,其中C1、C2均为铂电极,A烧杯中为KI溶液,B烧杯中为Na3AsO4溶液。以下关于该装置的说法错误的是
 +2I-+2H+
+2I-+2H+ AsO
AsO +I2+H2O。据此设计出如图所示的实验装置,其中C1、C2均为铂电极,A烧杯中为KI溶液,B烧杯中为Na3AsO4溶液。以下关于该装置的说法错误的是
+I2+H2O。据此设计出如图所示的实验装置,其中C1、C2均为铂电极,A烧杯中为KI溶液,B烧杯中为Na3AsO4溶液。以下关于该装置的说法错误的是
| A.盐桥中的阳离子向B烧杯移动 |
| B.电流的方向由C2极到C1极 |
| C.电流表读数为0时,再向B烧杯中滴加浓NaOH溶液,C2作正极 |
| D.电流表读数为0时,表明该可逆反应达到了平衡状态 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】已知:SO2(g)+NO2(g) SO3(g)+NO(g) △H1=-41.8 kJ·mol-1。标准状况下,SO2(g)+NO2(g)
SO3(g)+NO(g) △H1=-41.8 kJ·mol-1。标准状况下,SO2(g)+NO2(g) SO3(s)+NO(g) △H2.下列有关说法
SO3(s)+NO(g) △H2.下列有关说法不正确 的是
 SO3(g)+NO(g) △H1=-41.8 kJ·mol-1。标准状况下,SO2(g)+NO2(g)
SO3(g)+NO(g) △H1=-41.8 kJ·mol-1。标准状况下,SO2(g)+NO2(g) SO3(s)+NO(g) △H2.下列有关说法
SO3(s)+NO(g) △H2.下列有关说法| A.该反应的△S>0 |
| B.△H2<-41.8 kJ·mol-1 |
| C.SO2的生成速率和NO2的消耗速率相等说明该反应到达平衡状态 |
| D.标准状况下,该反应中每生成22.4 L NO转移电子的数目约等于2×6.02×1023 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】恒容密闭容器中进行反应FeO(s)+CO(g) Fe(s)+CO2(g)
Fe(s)+CO2(g)  H<0。下列说法正确的是
H<0。下列说法正确的是
 Fe(s)+CO2(g)
Fe(s)+CO2(g)  H<0。下列说法正确的是
H<0。下列说法正确的是| A.当混合气体的密度不再变化时,反应达到平衡状态 |
| B.增大CO浓度,因为增大了活化分子百分数,导致反应速率增大 |
| C.该反应在高温下为自发反应 |
| D.平衡时,向容器中加入FeO可促使平衡正向移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】采用一定的脱硫技术可以把硫元素以 的形式固定,从而降低
的形式固定,从而降低 的排放,但是煤炭燃烧过程中产生的CO又会与
的排放,但是煤炭燃烧过程中产生的CO又会与 发生反应,降低了脱硫效率,涉及的反应之一是
发生反应,降低了脱硫效率,涉及的反应之一是
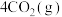
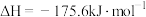 。上述反应在密闭容器中进行并达到平衡,下列说法正确的是
。上述反应在密闭容器中进行并达到平衡,下列说法正确的是
 的形式固定,从而降低
的形式固定,从而降低 的排放,但是煤炭燃烧过程中产生的CO又会与
的排放,但是煤炭燃烧过程中产生的CO又会与 发生反应,降低了脱硫效率,涉及的反应之一是
发生反应,降低了脱硫效率,涉及的反应之一是
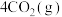
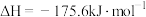 。上述反应在密闭容器中进行并达到平衡,下列说法正确的是
。上述反应在密闭容器中进行并达到平衡,下列说法正确的是| A.该反应在常温下能自发进行,且反应速率较快 |
| B.降低温度,混合气体的密度增大 |
| C.压缩容器,该反应放出的热量减小 |
| D.分离出部分CaS(s),CO的转化率变大 |
您最近一年使用:0次

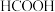 可以制得
可以制得 。在催化剂作用下,
。在催化剂作用下,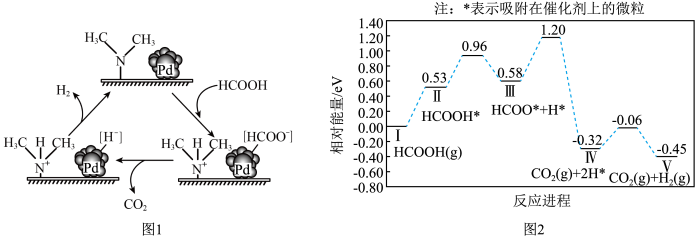
 催化释放氢反应除生成
催化释放氢反应除生成 外,还生成
外,还生成
 键比解离
键比解离 键难
键难