某温度时,在一个容积为2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图1所示。根据图中数据,试填写下列空白:

(1)该反应的化学方程式为_______ 。
(2)若X、Y、Z均为气体,反应恰好达到平衡时,用Z表示的平均反应速率为_______ ;
(3)在一密闭容器中发生反应 ,达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图2所示。
,达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图2所示。
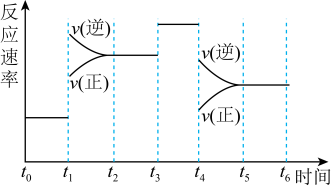
判断t1、t3、t4时刻分别改变的一个条件是:t1时刻_______ ;t3时刻_______ ;t4时刻_______
(填字母代号)
A.增大压强 B.减小压强 C.升高温度 D.降低温度 E.加催化剂 F.恒温恒容时充入氮气

(1)该反应的化学方程式为
(2)若X、Y、Z均为气体,反应恰好达到平衡时,用Z表示的平均反应速率为
(3)在一密闭容器中发生反应
 ,达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图2所示。
,达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图2所示。
判断t1、t3、t4时刻分别改变的一个条件是:t1时刻
(填字母代号)
A.增大压强 B.减小压强 C.升高温度 D.降低温度 E.加催化剂 F.恒温恒容时充入氮气
更新时间:2022-12-03 14:41:24
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】新工艺采用金属氧化物 催化尿素与甲醇合成碳酸二甲酯
催化尿素与甲醇合成碳酸二甲酯 ,副产物氨气回收重新生成尿素,有关的方程式如下:
,副产物氨气回收重新生成尿素,有关的方程式如下:
反应①: +2CH3OH(g)
+2CH3OH(g)
 +2NH3(g)
+2NH3(g)
反应②:2NH3(g)+CO2(g)
 +H2O(l)
+H2O(l)
完成下列填空:
(1)C原子核外能量最高的电子有______ 个,比较 、N、O简单离子的半径大小
、N、O简单离子的半径大小__________ 。
(2)下列事实能说明氮的非金属性比碳强的是______ (选填编号)。
a.酸性: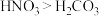 b.最高正价:氮>碳
b.最高正价:氮>碳
c.沸点: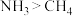 d.吸引电子能力强弱:氮>碳
d.吸引电子能力强弱:氮>碳
(3)达到平衡时,反应①碳酸二甲酯的产率 随温度T的变化关系如图所示,则反应是
随温度T的变化关系如图所示,则反应是__________ 反应(选填“放热”或“吸热”),
______  (选填“>”或“<”)。
(选填“>”或“<”)。

(4)某一恒温恒容 装置内,
装置内, 与
与 发生反应②,
发生反应②,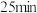 后,气体的密度减少
后,气体的密度减少 ,则
,则 内氨气的平均反应速率为
内氨气的平均反应速率为__________ 。
(5)传统合成DMC的方法是以光气( ,有剧毒)和甲醇为原料,请写出相应的化学方程式
,有剧毒)和甲醇为原料,请写出相应的化学方程式__________ 。
(6)新工艺合成DMC的方法和传统方法相比,优点有__________ (任写两点)。
 催化尿素与甲醇合成碳酸二甲酯
催化尿素与甲醇合成碳酸二甲酯 ,副产物氨气回收重新生成尿素,有关的方程式如下:
,副产物氨气回收重新生成尿素,有关的方程式如下:反应①:
 +2CH3OH(g)
+2CH3OH(g)
 +2NH3(g)
+2NH3(g)反应②:2NH3(g)+CO2(g)

 +H2O(l)
+H2O(l)完成下列填空:
(1)C原子核外能量最高的电子有
 、N、O简单离子的半径大小
、N、O简单离子的半径大小(2)下列事实能说明氮的非金属性比碳强的是
a.酸性:
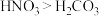 b.最高正价:氮>碳
b.最高正价:氮>碳c.沸点:
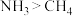 d.吸引电子能力强弱:氮>碳
d.吸引电子能力强弱:氮>碳(3)达到平衡时,反应①碳酸二甲酯的产率
 随温度T的变化关系如图所示,则反应是
随温度T的变化关系如图所示,则反应是
 (选填“>”或“<”)。
(选填“>”或“<”)。
(4)某一恒温恒容
 装置内,
装置内, 与
与 发生反应②,
发生反应②,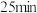 后,气体的密度减少
后,气体的密度减少 ,则
,则 内氨气的平均反应速率为
内氨气的平均反应速率为(5)传统合成DMC的方法是以光气(
 ,有剧毒)和甲醇为原料,请写出相应的化学方程式
,有剧毒)和甲醇为原料,请写出相应的化学方程式(6)新工艺合成DMC的方法和传统方法相比,优点有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Ⅰ.一定温度下,在2L的密闭容器中,X、Y、Z三种气体的量随时间变化的曲线如图:

(1)从反应开始到10s时,用Z表示的反应速率为_____ ,Y的转化率为 _______ 。
(2)该反应的化学方程式为_____________ 。
Ⅱ.KI溶液在酸性条件下能与氧气反应。现有以下实验记录:回答下列问题:
(3)该反应的离子方程式为 _____ 。
(4)该实验的目的是探究_____ 。
(5)实验试剂除了1mol•L﹣1KI溶液、0.1mol•L﹣1H2SO4溶液外,还需要的试剂是_____ ;
(6)上述实验操作中除了需要(3)的条件外,还必须控制不变的是 (填字母)。

(1)从反应开始到10s时,用Z表示的反应速率为
(2)该反应的化学方程式为
Ⅱ.KI溶液在酸性条件下能与氧气反应。现有以下实验记录:回答下列问题:
| 实验编号 | ① | ② | ③ | ④ | ⑤ |
| 温度/℃ | 30 | 40 | 50 | 60 | 70 |
| 显色时间/s | 160 | 80 | 40 | 20 | 10 |
(4)该实验的目的是探究
(5)实验试剂除了1mol•L﹣1KI溶液、0.1mol•L﹣1H2SO4溶液外,还需要的试剂是
(6)上述实验操作中除了需要(3)的条件外,还必须控制不变的是 (填字母)。
| A.温度 | B.试剂的浓度 | C.试剂的用量(体积) | D.试剂添加的顺序 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】CO2的资源化利用能有效减少CO2排放,充分利用碳资源。
(1) CO2经催化加氢可合成低碳烯烃: 2CO2(g)+6H2(g)⇌CH4(g)+4H2O(g),正反应放热。在1L恒容密闭容器内,按n(CO2): n(H2)=1:3投料,测得各组分物质的量随时间变化如下图所示:

①该反应的△H____ (填 “>”,“=”或“<" )0。
②曲线b表示的物质为____ (填化学式),该物质在0~4min内的平均反应速率为______ 。(保留2位小数)
(2)一定条件下Pd-Mg/SiO2催化剂可使CO2“甲烷化”从而变废为宝,其反应机理如下图所示

①该反应的化学方程式为_________ ;
②理论上每有1mol CO2参加反应,反应过程中转移的电子数为_______ mol.
(1) CO2经催化加氢可合成低碳烯烃: 2CO2(g)+6H2(g)⇌CH4(g)+4H2O(g),正反应放热。在1L恒容密闭容器内,按n(CO2): n(H2)=1:3投料,测得各组分物质的量随时间变化如下图所示:

①该反应的△H
②曲线b表示的物质为
(2)一定条件下Pd-Mg/SiO2催化剂可使CO2“甲烷化”从而变废为宝,其反应机理如下图所示

①该反应的化学方程式为
②理论上每有1mol CO2参加反应,反应过程中转移的电子数为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】在下列事实中,什么因素影响了化学反应的速率?
(1)黄铁矿煅烧时要粉碎成细小的矿粒__________ ;
(2)熔化的KClO3放出气泡很慢,撒入少量MnO2则很快产生气体________ ;
(3)同浓度、同体积的盐酸中放入同样大小的锌粒和镁块,产生气体有快有慢____________ ;
(4)同样大小的石灰石分别在0.1 mol·L-1的盐酸和1 mol·L-1的盐酸中反应速率不同__________ ;
(5)夏天的食品易霉变,冬天就不易发生该现象______________________ ;
(6)葡萄糖在空气中燃烧时需要较高的温度,可是在人体正常体温(37 ℃)时就可以被氧化_______________________ 。
(1)黄铁矿煅烧时要粉碎成细小的矿粒
(2)熔化的KClO3放出气泡很慢,撒入少量MnO2则很快产生气体
(3)同浓度、同体积的盐酸中放入同样大小的锌粒和镁块,产生气体有快有慢
(4)同样大小的石灰石分别在0.1 mol·L-1的盐酸和1 mol·L-1的盐酸中反应速率不同
(5)夏天的食品易霉变,冬天就不易发生该现象
(6)葡萄糖在空气中燃烧时需要较高的温度,可是在人体正常体温(37 ℃)时就可以被氧化
您最近一年使用:0次
【推荐2】碘及其化合物在生产生活中有重要作用。
(1)单质碘可与氢气反应生成碘化氢。将物质的量比为 的氢气和碘蒸气放入密闭容器中进行反应:
的氢气和碘蒸气放入密闭容器中进行反应: ,反应经过
,反应经过 分钟测得碘化氢的浓度为
分钟测得碘化氢的浓度为 ,碘蒸气的浓度为
,碘蒸气的浓度为 。
。
 前
前 分钟平均反应速率
分钟平均反应速率
________ 。
 下列能说明反应已达平衡状态的是
下列能说明反应已达平衡状态的是________  填序号
填序号 。
。
a. 氢气的生成速率等于碘化氢的消耗速率
b. 单位时间内断裂的 键数目与断裂的
键数目与断裂的 键数目相等
键数目相等
c.
d.
e. 反应混合体系的颜色不再发生变化
(2)某小组同学在室温下进行“碘钟实验”:将浓度均为 的
的 、
、 、
、 、
、 溶液及淀粉混合,一定时间后溶液变为蓝色。已知:“碘钟实验”的总反应的离子方程式为
溶液及淀粉混合,一定时间后溶液变为蓝色。已知:“碘钟实验”的总反应的离子方程式为
反应分两步进行:
反应 :
:
反应 :
:
 反应
反应 的离子方程式是
的离子方程式是__________ ,对于总反应, 的作用是
的作用是__________ 。
 为探究溶液变蓝快慢的影响因素,进行实验Ⅰ、Ⅱ
为探究溶液变蓝快慢的影响因素,进行实验Ⅰ、Ⅱ 溶液浓度均为
溶液浓度均为 。
。
溶液从混合时的无色变为蓝色的时间:实验Ⅰ是 、实验Ⅱ是
、实验Ⅱ是 。
。
实验Ⅱ中, 、
、 、
、 所对应的数值分别是
所对应的数值分别是___ ;对比实验Ⅰ、Ⅱ,可得出的实验结论是_____ 。
(3)利用FeCl3溶液与KI溶液反应设计原电池,负极反应式________ 。
(1)单质碘可与氢气反应生成碘化氢。将物质的量比为
 的氢气和碘蒸气放入密闭容器中进行反应:
的氢气和碘蒸气放入密闭容器中进行反应: ,反应经过
,反应经过 分钟测得碘化氢的浓度为
分钟测得碘化氢的浓度为 ,碘蒸气的浓度为
,碘蒸气的浓度为 。
。 前
前 分钟平均反应速率
分钟平均反应速率
 下列能说明反应已达平衡状态的是
下列能说明反应已达平衡状态的是 填序号
填序号 。
。a. 氢气的生成速率等于碘化氢的消耗速率
b. 单位时间内断裂的
 键数目与断裂的
键数目与断裂的 键数目相等
键数目相等c.

d.

e. 反应混合体系的颜色不再发生变化
(2)某小组同学在室温下进行“碘钟实验”:将浓度均为
 的
的 、
、 、
、 、
、 溶液及淀粉混合,一定时间后溶液变为蓝色。已知:“碘钟实验”的总反应的离子方程式为
溶液及淀粉混合,一定时间后溶液变为蓝色。已知:“碘钟实验”的总反应的离子方程式为
反应分两步进行:
反应
 :
:
反应
 :
:
 反应
反应 的离子方程式是
的离子方程式是 的作用是
的作用是 为探究溶液变蓝快慢的影响因素,进行实验Ⅰ、Ⅱ
为探究溶液变蓝快慢的影响因素,进行实验Ⅰ、Ⅱ 溶液浓度均为
溶液浓度均为 。
。序号 | 试剂和用量 | ||||
|
|
|
|
| |
实验Ⅰ |
|
|
|
|
|
实验Ⅱ |
|
|
|
|
|
 、实验Ⅱ是
、实验Ⅱ是 。
。实验Ⅱ中,
 、
、 、
、 所对应的数值分别是
所对应的数值分别是(3)利用FeCl3溶液与KI溶液反应设计原电池,负极反应式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】乙烯(C2H4)是重要的化工原料,乙炔(C2H2)选择性加氢合成乙烯是科学家当前关注的热点。
(1)70℃时,反应 C2H2(g) +H2(g) C2H4(g) △H= -174 kJ • mol - 1在刚性容器中达到平衡。
C2H4(g) △H= -174 kJ • mol - 1在刚性容器中达到平衡。
①下列说法正确的是_________ (填标号).
A.选用合适的催化剂,可以增大平衡气体中C2H4的百分含量
B.投料时增大 的值,该反应的平衡常数K不变
的值,该反应的平衡常数K不变
C.通入一定量He,可以缩短反应达到平衡的时间
D.升高温度,正反应速率和逆反应速率都增大,K减小
②测得在某催化剂上生成乙烯的速率方程为v =0. 585 [ p( C2H2)] -0.36 • [ p( H2)]0.85,P(H2)—定时,若 p1(C2H2) >p2(C2H2),则 V1____ V2(填“>” “<”或“=”)。
(2)在催化剂作用下,110℃时按体积比V( C2H2): V( H2) =1: 4充入刚性容器中,发生反应C2H2 + H2=C2H4、C2H2 +2H2=C2H6。若乙炔完全反应时,乙烯的体积分数为20% ,则H2的转化率为_______ , C2H4的选择性为_______ ,( C2H4的选择性=
 100%)
100%)
(1)70℃时,反应 C2H2(g) +H2(g)
 C2H4(g) △H= -174 kJ • mol - 1在刚性容器中达到平衡。
C2H4(g) △H= -174 kJ • mol - 1在刚性容器中达到平衡。①下列说法正确的是
A.选用合适的催化剂,可以增大平衡气体中C2H4的百分含量
B.投料时增大
 的值,该反应的平衡常数K不变
的值,该反应的平衡常数K不变C.通入一定量He,可以缩短反应达到平衡的时间
D.升高温度,正反应速率和逆反应速率都增大,K减小
②测得在某催化剂上生成乙烯的速率方程为v =0. 585 [ p( C2H2)] -0.36 • [ p( H2)]0.85,P(H2)—定时,若 p1(C2H2) >p2(C2H2),则 V1
(2)在催化剂作用下,110℃时按体积比V( C2H2): V( H2) =1: 4充入刚性容器中,发生反应C2H2 + H2=C2H4、C2H2 +2H2=C2H6。若乙炔完全反应时,乙烯的体积分数为20% ,则H2的转化率为

 100%)
100%)
您最近一年使用:0次










