我国在南海北部神狐海域进行的可燃冰(甲烷的水合物)试采获得成功。甲烷是一种重要的化工原料。甲烷重整是提高甲烷利用率的重要方式。
回答下列问题:
(1)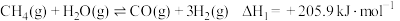 ①
①
 ②
②
写出 与
与 反应生成CO和
反应生成CO和 的热化学方程式:
的热化学方程式:_______ 。
(2)高温下,在1L密闭容器中通入1mol甲烷,发生如下反应: 。反应在初期阶段的速率方程为
。反应在初期阶段的速率方程为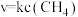 ,其中
,其中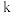 为反应速率常数。
为反应速率常数。
①设反应开始时的反应速率为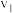 ,甲烷的转化率为
,甲烷的转化率为 时的反应速率为
时的反应速率为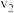 ,则
,则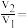
_______ 。
②对于处于初期阶段的该反应,下列说法正确的是_______ (填字母)。
A.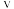 与甲烷浓度成正比
与甲烷浓度成正比
B.压强不变时,反应到达平衡状态
C.乙烷的生成速率逐渐增大
D.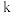 与温度无关
与温度无关
③平衡时,再通入1 mol甲烷,则反应的平衡常数K_______ (填“增大”“减小”或“不变”,下同),甲烷的转化率
_______ 。
(3) 和
和 都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如图所示:
都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如图所示:
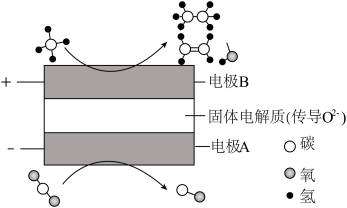
当在某电极上生成的两种有机物物质的量之比为1:1时,该电极上的电极反应式为_______ 。 和
和 的物质的量比为
的物质的量比为_______ 。
(4)我国科学家对甲烷和水蒸气催化重整反应机理也进行了广泛研究,通常认为该反应分两步进行。第一步: 催化裂解生成
催化裂解生成 和碳(或碳氢物种),其中碳(或碳氢物种)吸附在催化剂上,如
和碳(或碳氢物种),其中碳(或碳氢物种)吸附在催化剂上,如 ;第二步:碳(或碳氢物种)和
;第二步:碳(或碳氢物种)和 反应生成
反应生成 和
和 ,如
,如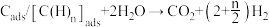 ,反应过程和能量变化残图如下:
,反应过程和能量变化残图如下:
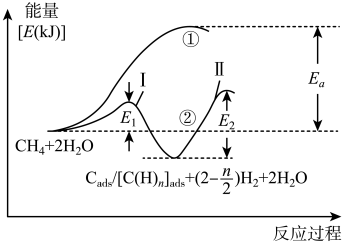
判断_______ (填序号)过程加入催化剂,原因是_______ 。控制整个过程②反应速率的是第Ⅱ步,其原因为_______ 。
回答下列问题:
(1)
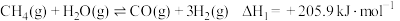 ①
① ②
②写出
 与
与 反应生成CO和
反应生成CO和 的热化学方程式:
的热化学方程式:(2)高温下,在1L密闭容器中通入1mol甲烷,发生如下反应:
 。反应在初期阶段的速率方程为
。反应在初期阶段的速率方程为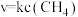 ,其中
,其中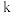 为反应速率常数。
为反应速率常数。①设反应开始时的反应速率为
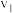 ,甲烷的转化率为
,甲烷的转化率为 时的反应速率为
时的反应速率为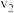 ,则
,则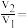
②对于处于初期阶段的该反应,下列说法正确的是
A.
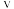 与甲烷浓度成正比
与甲烷浓度成正比B.压强不变时,反应到达平衡状态
C.乙烷的生成速率逐渐增大
D.
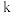 与温度无关
与温度无关③平衡时,再通入1 mol甲烷,则反应的平衡常数K

(3)
 和
和 都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如图所示:
都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如图所示:
当在某电极上生成的两种有机物物质的量之比为1:1时,该电极上的电极反应式为
 和
和 的物质的量比为
的物质的量比为(4)我国科学家对甲烷和水蒸气催化重整反应机理也进行了广泛研究,通常认为该反应分两步进行。第一步:
 催化裂解生成
催化裂解生成 和碳(或碳氢物种),其中碳(或碳氢物种)吸附在催化剂上,如
和碳(或碳氢物种),其中碳(或碳氢物种)吸附在催化剂上,如 ;第二步:碳(或碳氢物种)和
;第二步:碳(或碳氢物种)和 反应生成
反应生成 和
和 ,如
,如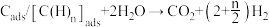 ,反应过程和能量变化残图如下:
,反应过程和能量变化残图如下:
判断
更新时间:2022-12-20 09:32:04
|
相似题推荐
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐1】砷(As)是第33号元素,可以形成As2S3、As2O5、H3AsO3、H3AsO4等化合物,有着广泛的用途。回答下列问题:
(1)砷在元素周期表中的位置是__________________________ 。
(2)工业上常将含砷废渣(主要成分为As2S3)制成浆状,通入O2氧化,生成H3AsO4和单质硫。写出发生反应的化学方程式_________________________________________ 。该反应需要在加压下进行,原因是__________________________ 。
(3)已知:2As(s)+3H2(g)+4O2(g)=2H3AsO4(s)△H1
H2(g)+ O2(g)=H2 O(l) △H2
O2(g)=H2 O(l) △H2
2As(s)+ O2(g) =As2O5(s)△H3
O2(g) =As2O5(s)△H3
则反应 As2O5(s) +3H2O(1)= 2H3AsO4(s)的△H=____________ 。
(4)298K时,将20mL3xmol·L-1Na3AsO3、20 mL 3xmol·L-1I2和20mL NaOH溶液混合,发生反应:AsO33-(aq)+I2+2OH- AsO43-+2I-+H2O。溶液中c(AsO43-) 与反应时间(t)的关系如图所示。
AsO43-+2I-+H2O。溶液中c(AsO43-) 与反应时间(t)的关系如图所示。
①下列不能判断反应达到平衡的是________ (填标号)。
a.溶液的pH不再变化 b.v(I-)=2v(AsO33-)
c.c(AsO43-)/c(AsO33-)不再变化 d.c(I-)=ymol·L-1
②tm时v逆______ tn时v逆(填“>”“<”或“=”),理由是_____________ 。
③若平衡时溶液的c(OH-)=lmol/L,则该反应的平衡常数K为____________ 。
(1)砷在元素周期表中的位置是
(2)工业上常将含砷废渣(主要成分为As2S3)制成浆状,通入O2氧化,生成H3AsO4和单质硫。写出发生反应的化学方程式
(3)已知:2As(s)+3H2(g)+4O2(g)=2H3AsO4(s)△H1
H2(g)+
 O2(g)=H2 O(l) △H2
O2(g)=H2 O(l) △H22As(s)+
 O2(g) =As2O5(s)△H3
O2(g) =As2O5(s)△H3则反应 As2O5(s) +3H2O(1)= 2H3AsO4(s)的△H=
(4)298K时,将20mL3xmol·L-1Na3AsO3、20 mL 3xmol·L-1I2和20mL NaOH溶液混合,发生反应:AsO33-(aq)+I2+2OH-
 AsO43-+2I-+H2O。溶液中c(AsO43-) 与反应时间(t)的关系如图所示。
AsO43-+2I-+H2O。溶液中c(AsO43-) 与反应时间(t)的关系如图所示。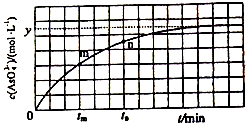
①下列不能判断反应达到平衡的是
a.溶液的pH不再变化 b.v(I-)=2v(AsO33-)
c.c(AsO43-)/c(AsO33-)不再变化 d.c(I-)=ymol·L-1
②tm时v逆
③若平衡时溶液的c(OH-)=lmol/L,则该反应的平衡常数K为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐2】NO、NO2是汽车尾气中主要的含氮氧化物。回答下列问题:
(1)已知氮氧化物转化过程中的能量变化如图(图中表示生成2 mol NO2的能量变化)。1 mol NO氧化为NO2的焓变△H=___________ 。
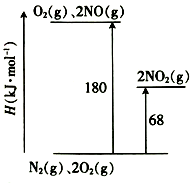
(2)某温度下,反应的平衡常数如下:
a.2NO2(g) N2(g)+2O2(g) K=6.7×1016
N2(g)+2O2(g) K=6.7×1016
b.2NO(g) N2(g)+O2(g) K=2.2×1030
N2(g)+O2(g) K=2.2×1030
分解反应趋势较大的反应是__________ (填“a”或“b”);反应2NO(g)+O2(g)  2NO2(g)的K=
2NO2(g)的K=_____________ 。
(3)已知反应2NO(g)+O2(g) 2NO2的正反应速率v正=k1Cm(NO)cn(O2),其中k为速率常数,可通过下列实验数据计算k、m、n。
2NO2的正反应速率v正=k1Cm(NO)cn(O2),其中k为速率常数,可通过下列实验数据计算k、m、n。

则k1=______________ ,m=______________ ,n=______________ ,
(4)已知该反应的历程为:
第一步:NO+NO N2O2 快速平衡
N2O2 快速平衡
第二步:N2O2+O2 2NO2慢反应
2NO2慢反应
其中可近似认为第二步反应不影响第一步的平衡,第一步反应中:v(正)=k1c2(NO),v(逆)=k-1c(N2O2)。下列叙述正确的是________ (填字母)。
A.第一步反应的平衡常数K=
B.v(第一步的正反应)<v(第二步的反应)
C.第二步的活化能比第一步的活化能高
D.第二步中N2O2与O2的碰撞100%有效
(5)一定条件下测得容器中NO、O2、NO2浓度发生如下变化。

①NO的平衡转化率为_______________ 。
②该温度下反应2NO(g)+O2(g) 2NO2(g)的平衡常数为
2NO2(g)的平衡常数为______________ (保留整数)
(1)已知氮氧化物转化过程中的能量变化如图(图中表示生成2 mol NO2的能量变化)。1 mol NO氧化为NO2的焓变△H=

(2)某温度下,反应的平衡常数如下:
a.2NO2(g)
 N2(g)+2O2(g) K=6.7×1016
N2(g)+2O2(g) K=6.7×1016b.2NO(g)
 N2(g)+O2(g) K=2.2×1030
N2(g)+O2(g) K=2.2×1030分解反应趋势较大的反应是
 2NO2(g)的K=
2NO2(g)的K=(3)已知反应2NO(g)+O2(g)
 2NO2的正反应速率v正=k1Cm(NO)cn(O2),其中k为速率常数,可通过下列实验数据计算k、m、n。
2NO2的正反应速率v正=k1Cm(NO)cn(O2),其中k为速率常数,可通过下列实验数据计算k、m、n。
则k1=
(4)已知该反应的历程为:
第一步:NO+NO
 N2O2 快速平衡
N2O2 快速平衡第二步:N2O2+O2
 2NO2慢反应
2NO2慢反应其中可近似认为第二步反应不影响第一步的平衡,第一步反应中:v(正)=k1c2(NO),v(逆)=k-1c(N2O2)。下列叙述正确的是
A.第一步反应的平衡常数K=

B.v(第一步的正反应)<v(第二步的反应)
C.第二步的活化能比第一步的活化能高
D.第二步中N2O2与O2的碰撞100%有效
(5)一定条件下测得容器中NO、O2、NO2浓度发生如下变化。

①NO的平衡转化率为
②该温度下反应2NO(g)+O2(g)
 2NO2(g)的平衡常数为
2NO2(g)的平衡常数为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐3】煤化工是以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业过程。
I.将水蒸气通过红热的炭即可产生水煤气。反应为:
C(s)+H2O(g) CO(g)+H2(g) ΔH=+131.3 kJ·mol-1
CO(g)+H2(g) ΔH=+131.3 kJ·mol-1
能使化学反应速率加快的措施有________ (填序号)。
①增加C的物质的量 ②升高反应温度
③随时吸收CO、H2转化为CH3OH ④密闭定容容器中充入CO(g)
II.工业上用CO生产燃料甲醇.一定条件下发生反应:CO(g)+2H2(g) CH3OH(g).
CH3OH(g).
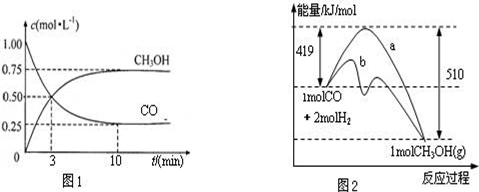
(1)图1是表示一定温度下,在体积为2L的密闭容器中加入4mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化情况.从反应开始到平衡,用CO浓度变化表示平均反应速率v(CO)=________________________ ;
(2)图2表示该反应进行过程中能量的变化.曲线a表示不使用催化剂时反应的能量变化,曲线b表示使用催化剂后的能量变化.写出该反应的热化学方程式___________ ;
(3)该反应平衡常数K为___________ ;
(4)恒容条件下,下列措施中能使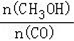 增大的有
增大的有__________ ;
a.升高温度 b.充入He气c.再充入2molH2 d.使用催化剂.
III. 下图是表示在一容积为2 L的密闭容器内加入2 mol的CO和6 mol的H2,在一定条件下发生如下反应:CO(g)+2H2(g) CH3OH(g) ΔH<0,该反应的逆反应速率与时间的关系曲线:
CH3OH(g) ΔH<0,该反应的逆反应速率与时间的关系曲线:

①由图可知反应在t1、t3、t7时都达到了平衡,而在t2、t8时都改变了条件,试判断t8时改变的条件可能是_______________ 。
②若t4时降压,t5时达到平衡,t6时增大反应物的浓度,请在图中画出t4~t6时逆反应速率与时间的关系曲线______________ 。
I.将水蒸气通过红热的炭即可产生水煤气。反应为:
C(s)+H2O(g)
 CO(g)+H2(g) ΔH=+131.3 kJ·mol-1
CO(g)+H2(g) ΔH=+131.3 kJ·mol-1能使化学反应速率加快的措施有
①增加C的物质的量 ②升高反应温度
③随时吸收CO、H2转化为CH3OH ④密闭定容容器中充入CO(g)
II.工业上用CO生产燃料甲醇.一定条件下发生反应:CO(g)+2H2(g)
 CH3OH(g).
CH3OH(g).
(1)图1是表示一定温度下,在体积为2L的密闭容器中加入4mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化情况.从反应开始到平衡,用CO浓度变化表示平均反应速率v(CO)=
(2)图2表示该反应进行过程中能量的变化.曲线a表示不使用催化剂时反应的能量变化,曲线b表示使用催化剂后的能量变化.写出该反应的热化学方程式
(3)该反应平衡常数K为
(4)恒容条件下,下列措施中能使
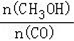 增大的有
增大的有a.升高温度 b.充入He气c.再充入2molH2 d.使用催化剂.
III. 下图是表示在一容积为2 L的密闭容器内加入2 mol的CO和6 mol的H2,在一定条件下发生如下反应:CO(g)+2H2(g)
 CH3OH(g) ΔH<0,该反应的逆反应速率与时间的关系曲线:
CH3OH(g) ΔH<0,该反应的逆反应速率与时间的关系曲线:
①由图可知反应在t1、t3、t7时都达到了平衡,而在t2、t8时都改变了条件,试判断t8时改变的条件可能是
②若t4时降压,t5时达到平衡,t6时增大反应物的浓度,请在图中画出t4~t6时逆反应速率与时间的关系曲线
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐1】习近平主席在第75届联合国大会提出,我国要在2030年前实现碳达峰,2060年前实现碳中和的目标。因此二氧化碳的固定和转化成为科学家研究的重要课题。
I.我国科学家王亮在CO2合成燃料CH4的催化剂选择方面取得了重大突破,其反应原理如下:CO2(g)+4H2(g) CH4(g)+2H2O(g) △H=-165.0kJ·mol-1,T℃时,将2molCO2(g)和8molH2(g)充入体积为2L的恒容密闭容器中发生如上反应,10min后反应达到平衡,此时容器内的压强变为起始的
CH4(g)+2H2O(g) △H=-165.0kJ·mol-1,T℃时,将2molCO2(g)和8molH2(g)充入体积为2L的恒容密闭容器中发生如上反应,10min后反应达到平衡,此时容器内的压强变为起始的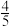 。
。
(1)T℃时,该反应的平衡常数K=____ ,0~10min内CO2的平均反应速率为____ 。
(2)下列情形能表示该反应达到平衡状态的有____ 。
A.容器内混合气体的平均摩尔质量不再改变
B.容器内气体的密度不再改变
C.H2O(g)的体积分数保持不变
D. 的值保持不变
的值保持不变
E.v正(CO2)=4逆v(H2)
II.2021年9月24日,我国科学家在《Science》上发表论文《无细胞化学酶法从二氧化碳合成淀粉》,代表着人类人工合成淀粉领域的重大颠覆性和原创性突破。CO2还原为甲醇是人工合成淀粉的第一步。CO2催化加氢主要反应有:
a.CO2(g)+3H2(g) CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
b.CO2(g)+H2(g) CO(g)+H2O(g)
CO(g)+H2O(g)
(3)已知CO2(g)、CH3OH(g)、H2O(g)的摩尔生成焓分别为-393.5kJ·mol-1、-200.6kJ·mol-1、-241.8kJ·mol-1(一定温度和压强下,由最稳定单质生成1mol化合物的焓变为该物质的摩尔生成焓,单质的摩尔生成焓为0)。则反应a的△H=____ kJ·mol-1。
(4)当压强分别为p1、p2时,将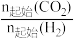 =1:3的混合气体置于密闭容器中反应,不同温度下体系中CO2的平衡转化率和CH3OH、CO的选择性如图所示。[CH3OH(或
=1:3的混合气体置于密闭容器中反应,不同温度下体系中CO2的平衡转化率和CH3OH、CO的选择性如图所示。[CH3OH(或 )的选择性=
)的选择性= ]
]
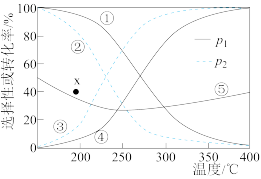
①曲线____ 代表CH3OH的选择性,原因是____ 。
②相同温度下,关于反应a和反应b的平衡常数判断,正确的是____ 。
A.K(a)>K(b) B.K(a)<K(b) C.无法判断
③保持反应温度不变,使CO2的平衡转化率达到x点,改变的条件可能是____ 。
I.我国科学家王亮在CO2合成燃料CH4的催化剂选择方面取得了重大突破,其反应原理如下:CO2(g)+4H2(g)
 CH4(g)+2H2O(g) △H=-165.0kJ·mol-1,T℃时,将2molCO2(g)和8molH2(g)充入体积为2L的恒容密闭容器中发生如上反应,10min后反应达到平衡,此时容器内的压强变为起始的
CH4(g)+2H2O(g) △H=-165.0kJ·mol-1,T℃时,将2molCO2(g)和8molH2(g)充入体积为2L的恒容密闭容器中发生如上反应,10min后反应达到平衡,此时容器内的压强变为起始的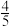 。
。(1)T℃时,该反应的平衡常数K=
(2)下列情形能表示该反应达到平衡状态的有
A.容器内混合气体的平均摩尔质量不再改变
B.容器内气体的密度不再改变
C.H2O(g)的体积分数保持不变
D.
 的值保持不变
的值保持不变E.v正(CO2)=4逆v(H2)
II.2021年9月24日,我国科学家在《Science》上发表论文《无细胞化学酶法从二氧化碳合成淀粉》,代表着人类人工合成淀粉领域的重大颠覆性和原创性突破。CO2还原为甲醇是人工合成淀粉的第一步。CO2催化加氢主要反应有:
a.CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)b.CO2(g)+H2(g)
 CO(g)+H2O(g)
CO(g)+H2O(g)(3)已知CO2(g)、CH3OH(g)、H2O(g)的摩尔生成焓分别为-393.5kJ·mol-1、-200.6kJ·mol-1、-241.8kJ·mol-1(一定温度和压强下,由最稳定单质生成1mol化合物的焓变为该物质的摩尔生成焓,单质的摩尔生成焓为0)。则反应a的△H=
(4)当压强分别为p1、p2时,将
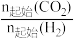 =1:3的混合气体置于密闭容器中反应,不同温度下体系中CO2的平衡转化率和CH3OH、CO的选择性如图所示。[CH3OH(或
=1:3的混合气体置于密闭容器中反应,不同温度下体系中CO2的平衡转化率和CH3OH、CO的选择性如图所示。[CH3OH(或 )的选择性=
)的选择性= ]
]
①曲线
②相同温度下,关于反应a和反应b的平衡常数判断,正确的是
A.K(a)>K(b) B.K(a)<K(b) C.无法判断
③保持反应温度不变,使CO2的平衡转化率达到x点,改变的条件可能是
您最近一年使用:0次
【推荐2】铬是电镀、制革和颜料等工业废水中的主要重金属污染物。在水溶液中, (Ⅲ)以
(Ⅲ)以 形态存在:
形态存在: (Ⅱ)主要以
(Ⅱ)主要以 和
和 形态存在,其毒性是
形态存在,其毒性是 (Ⅲ)的100倍,处理含
(Ⅲ)的100倍,处理含 (Ⅵ)废水的常用方法是先将其转化为
(Ⅵ)废水的常用方法是先将其转化为 (Ⅲ),再进一步将
(Ⅲ),再进一步将 转化为
转化为 沉淀,减少水体中总铬含量。
沉淀,减少水体中总铬含量。
(1)探究 (Ⅵ)的存在形式:
(Ⅵ)的存在形式: (Ⅵ)在水溶液中常有
(Ⅵ)在水溶液中常有 和
和 两种存在形式,该废水中两种离子的浓度与溶液
两种存在形式,该废水中两种离子的浓度与溶液 的关系如下图所示:
的关系如下图所示:
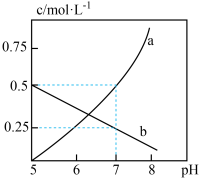
①加酸可以使 转化为
转化为 ,该反应的离子方程式为
,该反应的离子方程式为______ 。
②计算该反应的平衡常数为______ 。(已知 时,
时,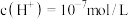 )
)
(2) (Ⅵ)转化为
(Ⅵ)转化为
在 时,向该废水中加入
时,向该废水中加入 溶液将
溶液将 (Ⅵ)还原为
(Ⅵ)还原为 ,然后再向其中加入浓氨水调节溶液
,然后再向其中加入浓氨水调节溶液 。
。
①加入 溶液后,发生反应的离子方程式为
溶液后,发生反应的离子方程式为______ 。
②还原 (Ⅵ)时,需控制溶液的
(Ⅵ)时,需控制溶液的 ,若酸性过高会造成的后果是
,若酸性过高会造成的后果是______ 。
(3) 也可用于直接还原去除废水中的
也可用于直接还原去除废水中的 ,反应时消耗大量
,反应时消耗大量 .废水的初始
.废水的初始 对去除溶液中的
对去除溶液中的 (Ⅵ)和总
(Ⅵ)和总 的影响关系如下图所示:
的影响关系如下图所示:
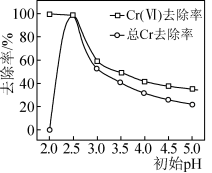
废水初始 时,
时, 和
和 反应生成
反应生成 、
、 和氢气,最终溶液的
和氢气,最终溶液的 约为9,反应生成的
约为9,反应生成的 转化为
转化为 沉淀得到有效去除,废水初始
沉淀得到有效去除,废水初始 时,虽然
时,虽然 (Ⅵ)的去除率达到100%,但总
(Ⅵ)的去除率达到100%,但总 的去除率为0.0%,其原因是
的去除率为0.0%,其原因是______ 。
 (Ⅲ)以
(Ⅲ)以 形态存在:
形态存在: (Ⅱ)主要以
(Ⅱ)主要以 和
和 形态存在,其毒性是
形态存在,其毒性是 (Ⅲ)的100倍,处理含
(Ⅲ)的100倍,处理含 (Ⅵ)废水的常用方法是先将其转化为
(Ⅵ)废水的常用方法是先将其转化为 (Ⅲ),再进一步将
(Ⅲ),再进一步将 转化为
转化为 沉淀,减少水体中总铬含量。
沉淀,减少水体中总铬含量。(1)探究
 (Ⅵ)的存在形式:
(Ⅵ)的存在形式: (Ⅵ)在水溶液中常有
(Ⅵ)在水溶液中常有 和
和 两种存在形式,该废水中两种离子的浓度与溶液
两种存在形式,该废水中两种离子的浓度与溶液 的关系如下图所示:
的关系如下图所示:
①加酸可以使
 转化为
转化为 ,该反应的离子方程式为
,该反应的离子方程式为②计算该反应的平衡常数为
 时,
时,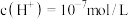 )
)(2)
 (Ⅵ)转化为
(Ⅵ)转化为
在
 时,向该废水中加入
时,向该废水中加入 溶液将
溶液将 (Ⅵ)还原为
(Ⅵ)还原为 ,然后再向其中加入浓氨水调节溶液
,然后再向其中加入浓氨水调节溶液 。
。①加入
 溶液后,发生反应的离子方程式为
溶液后,发生反应的离子方程式为②还原
 (Ⅵ)时,需控制溶液的
(Ⅵ)时,需控制溶液的 ,若酸性过高会造成的后果是
,若酸性过高会造成的后果是(3)
 也可用于直接还原去除废水中的
也可用于直接还原去除废水中的 ,反应时消耗大量
,反应时消耗大量 .废水的初始
.废水的初始 对去除溶液中的
对去除溶液中的 (Ⅵ)和总
(Ⅵ)和总 的影响关系如下图所示:
的影响关系如下图所示:
废水初始
 时,
时, 和
和 反应生成
反应生成 、
、 和氢气,最终溶液的
和氢气,最终溶液的 约为9,反应生成的
约为9,反应生成的 转化为
转化为 沉淀得到有效去除,废水初始
沉淀得到有效去除,废水初始 时,虽然
时,虽然 (Ⅵ)的去除率达到100%,但总
(Ⅵ)的去除率达到100%,但总 的去除率为0.0%,其原因是
的去除率为0.0%,其原因是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐3】甲醇、乙醇来源丰富、价格低廉、运输贮存方便,都有着重要的用途和应用前景。工业上用 和
和 反应生产甲醇、乙醇。回答下列问题:
反应生产甲醇、乙醇。回答下列问题:
(1)已知: 的燃烧热为285.8
的燃烧热为285.8 ,
, (l)的燃烧热为725.8
(l)的燃烧热为725.8 ,
,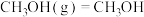
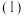
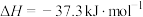 ,则
,则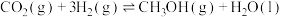

______  。
。
(2)为探究用 生产燃料甲醇的反应原理,在容积为2L的密闭容器中,充入1mol
生产燃料甲醇的反应原理,在容积为2L的密闭容器中,充入1mol 和3.25mol
和3.25mol 在一定条件下发生反应,测得
在一定条件下发生反应,测得 、
、 (g)和
(g)和 (g)的物质的量(n)随时间的变化如图1所示:
(g)的物质的量(n)随时间的变化如图1所示:
______ ( 。
。
②下列措施能使 的平衡转化率增大的是
的平衡转化率增大的是______ (填字母)。
A.在原容器中再充入1mol B.在原容器中再充入1mol
B.在原容器中再充入1mol
C.在原容器中充入1mol氦气 D.使用更有效的催化剂
(3) 也可通过催化加氢合成乙醇,其反应原理为
也可通过催化加氢合成乙醇,其反应原理为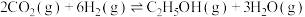 △H<0.设m为起始时的投料比,即
△H<0.设m为起始时的投料比,即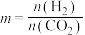 。通过实验得到如图2所示图像:
。通过实验得到如图2所示图像:______ 。
②乙中 、
、 、
、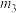 从大到小的顺序为
从大到小的顺序为______ 。
③丙表示在总压为5MPa的恒压条件下,且m=3时,平衡状态时各物质的物质的量分数与温度的关系,曲线a表示的物质是______ (填化学式), 温度时,该反应压强平衡常数
温度时,该反应压强平衡常数 的计算式为
的计算式为____________ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,代入数据,不用计算)。
 和
和 反应生产甲醇、乙醇。回答下列问题:
反应生产甲醇、乙醇。回答下列问题:(1)已知:
 的燃烧热为285.8
的燃烧热为285.8 ,
, (l)的燃烧热为725.8
(l)的燃烧热为725.8 ,
,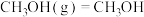
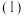
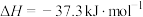 ,则
,则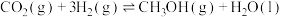

 。
。(2)为探究用
 生产燃料甲醇的反应原理,在容积为2L的密闭容器中,充入1mol
生产燃料甲醇的反应原理,在容积为2L的密闭容器中,充入1mol 和3.25mol
和3.25mol 在一定条件下发生反应,测得
在一定条件下发生反应,测得 、
、 (g)和
(g)和 (g)的物质的量(n)随时间的变化如图1所示:
(g)的物质的量(n)随时间的变化如图1所示:

 。
。②下列措施能使
 的平衡转化率增大的是
的平衡转化率增大的是A.在原容器中再充入1mol
 B.在原容器中再充入1mol
B.在原容器中再充入1mol
C.在原容器中充入1mol氦气 D.使用更有效的催化剂
(3)
 也可通过催化加氢合成乙醇,其反应原理为
也可通过催化加氢合成乙醇,其反应原理为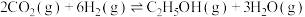 △H<0.设m为起始时的投料比,即
△H<0.设m为起始时的投料比,即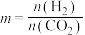 。通过实验得到如图2所示图像:
。通过实验得到如图2所示图像: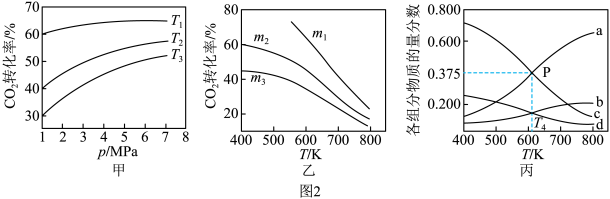
②乙中
 、
、 、
、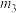 从大到小的顺序为
从大到小的顺序为③丙表示在总压为5MPa的恒压条件下,且m=3时,平衡状态时各物质的物质的量分数与温度的关系,曲线a表示的物质是
 温度时,该反应压强平衡常数
温度时,该反应压强平衡常数 的计算式为
的计算式为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐1】研究氮氧化物污染的治理是环保的一项重要工作.合理应用和处理氨氧化物,在生产生活中有重要意义.
(1)已知:①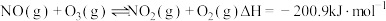 ;
;
② .
.
则由二氧化氮分解生成一氧化氮和氧气的热化学方程式为_______________________ .
(2)利用测压法在恒容刚性反应器中研究反应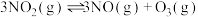 ,充入一定量
,充入一定量 ,T℃时,测得体系的总压强p随反应时间t的变化如表所示:
,T℃时,测得体系的总压强p随反应时间t的变化如表所示:
① 时,反应物的转化率
时,反应物的转化率
_____________ .若降低反应温度,则平衡后体系总压强小于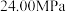 ,主要原因是
,主要原因是________________________ .
②T℃时反应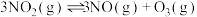 的平衡常数
的平衡常数
______ ( 为以分压表示的平衡常数).
为以分压表示的平衡常数).
(3)一定条件下,在体积为2L的密闭容器中充入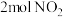 发生反应:
发生反应: 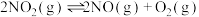 .实验测得
.实验测得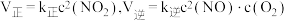 ,
, 是为速率常数,受温度影响.在温度为T℃时
是为速率常数,受温度影响.在温度为T℃时 的转化率随时间变化的情况如图所示.
的转化率随时间变化的情况如图所示.
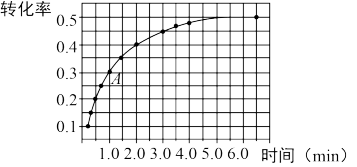
①要提高 的转化率,可采取的措施是
的转化率,可采取的措施是_____________ 、____________ (写两条).
②计算A点处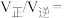
_____________ (保留一位小数).
(1)已知:①
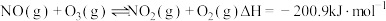 ;
;②
 .
.则由二氧化氮分解生成一氧化氮和氧气的热化学方程式为
(2)利用测压法在恒容刚性反应器中研究反应
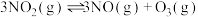 ,充入一定量
,充入一定量 ,T℃时,测得体系的总压强p随反应时间t的变化如表所示:
,T℃时,测得体系的总压强p随反应时间t的变化如表所示:| t/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| p/MPa | 20.00 | 21.38 | 22.30 | 23.00 | 23.58 | 24.00 | 24.00 |
 时,反应物的转化率
时,反应物的转化率
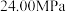 ,主要原因是
,主要原因是②T℃时反应
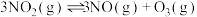 的平衡常数
的平衡常数
 为以分压表示的平衡常数).
为以分压表示的平衡常数).(3)一定条件下,在体积为2L的密闭容器中充入
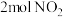 发生反应:
发生反应: 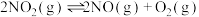 .实验测得
.实验测得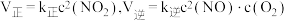 ,
, 是为速率常数,受温度影响.在温度为T℃时
是为速率常数,受温度影响.在温度为T℃时 的转化率随时间变化的情况如图所示.
的转化率随时间变化的情况如图所示.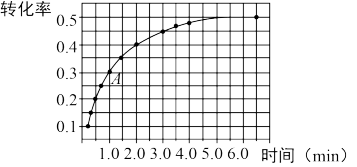
①要提高
 的转化率,可采取的措施是
的转化率,可采取的措施是②计算A点处
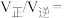
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐2】甲烷和水蒸气催化制氢主要有如下两个反应:
①
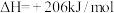
②

I.恒定压强时,将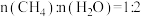 的混合气体投入反应器中,平衡时,各组分的物质的量分数与温度的关系如图所示。
的混合气体投入反应器中,平衡时,各组分的物质的量分数与温度的关系如图所示。
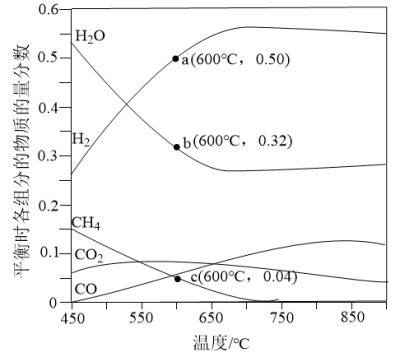
回答下列问题:
(1)已知在某种催化剂的作用下, 与
与 生成
生成 和CO的反应中,逆反应活化能
和CO的反应中,逆反应活化能 (逆)为
(逆)为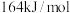 ,则该反应的
,则该反应的 (正)为
(正)为___________ kJ/mol。
(2)关于甲烷和水蒸气催化制氢反应,下列叙述正确的是___________(填标号)。
(3)系统中 的含量,在700℃左右出现峰值,试从化学平衡的角度解释出现峰值的原因:
的含量,在700℃左右出现峰值,试从化学平衡的角度解释出现峰值的原因:___________ 。
(4)600℃时 的平衡转化率为
的平衡转化率为___________ %(精确到小数点后一位)。
Ⅱ.将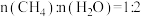 的混合气体投入恒温恒容的密闭容器中(压强为90KPa),发生反应①和②,容器内气体的压强随时间的变化如下表所示。
的混合气体投入恒温恒容的密闭容器中(压强为90KPa),发生反应①和②,容器内气体的压强随时间的变化如下表所示。
(5)用单位时间内气体分压的变化来表示反应速率,即 ,则反应①前150min内平均反应速率
,则反应①前150min内平均反应速率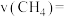
___________ kPa/min,250min末,测得氢气压强 为96kPa,
为96kPa, 为用气体分压表示的平衡常数,分压=总压×物质的量分数,则反应②平衡常数
为用气体分压表示的平衡常数,分压=总压×物质的量分数,则反应②平衡常数
___________ 。
①

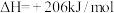
②


I.恒定压强时,将
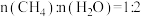 的混合气体投入反应器中,平衡时,各组分的物质的量分数与温度的关系如图所示。
的混合气体投入反应器中,平衡时,各组分的物质的量分数与温度的关系如图所示。
回答下列问题:
(1)已知在某种催化剂的作用下,
 与
与 生成
生成 和CO的反应中,逆反应活化能
和CO的反应中,逆反应活化能 (逆)为
(逆)为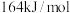 ,则该反应的
,则该反应的 (正)为
(正)为(2)关于甲烷和水蒸气催化制氢反应,下列叙述正确的是___________(填标号)。
| A.恒温、恒压条件下,若反应容器中气体密度不变,即可判断反应已达平衡状态 |
| B.恒温、恒容条件下,加入水蒸气,活化分子百分数增大,反应速率加快 |
| C.恒容、绝热条件下,若反应容器中温度不变,即可判断反应已达平衡状态 |
D.恒压、绝热条件下,向平衡后的混合气体中加入稀有气体,再次平衡后 的物质的量会减少 的物质的量会减少 |
 的含量,在700℃左右出现峰值,试从化学平衡的角度解释出现峰值的原因:
的含量,在700℃左右出现峰值,试从化学平衡的角度解释出现峰值的原因:(4)600℃时
 的平衡转化率为
的平衡转化率为Ⅱ.将
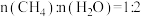 的混合气体投入恒温恒容的密闭容器中(压强为90KPa),发生反应①和②,容器内气体的压强随时间的变化如下表所示。
的混合气体投入恒温恒容的密闭容器中(压强为90KPa),发生反应①和②,容器内气体的压强随时间的变化如下表所示。| 时间/min | 0 | 50 | 100 | 150 | 200 | 250 | 300 |
| 压强/KPa | 90 | 111 | 123 | 132 | 139 | 144 | 144 |
 ,则反应①前150min内平均反应速率
,则反应①前150min内平均反应速率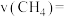
 为96kPa,
为96kPa, 为用气体分压表示的平衡常数,分压=总压×物质的量分数,则反应②平衡常数
为用气体分压表示的平衡常数,分压=总压×物质的量分数,则反应②平衡常数
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐3】氨气是重要的基础化工品。回答下列问题:
I. 在尿素合成塔中发生的反应可表示为: 2NH3(g)+CO2(g)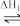 NH2COONH4(l)
NH2COONH4(l)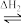 [CO(NH2)2](s)+H2O(g);已知第一步反应为快速反应,△H1=-119.2kJ·mol-1,第二步反应为慢速反应,△H2=+15.5kJ·mol-1,
[CO(NH2)2](s)+H2O(g);已知第一步反应为快速反应,△H1=-119.2kJ·mol-1,第二步反应为慢速反应,△H2=+15.5kJ·mol-1,
(1)下列图像能表示尿素合成塔中发生反应的能量变化历程的是_______(填标号)。
II.工业上使用氨气生产尿素,在一个体积恒为1L的恒温密闭容器中充入2mol CO2和4mol NH3的混合气体,经历反应1、2合成CO(NH2)2,经历如下两个过程:
反应1;2NH3(g)+CO2(g)⇌NH2COONH4(s) ΔH1= - 159.50kJ·mol-1
反应2:NH2COONH4(s)⇌CO(NH2)2(s) + H2O(g) ΔH2= + 72.50kJ·mol-1
(2)能说明反应1达到平衡状态的是(暂不考虑反应2)__ (填标号)。
①混合气体的压强不变
②混合气体的密度不变
③相同时间内断裂3molN-H键,同时形成1molCO2
④混合气体的平均相对分子质量不变
⑤NH3的体积分数不变
(3)混合气体中氨气体积分数及气体总浓度随时间变化如图所示,对于反应I,A点正反应速率与B点逆反应速率大小关系是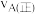
_______ 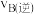 (填“>”“<”或“=”),在B点氨气的转化率为
(填“>”“<”或“=”),在B点氨气的转化率为__ 。

III.恒温恒容的密闭容器中,在某催化剂表面上发生2NH3(g)⇌N2(g)+3H2(g) 。测得在同种催化剂下分解的实验数据如下表所示:
。测得在同种催化剂下分解的实验数据如下表所示: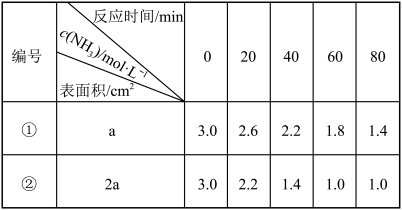
(4)根据组①数据,随着反应进行,c(NH3)减小,平均反应速率_______ (填“变大”“变小”或“不变”),对该变化的合理解释是_______ 。
(5)在科学家推出合成氨反应在接近平衡时净反应速率方程式为: ,
, ,
, 分别为正、逆反应速率常数,p代表各组分的分压,如
分别为正、逆反应速率常数,p代表各组分的分压,如 ,其中
,其中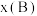 为平衡体系中B的体积分数,p为平衡总压强16MPa,以铁为催化剂时
为平衡体系中B的体积分数,p为平衡总压强16MPa,以铁为催化剂时 ,一定条件下,向容器中充入5mol N2和15mol
,一定条件下,向容器中充入5mol N2和15mol 的混合气体,平衡时氨气的质量分数为40%,试计算
的混合气体,平衡时氨气的质量分数为40%,试计算
_______ 。
I. 在尿素合成塔中发生的反应可表示为: 2NH3(g)+CO2(g)
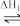 NH2COONH4(l)
NH2COONH4(l)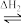 [CO(NH2)2](s)+H2O(g);已知第一步反应为快速反应,△H1=-119.2kJ·mol-1,第二步反应为慢速反应,△H2=+15.5kJ·mol-1,
[CO(NH2)2](s)+H2O(g);已知第一步反应为快速反应,△H1=-119.2kJ·mol-1,第二步反应为慢速反应,△H2=+15.5kJ·mol-1,(1)下列图像能表示尿素合成塔中发生反应的能量变化历程的是_______(填标号)。
A.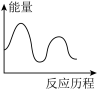 | B. | C. | D. |
II.工业上使用氨气生产尿素,在一个体积恒为1L的恒温密闭容器中充入2mol CO2和4mol NH3的混合气体,经历反应1、2合成CO(NH2)2,经历如下两个过程:
反应1;2NH3(g)+CO2(g)⇌NH2COONH4(s) ΔH1= - 159.50kJ·mol-1
反应2:NH2COONH4(s)⇌CO(NH2)2(s) + H2O(g) ΔH2= + 72.50kJ·mol-1
(2)能说明反应1达到平衡状态的是(暂不考虑反应2)
①混合气体的压强不变
②混合气体的密度不变
③相同时间内断裂3molN-H键,同时形成1molCO2
④混合气体的平均相对分子质量不变
⑤NH3的体积分数不变
(3)混合气体中氨气体积分数及气体总浓度随时间变化如图所示,对于反应I,A点正反应速率与B点逆反应速率大小关系是
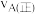
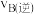 (填“>”“<”或“=”),在B点氨气的转化率为
(填“>”“<”或“=”),在B点氨气的转化率为
III.恒温恒容的密闭容器中,在某催化剂表面上发生2NH3(g)⇌N2(g)+3H2(g)
 。测得在同种催化剂下分解的实验数据如下表所示:
。测得在同种催化剂下分解的实验数据如下表所示:
(4)根据组①数据,随着反应进行,c(NH3)减小,平均反应速率
(5)在科学家推出合成氨反应在接近平衡时净反应速率方程式为:
 ,
, ,
, 分别为正、逆反应速率常数,p代表各组分的分压,如
分别为正、逆反应速率常数,p代表各组分的分压,如 ,其中
,其中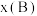 为平衡体系中B的体积分数,p为平衡总压强16MPa,以铁为催化剂时
为平衡体系中B的体积分数,p为平衡总压强16MPa,以铁为催化剂时 ,一定条件下,向容器中充入5mol N2和15mol
,一定条件下,向容器中充入5mol N2和15mol 的混合气体,平衡时氨气的质量分数为40%,试计算
的混合气体,平衡时氨气的质量分数为40%,试计算
您最近一年使用:0次
【推荐1】工业上可通过煤的液化合成甲醇,主反应为:CO(g)+2H2(g) CH3OH(l) △H=x。
CH3OH(l) △H=x。
(1)已知常温下CH3OH、H2和CO 的燃烧热分别为726.5kJ/mol、285.5 kJ/mol、283.0kJ/mol,则x=__ 。
(2)TK下,在容积为1.00L的某密闭容器中进行上述反应相关数据如图一。
①该化学反应0-10min的平均速率v(H2)=___ 。
②10min时容器内CO的体积分数为___ 。
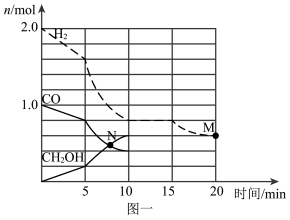
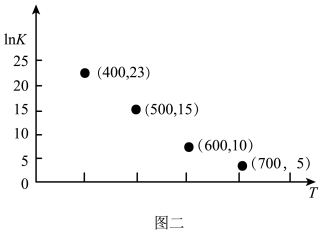
③对于气相反应,常用某组分(B)的平衡压强(pB)代替物质的量浓度(cB)表示平衡常数(以KP表示),其中,pB=p总×B的体积分数;若在TK下三种气体的平衡气体总压强为xMPa,则该反应Kp=__ (计算表达式表示)。实验测得不同温度下的lnK(化学平衡常数K的自然对数)如图二,请分析lnK随T呈现上述变化趋势的原因是__ 。
(3)干燥的甲醇可用于制造燃料电池。
某高校提出用CH3OH-O2燃料电池作电源电解处理水泥厂产生的CO2(以熔融碳酸盐为介质),产物为C和O2。其阳极电极反应式为__ 。
 CH3OH(l) △H=x。
CH3OH(l) △H=x。(1)已知常温下CH3OH、H2和CO 的燃烧热分别为726.5kJ/mol、285.5 kJ/mol、283.0kJ/mol,则x=
(2)TK下,在容积为1.00L的某密闭容器中进行上述反应相关数据如图一。
①该化学反应0-10min的平均速率v(H2)=
②10min时容器内CO的体积分数为

③对于气相反应,常用某组分(B)的平衡压强(pB)代替物质的量浓度(cB)表示平衡常数(以KP表示),其中,pB=p总×B的体积分数;若在TK下三种气体的平衡气体总压强为xMPa,则该反应Kp=

(3)干燥的甲醇可用于制造燃料电池。
某高校提出用CH3OH-O2燃料电池作电源电解处理水泥厂产生的CO2(以熔融碳酸盐为介质),产物为C和O2。其阳极电极反应式为
您最近一年使用:0次
【推荐2】羟基氧化镍( NiOOH)可作镍镉电池正极材料[放电时产物之一是Ni( OH)2];高纯度一氧化锰(MnO)可用于医药、冶炼、焊接、干电池的制造。某化工厂以含有MnS、NiS的工业料渣为原料制备NiOOH、MnO的流程如下:

请回答下列问题:
(1)写出一种能提高料渣利用率的方法:___________ ,操作X的名称是___________ 。
(2)NiOOH中Ni元素的化合价为___________ , 溶剂A必须具有的两种物理性质:一是不溶于水;二是___________ ;写出生成NiOOH的离子方程式:___________ 。
(3)热氧化过程中MnS发生反应时氧化剂与还原剂的物质的量之比为___________ 。214℃时MnC2O4分解(隔绝空气)的化学方程式为___________ 。
(4)镍镉碱性电池放电时发生还原反应的电极上的反应式为。___________ 。
(5)若10 kg料渣经过上述处理后得到a kg NiOOH,则料渣中Ni的质量分数为___________ (设转化过程中镍的损失率为2% ,列出计算式即可)。

请回答下列问题:
(1)写出一种能提高料渣利用率的方法:
(2)NiOOH中Ni元素的化合价为
(3)热氧化过程中MnS发生反应时氧化剂与还原剂的物质的量之比为
(4)镍镉碱性电池放电时发生还原反应的电极上的反应式为。
(5)若10 kg料渣经过上述处理后得到a kg NiOOH,则料渣中Ni的质量分数为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐3】锂电池的研发、使用及废电池的回收具有重要意义。
(1)比能量是指电池单位质量(或体积)输出的电能。锂金属电池放电时总反应为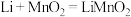 。下列关于锂金属电池说法正确的是
。下列关于锂金属电池说法正确的是___________ (填序号)。
A放电时Li作负极 B.比能量高于锌锰干电池 C.可用稀 作电解质
作电解质
(2)钴酸锂( )、磷酸铁锂(
)、磷酸铁锂( )等锂离子二次电池应用普遍。
)等锂离子二次电池应用普遍。
①钴酸锂电池放电时示意图如图1所示。放电时, 由
由 中脱嵌。写出放电至完全时
中脱嵌。写出放电至完全时 电极的电极反应式:
电极的电极反应式:___________ 。 脱嵌形成
脱嵌形成 。
。 晶胞中O围绕Fe和P分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构(如图2所示)。x=
晶胞中O围绕Fe和P分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构(如图2所示)。x=___________ 。 和NaCl溶液中使电池充分放电是电池回收工艺的首要步骤。电池在不同溶液中放电的残余电压随时间的变化如图3所示。对浸泡液中沉淀物热处理后,得到XRD示意图谱如图4所示。
和NaCl溶液中使电池充分放电是电池回收工艺的首要步骤。电池在不同溶液中放电的残余电压随时间的变化如图3所示。对浸泡液中沉淀物热处理后,得到XRD示意图谱如图4所示。___________ 。
②与 溶液相比,NaCl溶液的质量分数由5%增大至10%时,电池残余电压降低速率更快。依据图4XRD图谱,分析其主要原因:
溶液相比,NaCl溶液的质量分数由5%增大至10%时,电池残余电压降低速率更快。依据图4XRD图谱,分析其主要原因:___________ 。
(4)将放电完全的钴酸锂电池正极材料粉碎后进行酸浸处理。实验测得,在相同条件下,使用盐酸作浸取剂可使钴转化为 ,转化率达到99%,但工业生产使用
,转化率达到99%,但工业生产使用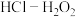 混合物作浸取剂。
混合物作浸取剂。
①写出盐酸作浸取剂发生酸浸反应的化学反应方程式:___________ 。
②工业生产时在盐酸中加入 ,
, 的作用是
的作用是___________ 。
(1)比能量是指电池单位质量(或体积)输出的电能。锂金属电池放电时总反应为
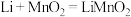 。下列关于锂金属电池说法正确的是
。下列关于锂金属电池说法正确的是A放电时Li作负极 B.比能量高于锌锰干电池 C.可用稀
 作电解质
作电解质(2)钴酸锂(
 )、磷酸铁锂(
)、磷酸铁锂( )等锂离子二次电池应用普遍。
)等锂离子二次电池应用普遍。①钴酸锂电池放电时示意图如图1所示。放电时,
 由
由 中脱嵌。写出放电至完全时
中脱嵌。写出放电至完全时 电极的电极反应式:
电极的电极反应式: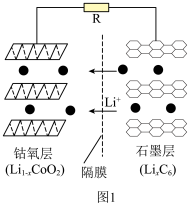
 脱嵌形成
脱嵌形成 。
。 晶胞中O围绕Fe和P分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构(如图2所示)。x=
晶胞中O围绕Fe和P分别形成正八面体和正四面体,它们通过共顶点、共棱形成空间链结构(如图2所示)。x=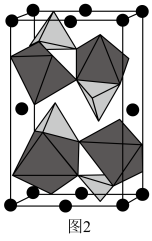
 和NaCl溶液中使电池充分放电是电池回收工艺的首要步骤。电池在不同溶液中放电的残余电压随时间的变化如图3所示。对浸泡液中沉淀物热处理后,得到XRD示意图谱如图4所示。
和NaCl溶液中使电池充分放电是电池回收工艺的首要步骤。电池在不同溶液中放电的残余电压随时间的变化如图3所示。对浸泡液中沉淀物热处理后,得到XRD示意图谱如图4所示。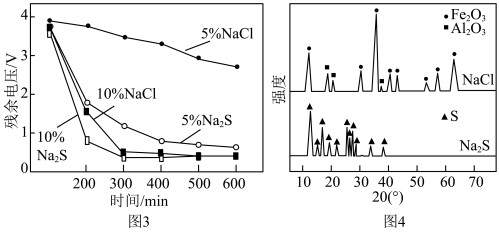
②与
 溶液相比,NaCl溶液的质量分数由5%增大至10%时,电池残余电压降低速率更快。依据图4XRD图谱,分析其主要原因:
溶液相比,NaCl溶液的质量分数由5%增大至10%时,电池残余电压降低速率更快。依据图4XRD图谱,分析其主要原因:(4)将放电完全的钴酸锂电池正极材料粉碎后进行酸浸处理。实验测得,在相同条件下,使用盐酸作浸取剂可使钴转化为
 ,转化率达到99%,但工业生产使用
,转化率达到99%,但工业生产使用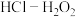 混合物作浸取剂。
混合物作浸取剂。①写出盐酸作浸取剂发生酸浸反应的化学反应方程式:
②工业生产时在盐酸中加入
 ,
, 的作用是
的作用是
您最近一年使用:0次



