研究氮氧化物污染的治理是环保的一项重要工作.合理应用和处理氨氧化物,在生产生活中有重要意义.
(1)已知:①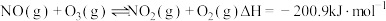 ;
;
② .
.
则由二氧化氮分解生成一氧化氮和氧气的热化学方程式为_______________________ .
(2)利用测压法在恒容刚性反应器中研究反应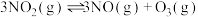 ,充入一定量
,充入一定量 ,T℃时,测得体系的总压强p随反应时间t的变化如表所示:
,T℃时,测得体系的总压强p随反应时间t的变化如表所示:
① 时,反应物的转化率
时,反应物的转化率
_____________ .若降低反应温度,则平衡后体系总压强小于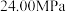 ,主要原因是
,主要原因是________________________ .
②T℃时反应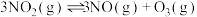 的平衡常数
的平衡常数
______ ( 为以分压表示的平衡常数).
为以分压表示的平衡常数).
(3)一定条件下,在体积为2L的密闭容器中充入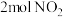 发生反应:
发生反应: 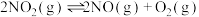 .实验测得
.实验测得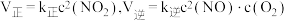 ,
, 是为速率常数,受温度影响.在温度为T℃时
是为速率常数,受温度影响.在温度为T℃时 的转化率随时间变化的情况如图所示.
的转化率随时间变化的情况如图所示.
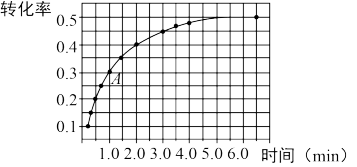
①要提高 的转化率,可采取的措施是
的转化率,可采取的措施是_____________ 、____________ (写两条).
②计算A点处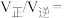
_____________ (保留一位小数).
(1)已知:①
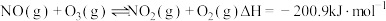 ;
;②
 .
.则由二氧化氮分解生成一氧化氮和氧气的热化学方程式为
(2)利用测压法在恒容刚性反应器中研究反应
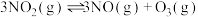 ,充入一定量
,充入一定量 ,T℃时,测得体系的总压强p随反应时间t的变化如表所示:
,T℃时,测得体系的总压强p随反应时间t的变化如表所示:| t/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| p/MPa | 20.00 | 21.38 | 22.30 | 23.00 | 23.58 | 24.00 | 24.00 |
 时,反应物的转化率
时,反应物的转化率
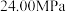 ,主要原因是
,主要原因是②T℃时反应
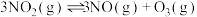 的平衡常数
的平衡常数
 为以分压表示的平衡常数).
为以分压表示的平衡常数).(3)一定条件下,在体积为2L的密闭容器中充入
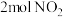 发生反应:
发生反应: 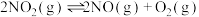 .实验测得
.实验测得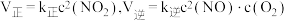 ,
, 是为速率常数,受温度影响.在温度为T℃时
是为速率常数,受温度影响.在温度为T℃时 的转化率随时间变化的情况如图所示.
的转化率随时间变化的情况如图所示.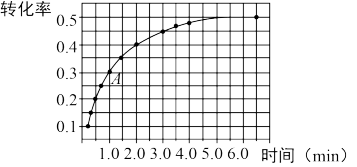
①要提高
 的转化率,可采取的措施是
的转化率,可采取的措施是②计算A点处
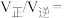
更新时间:2024-02-23 08:45:24
|
相似题推荐
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐1】汽车尾气中的 和
和 会对环境造成很大影响,我国科学家在以
会对环境造成很大影响,我国科学家在以 为还原剂清除
为还原剂清除 、
、 的研究方面取得了显著成果。回答下列问题:
的研究方面取得了显著成果。回答下列问题:
(1)以太阳能为热源分解 ,经热化学铁氧化合物循环分解水可以制
,经热化学铁氧化合物循环分解水可以制 。
。
已知: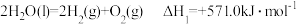
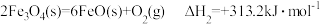
则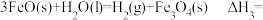
___________ 
(2) 还原
还原 的化学方程式为
的化学方程式为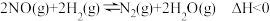 。
。
①研究表明上述反应历程分两步:
Ⅰ. (慢反应)
(慢反应)
Ⅱ.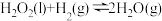 (快反应)
(快反应)
该总反应的速率由反应___________ (填“Ⅰ”或“Ⅱ”)决定,反应Ⅰ的活化能比反应Ⅱ的活化能___________ (填“高”或“低”)。
②)该反应常伴有副产物 和
和 。以
。以 作催化剂,用
作催化剂,用 还原某废气中的
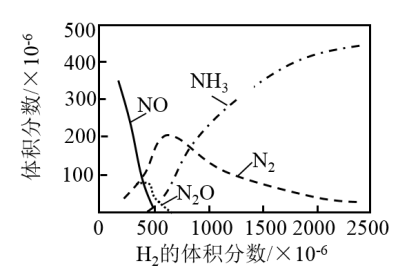
还原某废气中的 (其他气体不反应),270℃时
(其他气体不反应),270℃时 的体积分数对
的体积分数对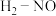 反应的影响如图所示。随着
反应的影响如图所示。随着 体积分数的增大,
体积分数的增大, 的体积分数呈下降趋势,原因是
的体积分数呈下降趋势,原因是___________ 。
在一定温度下,副产物 分解反应的化学方程式为
分解反应的化学方程式为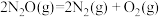 ,测得在恒容容器中
,测得在恒容容器中 分解的部分实验数据如下:
分解的部分实验数据如下:
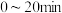 ,反应速率
,反应速率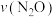 为
为___________  ;若
;若 的起始浓度为
的起始浓度为 ,则反应至
,则反应至 时
时 的转化率
的转化率
___________ 。
(3) 还原
还原 的化学方程式为
的化学方程式为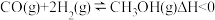 ,在密闭容器中,以浓度之比1∶2通入
,在密闭容器中,以浓度之比1∶2通入 和
和 ,反应经历相同时间,测得不同温度下
,反应经历相同时间,测得不同温度下 的转化率如图所示,则160℃时,
的转化率如图所示,则160℃时,
___________ 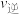 (填“>”或“<”)。若起始时
(填“>”或“<”)。若起始时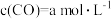 ,则380℃时该反应的化学平衡常数
,则380℃时该反应的化学平衡常数
___________ (用含有a的式子表示)。

 和
和 会对环境造成很大影响,我国科学家在以
会对环境造成很大影响,我国科学家在以 为还原剂清除
为还原剂清除 、
、 的研究方面取得了显著成果。回答下列问题:
的研究方面取得了显著成果。回答下列问题:(1)以太阳能为热源分解
 ,经热化学铁氧化合物循环分解水可以制
,经热化学铁氧化合物循环分解水可以制 。
。已知:
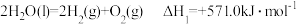
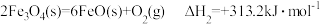
则
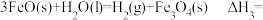

(2)
 还原
还原 的化学方程式为
的化学方程式为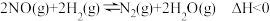 。
。①研究表明上述反应历程分两步:
Ⅰ.
 (慢反应)
(慢反应)Ⅱ.
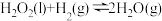 (快反应)
(快反应)该总反应的速率由反应
②)该反应常伴有副产物
 和
和 。以
。以 作催化剂,用
作催化剂,用 还原某废气中的
还原某废气中的 (其他气体不反应),270℃时
(其他气体不反应),270℃时 的体积分数对
的体积分数对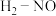 反应的影响如图所示。随着
反应的影响如图所示。随着 体积分数的增大,
体积分数的增大, 的体积分数呈下降趋势,原因是
的体积分数呈下降趋势,原因是
在一定温度下,副产物
 分解反应的化学方程式为
分解反应的化学方程式为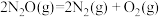 ,测得在恒容容器中
,测得在恒容容器中 分解的部分实验数据如下:
分解的部分实验数据如下:反应时间/ | 0 | 20 | 40 | 60 | 80 | 100 |
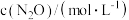 | 0.10 | 0.08 | 0.06 | 0.04 | 0.02 | 0.00 |
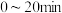 ,反应速率
,反应速率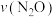 为
为 ;若
;若 的起始浓度为
的起始浓度为 ,则反应至
,则反应至 时
时 的转化率
的转化率
(3)
 还原
还原 的化学方程式为
的化学方程式为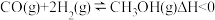 ,在密闭容器中,以浓度之比1∶2通入
,在密闭容器中,以浓度之比1∶2通入 和
和 ,反应经历相同时间,测得不同温度下
,反应经历相同时间,测得不同温度下 的转化率如图所示,则160℃时,
的转化率如图所示,则160℃时,
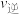 (填“>”或“<”)。若起始时
(填“>”或“<”)。若起始时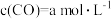 ,则380℃时该反应的化学平衡常数
,则380℃时该反应的化学平衡常数

您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐2】回答下列问题。
(1)已知下列热化学方程式:
Ⅰ.
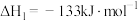
Ⅱ.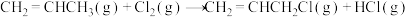
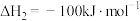
在相同条件下, 的正反应的活化能
的正反应的活化能 为
为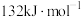 ,则逆反应的活化能
,则逆反应的活化能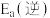 为
为___________  。
。
(2)查阅资料得知,反应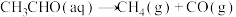 在含有少量I2的溶液中分两步进行:
在含有少量I2的溶液中分两步进行:
第Ⅰ步反应为 (慢反应);
(慢反应);
第Ⅱ步为快反应。
增大I2的浓度___________ (填“能”或“不能”)明显增大总反应的平均速率,理由为___________ 。
(3)氯化铜晶体( )常用作玻璃、陶瓷着色剂和饲料添加剂等。工业上用粗氧化铜粉(含杂质FeO和SiO2)制备无水氯化铜,制取流程如下:
)常用作玻璃、陶瓷着色剂和饲料添加剂等。工业上用粗氧化铜粉(含杂质FeO和SiO2)制备无水氯化铜,制取流程如下:
___________ (填字母,下同)。
a.KMnO4溶液 b.氯水 c.溴水 d.H2O2溶液
②溶液C中加入试剂y可以调节溶液pH,从而除去 而不引入杂质。试剂y可选用下列物质中的
而不引入杂质。试剂y可选用下列物质中的___________ 。
a.Cu b.CuO c. d.NaOH
d.NaOH
③SOCl2与水反应的化学方程式为___________ 。
④SOCl2与 混合并加热,可得到无水CuCl2的原因是
混合并加热,可得到无水CuCl2的原因是___________ 。
(1)已知下列热化学方程式:
Ⅰ.

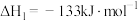
Ⅱ.
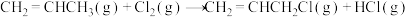
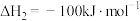
在相同条件下,
 的正反应的活化能
的正反应的活化能 为
为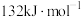 ,则逆反应的活化能
,则逆反应的活化能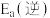 为
为 。
。(2)查阅资料得知,反应
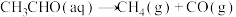 在含有少量I2的溶液中分两步进行:
在含有少量I2的溶液中分两步进行:第Ⅰ步反应为
 (慢反应);
(慢反应);第Ⅱ步为快反应。
增大I2的浓度
(3)氯化铜晶体(
 )常用作玻璃、陶瓷着色剂和饲料添加剂等。工业上用粗氧化铜粉(含杂质FeO和SiO2)制备无水氯化铜,制取流程如下:
)常用作玻璃、陶瓷着色剂和饲料添加剂等。工业上用粗氧化铜粉(含杂质FeO和SiO2)制备无水氯化铜,制取流程如下: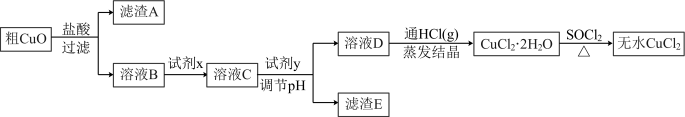
 |  |  | |
| 开始沉淀的pH | 1.9 | 7.0 | 4.7 |
| 沉淀完全的pH | 3.2 | 9.0 | 6.7 |
已知:氯化亚砜(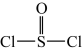 )熔点-105℃,沸点78.8℃,易水解。
)熔点-105℃,沸点78.8℃,易水解。
a.KMnO4溶液 b.氯水 c.溴水 d.H2O2溶液
②溶液C中加入试剂y可以调节溶液pH,从而除去
 而不引入杂质。试剂y可选用下列物质中的
而不引入杂质。试剂y可选用下列物质中的a.Cu b.CuO c.
 d.NaOH
d.NaOH③SOCl2与水反应的化学方程式为
④SOCl2与
 混合并加热,可得到无水CuCl2的原因是
混合并加热,可得到无水CuCl2的原因是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐3】 加氢是对温室气体的有效转化,也是生成再生能源与化工原料重要途径。
加氢是对温室气体的有效转化,也是生成再生能源与化工原料重要途径。
(1)由 加氢生成
加氢生成 的反应为
的反应为
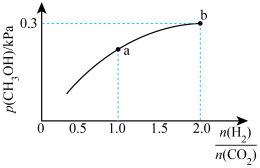
①若 为标准摩尔生成焓,其定义为标准状态下,由稳定相态的单质生成1mol该物质的焓变。则该反应的反应热
为标准摩尔生成焓,其定义为标准状态下,由稳定相态的单质生成1mol该物质的焓变。则该反应的反应热
___________ 
②若在一定温度下的容积固定的密闭容器中进行该反应,则可以提高 平衡转化率的措施有
平衡转化率的措施有___________ (写出两种)。
③下列说法可以证明该反应已达到平衡状态的是___________ (填字母)。
a.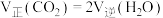 b.
b. 的物质的量分数不再改变
的物质的量分数不再改变
c.容器内气体密度不再改变 d. 和
和 的浓度之比为1:2
的浓度之比为1:2
e.混合气的平均摩尔质量不再变化 f.单位时间内生成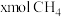 的同时又消耗
的同时又消耗
④ 催化加氢合成
催化加氢合成 过程中,
过程中, 活化的可能途径如有图所示,CO是
活化的可能途径如有图所示,CO是 活化的优势中间体,原因是
活化的优势中间体,原因是___________ 。
(2)一定条件下 与
与 也可以生成
也可以生成 ,某温度下在容积为2L的恒容密闭容器中充入
,某温度下在容积为2L的恒容密闭容器中充入 和一定量
和一定量 发生反应:
发生反应: 。
。 的平衡分压与起始投料比
的平衡分压与起始投料比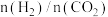 的变化关系如图所示,已知b点对应投料比的起始压强为1.5kPa,则
的变化关系如图所示,已知b点对应投料比的起始压强为1.5kPa,则
___________ 。b点时,再充入 和
和 ,使两者分压均增大0.2kPa,则此时平衡
,使两者分压均增大0.2kPa,则此时平衡___________ (填“正向”、“逆向”或“不”)移动。
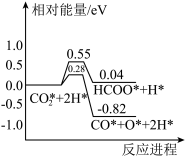
(3)一定条件下 与
与 还可以生成甲酸,方程式为
还可以生成甲酸,方程式为
 。恒定压强为100kPa时,向密闭容器中充入一定量的HCOOH气体,
。恒定压强为100kPa时,向密闭容器中充入一定量的HCOOH气体, 除了能分解成
除了能分解成 和
和 ,还能分解为CO和
,还能分解为CO和 ,反应为:
,反应为:
 ,则此平衡体系中CO或
,则此平衡体系中CO或 的选择性和HCOOH的转化率随温度变化曲线如图所示。
的选择性和HCOOH的转化率随温度变化曲线如图所示。

提示:CO(或氢气)的选择性
图中随着温度升高,HCOOH的转化率增大,请解释CO的选择性下降可能的原因:___________ ;400°C时 的体积分数为
的体积分数为___________ 。
 加氢是对温室气体的有效转化,也是生成再生能源与化工原料重要途径。
加氢是对温室气体的有效转化,也是生成再生能源与化工原料重要途径。(1)由
 加氢生成
加氢生成 的反应为
的反应为
①若
 为标准摩尔生成焓,其定义为标准状态下,由稳定相态的单质生成1mol该物质的焓变。则该反应的反应热
为标准摩尔生成焓,其定义为标准状态下,由稳定相态的单质生成1mol该物质的焓变。则该反应的反应热

| 物质 |  |  |  |  |
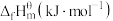 |  | 0 | 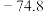 | 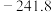 |
 平衡转化率的措施有
平衡转化率的措施有③下列说法可以证明该反应已达到平衡状态的是
a.
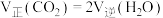 b.
b. 的物质的量分数不再改变
的物质的量分数不再改变c.容器内气体密度不再改变 d.
 和
和 的浓度之比为1:2
的浓度之比为1:2e.混合气的平均摩尔质量不再变化 f.单位时间内生成
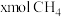 的同时又消耗
的同时又消耗
④
 催化加氢合成
催化加氢合成 过程中,
过程中, 活化的可能途径如有图所示,CO是
活化的可能途径如有图所示,CO是 活化的优势中间体,原因是
活化的优势中间体,原因是
(2)一定条件下
 与
与 也可以生成
也可以生成 ,某温度下在容积为2L的恒容密闭容器中充入
,某温度下在容积为2L的恒容密闭容器中充入 和一定量
和一定量 发生反应:
发生反应: 。
。 的平衡分压与起始投料比
的平衡分压与起始投料比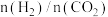 的变化关系如图所示,已知b点对应投料比的起始压强为1.5kPa,则
的变化关系如图所示,已知b点对应投料比的起始压强为1.5kPa,则
 和
和 ,使两者分压均增大0.2kPa,则此时平衡
,使两者分压均增大0.2kPa,则此时平衡
(3)一定条件下
 与
与 还可以生成甲酸,方程式为
还可以生成甲酸,方程式为
 。恒定压强为100kPa时,向密闭容器中充入一定量的HCOOH气体,
。恒定压强为100kPa时,向密闭容器中充入一定量的HCOOH气体, 除了能分解成
除了能分解成 和
和 ,还能分解为CO和
,还能分解为CO和 ,反应为:
,反应为:
 ,则此平衡体系中CO或
,则此平衡体系中CO或 的选择性和HCOOH的转化率随温度变化曲线如图所示。
的选择性和HCOOH的转化率随温度变化曲线如图所示。
提示:CO(或氢气)的选择性

图中随着温度升高,HCOOH的转化率增大,请解释CO的选择性下降可能的原因:
 的体积分数为
的体积分数为
您最近一年使用:0次
【推荐1】CO2的综合利用是当前研究的热点问题。2020年12月24日,中国科学院大气物理研究所碳中和研究中心(等)在北京挂牌成立。回答下列问题:
(1)已知:I.C(s)+O2(g)=CO2(g) ΔH1=-393.5kJ·mol-l;
Ⅱ.2H2(g)+O2(g)=2H2O(g) ΔH2=-483.6kJ·mol-l;
Ⅲ.C(s)+2H2(g)=CH4(g) ΔH3=-74.8kJ·mol-1。
利用光能和光催化剂,将CO2(g)和H2O(g)转化为CH4(g)和O2(g)的热化学方程式为_______ 。
(2)一定温度下,将1molCH4(g)和3molCO2(g)充入起始压强为4MPa、体积为10L的恒容密闭容器中,一定条件下发生反应CH4(g)+CO2(g) ⇌2CO(g)+2H2(g) ΔH=+247kJ·mol-1。
①下列事实可以判定反应达到平衡状态的是_______ (填选项字母)。
A.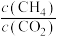 为定值
为定值
B.混合气体的密度不再改变
C.混合气体的平均相对分子质量不再改变
②若上述反应10min末达到平衡,容器内的压强变为起始压强的1.25倍,则0~10min内,用CO2的浓度变化表示的平均反应速率v(CO2)=_______ ;CH4的平衡转化率为_______ ;该反应的平衡常数Kp=_______ MPa2(用平衡分压代替平衡浓度表示的平衡常数,分压=总压×该物质的物质的量分数)。
(3)一定条件下,CO2催化加氢可以合成乙醇:2CO2(g)+6H2(g) ⇌C2H5OH(g)+3H2O(g)。向I、Ⅱ、Ⅲ三个容积均为1L的恒容密闭容器中均充入1molCO2(g)和3molH2(g),在不同温度下发生上述反应。反应5min,测得各容器内CO2的物质的量如图所示:
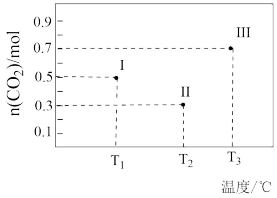
①该反应的ΔH_______ 0(填“>”或“<”)。
②5min后,向容器Ⅲ中再充入1molCO2(g)和1molH2O(g),此时v逆_______ v正(填“>”“<”或“=”)。
(4)人工光合作用能够借助太阳能,用CO2和H2O制备化学原料。通过人工光合作用制备HCOOH的原理示意图如图所示:
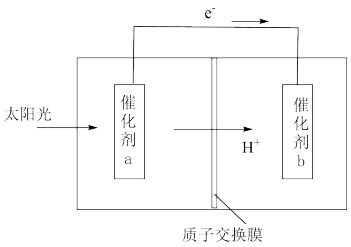
催化剂a表面发生____ (填“氧化”或“还原”)反应;催化剂b表面的电极反应式为___ 。
(1)已知:I.C(s)+O2(g)=CO2(g) ΔH1=-393.5kJ·mol-l;
Ⅱ.2H2(g)+O2(g)=2H2O(g) ΔH2=-483.6kJ·mol-l;
Ⅲ.C(s)+2H2(g)=CH4(g) ΔH3=-74.8kJ·mol-1。
利用光能和光催化剂,将CO2(g)和H2O(g)转化为CH4(g)和O2(g)的热化学方程式为
(2)一定温度下,将1molCH4(g)和3molCO2(g)充入起始压强为4MPa、体积为10L的恒容密闭容器中,一定条件下发生反应CH4(g)+CO2(g) ⇌2CO(g)+2H2(g) ΔH=+247kJ·mol-1。
①下列事实可以判定反应达到平衡状态的是
A.
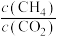 为定值
为定值B.混合气体的密度不再改变
C.混合气体的平均相对分子质量不再改变
②若上述反应10min末达到平衡,容器内的压强变为起始压强的1.25倍,则0~10min内,用CO2的浓度变化表示的平均反应速率v(CO2)=
(3)一定条件下,CO2催化加氢可以合成乙醇:2CO2(g)+6H2(g) ⇌C2H5OH(g)+3H2O(g)。向I、Ⅱ、Ⅲ三个容积均为1L的恒容密闭容器中均充入1molCO2(g)和3molH2(g),在不同温度下发生上述反应。反应5min,测得各容器内CO2的物质的量如图所示:

①该反应的ΔH
②5min后,向容器Ⅲ中再充入1molCO2(g)和1molH2O(g),此时v逆
(4)人工光合作用能够借助太阳能,用CO2和H2O制备化学原料。通过人工光合作用制备HCOOH的原理示意图如图所示:

催化剂a表面发生
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐2】用H2O2、KI 和洗洁精可完成“大象牙膏”实验(短时间内产生大量泡沫),某同学依据文献资料对该实验进行探究。
(1)资料1:KI 在该反应中的作用:H2O2 + I = H2O+ IO ;H2O2 + IO = H2O+ O2↑+ I 。总反应的化学方程式是________ 。
(2)资料 2:H2O2 分解反应过程中能量变化如图所示,其中①有 KI 加入,②无 KI 加入。下列 判断正确的是___________ (填字母)。

a.加入KI 后改变了反应的路径
b.加入KI 后改变了总反应的能量变化
c.H2O2 + I = H2O + IO 是放热反应
(3)实验中发现,H2O2与 KI 溶液混合后,产生大量气泡,溶液颜色变黄。再加入 CCl4,振荡、静置,气泡明显减少。
资料 3:I2 也可催化H2O2的分解反应。
① 加CCl4 并振荡、静置后还可观察到________ ,说明有 I2 生成。
② 气泡明显减少的原因可能是:ⅰ.H2O2 浓度降低;ⅱ.________ 。以下对照实验说明ⅰ不是主要原因:向H2O2溶液中加入 KI 溶液,待溶液变黄后,分成两等份于A、B 两试管中。A 试管加入 CCl4,B 试管不加CCl4,分别振荡、静置。观察到的现象是________ 。
(4)资料 4: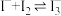 K= 640。
K= 640。
为了探究体系中含碘微粒的存在形式,进行实验:向 20 mL 一定浓度的H2O2溶液中加入10 mL 0.10 mol·L−1 KI 溶液,达平衡后,相关微粒浓度如下:
① a =___________ 。
② 该平衡体系中除了含有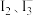 和
和 外,一定还含有其他含碘微粒,理由是
外,一定还含有其他含碘微粒,理由是___________ 。
(1)资料1:KI 在该反应中的作用:H2O2 + I = H2O+ IO ;H2O2 + IO = H2O+ O2↑+ I 。总反应的化学方程式是
(2)资料 2:H2O2 分解反应过程中能量变化如图所示,其中①有 KI 加入,②无 KI 加入。下列 判断正确的是

a.加入KI 后改变了反应的路径
b.加入KI 后改变了总反应的能量变化
c.H2O2 + I = H2O + IO 是放热反应
(3)实验中发现,H2O2与 KI 溶液混合后,产生大量气泡,溶液颜色变黄。再加入 CCl4,振荡、静置,气泡明显减少。
资料 3:I2 也可催化H2O2的分解反应。
① 加CCl4 并振荡、静置后还可观察到
② 气泡明显减少的原因可能是:ⅰ.H2O2 浓度降低;ⅱ.
(4)资料 4:
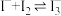 K= 640。
K= 640。为了探究体系中含碘微粒的存在形式,进行实验:向 20 mL 一定浓度的H2O2溶液中加入10 mL 0.10 mol·L−1 KI 溶液,达平衡后,相关微粒浓度如下:
| 微粒 |  |  |  |
| 浓度(mol·L−1) | 2.5×10−3 | a | 4.0×10−3 |
② 该平衡体系中除了含有
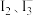 和
和 外,一定还含有其他含碘微粒,理由是
外,一定还含有其他含碘微粒,理由是
您最近一年使用:0次
【推荐3】二甲醚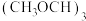 具有优良的燃烧性能,被称为21世纪的“清洁能源”。一步法合成二甲醚是以合成气(CO/H2)为原料,在一定温度、压强和催化剂作用下进行,反应器中发生了下列反应:
具有优良的燃烧性能,被称为21世纪的“清洁能源”。一步法合成二甲醚是以合成气(CO/H2)为原料,在一定温度、压强和催化剂作用下进行,反应器中发生了下列反应:
①
②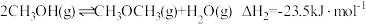
③
(1)①一种合成二甲醚的新方法为一定条件下: ,该反应的ΔH=
,该反应的ΔH=_______ kJ/mol。
②在一定温度下、体积恒定的密闭容器中,下列不能作为判断该反应达到化学平衡状态的依据的是_______ (填标号)。
A.容器内气体的平均摩尔质量保持不变
B.容器内气体的密度不变
C.容器内气体的压强保持不变
D.单位时间内消耗2mol CO2,同时消耗1mol二甲醚
(2)CO2可制取CH3OH(g)和水蒸气。将1mol CO2和3mol H2充入0.5恒容密闭容器中,在两种不同催化剂作用下发生反应,相同时间内CO2的转化率随温度变化曲线如图所示。
①a点时v正_______ v逆(填“>”“<”或“=”);
②随温度的升高,CO2的转化率先增大后减小,理由是_______ ;
③已知c点时容器内的压强为p,在T5温度下该反应的平衡常数Kp为_______ (用含p的关系式表示,Kp为分压表示的平衡常数,分压=总压×物质的量分数)。

(3)在某催化剂作用下,CO2和H2还能发生如下反应: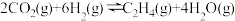 ,下图中所示为在体积为1L的恒容密闭容器中,通入1mol CO2和3mol H2时,测得的温度对CO2的平衡转化率和催化剂催化效率的影响。
,下图中所示为在体积为1L的恒容密闭容器中,通入1mol CO2和3mol H2时,测得的温度对CO2的平衡转化率和催化剂催化效率的影响。

①e、f两点平衡常数的大小关系为Ke_______ Kf(填“>”或“<”);
②如果不用催化剂,其他条件不变,则250℃时CO2的平衡转化率位于_______ 点(填“e”“g”或“h”)。
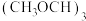 具有优良的燃烧性能,被称为21世纪的“清洁能源”。一步法合成二甲醚是以合成气(CO/H2)为原料,在一定温度、压强和催化剂作用下进行,反应器中发生了下列反应:
具有优良的燃烧性能,被称为21世纪的“清洁能源”。一步法合成二甲醚是以合成气(CO/H2)为原料,在一定温度、压强和催化剂作用下进行,反应器中发生了下列反应:①

②
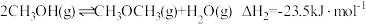
③

(1)①一种合成二甲醚的新方法为一定条件下:
 ,该反应的ΔH=
,该反应的ΔH=②在一定温度下、体积恒定的密闭容器中,下列不能作为判断该反应达到化学平衡状态的依据的是
A.容器内气体的平均摩尔质量保持不变
B.容器内气体的密度不变
C.容器内气体的压强保持不变
D.单位时间内消耗2mol CO2,同时消耗1mol二甲醚
(2)CO2可制取CH3OH(g)和水蒸气。将1mol CO2和3mol H2充入0.5恒容密闭容器中,在两种不同催化剂作用下发生反应,相同时间内CO2的转化率随温度变化曲线如图所示。
①a点时v正
②随温度的升高,CO2的转化率先增大后减小,理由是
③已知c点时容器内的压强为p,在T5温度下该反应的平衡常数Kp为

(3)在某催化剂作用下,CO2和H2还能发生如下反应:
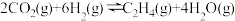 ,下图中所示为在体积为1L的恒容密闭容器中,通入1mol CO2和3mol H2时,测得的温度对CO2的平衡转化率和催化剂催化效率的影响。
,下图中所示为在体积为1L的恒容密闭容器中,通入1mol CO2和3mol H2时,测得的温度对CO2的平衡转化率和催化剂催化效率的影响。
①e、f两点平衡常数的大小关系为Ke
②如果不用催化剂,其他条件不变,则250℃时CO2的平衡转化率位于
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐1】氨气是国民经济基础,提高粮食产量离不开氨气及铵态氮肥。工业合成氨的原理是
 。
。
(1)在恒容条件下发生上述反应,达到平衡后除改变温度、压强外,提高 平衡转化率的措施还有
平衡转化率的措施还有_______ (答一条)。
(2)一定温度下,在某催化剂表面发生反应 ,该反应的速率方程为
,该反应的速率方程为 (k是速率常数,只与温度、催化剂有关;
(k是速率常数,只与温度、催化剂有关; 、
、 、
、 可以取整数、分数或负数,它们的和为反应级数)。某温度下,不同浓度下测得的该反应速率如表所示:
可以取整数、分数或负数,它们的和为反应级数)。某温度下,不同浓度下测得的该反应速率如表所示:
①该反应级数为_______ 。表中x的值为_______ 。
②该反应体系的三种物质中,_______ (填化学式)的浓度对反应速率的影响最大。
(3)在体积相等的甲、乙两个密闭容器中分别充入 和
和 ,一个在绝热恒容、一个在恒温恒容条件下合成氨,测得气体的压强与时间的关系如图所示。
,一个在绝热恒容、一个在恒温恒容条件下合成氨,测得气体的压强与时间的关系如图所示。
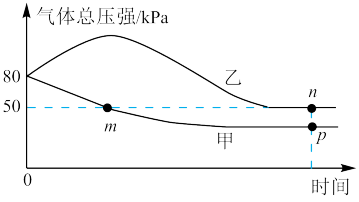
提示:净反应速率等于正、逆反应速率之差; 为用分压表示的平衡常数,分压=总压×物质的量分数。
为用分压表示的平衡常数,分压=总压×物质的量分数。
①p点的压强平衡常数
_______ 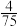 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
②下列说法正确的是_______ (填字母)。
A.m点气体的总物质的量大于n点
B.反应速率:n点的逆反应速率小于p点的正反应速率
C.甲为恒温恒容容器
D.净反应速率:n点大于p点

 。
。(1)在恒容条件下发生上述反应,达到平衡后除改变温度、压强外,提高
 平衡转化率的措施还有
平衡转化率的措施还有(2)一定温度下,在某催化剂表面发生反应
 ,该反应的速率方程为
,该反应的速率方程为 (k是速率常数,只与温度、催化剂有关;
(k是速率常数,只与温度、催化剂有关; 、
、 、
、 可以取整数、分数或负数,它们的和为反应级数)。某温度下,不同浓度下测得的该反应速率如表所示:
可以取整数、分数或负数,它们的和为反应级数)。某温度下,不同浓度下测得的该反应速率如表所示:| 序号 | 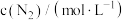 |  | 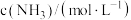 | 反应速率 |
| Ⅰ | 0.1 | 0.1 | 2 |  |
| Ⅱ | 0.1 | 0.4 | 2 | 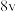 |
| Ⅲ | 0.2 | 0.4 | 2 |  |
| Ⅳ | 0.4 | 0.1 | 4 | 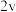 |
| Ⅴ | 0.2 | 0.1 | x | 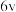 |
②该反应体系的三种物质中,
(3)在体积相等的甲、乙两个密闭容器中分别充入
 和
和 ,一个在绝热恒容、一个在恒温恒容条件下合成氨,测得气体的压强与时间的关系如图所示。
,一个在绝热恒容、一个在恒温恒容条件下合成氨,测得气体的压强与时间的关系如图所示。
提示:净反应速率等于正、逆反应速率之差;
 为用分压表示的平衡常数,分压=总压×物质的量分数。
为用分压表示的平衡常数,分压=总压×物质的量分数。①p点的压强平衡常数

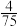 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。②下列说法正确的是
A.m点气体的总物质的量大于n点
B.反应速率:n点的逆反应速率小于p点的正反应速率
C.甲为恒温恒容容器
D.净反应速率:n点大于p点
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐2】随着我国碳达峰、碳中和目标的确定,二氧化碳资源化利用倍受关注。
Ⅰ.研究发现,以 和
和 为原料合成尿素的反应
为原料合成尿素的反应 ΔH,分两步完成,其能量变化如图甲所示:
ΔH,分两步完成,其能量变化如图甲所示:
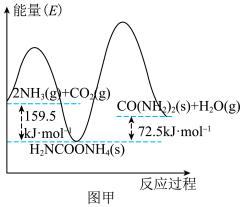
第一步: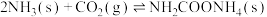

第二步: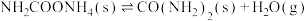

(1)合成尿素的决速反应是______ 反应(填“第一步”或“第二步”)。
(2)已知合成尿素 ΔH的活化能Ea(逆)为194
ΔH的活化能Ea(逆)为194 ,则该反应的活化能Ea(正)为
,则该反应的活化能Ea(正)为______  。
。
Ⅱ.以 和
和 催化重整制备合成气发生反应:
催化重整制备合成气发生反应: 。
。
(3)在一定条件下,在密闭容器中通入一定量的 和
和 ,
, 的平衡转化率随温度、压强的变化关系如图乙所示。
的平衡转化率随温度、压强的变化关系如图乙所示。
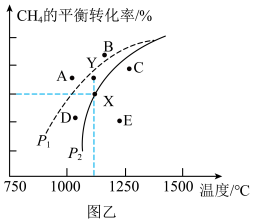
①若反应在恒温、恒压密闭容器中进行,下列叙述能说明反应达到平衡状态的是____ (填序号)。
A.容器中混合气体的密度保持不变 B.容器内CO与 的物质的量之比保持不变
的物质的量之比保持不变
C.反应速率: D.断裂2mol C—H同时断裂1mol H—H键
D.断裂2mol C—H同时断裂1mol H—H键
②由图乙可知,压强
____  (填“>”、“<”或“=”,下同);压强为
(填“>”、“<”或“=”,下同);压强为 时,对应温度下Y点速率
时,对应温度下Y点速率
____  。
。
③若在Y点时对反应容器升温的同时扩大容器体积使体系压强减小,重新达到新的平衡状态时,可能是图中:A、B、C、D、E点中的____ 点。
④一定温度下,向容积不变的密闭容器中通入总压强为P kPa的等物质的量的 和
和 以及一定量的水蒸气(水蒸气不参与反应),达到平衡后总压强1.48P kPa,
以及一定量的水蒸气(水蒸气不参与反应),达到平衡后总压强1.48P kPa, 的转化率为60%,则该温度下的
的转化率为60%,则该温度下的
____ (用含P的代数式表示,只列计算表达式:用平衡分压代替平衡浓度,已知气体分压=气体总压×气体的物质的量分数)。
Ⅲ.在稀硫酸中利用电催化可将 同时转化为多种燃料,其原理如图丙所示。
同时转化为多种燃料,其原理如图丙所示。
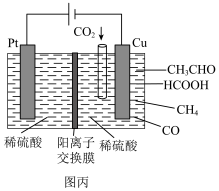
(4)铜电极上产生 的电极反应式为
的电极反应式为______ ,若铜电极上只生成5.6g CO,则铜极区溶液质量变化了____ g;若铜极上只生成0.3mol  和0.4mol HCOOH,则电路中转移
和0.4mol HCOOH,则电路中转移_____ mol电子。
Ⅰ.研究发现,以
 和
和 为原料合成尿素的反应
为原料合成尿素的反应 ΔH,分两步完成,其能量变化如图甲所示:
ΔH,分两步完成,其能量变化如图甲所示:
第一步:
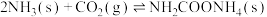

第二步:
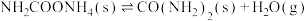

(1)合成尿素的决速反应是
(2)已知合成尿素
 ΔH的活化能Ea(逆)为194
ΔH的活化能Ea(逆)为194 ,则该反应的活化能Ea(正)为
,则该反应的活化能Ea(正)为 。
。Ⅱ.以
 和
和 催化重整制备合成气发生反应:
催化重整制备合成气发生反应: 。
。(3)在一定条件下,在密闭容器中通入一定量的
 和
和 ,
, 的平衡转化率随温度、压强的变化关系如图乙所示。
的平衡转化率随温度、压强的变化关系如图乙所示。
①若反应在恒温、恒压密闭容器中进行,下列叙述能说明反应达到平衡状态的是
A.容器中混合气体的密度保持不变 B.容器内CO与
 的物质的量之比保持不变
的物质的量之比保持不变C.反应速率:
 D.断裂2mol C—H同时断裂1mol H—H键
D.断裂2mol C—H同时断裂1mol H—H键②由图乙可知,压强

 (填“>”、“<”或“=”,下同);压强为
(填“>”、“<”或“=”,下同);压强为 时,对应温度下Y点速率
时,对应温度下Y点速率
 。
。③若在Y点时对反应容器升温的同时扩大容器体积使体系压强减小,重新达到新的平衡状态时,可能是图中:A、B、C、D、E点中的
④一定温度下,向容积不变的密闭容器中通入总压强为P kPa的等物质的量的
 和
和 以及一定量的水蒸气(水蒸气不参与反应),达到平衡后总压强1.48P kPa,
以及一定量的水蒸气(水蒸气不参与反应),达到平衡后总压强1.48P kPa, 的转化率为60%,则该温度下的
的转化率为60%,则该温度下的
Ⅲ.在稀硫酸中利用电催化可将
 同时转化为多种燃料,其原理如图丙所示。
同时转化为多种燃料,其原理如图丙所示。
(4)铜电极上产生
 的电极反应式为
的电极反应式为 和0.4mol HCOOH,则电路中转移
和0.4mol HCOOH,则电路中转移
您最近一年使用:0次
【推荐3】I. 已知:H2O2可看作二元弱酸。
(1)请写出H2O2与Ba(OH)2溶液反应生成的酸式盐的电子式________________ 。
某兴趣小组分析H2O2的催化分解原理。
(2)I-催化H2O2分解的原理分为两步,总反应可表示为:2H2O2(aq)=2H2O(l)+O2(g) △H<0,若第一步反应的热化学方程式为:H2O2(aq)+I-(aq)=IO-(aq)+H2O(l) △H>0 慢反应,则第二步反应的热化学方程式为:___________ △H <0 快反应
(3)能正确表示I-催化H2O2分解原理的示意图为______ 。

II. 丙烯(C3H6)是重要的有机化工原料。丙烷脱氢制丙烯发生的主要反应及能量变化如下图,主反应为丙烷脱氢反应,副反应为丙烷裂解反应
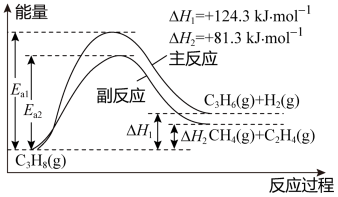
已知主反应:v正= k正p(C3H8),v逆= k逆p(C3H6)·p(H2)。
其中v正、v逆 为正、逆反应速率,k正、k逆为速率常数,p为各组分的分压。
(4)下表中为各物质的燃烧热,计算丙烯的燃烧热为△H =______ kJ·mol-1。
副反应丙烷裂解制乙烯的过程中,其原子利用率为_______ (保留三位有效数字)。
(5)在T1、T2、T3不同温度下,向体积为1L的恒容密闭容器中充入1molC3H8,开始时容器的压强分别为p1、p2、p3,仅发生主反应,丙烷转化率(α)随时间(t)的变化关系如图所示:
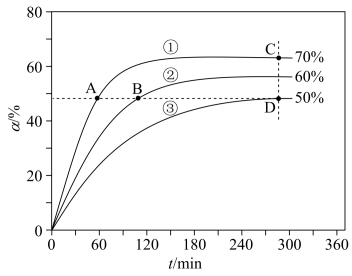
①A、B、D三点中,k正/k逆 值最大的是_________ ,
②A、B、C、D四点中,v逆 最大的是_________ 。
(1)请写出H2O2与Ba(OH)2溶液反应生成的酸式盐的电子式
某兴趣小组分析H2O2的催化分解原理。
(2)I-催化H2O2分解的原理分为两步,总反应可表示为:2H2O2(aq)=2H2O(l)+O2(g) △H<0,若第一步反应的热化学方程式为:H2O2(aq)+I-(aq)=IO-(aq)+H2O(l) △H>0 慢反应,则第二步反应的热化学方程式为:
(3)能正确表示I-催化H2O2分解原理的示意图为

II. 丙烯(C3H6)是重要的有机化工原料。丙烷脱氢制丙烯发生的主要反应及能量变化如下图,主反应为丙烷脱氢反应,副反应为丙烷裂解反应

已知主反应:v正= k正p(C3H8),v逆= k逆p(C3H6)·p(H2)。
其中v正、v逆 为正、逆反应速率,k正、k逆为速率常数,p为各组分的分压。
(4)下表中为各物质的燃烧热,计算丙烯的燃烧热为△H =
| H2 | CH4 | C2H4 | |
| △H /kJ·mol—1 | -285.8 | -890.3 | -1411.0 |
副反应丙烷裂解制乙烯的过程中,其原子利用率为
(5)在T1、T2、T3不同温度下,向体积为1L的恒容密闭容器中充入1molC3H8,开始时容器的压强分别为p1、p2、p3,仅发生主反应,丙烷转化率(α)随时间(t)的变化关系如图所示:

①A、B、D三点中,k正/k逆 值最大的是
②A、B、C、D四点中,v逆 最大的是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐1】氮氧化物(主要为NO和NO2)是大气污染物,如何有效地消除氮氧化物的污染是目前科学家们研究的热点问题。
(1)用尿素[CO(NH2)2]吸收氮氧化物是一种可行的方法。
①尿素在高温条件下与NO2反应转化成无毒气体,该反应的化学方程式为___ 。用尿素溶液也可吸收氮氧化物,研究表明,当混合气体中 =1时,总氮还原率最高,随着,
=1时,总氮还原率最高,随着, 比值增大,总氮还原率降低的主要原因是
比值增大,总氮还原率降低的主要原因是___ 。
②在一个体积为1L的恒容密闭容器中充入1molCO2和1molNH3,在恒定温度下使其发生反应2NH3(g)+CO2(g) NH2CONH2(s)+H2O(g) △H<0并达到平衡,混合气体中氨气的体积分数随时间的变化如图所示。
NH2CONH2(s)+H2O(g) △H<0并达到平衡,混合气体中氨气的体积分数随时间的变化如图所示。
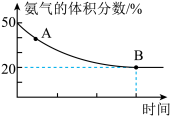
则A点时v正(CO2)___ (填“>”“<”或“=”)B点时v正(CO2),原因是___ 。B点时,NH3的转化率为___ 。
③下列有关反应2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(g)的说法正确的是
CO(NH2)2(s)+H2O(g)的说法正确的是___ 。
A.分离出少量的尿素,NH3的转化率将增大
B.反应达到平衡时,降低反应体系的温度,CO2的浓度减小
C.NH3的转化率始终等于CO2的转化率
D.加入有效的催化剂能够提高尿素的产率
(2)已知O3氧化氮氧化物的主要反应的热化学方程式如下:
2NO(g)+O2(g)=2NO2(g) △H1=akJ·mol-1
NO(g)+O3(g)=NO2(g)+O2(g) △H2=bkJ·mol-1
6NO2(g)+O3(g)=3N2O5(g) △H3=ckJ·mol-1
则反应4NO2(g)+O2(g)=2N2O5(g)△H=___ (用含a、b、c的代数式表示)kJ·mol-1。
(3)氮氧化物也可用碱液吸收。若NO和NO2的混合气体被NaOH溶液完全吸收,只生成一种盐,则该盐的化学式为___ ;已知常温下Ka(HNO2)=5×10-4,则反应HNO2(aq)+NaOH(aq) NaNO2(aq)+H2O(l)的平衡常数K=
NaNO2(aq)+H2O(l)的平衡常数K=___ 。
(1)用尿素[CO(NH2)2]吸收氮氧化物是一种可行的方法。
①尿素在高温条件下与NO2反应转化成无毒气体,该反应的化学方程式为
 =1时,总氮还原率最高,随着,
=1时,总氮还原率最高,随着, 比值增大,总氮还原率降低的主要原因是
比值增大,总氮还原率降低的主要原因是②在一个体积为1L的恒容密闭容器中充入1molCO2和1molNH3,在恒定温度下使其发生反应2NH3(g)+CO2(g)
 NH2CONH2(s)+H2O(g) △H<0并达到平衡,混合气体中氨气的体积分数随时间的变化如图所示。
NH2CONH2(s)+H2O(g) △H<0并达到平衡,混合气体中氨气的体积分数随时间的变化如图所示。
则A点时v正(CO2)
③下列有关反应2NH3(g)+CO2(g)
 CO(NH2)2(s)+H2O(g)的说法正确的是
CO(NH2)2(s)+H2O(g)的说法正确的是A.分离出少量的尿素,NH3的转化率将增大
B.反应达到平衡时,降低反应体系的温度,CO2的浓度减小
C.NH3的转化率始终等于CO2的转化率
D.加入有效的催化剂能够提高尿素的产率
(2)已知O3氧化氮氧化物的主要反应的热化学方程式如下:
2NO(g)+O2(g)=2NO2(g) △H1=akJ·mol-1
NO(g)+O3(g)=NO2(g)+O2(g) △H2=bkJ·mol-1
6NO2(g)+O3(g)=3N2O5(g) △H3=ckJ·mol-1
则反应4NO2(g)+O2(g)=2N2O5(g)△H=
(3)氮氧化物也可用碱液吸收。若NO和NO2的混合气体被NaOH溶液完全吸收,只生成一种盐,则该盐的化学式为
 NaNO2(aq)+H2O(l)的平衡常数K=
NaNO2(aq)+H2O(l)的平衡常数K=
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐2】(1)铑的配合物离子[Rh(CO)2I2]-可催化甲醇羰基化,反应过程如图所示。

该反应过程的总反应式为:___ 。
(2)用氮化硅(Si3N4)陶瓷代替金属制造发动机的耐热部件,能大幅度提高发动机的热效率。工业上用化学气相沉积法制备氮化硅,在特定温度下其反应为:3SiCl4(g)+2N2(g)+6H2(g) Si3N4(s)+12HCl(g) ΔH<0,一定条件下,在密闭恒容的容器中,上述反应达到化学平衡状态时下列说法一定正确的是(填字母)
Si3N4(s)+12HCl(g) ΔH<0,一定条件下,在密闭恒容的容器中,上述反应达到化学平衡状态时下列说法一定正确的是(填字母)___ 。
a.3v逆(N2)=v正(H2)
b.v正(HCl)=4v正(SiCl4)
c.混合气体密度保持不变
d.c(N2)∶c (H2)∶c (HCl)=1∶3∶6
(3)已知t ℃时,反应FeO(s)+CO(g) Fe(s)+CO2(g)的平衡常数K=0.25。
Fe(s)+CO2(g)的平衡常数K=0.25。
①t ℃时,反应达到平衡时n(CO)∶n(CO2)=___ 。
②若在1 L密闭容器中加入0.020 mol FeO(s)和x mol CO,t ℃时反应达到平衡。此时FeO(s)转化率为50%,则x=___ 。
(4)用Cl2生产某些含氯有机物时会产生副产物HCl。为实现氯的循环利用利用反应A:4HCl+O2 2Cl2+2H2O。对于反应A,如图是4种投料比[n(HCl)∶n(O2)分别为1∶1、2∶1、4∶1和6∶1]下,反应温度对HCl平衡转化率影响的曲线。
2Cl2+2H2O。对于反应A,如图是4种投料比[n(HCl)∶n(O2)分别为1∶1、2∶1、4∶1和6∶1]下,反应温度对HCl平衡转化率影响的曲线。
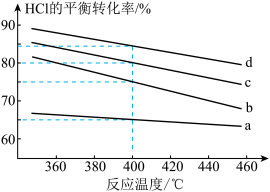
①当曲线b、c、d对应的投料比达到相同的HCl平衡转化率时,对应的反应温度Tb、Tc、Td由大到小的顺序是___ 。
②投料比为2∶1,温度为400℃时,平衡混合气中Cl2的物质的量分数是__ 。

该反应过程的总反应式为:
(2)用氮化硅(Si3N4)陶瓷代替金属制造发动机的耐热部件,能大幅度提高发动机的热效率。工业上用化学气相沉积法制备氮化硅,在特定温度下其反应为:3SiCl4(g)+2N2(g)+6H2(g)
 Si3N4(s)+12HCl(g) ΔH<0,一定条件下,在密闭恒容的容器中,上述反应达到化学平衡状态时下列说法一定正确的是(填字母)
Si3N4(s)+12HCl(g) ΔH<0,一定条件下,在密闭恒容的容器中,上述反应达到化学平衡状态时下列说法一定正确的是(填字母)a.3v逆(N2)=v正(H2)
b.v正(HCl)=4v正(SiCl4)
c.混合气体密度保持不变
d.c(N2)∶c (H2)∶c (HCl)=1∶3∶6
(3)已知t ℃时,反应FeO(s)+CO(g)
 Fe(s)+CO2(g)的平衡常数K=0.25。
Fe(s)+CO2(g)的平衡常数K=0.25。①t ℃时,反应达到平衡时n(CO)∶n(CO2)=
②若在1 L密闭容器中加入0.020 mol FeO(s)和x mol CO,t ℃时反应达到平衡。此时FeO(s)转化率为50%,则x=
(4)用Cl2生产某些含氯有机物时会产生副产物HCl。为实现氯的循环利用利用反应A:4HCl+O2
 2Cl2+2H2O。对于反应A,如图是4种投料比[n(HCl)∶n(O2)分别为1∶1、2∶1、4∶1和6∶1]下,反应温度对HCl平衡转化率影响的曲线。
2Cl2+2H2O。对于反应A,如图是4种投料比[n(HCl)∶n(O2)分别为1∶1、2∶1、4∶1和6∶1]下,反应温度对HCl平衡转化率影响的曲线。
①当曲线b、c、d对应的投料比达到相同的HCl平衡转化率时,对应的反应温度Tb、Tc、Td由大到小的顺序是
②投料比为2∶1,温度为400℃时,平衡混合气中Cl2的物质的量分数是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐3】 资源化利用是实现
资源化利用是实现 减排的首要途径。已知
减排的首要途径。已知 加氢制甲醇的反应体系中,主要反应有
加氢制甲醇的反应体系中,主要反应有
①

②

③

回答下列问题:
(1)有利于反应①自发进行的条件是___________ (填“高温”或“低温”)。
(2)下列说法正确的是___________ (填标号)。
a.高温、低压的条件有利于提高 的转化率
的转化率
b. 加氢制甲醇工艺具有较好的环保、经济效益与工艺前景
加氢制甲醇工艺具有较好的环保、经济效益与工艺前景
c. 和
和 的物质的量相等时,说明该反应体系达到了平衡状态
的物质的量相等时,说明该反应体系达到了平衡状态
d.升温或加压(缩小容器体积)都能增大该反应体系中反应物活化分子百分数,从而加快化学反应速率
(3)在一定条件下,选择合适的催化剂只进行反应②。实验测得,反应速率
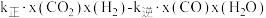 (
( 、
、 分别为正、逆反应速率常数,只与温度有关,x为物质的量分数)。
分别为正、逆反应速率常数,只与温度有关,x为物质的量分数)。
①达到平衡后,仅升高温度, 增大的倍数
增大的倍数___________  (填“>”“<”或“=”)增大的倍数。
(填“>”“<”或“=”)增大的倍数。
②若在密闭容器中通入2mol 和2mol
和2mol  ,在一定温度下达到平衡时,
,在一定温度下达到平衡时, 的平衡转化率为50%,则
的平衡转化率为50%,则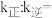
___________ 。
(4)在一定条件下,向体积为2L的密闭容器中通入2.0mol 和6.0mol
和6.0mol  ,
, 和
和 物质的量随时间的变化如图所示,则平衡时CO的浓度为
物质的量随时间的变化如图所示,则平衡时CO的浓度为___________ ,反应①的化学平衡常数是___________ 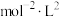 。
。

(5) 还原CO电化学法制备甲醇[
还原CO电化学法制备甲醇[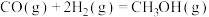 ]的工作原理如图所示。放电时,电流由电极
]的工作原理如图所示。放电时,电流由电极___________ (填“a”或“b”)沿导线流向另一电极。该电池工作时,通入CO一端硫酸溶液的质量变化16g,理论上通过电路转移的电子数为___________ mol。

 资源化利用是实现
资源化利用是实现 减排的首要途径。已知
减排的首要途径。已知 加氢制甲醇的反应体系中,主要反应有
加氢制甲醇的反应体系中,主要反应有①


②


③


回答下列问题:
(1)有利于反应①自发进行的条件是
(2)下列说法正确的是
a.高温、低压的条件有利于提高
 的转化率
的转化率b.
 加氢制甲醇工艺具有较好的环保、经济效益与工艺前景
加氢制甲醇工艺具有较好的环保、经济效益与工艺前景c.
 和
和 的物质的量相等时,说明该反应体系达到了平衡状态
的物质的量相等时,说明该反应体系达到了平衡状态d.升温或加压(缩小容器体积)都能增大该反应体系中反应物活化分子百分数,从而加快化学反应速率
(3)在一定条件下,选择合适的催化剂只进行反应②。实验测得,反应速率

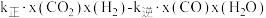 (
( 、
、 分别为正、逆反应速率常数,只与温度有关,x为物质的量分数)。
分别为正、逆反应速率常数,只与温度有关,x为物质的量分数)。①达到平衡后,仅升高温度,
 增大的倍数
增大的倍数 (填“>”“<”或“=”)增大的倍数。
(填“>”“<”或“=”)增大的倍数。②若在密闭容器中通入2mol
 和2mol
和2mol  ,在一定温度下达到平衡时,
,在一定温度下达到平衡时, 的平衡转化率为50%,则
的平衡转化率为50%,则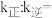
(4)在一定条件下,向体积为2L的密闭容器中通入2.0mol
 和6.0mol
和6.0mol  ,
, 和
和 物质的量随时间的变化如图所示,则平衡时CO的浓度为
物质的量随时间的变化如图所示,则平衡时CO的浓度为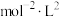 。
。
(5)
 还原CO电化学法制备甲醇[
还原CO电化学法制备甲醇[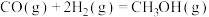 ]的工作原理如图所示。放电时,电流由电极
]的工作原理如图所示。放电时,电流由电极
您最近一年使用:0次



