常温下,用 溶液分别滴定浓度均为
溶液分别滴定浓度均为 的
的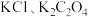 溶液,所得的沉淀溶解平衡图像如图所示(不考虑
溶液,所得的沉淀溶解平衡图像如图所示(不考虑 的水解)。下列叙述正确的是
的水解)。下列叙述正确的是

 溶液分别滴定浓度均为
溶液分别滴定浓度均为 的
的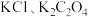 溶液,所得的沉淀溶解平衡图像如图所示(不考虑
溶液,所得的沉淀溶解平衡图像如图所示(不考虑 的水解)。下列叙述正确的是
的水解)。下列叙述正确的是
| A.n点表示AgCl的不饱和溶液 |
B. 的数量级等于 的数量级等于 |
C.向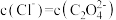 的混合液中滴入 的混合液中滴入 溶液时,先生成 溶液时,先生成 沉淀 沉淀 |
D.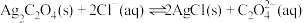 的平衡常数为 的平衡常数为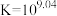 |
更新时间:2023-01-02 15:26:41
|
相似题推荐
多选题
|
较难
(0.4)
名校
【推荐1】298K时,用NaOH溶液分别滴定等物质的量浓度的HR、 、
、 三种溶液。pM[p表示负对数,M表示
三种溶液。pM[p表示负对数,M表示 、
、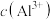 .
. ]随溶液pH变化的关系如图所示。已知:常温下,
]随溶液pH变化的关系如图所示。已知:常温下,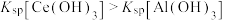 ,当离子浓度
,当离子浓度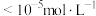 时,该离子完全沉淀。下列推断正确的是
时,该离子完全沉淀。下列推断正确的是
 、
、 三种溶液。pM[p表示负对数,M表示
三种溶液。pM[p表示负对数,M表示 、
、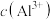 .
. ]随溶液pH变化的关系如图所示。已知:常温下,
]随溶液pH变化的关系如图所示。已知:常温下,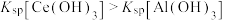 ,当离子浓度
,当离子浓度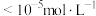 时,该离子完全沉淀。下列推断正确的是
时,该离子完全沉淀。下列推断正确的是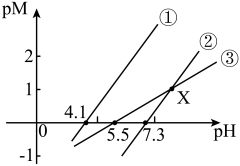
A.①代表滴定 溶液的变化关系 溶液的变化关系 |
B.调节pH=5时,溶液中 完全沉淀 完全沉淀 |
C.滴定HR溶液至X点时,溶液中: |
D.经计算, 不能完全溶于HR溶液 不能完全溶于HR溶液 |
您最近一年使用:0次
多选题
|
较难
(0.4)
【推荐2】已知下表数据:
对含等物质的量的CuSO4、FeSO4、Fe2(SO4)3的混合溶液的说法,不正确的是
物质 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
Ksp(25℃) | 8.0×10-16 | 2.2×10-20 | 4.0×10-38 |
完全沉淀时的pH | 9.6 | 6.4 | 3.4 |
| A.向该混合溶液中逐滴加入NaOH溶液,最先看到红褐色沉淀 |
B.该溶液中c(SO ):[c(Cu2+)+c(Fe2+)+c(Fe3+)]=5:4 ):[c(Cu2+)+c(Fe2+)+c(Fe3+)]=5:4 |
| C.向该溶液中加入适量氯水,并调节pH到3.4后过滤,可获得纯净的CuSO4溶液 |
| D.在pH=5的溶液中Fe3+不能大量存在 |
您最近一年使用:0次
多选题
|
较难
(0.4)
名校
解题方法
【推荐1】25℃时,lgS(CaF2)随pH变化如图所示,下列说法错误的是
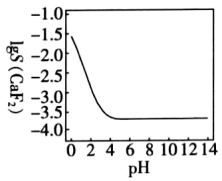
已知:S(CaF2)(单位:mol·L−1)表示CaF2的溶解度。

已知:S(CaF2)(单位:mol·L−1)表示CaF2的溶解度。
| A.CaF2饱和溶液中2c(Ca2+)=c(F-)+c(HF) |
| B.已知Ksp(CaF2)=4×10-11.1,则水中S(CaF2)=10-3.7mol·L-1 |
| C.pH变化时,CaF2溶液中始终存在:c(F-)>c(Ca2+) |
| D.当pH<7时,2c(Ca2+)+c(H+)>c(F-)+c(OH-) |
您最近一年使用:0次
多选题
|
较难
(0.4)
【推荐2】已知常温下Ksp[Mg(OH)2]=3.2×10﹣11、Ksp[Fe(OH)3]=2.7×10﹣39,下列说法正确的是
| A.将10g氢氧化铁粉末加入100mL水中,充分搅拌后仍有固体剩余,静置后上层清液为饱和氢氧化铁溶液,c(OH﹣)=3×10﹣10mol/L |
| B.将10g氢氧化镁粉末加入100mL水中,充分搅拌后仍有固体剩余,静置后上层清液为饱和氢氧化镁溶液,加入酚酞试液后不能变红 |
| C.若1mol/L氯化镁溶液中混有氯化铁,调节pH=9,可以保证镁离子不沉淀而铁离子沉淀完全 |
| D.根据溶度积数据,可以计算出氢氧化铁固体与盐酸反应:Fe(OH)3+3H+⇌Fe3++3H2O的平衡常数为2.7×103 |
您最近一年使用:0次

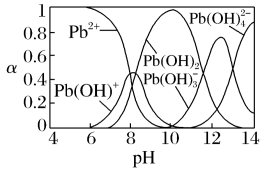
 )>c(OH-)>c(H+)
)>c(OH-)>c(H+) 、Pb(OH)
、Pb(OH) 、OH-和H+
、OH-和H+ ,还含有少量
,还含有少量 及Si、Mg、Fe的氧化物等杂质,现以天青石为原料制备
及Si、Mg、Fe的氧化物等杂质,现以天青石为原料制备 的工艺流程如下:
的工艺流程如下: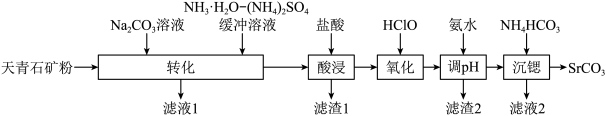
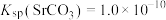 ,
,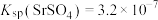
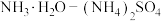 缓冲溶液可使
缓冲溶液可使 转化为
转化为 溶液中,反应后
溶液中,反应后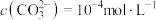 时,
时,

