以绿矾(主要成分为 ,部分
,部分 已被氧化为
已被氧化为 )为原料,生产铁红(
)为原料,生产铁红( )的工艺流程如下:
)的工艺流程如下:
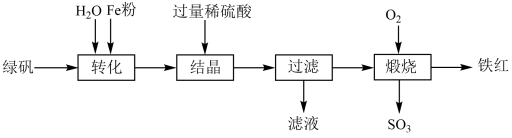
回答下列问题:
(1)“转化”过程中,加入Fe粉的作用是_______ 。“转化”前将绿矾研碎,“转化”中进行搅拌,目的是_______ 。
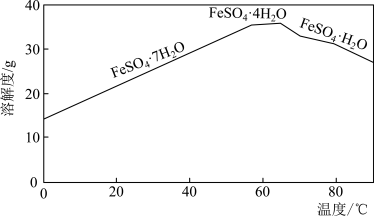
(2)“结晶”时,不同温度下得到的晶体的成分不同(如下图),实验过程中控制温度为75℃左右进行结晶,故得到的晶体的主要成分为_______ (填化学式)。
(3)利用该滤液将工业废水中的 还原为
还原为 ,然后投加石灰乳,使
,然后投加石灰乳,使 转化为
转化为 沉淀,理论上完全反应消耗的
沉淀,理论上完全反应消耗的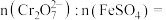
_______ 。
(4)“煅烧”过程中,每生成1mol铁红,需消耗_______ mol ,同时生成
,同时生成_______ mol 和
和_______ mol 。
。
 ,部分
,部分 已被氧化为
已被氧化为 )为原料,生产铁红(
)为原料,生产铁红( )的工艺流程如下:
)的工艺流程如下:
回答下列问题:
(1)“转化”过程中,加入Fe粉的作用是
(2)“结晶”时,不同温度下得到的晶体的成分不同(如下图),实验过程中控制温度为75℃左右进行结晶,故得到的晶体的主要成分为

(3)利用该滤液将工业废水中的
 还原为
还原为 ,然后投加石灰乳,使
,然后投加石灰乳,使 转化为
转化为 沉淀,理论上完全反应消耗的
沉淀,理论上完全反应消耗的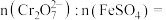
(4)“煅烧”过程中,每生成1mol铁红,需消耗
 ,同时生成
,同时生成 和
和 。
。
更新时间:2023-01-07 22:15:07
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】化工生产中常利用硫酸厂煅烧黄铁矿石的烧渣(主要成分为 及少量
及少量 、
、 等)来制取绿矾
等)来制取绿矾 。具体制备流程如下:
。具体制备流程如下:

回答下列关于上述流程图中转化关系及操作的有关问题:
(1)在“灼烧”过程中发生的主要反应为: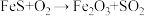 (未配平),该反应中氧化剂与还原剂的物质的量之比为
(未配平),该反应中氧化剂与还原剂的物质的量之比为___________ ,氧化产物是___________ (填化学式)。
(2)足量“气体产物”通入下列溶液中,溶液会褪色的是___________(填字母序号)。
(3)“气体产物”易形成酸雨,酸雨是指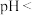
___________ 的雨水。技术员用氨水对“气体产物”进行吸收后再处理,可以回收 ,请你写出用过量氨水吸收
,请你写出用过量氨水吸收 时发生反应的化学方程式
时发生反应的化学方程式___________ 。
(4)加入足量稀硫酸时发生反应的离子方程式为:___________ 。
(5)“滤渣”的主要成分是___________ (填化学式)。
(6)加入足量X时发生反应的离子方程式为:___________ 。
(7)系列操作包括:___________ 、过滤、洗涤、干燥。
(8)绿矾保存不当,容易被氧化变质,为了检验所得产品是否变质,技术人员进行了以下操作:取少量产品(绿矾)置于试管中,加水溶解,向溶液中加入___________ 溶液,发现___________ (填现象),则绿矾已经变质。
 及少量
及少量 、
、 等)来制取绿矾
等)来制取绿矾 。具体制备流程如下:
。具体制备流程如下:
回答下列关于上述流程图中转化关系及操作的有关问题:
(1)在“灼烧”过程中发生的主要反应为:
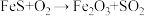 (未配平),该反应中氧化剂与还原剂的物质的量之比为
(未配平),该反应中氧化剂与还原剂的物质的量之比为(2)足量“气体产物”通入下列溶液中,溶液会褪色的是___________(填字母序号)。
| A.品红溶液 | B.紫色石蕊溶液 | C.酸性 溶液 溶液 | D.溴水 |
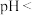
 ,请你写出用过量氨水吸收
,请你写出用过量氨水吸收 时发生反应的化学方程式
时发生反应的化学方程式(4)加入足量稀硫酸时发生反应的离子方程式为:
(5)“滤渣”的主要成分是
(6)加入足量X时发生反应的离子方程式为:
(7)系列操作包括:
(8)绿矾保存不当,容易被氧化变质,为了检验所得产品是否变质,技术人员进行了以下操作:取少量产品(绿矾)置于试管中,加水溶解,向溶液中加入
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】从制造印刷电路板的腐蚀废液(主要含FeCl3、FeCl2、CuCl2)中回收铜,并重新获得FeCl3溶液,处理流程如图所示:
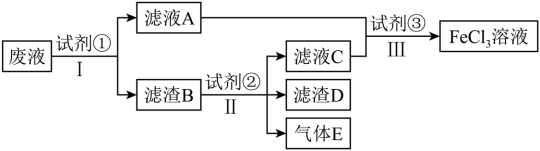
已知试剂①为铁,试剂②为稀盐酸;
则滤渣B的成分为_______ ,若试剂③为氯水,则步骤Ⅲ的离子反应方程式为_______ ,检验废液中 存在的最佳试剂是
存在的最佳试剂是_______ (填化学式),检验时实验现象为_______ 。反应的离子方程式_______ 。

已知试剂①为铁,试剂②为稀盐酸;
则滤渣B的成分为
 存在的最佳试剂是
存在的最佳试剂是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】煤燃烧产生的粉煤灰(主要含有SiO2、Fe2O3、Al2O3等)是火电厂产生的废渣,若不加处理会污染环境。为综合利用,研究人员对其进行如下处理:

(1)滤渣主要成分是________________ ;滤液①中的阳离子为_____________________ 。
(2)滤液①中还加入还原剂原因是________________ ;若加入的还原剂为铁粉,反应的离子方程式为_____________________________________ 。
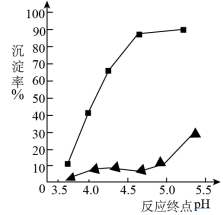
(3)加入氨水是为了调节pH使铝离子沉淀,其离子方程式为_________________ ;反应终点的pH对铝和铁分离效果的影响如右图。根据实验结果,为达到好的分离效果,反应过程中控制pH的范围是__________ ,选择该范围的理由是_________ 。
(4)NH4HSO4和H2SO4按物质的量比1:1混合溶于水配制成浸取液,220℃时可将高铝粉煤灰中Al2O3转化为硫酸铝铵[NH4Al(SO4) 2],然后分离、煅烧获得纯Al2O3。
查阅资料知硫酸铝铵:①溶解度:0℃时,S=5.2g;100℃时,S=421.9g 。②280℃时分解。
①依据资料可知,将硫酸铝铵与其他溶质分离的方法是_____________ 。
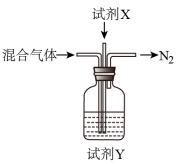
②煅烧NH4Al(SO4) 2时发生4NH4Al(SO4)2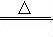 2Al2O3+5SO3↑+3SO2↑+2NH3↑+N2↑+5H2O↑,得到混合气体(NH3、N2、SO2、SO3、H2O )。若16mol混合气体按如下装置被完全吸收制得浸取液。则右下图中,试剂X是
2Al2O3+5SO3↑+3SO2↑+2NH3↑+N2↑+5H2O↑,得到混合气体(NH3、N2、SO2、SO3、H2O )。若16mol混合气体按如下装置被完全吸收制得浸取液。则右下图中,试剂X是___________ (填化学式);试剂Y是_________ (填名称),其中溶质的物质的量为_____________ 。

(1)滤渣主要成分是
(2)滤液①中还加入还原剂原因是
(3)加入氨水是为了调节pH使铝离子沉淀,其离子方程式为

(4)NH4HSO4和H2SO4按物质的量比1:1混合溶于水配制成浸取液,220℃时可将高铝粉煤灰中Al2O3转化为硫酸铝铵[NH4Al(SO4) 2],然后分离、煅烧获得纯Al2O3。
查阅资料知硫酸铝铵:①溶解度:0℃时,S=5.2g;100℃时,S=421.9g 。②280℃时分解。
①依据资料可知,将硫酸铝铵与其他溶质分离的方法是
②煅烧NH4Al(SO4) 2时发生4NH4Al(SO4)2
 2Al2O3+5SO3↑+3SO2↑+2NH3↑+N2↑+5H2O↑,得到混合气体(NH3、N2、SO2、SO3、H2O )。若16mol混合气体按如下装置被完全吸收制得浸取液。则右下图中,试剂X是
2Al2O3+5SO3↑+3SO2↑+2NH3↑+N2↑+5H2O↑,得到混合气体(NH3、N2、SO2、SO3、H2O )。若16mol混合气体按如下装置被完全吸收制得浸取液。则右下图中,试剂X是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】铜转炉烟灰主要含有Zn[还有少量的Fe(+2价)、Pb、Cu、As等元素]的硫酸盐和氧化物,少量为砷酸盐。制备重要化工原料活性氧化锌的工艺流程如图所示。请回答以下问题:
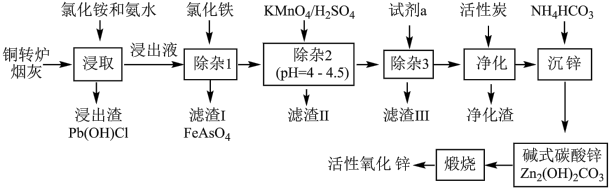
已知:活性炭净化主要是除去有机杂质。
(1)写出氯化铵的电子式___ ,“净化”过程属于___ (填“物理”、“化学”)变化。
(2)在反应温度为50℃,反应时间为1h时,测定各元素的浸出率与氯化铵溶液浓度的关系如图,则氯化铵适宜的浓度为___ mol·L-1。若浸出液中锌元素以[Zn(NH3)4]2+形式存在,则浸取时ZnO发生反应的离子方程式为___ 。

(3)滴加KMnO4溶液有MnO2生成,目的是除___ 元素,除杂3是置换除杂过程,则试剂a是___ ,“滤渣Ⅲ”的主要成分为___ (填化学式)。
(4)写出“沉锌”时发生反应的离子方程式___ ,此过程中可以循环利用的副产品是___ 。
(5)取mg活性氧化锌样品配成待测液,加入指示剂3、4滴,再加入适量六亚甲基四胺,用amol•L-1EDTA标准液进行滴定,消耗标准液VmL。已知:与1.0mLEDTA标准液[c(EDTA)=1.000mol•L-1]相当的以克表示的氧化锌质量为0.08139,则样品中氧化锌的质量分数为___ (用代数式表示)。

已知:活性炭净化主要是除去有机杂质。
(1)写出氯化铵的电子式
(2)在反应温度为50℃,反应时间为1h时,测定各元素的浸出率与氯化铵溶液浓度的关系如图,则氯化铵适宜的浓度为

(3)滴加KMnO4溶液有MnO2生成,目的是除
(4)写出“沉锌”时发生反应的离子方程式
(5)取mg活性氧化锌样品配成待测液,加入指示剂3、4滴,再加入适量六亚甲基四胺,用amol•L-1EDTA标准液进行滴定,消耗标准液VmL。已知:与1.0mLEDTA标准液[c(EDTA)=1.000mol•L-1]相当的以克表示的氧化锌质量为0.08139,则样品中氧化锌的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】浅绿色的硫酸亚铁铵晶体[又名莫尔盐,(NH4)2SO4·FeSO4·6H2O]比绿矾(FeSO4·7H2O)更稳定,常用于定量分析。莫尔盐的一种实验室制法如下:
废铁屑
 溶液A
溶液A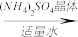

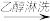 莫尔盐
莫尔盐
(1)向废铁屑中加入稀硫酸后,并不等铁屑完全溶解而是剩余少量时就进行过滤,其目的是___ ;证明溶液A不含Fe3+的最佳试剂是___ (填序号字母)。
A 酚酞溶液 B KSCN溶液
C 烧碱溶液 D KMnO4溶液
操作Ⅰ的步骤是:加热蒸发、___ 、过滤。
(2)操作Ⅰ得到的莫尔盐晶体用少量乙醇淋洗,其目的是:①除去晶体表面附着的硫酸、水等杂质②______ 。
(3)用托盘天平称量(NH4)2SO4晶体,晶体要放在天平___ (填“左”或“右”)盘。
(4)从下列装置中选取必要的装置制取(NH4)2SO4溶液,连接的顺序(用接口序号字母表示)是:a接___ ;__ 接___ 。

将装置C中两种液体分离开的操作名称是____ 。装置D的作用是__ 。
废铁屑
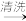
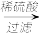 溶液A
溶液A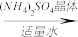

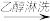 莫尔盐
莫尔盐(1)向废铁屑中加入稀硫酸后,并不等铁屑完全溶解而是剩余少量时就进行过滤,其目的是
A 酚酞溶液 B KSCN溶液
C 烧碱溶液 D KMnO4溶液
操作Ⅰ的步骤是:加热蒸发、
(2)操作Ⅰ得到的莫尔盐晶体用少量乙醇淋洗,其目的是:①除去晶体表面附着的硫酸、水等杂质②
(3)用托盘天平称量(NH4)2SO4晶体,晶体要放在天平
(4)从下列装置中选取必要的装置制取(NH4)2SO4溶液,连接的顺序(用接口序号字母表示)是:a接

将装置C中两种液体分离开的操作名称是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】用氯化铁浸出一重铬酸钾(K2Cr2O7)滴定法测定钛精粉试样中单质铁的质量分数[ω(Fe)%],实验步骤如下:
步骤1:称取试样0.100g于250mL洗净的锥形瓶中。
步骤2:加入FeCl3溶液100mL,迅速塞上胶塞,用电磁搅拌器搅拌30min。
步骤3:过滤,用水洗涤锥形瓶和滤渣各3~4次,洗液全部并入滤液中。
步骤4:将滤液稀释至500mL,再移取100mL稀释液于锥形瓶中,加入20mL硫酸和磷酸的混合酸,加0.5%二苯胺磺酸钠指示剂4滴。
步骤5:以K2Cr2O7标准溶液滴定至出现明显紫色为终点。发生的反应:Cr2O +6Fe2++14H+=2Cr3++6Fe3++7H2O。
+6Fe2++14H+=2Cr3++6Fe3++7H2O。
步骤6:重复测定两次。
步骤7:数据处理。
(1)步骤2中加入FeCl3溶液后锥形瓶中发生反应的离子方程式为_______ ,迅速塞上胶塞的原因是_______ 。
(2)步骤3中判断滤纸上残渣已洗净的方法是_______ 。
(3)实验中需用到100mL浓度约为0.01mol·L-1K2Cr2O7标准溶液,配制时用到的玻璃仪器有_______ 。称量K2Cr2O7固体前应先将其烘干至恒重,若未烘干,对测定结果的影响是_______ (填“偏高”、“偏低”或“无影响”);滴定时,K2Cr2O7溶液应置于_______ (填仪器名称)中。
步骤1:称取试样0.100g于250mL洗净的锥形瓶中。
步骤2:加入FeCl3溶液100mL,迅速塞上胶塞,用电磁搅拌器搅拌30min。
步骤3:过滤,用水洗涤锥形瓶和滤渣各3~4次,洗液全部并入滤液中。
步骤4:将滤液稀释至500mL,再移取100mL稀释液于锥形瓶中,加入20mL硫酸和磷酸的混合酸,加0.5%二苯胺磺酸钠指示剂4滴。
步骤5:以K2Cr2O7标准溶液滴定至出现明显紫色为终点。发生的反应:Cr2O
 +6Fe2++14H+=2Cr3++6Fe3++7H2O。
+6Fe2++14H+=2Cr3++6Fe3++7H2O。步骤6:重复测定两次。
步骤7:数据处理。
(1)步骤2中加入FeCl3溶液后锥形瓶中发生反应的离子方程式为
(2)步骤3中判断滤纸上残渣已洗净的方法是
(3)实验中需用到100mL浓度约为0.01mol·L-1K2Cr2O7标准溶液,配制时用到的玻璃仪器有
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】某同学在用稀硫酸与锌反应制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。
(1)硫酸铜溶液可以加快氢气生成速率的原因是____ 。
(2)25℃,该同学设计三个实验探究影响锌粉(足量)与稀硫酸反应速率的因素,有关数据如下表所示:
①本实验待测数据可以是____ 。
②利用实验I和实验I来探究硫酸浓度对锌粉与稀硫酸反应速率的影响,Vx=__ ,理由是__ 。
③实验I和实验III的目的是__ 。
(3)用排水集气法收集实验I反应放出的氢气(气体体积已折合成标准状况),实验记录如表(累计值):
①反应速率最大时间段是__ min(填“0~1”、“1~2”、“2~3”、“3~4”、“4~5”或“5~6”下同),原因是____ 。
②反应速率最小时段是__ min,原因是___ 。
③第2~3min时间段以稀硫酸的浓度表示的该反应速率(设溶液体积不变)是v(H2SO4)=___ 。
(4)如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,在稀硫酸中分别加入等体积的下列溶液,可行的是____ (填字母)。
A.KNO3溶液 B.蒸馏水 C.Na2SO4溶液 D.Na2CO3溶液
(1)硫酸铜溶液可以加快氢气生成速率的原因是
(2)25℃,该同学设计三个实验探究影响锌粉(足量)与稀硫酸反应速率的因素,有关数据如下表所示:
| 实验序号 | 体积/mL | ||
| 1.0mol·L-1硫酸溶液 | 饱和CuSO4溶液 | 水 | |
I | 30.0 | 1.0 | 9.0 |
II | 20.0 | 1.0 | Vx |
III | 30.0 | 3.0 | 7.0 |
①本实验待测数据可以是
②利用实验I和实验I来探究硫酸浓度对锌粉与稀硫酸反应速率的影响,Vx=
③实验I和实验III的目的是
(3)用排水集气法收集实验I反应放出的氢气(气体体积已折合成标准状况),实验记录如表(累计值):
| 时间/min | 1 | 2 | 3 | 4 | 5 | 6 |
| 氢气体积/mL | 60 | 140 | 252 | 420 | 510 | 540 |
①反应速率最大时间段是
②反应速率最小时段是
③第2~3min时间段以稀硫酸的浓度表示的该反应速率(设溶液体积不变)是v(H2SO4)=
(4)如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,在稀硫酸中分别加入等体积的下列溶液,可行的是
A.KNO3溶液 B.蒸馏水 C.Na2SO4溶液 D.Na2CO3溶液
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】碲被誉为现代工业的维生素,某工艺从精炼铜的阳极泥(主要含有Cu2Te,还有Au、Ag、SiO2等)中分别回收碲和重金属的流程如下图所示:
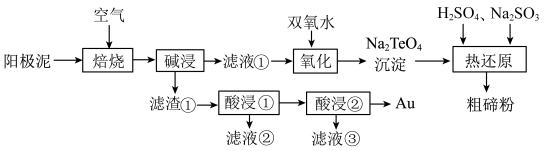
已知:“焙烧”后,碲主要以TeO2形式存在,TeO2溶于强碱生成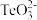 。
。
(1)基态Te原子的价电子排布式为___________ 。
(2)“焙烧”时气体与固体原料逆流而行,目的是___________ ;“滤液①”中 的成分为___________ (填化学式)。
(3)“氧化”步骤中,双氧水需分批加入的目的是___________ 。
(4)写出“热还原”时发生反应的化学方程式___________ 。
(5)滤渣①中含CuO、Au和Ag,“酸浸①”可用________ 浸取(填选项,下同),“酸浸②”可用______ 浸取。
A.王水 B.稀硝酸 C.浓氢氧化钠溶液 D.稀硫酸
(6)粗碲粉中碲质量分数的测定步骤如下:取mg粗碲粉,加入酸使其转化为亚碲酸(H2TeO3),配制成100mL 溶液,取25.00mL 于锥形瓶中。向锥形瓶中加入V1mLc1mol·L-1酸性K2Cr2O7溶液,充分反应使亚碲酸转化为原碲酸(H6TeO6)。用c2mol·L-1硫酸亚铁铵[ (NH4)2 Fe(SO4)2 ]标准溶液滴定剩余的酸性K2Cr2O7溶液,消耗V2mL硫酸亚铁铵标准溶液。该粗碲粉中碲的质量分数为___________ 。

已知:“焙烧”后,碲主要以TeO2形式存在,TeO2溶于强碱生成
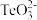 。
。(1)基态Te原子的价电子排布式为
(2)“焙烧”时气体与固体原料逆流而行,目的是
(3)“氧化”步骤中,双氧水需分批加入的目的是
(4)写出“热还原”时发生反应的化学方程式
(5)滤渣①中含CuO、Au和Ag,“酸浸①”可用
A.王水 B.稀硝酸 C.浓氢氧化钠溶液 D.稀硫酸
(6)粗碲粉中碲质量分数的测定步骤如下:取mg粗碲粉,加入酸使其转化为亚碲酸(H2TeO3),配制成100mL 溶液,取25.00mL 于锥形瓶中。向锥形瓶中加入V1mLc1mol·L-1酸性K2Cr2O7溶液,充分反应使亚碲酸转化为原碲酸(H6TeO6)。用c2mol·L-1硫酸亚铁铵[ (NH4)2 Fe(SO4)2 ]标准溶液滴定剩余的酸性K2Cr2O7溶液,消耗V2mL硫酸亚铁铵标准溶液。该粗碲粉中碲的质量分数为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】ZnO有优异的常温发光性能,在半导体领域的液晶显示器、薄膜晶体管、发光二极管等产品中均有应用。工业上利用锌焙砂(主要成分为ZnO、ZnFe2O4,还含有Fe3O4、Al2O3、SiO2等)制取氧化锌的工艺流程如图所示:
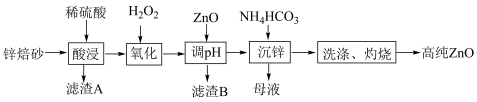
已知:相关金属离子c(Mn+)=0.1mol·L-1生成氢氧化物沉淀的pH如下表所示:
回答下列问题:
(1)“酸浸”时为了提高浸取速率,可以采取的措施是________ (任写一种)。
(2)“氧化”步骤中发生的离子方程式为________ ,H2O2的实际用量比理论用量要大,原因是___________ 。
(3)滤渣B的主要成分为________ ;加ZnO时,为了不生成Zn(OH)2,该步骤需要控制溶液pH的范围是_______ 。
(4)“沉锌”反应中,往滤液加入NH4HCO3溶液,生成ZnCO3·Zn(OH)2及CO2,写出相应的离子方程式_______ 。“沉锌”后的母液可进一步处理,获得一种化工原料,写出该原料在生产中的一种用途________ 。

已知:相关金属离子c(Mn+)=0.1mol·L-1生成氢氧化物沉淀的pH如下表所示:
| Fe2+ | Fe3+ | Al3+ | Zn2+ | |
| 开始沉淀 | 6.5 | 2.7 | 3.4 | 6.5 |
| 沉淀完全 | 9.7 | 3.7 | 4.7 | 8.5 |
(1)“酸浸”时为了提高浸取速率,可以采取的措施是
(2)“氧化”步骤中发生的离子方程式为
(3)滤渣B的主要成分为
(4)“沉锌”反应中,往滤液加入NH4HCO3溶液,生成ZnCO3·Zn(OH)2及CO2,写出相应的离子方程式
您最近一年使用:0次



