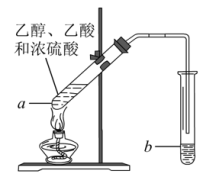
红葡萄酒密封储存时间越长,质量越好,原因之一是储存过程中生成了有香味的酯。在实验室也可以用如图所示的装置制取乙酸乙酯,请回答下列问题:
(1)乙醇分子中官能团的名称是_______ 。
(2)试管a中加入几块碎瓷片的目的是_______ 。
(3)试管a中发生反应的化学方程式为_______ 。
(4)反应开始前,试管b中盛放的是_______ 溶液,其作用为_______ 、_______ 、_______ 。
(5)可用_______ 的方法把制得的乙酸乙酯分离出来。

(1)乙醇分子中官能团的名称是
(2)试管a中加入几块碎瓷片的目的是
(3)试管a中发生反应的化学方程式为
(4)反应开始前,试管b中盛放的是
(5)可用
更新时间:2023-01-09 21:03:59
|
相似题推荐
解答题-有机推断题
|
适中
(0.65)
名校
【推荐1】高分子化合物V: 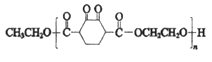 是人造棉的主要成分之一,合成路线如下:
是人造棉的主要成分之一,合成路线如下:
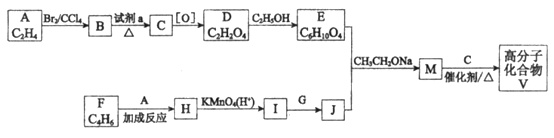
已知:

(R、R1、R2、R3表示烃基)
(1)试剂a是____________________________ 。
(2)F与A以物质的量之比1:1发生反应生成六元环状化合物H,H的结构简式是________________ 。
(3)I的结构简式是____________ 。
(4)G中所含官能团是________________ ;M的结构简式是____________ 。
(5)M与C反应生成V的化学方程式为____________ 。
(6)E的同分异构体N也可以和J反应生成M,N可能的结构简式为____________ (写一种)。
 是人造棉的主要成分之一,合成路线如下:
是人造棉的主要成分之一,合成路线如下:
已知:

(R、R1、R2、R3表示烃基)
(1)试剂a是
(2)F与A以物质的量之比1:1发生反应生成六元环状化合物H,H的结构简式是
(3)I的结构简式是
(4)G中所含官能团是
(5)M与C反应生成V的化学方程式为
(6)E的同分异构体N也可以和J反应生成M,N可能的结构简式为
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
【推荐2】(B)有机化学基础
(1)有机物所含官能团对其性质影响显著
① 下列有机物能使酸性KMnO4褪色的是__________ (填字母)。
a.甲烷 b.乙烯 c.苯
② 区分甲苯和苯酚,不可用的试剂是__________ (填字母)。
a.FeCl3 溶液 b.酸性KMnO4溶液 c.溴水
③ 除去乙酸乙酯中的乙酸,可用的试剂是____________ (填字母)。
a.NaOH溶液 b.饱和Na2CO3溶液 c.NaCl溶液
④ 下列物质能发生银镜反应的是___________ (填字母)。
a.乙醇 b.乙醛 c.乙酸
⑤ 下列物质不能发生水解反应的是____________ (填字母)。
a.葡萄糖 b.纤维素 c.蔗糖
(2)金银花的有效成分为绿原酸,具有广泛的杀菌、消炎功能,其结构简式见右图。
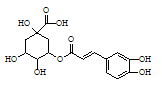
① 绿原酸分子式为______________ 。
② 绿原酸分子中有_________ 个手性碳原子。
③ 绿原酸含有羟基、__________ 、__________ (填含氧官能团名称)。
④ 每摩尔绿原酸最多与__________ mol NaOH反应。
(3)非诺洛芬是一种治疗类风湿性关节炎的药物,可通过以下方法合成:
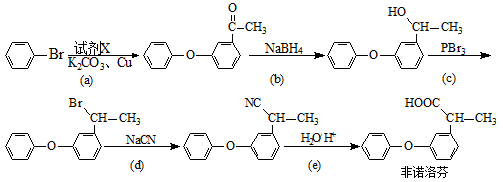
① 反应中加入的试剂X的分子式为C8H8O2,X的结构简式为_____________ 。
② 上述反应中,属于取代反应的是__________ ,属于还原反应的是___________ 。(填字母)
③ 非诺洛芬的一种同分异构体满足下列条件,写出该异构体的结构简式:___________ 。
Ⅰ.不能与FeCl3发生显色反应,但其一种水解产物能与FeCl3发生显色反应。
Ⅱ.分子中有3种不同化学环境的氢,且分子中含有两个苯环。
(1)有机物所含官能团对其性质影响显著
① 下列有机物能使酸性KMnO4褪色的是
a.甲烷 b.乙烯 c.苯
② 区分甲苯和苯酚,不可用的试剂是
a.FeCl3 溶液 b.酸性KMnO4溶液 c.溴水
③ 除去乙酸乙酯中的乙酸,可用的试剂是
a.NaOH溶液 b.饱和Na2CO3溶液 c.NaCl溶液
④ 下列物质能发生银镜反应的是
a.乙醇 b.乙醛 c.乙酸
⑤ 下列物质不能发生水解反应的是
a.葡萄糖 b.纤维素 c.蔗糖
(2)金银花的有效成分为绿原酸,具有广泛的杀菌、消炎功能,其结构简式见右图。

① 绿原酸分子式为
② 绿原酸分子中有
③ 绿原酸含有羟基、
④ 每摩尔绿原酸最多与
(3)非诺洛芬是一种治疗类风湿性关节炎的药物,可通过以下方法合成:

① 反应中加入的试剂X的分子式为C8H8O2,X的结构简式为
② 上述反应中,属于取代反应的是
③ 非诺洛芬的一种同分异构体满足下列条件,写出该异构体的结构简式:
Ⅰ.不能与FeCl3发生显色反应,但其一种水解产物能与FeCl3发生显色反应。
Ⅱ.分子中有3种不同化学环境的氢,且分子中含有两个苯环。
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
【推荐3】某种非天然氨基酸Z合成路线如图所示(Ph-表示苯基):
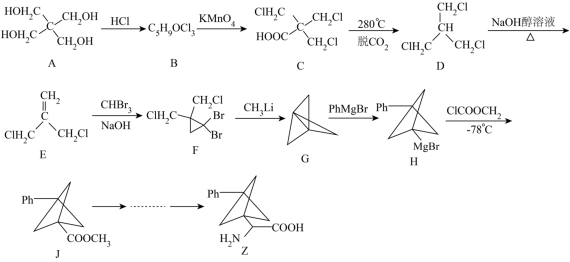
已知: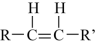

请回答下列问题:
(1)物质B的结构简式为_______ ;E所含官能团名称为_______ ;物质Z的分子式为_______ 。
(2)B →C 的反应类型为_______ ;D→E反应的化学方程式为_______ 。
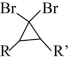
(3)符合下列条件的J物质的同分异构体的结构简式为_______ (写出一种即可)。
①包含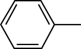 ;②
;② (双键两端的C不再连接H)片段;③除②中片段外只含有1个-CH2-。
(双键两端的C不再连接H)片段;③除②中片段外只含有1个-CH2-。
(4)已知: RMgBr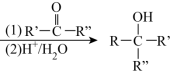 (R'、R"均表示H或烃基),试用化合物G、PhMgBr、甲醛为原料,设计
(R'、R"均表示H或烃基),试用化合物G、PhMgBr、甲醛为原料,设计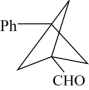 的合成路线(用流程图表示,无机试剂任选):
的合成路线(用流程图表示,无机试剂任选):_______ 。

已知:
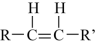


请回答下列问题:
(1)物质B的结构简式为
(2)B →C 的反应类型为
(3)符合下列条件的J物质的同分异构体的结构简式为
①包含
 ;②
;② (双键两端的C不再连接H)片段;③除②中片段外只含有1个-CH2-。
(双键两端的C不再连接H)片段;③除②中片段外只含有1个-CH2-。(4)已知: RMgBr
 (R'、R"均表示H或烃基),试用化合物G、PhMgBr、甲醛为原料,设计
(R'、R"均表示H或烃基),试用化合物G、PhMgBr、甲醛为原料,设计 的合成路线(用流程图表示,无机试剂任选):
的合成路线(用流程图表示,无机试剂任选):
您最近一年使用:0次
【推荐1】淀粉是一种多糖,以淀粉为主要原料合成一种具有果香味的物质C和化合物D的合成路线如图所示。
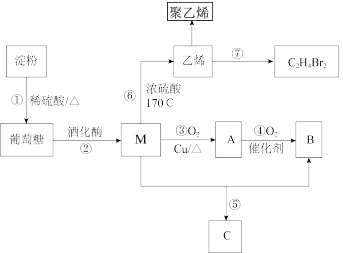
(1)葡萄糖的结构简式为____ 。
(2)M中的官能团的名称为____ ,⑦的反应类型是____ 。
(3)③的化学方程式是____ 。
(4)聚乙烯和聚丙烯都是生产塑料的合成树脂,写出由丙烯制备聚丙烯的化学方程式:____ 。
(5)⑤的化学方程式是____ 。
(6)C是一种油状、有香味的物质,实验室制取C的装置如图所示。
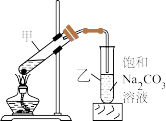
试管乙中饱和Na2CO3溶液的作用是____ 。

(1)葡萄糖的结构简式为
(2)M中的官能团的名称为
(3)③的化学方程式是
(4)聚乙烯和聚丙烯都是生产塑料的合成树脂,写出由丙烯制备聚丙烯的化学方程式:
(5)⑤的化学方程式是
(6)C是一种油状、有香味的物质,实验室制取C的装置如图所示。

试管乙中饱和Na2CO3溶液的作用是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】已知下列数据:
学生在实验室制取乙酸乙酯的主要步骤如下:
①在30mL的大试管A中按体积比1∶4∶4的比例配制浓硫酸、乙醇和乙酸的混合溶液;
②按下图连接好装置,用小火均匀地加热装有混合溶液的大试管5~10min;
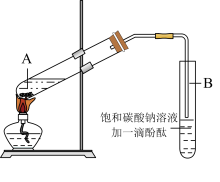
③待试管B收集到一定量的产物后停止加热,撤去试管B并用力振荡,然后静置待分层;
④分离出乙酸乙酯层、洗涤、干燥。请根据题目要求回答下列问题:
(1)配制该混合溶液的主要操作步骤为___ 。
(2)上述实验中饱和碳酸钠溶液的作用是(填字母)__ 。
A. 中和乙酸和乙醇
B. 中和乙酸并吸收部分乙醇
C. 加速酯的生成,提高其产率
D. 乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中更小,有利于分层析出
(3)步骤②中需要小火均匀加热操作,其主要理由是__ 。
(4)分离出乙酸乙酯后,为了干燥乙酸乙酯可选用的干燥剂为(填字母)__ 。
A. P2O5 B. 无水Na2SO4 C. 碱石灰 D. NaOH固体
| 物质 | 熔点(℃) | 沸点(℃) | 密度(g·cm-3) |
| 乙醇 | -117.0 | 78.0 | 0.79 |
| 乙酸 | 16.6 | 117.9 | 1.05 |
| 乙酸乙酯 | -83.6 | 77.5 | 0.90 |
| 浓硫酸(98%) | — | 338.0 | 1.84 |
①在30mL的大试管A中按体积比1∶4∶4的比例配制浓硫酸、乙醇和乙酸的混合溶液;
②按下图连接好装置,用小火均匀地加热装有混合溶液的大试管5~10min;

③待试管B收集到一定量的产物后停止加热,撤去试管B并用力振荡,然后静置待分层;
④分离出乙酸乙酯层、洗涤、干燥。请根据题目要求回答下列问题:
(1)配制该混合溶液的主要操作步骤为
(2)上述实验中饱和碳酸钠溶液的作用是(填字母)
A. 中和乙酸和乙醇
B. 中和乙酸并吸收部分乙醇
C. 加速酯的生成,提高其产率
D. 乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中更小,有利于分层析出
(3)步骤②中需要小火均匀加热操作,其主要理由是
(4)分离出乙酸乙酯后,为了干燥乙酸乙酯可选用的干燥剂为(填字母)
A. P2O5 B. 无水Na2SO4 C. 碱石灰 D. NaOH固体
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】Ⅰ.为研究海水提溴工艺,甲、乙两同学分别设计了如下实验流程;
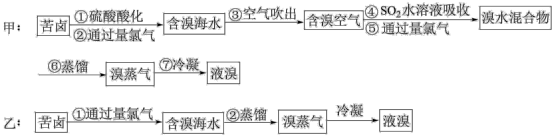
(1)甲同学步骤④所发生反应的离子方程式为___________ 。
(2)对比甲、乙两流程,最大的区别在于对含溴海水的处理方法不同,其中符合工业生产要求的是___________ (填“甲”或“乙”),理由是___________ 。
Ⅱ.如图是乙酸乙酯的绿色合成路线之一:
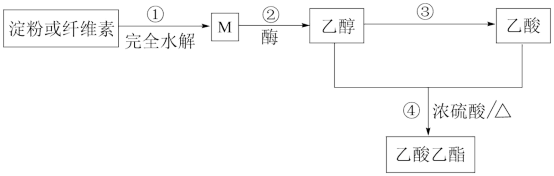
(1)M的分子式为___________ 。
(2)下列说法不正确的是___________ (填字母)
A.淀粉和纤维素都属于天然高分子化合物
B.M可与新制的氢氧化铜在加热条件下反应生成砖红色沉淀
C.所有的糖类都有甜味,都可以发生水解反应
D.用饱和碳酸钠溶液可以鉴别乙醇、乙酸和乙酸乙酯
(3)乙醇和乙酸在一定条件下制备乙酸乙酯。
①乙酸中官能团的名称是___________ 。
②生成乙酸乙酯的反应是可逆反应,下列能说明该反应已达到化学平衡状态的是___________ (填字母)。
A.单位时间里,生成1mol乙酸乙酯,同时生成1mol水
B.单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸
C.单位时间里,消耗1mol乙醇,同时消耗1mol乙酸
D.正反应的速率与逆反应的速率相等
E.混合物中各物质的物质的量相等

(1)甲同学步骤④所发生反应的离子方程式为
(2)对比甲、乙两流程,最大的区别在于对含溴海水的处理方法不同,其中符合工业生产要求的是
Ⅱ.如图是乙酸乙酯的绿色合成路线之一:

(1)M的分子式为
(2)下列说法不正确的是
A.淀粉和纤维素都属于天然高分子化合物
B.M可与新制的氢氧化铜在加热条件下反应生成砖红色沉淀
C.所有的糖类都有甜味,都可以发生水解反应
D.用饱和碳酸钠溶液可以鉴别乙醇、乙酸和乙酸乙酯
(3)乙醇和乙酸在一定条件下制备乙酸乙酯。
①乙酸中官能团的名称是
②生成乙酸乙酯的反应是可逆反应,下列能说明该反应已达到化学平衡状态的是
A.单位时间里,生成1mol乙酸乙酯,同时生成1mol水
B.单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸
C.单位时间里,消耗1mol乙醇,同时消耗1mol乙酸
D.正反应的速率与逆反应的速率相等
E.混合物中各物质的物质的量相等
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】实验室制取乙酸乙酯的主要步骤如下:
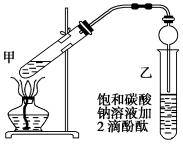
①在甲试管(如图)中加入2 mL浓硫酸、3 mL乙醇和2 mL乙酸的混合溶液。
②按图连接好装置(装置气密性良好)并加入混合液,用小火均匀地加热3~5 min。
③待试管乙收集到一定量产物后停止加热,撤出试管乙,并用力振荡,然后静置待分层。
④分离出乙酸乙酯层,洗涤、干燥。
(1)配制该混合溶液的主要操作步骤为_______ ;反应中浓硫酸的作用是_______ 。
(2)试管甲中发生反应的化学方程式为_______ 。
(3)上述实验中饱和碳酸钠溶液的作用是(填字母)_______。
(4)欲将乙试管中的物质分离开以得到乙酸乙酯,必须使用的仪器有_______ ;分离时,乙酸乙酯应该从仪器_______ (填“下口放出”或“上口倒出”)。

①在甲试管(如图)中加入2 mL浓硫酸、3 mL乙醇和2 mL乙酸的混合溶液。
②按图连接好装置(装置气密性良好)并加入混合液,用小火均匀地加热3~5 min。
③待试管乙收集到一定量产物后停止加热,撤出试管乙,并用力振荡,然后静置待分层。
④分离出乙酸乙酯层,洗涤、干燥。
(1)配制该混合溶液的主要操作步骤为
(2)试管甲中发生反应的化学方程式为
(3)上述实验中饱和碳酸钠溶液的作用是(填字母)_______。
| A.中和乙酸和乙醇 |
| B.中和乙酸并吸收部分乙醇 |
| C.乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中更小,有利于分层析出 |
| D.加速酯的生成,提高其产率 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】实验室用乳酸与异戊醇反应制备乳酸异戊酯,有关数据和装置示意图如下: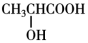 +
+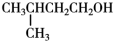

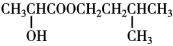 +H2O
+H2O
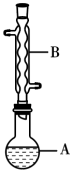
实验步骤:
①如图连接好装置,在A中加入9g乳酸和17.6g异戊醇、数滴浓硫酸和2~3片碎瓷片开始缓慢加热A。
②回流1h,反应液冷却至室温后,倒入分液漏斗中,先水洗,再用饱和碳酸钠溶液洗涤至中性,最后用饱和食盐水和水洗涤,分出的产物加入少量无水硫酸镁固体,静置片刻。
③过滤除去硫酸镁固体,进行蒸馏纯化,收集200~203℃馏分,得乳酸异戊酯13.6g。
回答下列问题:
(1)图中A仪器的名称是__________ ,B仪器的作用是__________ 。
(2)在该实验中,A的容积最适合的是__________ (填入正确选项前的字母)。
A.150mL B.100mL C.50mL
(3)分离提纯过程中加入无水硫酸镁的目的是__________ 。
(4)在蒸馏纯化过程中,下列说法错误的是__________。
(5)本实验的产率是__________ 。
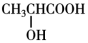 +
+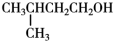

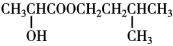 +H2O
+H2O| 相对分子质量 | 密度/(g/cm3) | 沸点/℃ | 水中溶解度 | |
| 乳酸 | 90 | 1.209 | 122 | 溶 |
| 异戊醇 | 88 | 0.8123 | 131 | 微溶 |
| 乳酸异戊酯 | 160 | 0.96 | 202 | 不溶 |

实验步骤:
①如图连接好装置,在A中加入9g乳酸和17.6g异戊醇、数滴浓硫酸和2~3片碎瓷片开始缓慢加热A。
②回流1h,反应液冷却至室温后,倒入分液漏斗中,先水洗,再用饱和碳酸钠溶液洗涤至中性,最后用饱和食盐水和水洗涤,分出的产物加入少量无水硫酸镁固体,静置片刻。
③过滤除去硫酸镁固体,进行蒸馏纯化,收集200~203℃馏分,得乳酸异戊酯13.6g。
回答下列问题:
(1)图中A仪器的名称是
(2)在该实验中,A的容积最适合的是
A.150mL B.100mL C.50mL
(3)分离提纯过程中加入无水硫酸镁的目的是
(4)在蒸馏纯化过程中,下列说法错误的是__________。
| A.温度计应该插入液面以下 |
| B.加热一段时间后发现忘记加瓷片,应该冷却后补加 |
| C.冷却水的方向是上进下出,保证冷却水快速流动 |
| D.蒸馏时用到的主要玻璃仪器有:酒精灯、蒸馏烧瓶、冷凝管、温度计、牛角管、锥形瓶 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】如下图是乙酸乙酯的合成路线图,已知B的水溶液可以溶解 ,E可作果实催熟剂。
,E可作果实催熟剂。
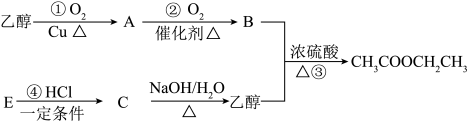
请完成下列问题:
(1)B中所含官能团的名称是___________ ,E的结构简式为:___________ ;反应④的反应类型是___________ 。
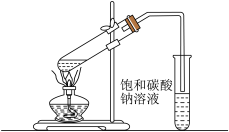
(2)实验室我们可以用如图所示的装置制取乙酸乙酯。回答下列问题。
①写出制取乙酸乙酯的化学反应方程式:___________ ;
②试剂B、乙醇和浓硫酸的添加顺序为:___________ :
③装置中导管要在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是___________ ;
④如果用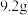 的乙醇和
的乙醇和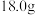 的B反应制得乙酸乙酯
的B反应制得乙酸乙酯 ,则本实验的产率是
,则本实验的产率是___________ ;(产率指的是某种生成物的实际产量与理论产量的比值)。
 ,E可作果实催熟剂。
,E可作果实催熟剂。
请完成下列问题:
(1)B中所含官能团的名称是
(2)实验室我们可以用如图所示的装置制取乙酸乙酯。回答下列问题。

①写出制取乙酸乙酯的化学反应方程式:
②试剂B、乙醇和浓硫酸的添加顺序为:
③装置中导管要在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是
④如果用
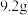 的乙醇和
的乙醇和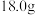 的B反应制得乙酸乙酯
的B反应制得乙酸乙酯 ,则本实验的产率是
,则本实验的产率是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
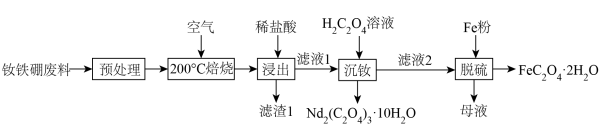
【推荐1】钕铁硼废料是一种具有较高经济价值的废弃物,主要成分为稀土元素钕(Nd)、Fe、B.一种采用分步沉淀从钕铁硼油泥中回收Nd2(C2O4)3·10H2O和FeC2O4·2H2O的工艺流程如图:
②H2CO4易与Fe3+形成多种配合物离子,易与Fe2+形成FeC2O4·2H2O沉淀。
回答下列问题:
(1)“预处理”是洗去钕铁硼表面的油污,可选择___________ (填化学式)溶液。
(2)“滤渣1”的主要成分是___________ (填名称)。“浸出”时,盐酸浓度和液固比对钕、铁的浸出率影响如图所示,则浸出过程的最佳条件是___________ 。___________ 。
(4)“沉铁”时,加入铁粉的作用是___________ 。
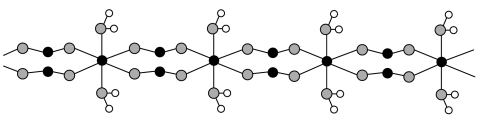
(5)FeC2O4·2H2O晶体结构片段如图所示。___________ ;碳原子采用___________ 杂化。现测定草酸亚铁晶体纯度。准确称取Wg样品于锥形瓶,加入适量的稀硫酸,用cmol·L-1KMnO4溶液滴定至终点,消耗KMnO4溶液bmL。滴定反应: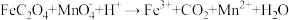 (未配平)。该样品纯度为
(未配平)。该样品纯度为___________ %。
②H2CO4易与Fe3+形成多种配合物离子,易与Fe2+形成FeC2O4·2H2O沉淀。
回答下列问题:
(1)“预处理”是洗去钕铁硼表面的油污,可选择
(2)“滤渣1”的主要成分是
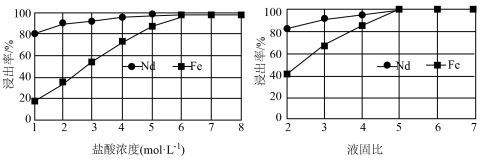
(4)“沉铁”时,加入铁粉的作用是
(5)FeC2O4·2H2O晶体结构片段如图所示。
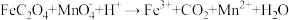 (未配平)。该样品纯度为
(未配平)。该样品纯度为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
真题
解题方法
【推荐2】由黄铜矿(主要成分是CuFeS2)炼制精铜的工艺流程示意图如下:

(1)在反射炉中,把铜精矿砂和石英砂混合加热到1000°C左右,黄铜矿与空气反应生成Cu和Fe的低价硫化物,且部分Fe的硫化物转变为低价氧化物,该过程中两个主要反应的化学方程式分别是_______ ,
_______ 反射炉内生成炉渣的主要成分是________ ;
(2)冰铜(Cu2S和FeS互相熔合而成)含Cu量为20%~50%。转炉中,将冰铜加熔剂(石英砂)在1200°C左右吹入空气进行吹炼。冰铜中的Cu2S被氧化成Cu2O,生成的Cu2O与Cu2S反应,生成含Cu量约为98.5%的粗铜,该过程发生反应的化学方程式分别是________ 、________ ;
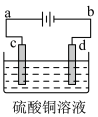
(3)粗铜的电解精炼如图所示。在粗铜的电解过程中,粗铜板应是图中电极 (填图中的字母);在电极d上发生的电极反应式为_______ ;若粗铜中还含有Au、Ag、Fe,它们在电解槽中的存在形式和位置为______ 。

(1)在反射炉中,把铜精矿砂和石英砂混合加热到1000°C左右,黄铜矿与空气反应生成Cu和Fe的低价硫化物,且部分Fe的硫化物转变为低价氧化物,该过程中两个主要反应的化学方程式分别是
(2)冰铜(Cu2S和FeS互相熔合而成)含Cu量为20%~50%。转炉中,将冰铜加熔剂(石英砂)在1200°C左右吹入空气进行吹炼。冰铜中的Cu2S被氧化成Cu2O,生成的Cu2O与Cu2S反应,生成含Cu量约为98.5%的粗铜,该过程发生反应的化学方程式分别是
(3)粗铜的电解精炼如图所示。在粗铜的电解过程中,粗铜板应是图中电极 (填图中的字母);在电极d上发生的电极反应式为

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
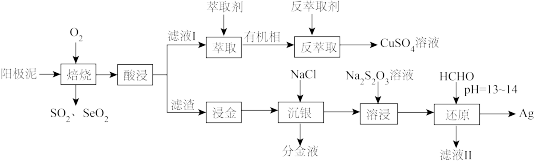
【推荐3】从某阳极泥(主要成分有Cu、Ag、Au、Ag2Se、Cu2S和NiSO4等)中回收Se和部分金属的工艺流程如图所示。回答下列问题:
已知:①硒的沸点:684.9℃。
②该工艺中萃取与反萃取原理为2RH+M2+ R2M+2H+(其中RH表示萃取剂,M表示金属)。
R2M+2H+(其中RH表示萃取剂,M表示金属)。
(1)“焙烧”前需对阳极泥进行____ 处理,以提高原料利用率。
(2)“焙烧”产生的SO2与SeO2的混合烟气用水吸收可制得单质Se,该反应的化学方程式为____ ;过滤所得粗硒可采用减压蒸馏的方法提纯单质硒,采用减压蒸馏的目的是____ 。
(3)“滤液I”中主要含有Cu2+、Ni2+的硫酸盐,可通过调节pH进行萃取分离。已知在使用萃取剂(RH)时,Cu2+、Ni2+的萃取率与平衡时溶液pH的关系如图所示:
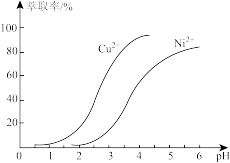
则萃取Cu2+最佳的pH范围约为____ (填“2~3”或“3~3.5”;“反萃取剂”最好选用____ (填化学式)。
(4)已知:①AgCl(s)+2S2O (aq)
(aq) [Ag(S2O3)2]3-(aq)+Cl-(aq) K1=6.66×103
[Ag(S2O3)2]3-(aq)+Cl-(aq) K1=6.66×103
②Ag+(aq)+2S2O (aq)
(aq) [Ag(S2O3)2]3-(aq) K2=3.7×1013
[Ag(S2O3)2]3-(aq) K2=3.7×1013
溶液中c(Cl-)>____ mol·L-1时,可使“溶浸”所得浸出液中c(Ag+)<10-5mol·L-1。
(5)“滤液II”中含有CO 和S2O
和S2O ,则“还原”反应的离子方程式为
,则“还原”反应的离子方程式为____ 。
(6)研究发现,硫代硫酸盐浸出金的过程是电化学催化腐蚀过程,催化机理模型如图所示:
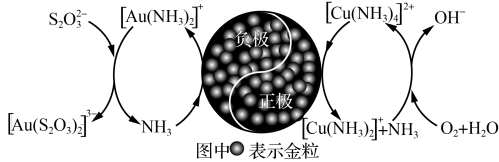
图中表示金粒负极的电极反应式为___ ,浸金的催化剂是____ (填化学式)。

已知:①硒的沸点:684.9℃。
②该工艺中萃取与反萃取原理为2RH+M2+
 R2M+2H+(其中RH表示萃取剂,M表示金属)。
R2M+2H+(其中RH表示萃取剂,M表示金属)。(1)“焙烧”前需对阳极泥进行
(2)“焙烧”产生的SO2与SeO2的混合烟气用水吸收可制得单质Se,该反应的化学方程式为
(3)“滤液I”中主要含有Cu2+、Ni2+的硫酸盐,可通过调节pH进行萃取分离。已知在使用萃取剂(RH)时,Cu2+、Ni2+的萃取率与平衡时溶液pH的关系如图所示:

则萃取Cu2+最佳的pH范围约为
(4)已知:①AgCl(s)+2S2O
 (aq)
(aq) [Ag(S2O3)2]3-(aq)+Cl-(aq) K1=6.66×103
[Ag(S2O3)2]3-(aq)+Cl-(aq) K1=6.66×103②Ag+(aq)+2S2O
 (aq)
(aq) [Ag(S2O3)2]3-(aq) K2=3.7×1013
[Ag(S2O3)2]3-(aq) K2=3.7×1013溶液中c(Cl-)>
(5)“滤液II”中含有CO
 和S2O
和S2O ,则“还原”反应的离子方程式为
,则“还原”反应的离子方程式为(6)研究发现,硫代硫酸盐浸出金的过程是电化学催化腐蚀过程,催化机理模型如图所示:

图中表示金粒负极的电极反应式为
您最近一年使用:0次



