由黄铜矿(主要成分是CuFeS2)炼制精铜的工艺流程示意图如下:

(1)在反射炉中,把铜精矿砂和石英砂混合加热到1000°C左右,黄铜矿与空气反应生成Cu和Fe的低价硫化物,且部分Fe的硫化物转变为低价氧化物,该过程中两个主要反应的化学方程式分别是_______ ,
_______ 反射炉内生成炉渣的主要成分是________ ;
(2)冰铜(Cu2S和FeS互相熔合而成)含Cu量为20%~50%。转炉中,将冰铜加熔剂(石英砂)在1200°C左右吹入空气进行吹炼。冰铜中的Cu2S被氧化成Cu2O,生成的Cu2O与Cu2S反应,生成含Cu量约为98.5%的粗铜,该过程发生反应的化学方程式分别是________ 、________ ;
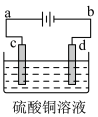
(3)粗铜的电解精炼如图所示。在粗铜的电解过程中,粗铜板应是图中电极 (填图中的字母);在电极d上发生的电极反应式为_______ ;若粗铜中还含有Au、Ag、Fe,它们在电解槽中的存在形式和位置为______ 。

(1)在反射炉中,把铜精矿砂和石英砂混合加热到1000°C左右,黄铜矿与空气反应生成Cu和Fe的低价硫化物,且部分Fe的硫化物转变为低价氧化物,该过程中两个主要反应的化学方程式分别是
(2)冰铜(Cu2S和FeS互相熔合而成)含Cu量为20%~50%。转炉中,将冰铜加熔剂(石英砂)在1200°C左右吹入空气进行吹炼。冰铜中的Cu2S被氧化成Cu2O,生成的Cu2O与Cu2S反应,生成含Cu量约为98.5%的粗铜,该过程发生反应的化学方程式分别是
(3)粗铜的电解精炼如图所示。在粗铜的电解过程中,粗铜板应是图中电极 (填图中的字母);在电极d上发生的电极反应式为

12-13高三·河南许昌·阶段练习 查看更多[11]
(已下线)2014届河南省许昌平顶山新乡三市高三第一次调研理综化学试卷(已下线)2014届江西省赣州市四所重点中学高三上学期期末联考理综化学试卷2012年普通高等学校招生全国统一考试化学(新课标)(已下线)2014高考名师推荐化学--预测102015届江西省上饶市高三第二次高考模拟化学试卷2016届重庆市巴蜀中学高三上学期期中考试理综化学试卷2016届宁夏回族自治区银川一中高三上第四次月考理化学试卷2016届黑龙江省牡丹江高级中学高三上期末热身理综化学试卷2016届福建省福安市高级中学高三3月月考化学试卷2016届宁夏六盘山高中高三三模理综化学试卷2016届福建省龙岩市高中毕业班3月质量检查理综化学试卷
更新时间:2016-12-09 04:56:41
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】钼是人体必须的微量元素之一,在电子行业有可能取代石墨烯,其化合物钼酸钠晶体(Na2MoO4▪2H2O)可制造阻燃剂和无公害型冷水系统的金属抑制剂。由钼精矿(主要成分MoS2,含少量PbS等)制备钼及钼酸钠晶体的部分流程如下:
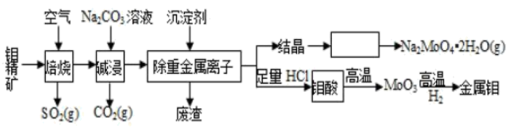
(1)焙烧时,下列措施有利于使钼精矿充分反应的是______ (填序号)。
a.增大空气的进入量 b.将矿石粉碎 c.采用逆流原理
(2)焙烧过程中,每生成1mol MoO3,转移电子数目为_____ 。
(3)写出“碱浸”过程中反应的离子方程式_____ 。
(4)经“结晶”过程可得到钼酸钠晶体的粗品,要得到纯净的钼酸钠晶体,题中方框内需要进行的操作是___ 。
(5)焙烧钼精矿所用的装置是多层焙烧炉,如图为各炉层固体物料的物质的量的百分组成。
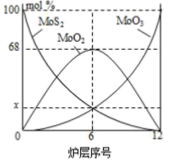
①图象中纵坐标x=_____ 。
②焙烧炉中也会发生MoS2与MoO3反应生成MoO2和SO2的反应,该反应的化学方程式_____ 。每生成标准状况下22.4L SO2,消耗氧化剂的物质的量为_____ 。

(1)焙烧时,下列措施有利于使钼精矿充分反应的是
a.增大空气的进入量 b.将矿石粉碎 c.采用逆流原理
(2)焙烧过程中,每生成1mol MoO3,转移电子数目为
(3)写出“碱浸”过程中反应的离子方程式
(4)经“结晶”过程可得到钼酸钠晶体的粗品,要得到纯净的钼酸钠晶体,题中方框内需要进行的操作是
(5)焙烧钼精矿所用的装置是多层焙烧炉,如图为各炉层固体物料的物质的量的百分组成。

①图象中纵坐标x=
②焙烧炉中也会发生MoS2与MoO3反应生成MoO2和SO2的反应,该反应的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】一种磁性材料的磨削废料的主要成分是铁镍合金(含镍质量分数约21%),还含有铜、钙、镁、硅的氧化物。由该废料制备氢氧化镍,工艺流程如下:
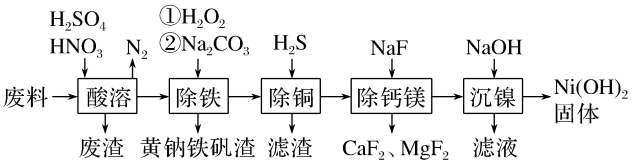
回答下列问题:
(1)“酸溶”时,溶液中有Fe3+、Fe2+、Ni2+等生成,废渣的主要成分是_______ ;金属镍溶解的离子方程式为_______ 。
(2)“除铁”时H2O2的作用是_______ ,加入碳酸钠的目的是_______ 。
(3)“除铜”时,反应的离子方程式为_______ ,若用Na2S代替H2S除铜,优点是_______ 。
(4)已知除钙镁过程在陶瓷容器中进行,NaF的实际用量不能过多的理由为_______ 。
(5)已知常温下Ksp[Ni(OH)2]=2.0×10-15,该流程在“沉镍”过程中,需调节溶液pH约为_______ 时,Ni2+才刚好沉淀完全(离子沉淀完全的浓度≤1.0×10-5mol/L;lg 2=0.30)。
(6)100 kg废料经上述工艺制得Ni(OH)2固体的质量为31 kg,则镍回收率为_______ (列式即可)。
(7)镍氢电池已成为混合动力汽车的主要电池类型,其工作原理如下:M+Ni(OH)2 HM+NiOOH(式中M为储氢合金)。写出电池放电过程中正极的电极反应式
HM+NiOOH(式中M为储氢合金)。写出电池放电过程中正极的电极反应式_______ 。

回答下列问题:
(1)“酸溶”时,溶液中有Fe3+、Fe2+、Ni2+等生成,废渣的主要成分是
(2)“除铁”时H2O2的作用是
(3)“除铜”时,反应的离子方程式为
(4)已知除钙镁过程在陶瓷容器中进行,NaF的实际用量不能过多的理由为
(5)已知常温下Ksp[Ni(OH)2]=2.0×10-15,该流程在“沉镍”过程中,需调节溶液pH约为
(6)100 kg废料经上述工艺制得Ni(OH)2固体的质量为31 kg,则镍回收率为
(7)镍氢电池已成为混合动力汽车的主要电池类型,其工作原理如下:M+Ni(OH)2
 HM+NiOOH(式中M为储氢合金)。写出电池放电过程中正极的电极反应式
HM+NiOOH(式中M为储氢合金)。写出电池放电过程中正极的电极反应式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
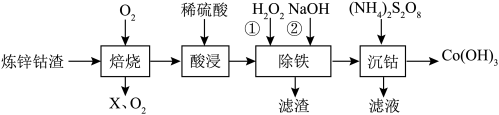
【推荐3】某校化学研究小组以炼锌钴渣(主要含有Co、Zn、Fe、Ni的金属硫化物)为原料制备Co(OH)3(氢氧化高钴)的流程如图,以实现“变废为宝”。 )时的
)时的 如表所示。
如表所示。
回答下列问题:
(1)在“焙烧”前,将炼锌钴渣磨成细粉,目的是_______ ,“ ”是
”是_______ (写化学式)。
(2)加入硫酸“酸浸”时发生的反应有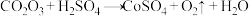 (未配平),该反应中的氧化产物与还原产物的物质的量之比为
(未配平),该反应中的氧化产物与还原产物的物质的量之比为_______ 。
(3)“除铁”时 与先加入的
与先加入的 发生反应的化学方程式为
发生反应的化学方程式为_______ ,反应温度不宜超过55℃的原因是_______ 。
(4)“沉钴”时,使用 调节溶液
调节溶液 ,
, 可将
可将 转化为
转化为 ,自身被还原为
,自身被还原为 ,发生该反应的离子方程式为
,发生该反应的离子方程式为___ ,得到的 经过滤、洗涤、干燥得到较纯产品,检验沉淀是否洗涤干净的操作及现象为
经过滤、洗涤、干燥得到较纯产品,检验沉淀是否洗涤干净的操作及现象为_______ 。
(5)若调节“沉钴”后滤液的 ,同时出现
,同时出现 和
和 沉淀,此时溶液中
沉淀,此时溶液中
_______ 。
 )时的
)时的 如表所示。
如表所示。| 离子 |  |  |  |  |  |  |
开始沉淀时的 | 1.5 | 6.3 | 7.0 | — | 6.4 | 7.2 |
完全沉淀时的 | 2.8 | 8.3 | 9.0 | 1.0 | 8.4 | 9.2 |
(1)在“焙烧”前,将炼锌钴渣磨成细粉,目的是
 ”是
”是(2)加入硫酸“酸浸”时发生的反应有
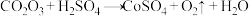 (未配平),该反应中的氧化产物与还原产物的物质的量之比为
(未配平),该反应中的氧化产物与还原产物的物质的量之比为(3)“除铁”时
 与先加入的
与先加入的 发生反应的化学方程式为
发生反应的化学方程式为(4)“沉钴”时,使用
 调节溶液
调节溶液 ,
, 可将
可将 转化为
转化为 ,自身被还原为
,自身被还原为 ,发生该反应的离子方程式为
,发生该反应的离子方程式为 经过滤、洗涤、干燥得到较纯产品,检验沉淀是否洗涤干净的操作及现象为
经过滤、洗涤、干燥得到较纯产品,检验沉淀是否洗涤干净的操作及现象为(5)若调节“沉钴”后滤液的
 ,同时出现
,同时出现 和
和 沉淀,此时溶液中
沉淀,此时溶液中
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】银铜合金广泛用于航空工业。从切割废料中回收银并制备铜化工产品的工艺如下:

[注:Al(OH)3和Cu(OH)2开始分解的温度分别为450 ℃和80 ℃]
(1)电解精炼银时,阴极反应式为___________________________ 。
滤渣A与稀硝酸反应,产生的气体在空气中迅速变为红棕色,该气体变色的化学反应方程式为________________________ 。
(2)固体混合物B的组成为________ ;
(3)完成煅烧过程中一个反应的化学方程式:__
________CuO+________Al2O3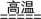 ________CuAlO2+________。
________CuAlO2+________。
(4)CuSO4溶液也可用于制备胆矾,其基本操作是____________ 、过滤、洗涤和干燥。

[注:Al(OH)3和Cu(OH)2开始分解的温度分别为450 ℃和80 ℃]
(1)电解精炼银时,阴极反应式为
滤渣A与稀硝酸反应,产生的气体在空气中迅速变为红棕色,该气体变色的化学反应方程式为
(2)固体混合物B的组成为
(3)完成煅烧过程中一个反应的化学方程式:
________CuO+________Al2O3
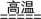 ________CuAlO2+________。
________CuAlO2+________。(4)CuSO4溶液也可用于制备胆矾,其基本操作是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】从银精矿(其化学成分有Ag、Zn、Cu、Pb、S及SiO2)中提取银、铜和铅的工艺流程如图所示。

(1)步骤①中当盐酸的浓度和KClO3的量一定时,写出两点可提高浸取率的措施:___________ ;步骤②中试剂X为___________ (填化学式)。
(2)步骤③中Na2SO3的作用___________ (填序号)
a.氧化剂 b.还原剂 c.提供 溶解沉淀 d.水解以提供碱性环境
溶解沉淀 d.水解以提供碱性环境
(3)步骤④滤渣中主要含有两种杂质。为了回收其中有经济效益的非金属单质,某实验小组选择合理试剂,设计实验流程如下,补充完善___________ 。(已知该单质在碱性溶液中易歧化)

(4)步骤⑤中反应的离子方程式为___________ ;
(5)粗银可用立式电解精炼。纯银作阴极,电解液采用硝酸和硝酸银的混合溶液。硝酸浓度不能过大,可能的原因是___________ ;(答1点)
(6)电解精炼的废水中含有 ,任意排放会造成水体污染。科技人员在碱性条件下用Al粉将
,任意排放会造成水体污染。科技人员在碱性条件下用Al粉将 还原成无污染气体排放,离子方程式为:
还原成无污染气体排放,离子方程式为:___________ ;已知25℃,当调节溶液pH=7时,可以将 的浓度降到1.0×10-6 mol/L,求反应Al(OH)3 + OH-⇌
的浓度降到1.0×10-6 mol/L,求反应Al(OH)3 + OH-⇌  +2 H2O的K值
+2 H2O的K值___________ 。

(1)步骤①中当盐酸的浓度和KClO3的量一定时,写出两点可提高浸取率的措施:
(2)步骤③中Na2SO3的作用
a.氧化剂 b.还原剂 c.提供
 溶解沉淀 d.水解以提供碱性环境
溶解沉淀 d.水解以提供碱性环境(3)步骤④滤渣中主要含有两种杂质。为了回收其中有经济效益的非金属单质,某实验小组选择合理试剂,设计实验流程如下,补充完善

(4)步骤⑤中反应的离子方程式为
(5)粗银可用立式电解精炼。纯银作阴极,电解液采用硝酸和硝酸银的混合溶液。硝酸浓度不能过大,可能的原因是
(6)电解精炼的废水中含有
 ,任意排放会造成水体污染。科技人员在碱性条件下用Al粉将
,任意排放会造成水体污染。科技人员在碱性条件下用Al粉将 还原成无污染气体排放,离子方程式为:
还原成无污染气体排放,离子方程式为: 的浓度降到1.0×10-6 mol/L,求反应Al(OH)3 + OH-⇌
的浓度降到1.0×10-6 mol/L,求反应Al(OH)3 + OH-⇌  +2 H2O的K值
+2 H2O的K值
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】我国科学家开发催化剂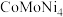 来提高CO/
来提高CO/ 燃料电池的性能。某小组以含镍废料(主要含Ni、NiO,以及少量CuO、FeO、
燃料电池的性能。某小组以含镍废料(主要含Ni、NiO,以及少量CuO、FeO、 、MgO、ZnO、
、MgO、ZnO、 和
和 等)为原料提取镍的流程如下:
等)为原料提取镍的流程如下: 如表所示:
如表所示:
回答下列问题:
(1)基态Ni原子的价层电子排布式为_______ ,位于元素周期表_______ 区。
(2)“酸浸”中产生了一种还原性气体,它是_______ (填化学式);“除铁铝”中双氧水的作用是_______ 。
(3)常温下,在“除铁铝”中,当滤液中 时,其pH=
时,其pH=_______ 。
(4)“电沉积”得到的粗镍,可通过电解法提纯,粗镍作_______ (填“阳”或“阴”)极,用硫酸镍溶液作电解质溶液,阴极的电极反应式为_______ 。
(5)纳米硫化铜具有优异的光电特性、催化能力、电导和电容特性等,在光学、电学、传感、催化等领域都具有广泛的应用前景。硫化铜的立方晶胞结构如图所示,已知 与
与 的核间距最小为anm,则该晶胞的棱长b=
的核间距最小为anm,则该晶胞的棱长b=_______ (用含a的代数式表示)nm。
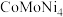 来提高CO/
来提高CO/ 燃料电池的性能。某小组以含镍废料(主要含Ni、NiO,以及少量CuO、FeO、
燃料电池的性能。某小组以含镍废料(主要含Ni、NiO,以及少量CuO、FeO、 、MgO、ZnO、
、MgO、ZnO、 和
和 等)为原料提取镍的流程如下:
等)为原料提取镍的流程如下: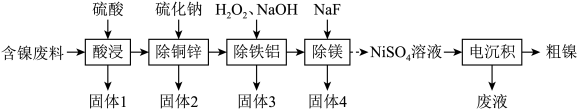
 如表所示:
如表所示:| 物质 | CuS | ZnS |  |  |  |  |  |
 |  | 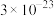 | 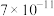 | 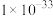 | 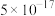 | 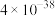 | 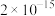 |
(1)基态Ni原子的价层电子排布式为
(2)“酸浸”中产生了一种还原性气体,它是
(3)常温下,在“除铁铝”中,当滤液中
 时,其pH=
时,其pH=(4)“电沉积”得到的粗镍,可通过电解法提纯,粗镍作
(5)纳米硫化铜具有优异的光电特性、催化能力、电导和电容特性等,在光学、电学、传感、催化等领域都具有广泛的应用前景。硫化铜的立方晶胞结构如图所示,已知
 与
与 的核间距最小为anm,则该晶胞的棱长b=
的核间距最小为anm,则该晶胞的棱长b=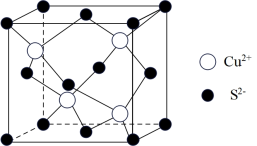
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】钴基合金中含少量镁、镍和铁元素,在化工、航空航天和机械工业应用广泛。现有钴基废合金需要回收再利用,设计流程如图:

已知:1)有关钴、镍、镁、铁化合物的性质见下表:
2)25℃ Ksp(MgF2)=7.4×10—11、Ksp(MgCO3)=3.5×10—3
请回答:
(1)“除镍”步骤必须控制在一定时间内完成,否则沉淀中将有部分Co(OH)2转化为Co(OH)3,此反应的化学方程式为________________ 。
(2)在“盐酸调pH=4”步骤中,加入盐酸的作用是______________________ 。
(3)“净化”步骤中加入H2O2的作用是_____________________ (请用离子方程式表示)。废渣的成分___________________ (请用化学式表示)。
(4)已知25℃时,Ksp[Fe(OH)3]=4.0×10-38,则该温度下反应Fe3++3H2O Fe(OH)3+3H+的平衡常数K=
Fe(OH)3+3H+的平衡常数K=_________________________ 。
(5)二水合草酸钴晶体(CoC2O4·2H2O)中C元素的化合价为________ ,在空气中高温反应的化学方程式为_______________________ 。

已知:1)有关钴、镍、镁、铁化合物的性质见下表:
| 化学式 | 沉淀开始时的pH | 沉淀完全时的pH | 有关性质 |
| Co(OH)2 | 7.2 | 9.4 | Co+2HCl=CoCl2+H2↑ Co2++2NH3·H2O=Co(OH)2↓+2NH4+ Co2++2H2O  Co(OH)2+2H+ Co(OH)2+2H+Ni+2HCl=NiCl2+H2↑ Ni2++6NH3·H2O=[Ni(NH3)6]2++6H2O |
| Fe(OH)2 | 7.1 | 9.6 | |
| Fe(OH)3 | 2.3 | 3.7 | |
| Mg(OH)2 | 10.8 | 12.4 |
2)25℃ Ksp(MgF2)=7.4×10—11、Ksp(MgCO3)=3.5×10—3
请回答:
(1)“除镍”步骤必须控制在一定时间内完成,否则沉淀中将有部分Co(OH)2转化为Co(OH)3,此反应的化学方程式为
(2)在“盐酸调pH=4”步骤中,加入盐酸的作用是
(3)“净化”步骤中加入H2O2的作用是
(4)已知25℃时,Ksp[Fe(OH)3]=4.0×10-38,则该温度下反应Fe3++3H2O
 Fe(OH)3+3H+的平衡常数K=
Fe(OH)3+3H+的平衡常数K=(5)二水合草酸钴晶体(CoC2O4·2H2O)中C元素的化合价为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】其同学采用硫铁矿焙烧取硫后的烧渣(主要成分为Fe2O3、SiO2、A12O3),不考虑其他杂质)制取七水合硫酸亚铁(FeSO4·7H2O),设计了如图流程:
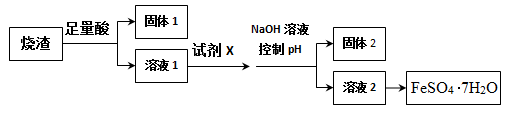
已知,某些金属阳离子可以通过“控制pH”[既调节溶液的酸碱性,pH=-lgc(H+)),pH值越大,碱性越强]使其转化为沉淀。固体2为白色沉淀。
(1)加足量酸之前,烧渣需经过进一步粉碎处理,粉碎的目的是__________ 。
(2)溶解烧渣选用的足量酸能否是盐酸,并说明理由_____ 。
(3)固体1有诸多用途,请列举其中一个____ ,试剂X的作用是______ 。
(4)某同学在控制pH这步操作时不慎将氢氧化钠溶液加过量了,结果得到的白色沉淀迅速转化为灰绿色,最终变为红褐色沉淀。请用化学用语解释固体2白色变成红褐色的原_____________ 。
(5)从溶液2中得到绿矾的过程中除需控制温度,防止产品分解外还应注意______ 。
(6)唐代苏敬《新修本草》对绿矾有如下描述:“本来绿色,新出窑未见风者,正如琉璃。陶及今人谓之石胆,烧之赤色。”另已知1mol绿矾隔绝空气高温煅烧完全分解,转移NA个电子。试写出绿矾隔绝空气高温煅烧分解的化学反应方程式____________ 。

已知,某些金属阳离子可以通过“控制pH”[既调节溶液的酸碱性,pH=-lgc(H+)),pH值越大,碱性越强]使其转化为沉淀。固体2为白色沉淀。
(1)加足量酸之前,烧渣需经过进一步粉碎处理,粉碎的目的是
(2)溶解烧渣选用的足量酸能否是盐酸,并说明理由
(3)固体1有诸多用途,请列举其中一个
(4)某同学在控制pH这步操作时不慎将氢氧化钠溶液加过量了,结果得到的白色沉淀迅速转化为灰绿色,最终变为红褐色沉淀。请用化学用语解释固体2白色变成红褐色的原
(5)从溶液2中得到绿矾的过程中除需控制温度,防止产品分解外还应注意
(6)唐代苏敬《新修本草》对绿矾有如下描述:“本来绿色,新出窑未见风者,正如琉璃。陶及今人谓之石胆,烧之赤色。”另已知1mol绿矾隔绝空气高温煅烧完全分解,转移NA个电子。试写出绿矾隔绝空气高温煅烧分解的化学反应方程式
您最近一年使用:0次
【推荐3】以含锑的废料(主要成分是Sb,含少量Cu、Fe杂质)为原料制备焦锑酸钠的流程如下:
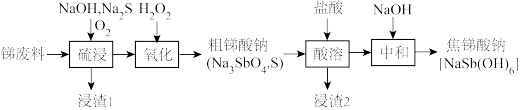
已知:硫浸时,锑转化成Na3SbS3,Fe、Cu不参与反应;Na3SbO4和NaSb(OH)6不溶于水,易溶于酸。
请回答下列问题:
(1)焦锑酸钠中锑的化合价为_______ 。
(2)提高“硫浸”速率的措施有_______ (答一条)。从上述分离出来的浸渣1中提取铜的操作包括_______ 、_______ 、洗涤、干燥等。
(3)“硫浸”中锑转化的化学方程式为_______ 。
(4)“氧化”中氧化剂与还原剂的物质的量之比为_______ 。
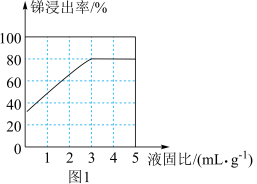
(5)其他条件相同时,“硫浸”中锑浸出率与液固比(一定浓度的NaOH和Na2S组成的混合液体积与锑渣质量之比)关系如图1所示。最佳液固比为_______ mL·g-1。
(6)当液固比一定时,“氧化”中相同时间内锑的氧化率与温度关系如图2所示,解释40℃氧化率达到峰值的原因是_______ 。

已知:硫浸时,锑转化成Na3SbS3,Fe、Cu不参与反应;Na3SbO4和NaSb(OH)6不溶于水,易溶于酸。
请回答下列问题:
(1)焦锑酸钠中锑的化合价为
(2)提高“硫浸”速率的措施有
(3)“硫浸”中锑转化的化学方程式为
(4)“氧化”中氧化剂与还原剂的物质的量之比为
(5)其他条件相同时,“硫浸”中锑浸出率与液固比(一定浓度的NaOH和Na2S组成的混合液体积与锑渣质量之比)关系如图1所示。最佳液固比为

(6)当液固比一定时,“氧化”中相同时间内锑的氧化率与温度关系如图2所示,解释40℃氧化率达到峰值的原因是

您最近一年使用:0次



