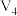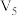如图中曲线表示一定条件下一定量的锌粒与足量的稀硫酸反应的过程。若使曲线b变为曲线a,可采取的措施是


| A.加入硫酸铜固体 | B.加入醋酸钠固体 |
| C.稀硫酸换成浓硫酸 | D.加热使溶液温度升高 |
更新时间:2023-01-13 10:05:11
|
相似题推荐
单选题
|
较易
(0.85)
解题方法
【推荐1】碰撞理论是一种较直观的反应速率理论,下列有关碰撞理论叙述正确的是( )
| A.分子发生碰撞就一定发生反应 |
| B.发生有效碰撞的分子具有最高的能量 |
| C.有效碰撞是活化分子在一定方向上的碰撞 |
| D.活化分子的平均能量称之活化能 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】2021年诺贝尔化学奖授予BenjaminList和DavidMacMillan,以表彰他们对不对称有机催化剂的发展做出的贡献,用催化剂Fe3(CO)12和ZMS-5催化CO2加氢合成乙烯,最终得到C3H6、C4H8等副产物。下列说法正确的是


| A.CO2、C2H4、C3H6分子中所有原子均共平面 |
| B.催化剂减小了反应的活化能和焓变 |
| C.(CH2)n异构反应中所得副产物C3H6和C4H8一定能使酸性高锰酸钾褪色 |
| D.第Ⅰ步为决速步骤,该步反应的活化能大于第Ⅱ步反应的活化能 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】把石灰石浸入盐酸中,下列措施能使反应速率增大的是( )
①加大盐酸用量 ②增大盐酸浓度 ③粉碎石灰石 ④增大体系压强
①加大盐酸用量 ②增大盐酸浓度 ③粉碎石灰石 ④增大体系压强
| A.①③ | B.②③ |
| C.①④ | D.③④ |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】一定量盐酸跟过量的铁粉反应时,为了减缓反应速率,且不影响生成氢气的总量,可向盐酸中加入适量的
①NaOH 固体 ②NaCl 溶液 ③KNO3 溶液 ④CH3COONa 固体
①NaOH 固体 ②NaCl 溶液 ③KNO3 溶液 ④CH3COONa 固体
| A.①③ | B.②④ | C.②③ | D.③④ |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】在密闭容器中发生反应:C(s)+CO2(g) 2CO(g),下列说法不正确的是
2CO(g),下列说法不正确的是
 2CO(g),下列说法不正确的是
2CO(g),下列说法不正确的是| A.该反应达到平衡后将碳块磨成粉末可以使平衡右移 |
| B.升高温度可以加快反应速率 |
| C.容器体积不变时,向其中充入N2,反应速率不变 |
| D.增加碳的质量不能加快反应速率 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】反应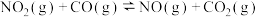 的能量变化如图所示,下列说法正确的是
的能量变化如图所示,下列说法正确的是

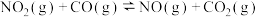 的能量变化如图所示,下列说法正确的是
的能量变化如图所示,下列说法正确的是
| A.图中X→Y为放热过程 |
| B.升高温度,可减少反应达到平衡的时间 |
| C.恒容条件下充入He,可加快该反应的速率 |
| D.加入合适的催化剂,可使a、b、c的数值均减小 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】某兴趣小组将下表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,以研究硫酸铜的浓度对稀硫酸与锌反应生成氢气速率的影响。下列判断不正确的是
实验组别混合溶液 | A | B | C | D | E | F |
| 30 |
|
|
|
|
|
饱和 | 0 | 0.5 | 2.5 | 5 |
| 20 |
|
|
|
|
| 10 | 0 |
A. , , , , |
B.本实验利用了控制变量思想,变量为 溶液的浓度 溶液的浓度 |
| C.反应一段时间后,实验F的金属表面可能呈现红色 |
| D.该小组的实验结论是硫酸铜对稀硫酸与锌反应生成氢气有催化作用 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】关于下列说法正确的是
| A.增大反应物的浓度,能够增大活化分子的百分含量,所以反应速率增大 |
B.对可逆反应 ,增加氯化钾浓度,逆反应速率加快 ,增加氯化钾浓度,逆反应速率加快 |
| C.工业合成氨反应是一个熵增加的过程 |
D.用稀硫酸和锌粒制取 时,加几滴 时,加几滴 溶液以加快反应速率 溶液以加快反应速率 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐3】下列关于化学反应速率的说法中,正确的是( )
①用铁片和稀硫酸反应制取氢气时,改用98%的浓硫酸可以加快产生氢气的速率
②决定化学反应速率的主要因素是反应物的浓度.
③一定量的锌与过量的稀硫酸反应制取氢气,为减慢反应速率而又不影响生成H2的量,可向其中加入KNO3溶液.
④汽车尾气中的NO和CO反应转化为无害的N2和CO2,减小压强,反应速率减慢
⑤增大压强,一定能加快化学反应速率
⑥用锌与稀硫酸反应制H2时,滴加几滴硫酸铜溶液能加快反应速率
⑦光是影响某些化学反应速率的外界条件之一
①用铁片和稀硫酸反应制取氢气时,改用98%的浓硫酸可以加快产生氢气的速率
②决定化学反应速率的主要因素是反应物的浓度.
③一定量的锌与过量的稀硫酸反应制取氢气,为减慢反应速率而又不影响生成H2的量,可向其中加入KNO3溶液.
④汽车尾气中的NO和CO反应转化为无害的N2和CO2,减小压强,反应速率减慢
⑤增大压强,一定能加快化学反应速率
⑥用锌与稀硫酸反应制H2时,滴加几滴硫酸铜溶液能加快反应速率
⑦光是影响某些化学反应速率的外界条件之一
| A.①⑤⑥ | B.④⑥⑦ | C.④⑥ | D.③④⑥⑦ |
您最近一年使用:0次