已知A、B、C、D、E为原子序数依次增大的前36号元素,A的2p轨道有3个电子;B是地壳中含量最多的元素;C元素的M层有一个电子;D元素形成的单质具有两性;E的基态原子的电子排布为[Ar]3d104S1。回答下列问题(用元素符号或化学式表示):
(1)A的最高能级电子云呈_______ 形,B的价层电子轨道表达式是_______ 。
(2)D的基态原子核外电子排布式为_______ 。
(3)A、B的第一电离能由小到大顺序是_______ (填元素符号)。
(4)B、C、D的电负性由小到大的顺序为_______ (填元素符号)。
(5)B、C、D的原子半径由小到大的顺序为_______ (填元素符号)。
(6)E在元素周期表中的位置_______ ,位于_______ 区。
(1)A的最高能级电子云呈
(2)D的基态原子核外电子排布式为
(3)A、B的第一电离能由小到大顺序是
(4)B、C、D的电负性由小到大的顺序为
(5)B、C、D的原子半径由小到大的顺序为
(6)E在元素周期表中的位置
更新时间:2023-01-11 17:10:39
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】已知A、B、C、D、E、F为周期表前四周期原子序数依次增大的六种元素。其中A是元素周期表中原子半径最小的元素。B原子最外层电子数是内层电子数的2倍。D、E为同主族元素,且E的原子序数为D的2倍。F元素在地壳中的含量位于金属元素的第二位。试回答下列问题:
(1)F元素原子的价电子排布式为___________ 。
(2)下列关于B2A2的说法中正确的是___________(填序号)。
(3)B和D形成的一种三原子分子与C和D形成的一种化合物互为等电子体,则满足上述条件的B和D形成的化合物的结构式为___________ 。
(4)C元素原子的第一电离能比B、D两元素原子的第一电离能高的主要原因是___________ 。
(5)E的氢化物的价电子对互斥理论模型为___________ ,E原子的杂化方式为___________ 杂化。
(1)F元素原子的价电子排布式为
(2)下列关于B2A2的说法中正确的是___________(填序号)。
| A.B2A2中的所有原子都满足8电子结构 |
| B.每个B2A2分子中σ键和π键数目比为1:1 |
| C.B2A2是含极性键和非极性键的非极性分子 |
| D.B2A2分子中的B-A键属于s-sp σ键 |
(4)C元素原子的第一电离能比B、D两元素原子的第一电离能高的主要原因是
(5)E的氢化物的价电子对互斥理论模型为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】X、Y、Z、W、R、Q为前30号元素,且原子序数依次增大。X是所有元素中原子半径最小的,Y有三个能级,且每个能级上的电子数相等,Z原子单电子数在同周期元素中最多,W与Z同周期,第一电离能比Z的低,R与Y同一主族,Q的最外层只有一个电子,其他电子层电子均处于饱和状态。请回答下列问题:
(1)R核外电子排布式为__________________ 。
(2)X、Y、Z、W形成的有机物YW(ZX2)2中Y、Z的杂化轨道类型分别为__________ ,ZW3-离子的立体构型是__________ 。
(3)Y、R的最高价氧化物的沸点较高的是_____________ (填化学式),原因是_________________ 。
(4)将Q单质的粉末加入到ZX3的浓溶液中,并通入W2,充分反应后溶液呈深蓝色,该反应的离子方程式为______________________________________ 。
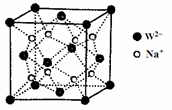
(5)W和Na的一种离子化合物的晶胞结构如图,该离子化合物为____________ (填化学式)。Na+的配位数为_____________ ,距一个阴离子周围最近的所有阳离子为顶点构成的几何体为__________ 。已知该晶胞的密度为ρg·cm-3,阿伏加德罗常数为NA,则两个最近的W离子间距离为____________ nm(用含ρ、NA的计算式表示)。
(1)R核外电子排布式为
(2)X、Y、Z、W形成的有机物YW(ZX2)2中Y、Z的杂化轨道类型分别为
(3)Y、R的最高价氧化物的沸点较高的是
(4)将Q单质的粉末加入到ZX3的浓溶液中,并通入W2,充分反应后溶液呈深蓝色,该反应的离子方程式为
(5)W和Na的一种离子化合物的晶胞结构如图,该离子化合物为

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】按要求填空:
(1)①基态A原子的电子排布式为1s22s22p5,则A元素位于周期表______ 。
②化合物M可通过石油工业获取,其产量标志着一个国家石油化工水平,该化合物中σ键与π键个数比为______ 。
③XY2是红棕色气体,X与氢元素可形成XH3,X基态原子的价层电子轨道表示式为______ 。
④1~36号元素的基态原子中,未成对电子数最多的元素是______ (写元素符号)。
(2)蓝矾(CuSO4•5H2O)的结构如图所示,SO 中S原子的杂化轨道类型是
中S原子的杂化轨道类型是_____ 。

(1)①基态A原子的电子排布式为1s22s22p5,则A元素位于周期表
②化合物M可通过石油工业获取,其产量标志着一个国家石油化工水平,该化合物中σ键与π键个数比为
③XY2是红棕色气体,X与氢元素可形成XH3,X基态原子的价层电子轨道表示式为
④1~36号元素的基态原子中,未成对电子数最多的元素是
(2)蓝矾(CuSO4•5H2O)的结构如图所示,SO
 中S原子的杂化轨道类型是
中S原子的杂化轨道类型是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】下表是元素周期表的一部分,表中所列的字母分别代表某一化学元素。 和
和 形成的
形成的 分子的结构式是
分子的结构式是___________ ,分子中含有___________ (填“极性”或“非极性”)键。
(2)元素 的最简单气态氢化物的电子式是
的最简单气态氢化物的电子式是___________ 。元素 和
和 中,最简单气态氢化物的沸点较高的是
中,最简单气态氢化物的沸点较高的是___________ (用化学式表示),原因是___________ 。
(3)元素 和
和 形成的最简单化合物分子的空间结构是
形成的最简单化合物分子的空间结构是___________ (用文字表述)。元素 、
、 、
、 中,简单离子半径从大到小的顺序是
中,简单离子半径从大到小的顺序是___________ (用离子符号表示)。
(4)元素 的外围电子轨道表示式是
的外围电子轨道表示式是___________ 。元素 、
、 、
、 中,第一电离能从大到小的顺序是
中,第一电离能从大到小的顺序是___________ (用元素符号表示)。
(5)元素 的最简单气态氢化物和最高价氧化物对应的水化物可以发生反应,该反应的化学方程式是
的最简单气态氢化物和最高价氧化物对应的水化物可以发生反应,该反应的化学方程式是___________ 。元素 和
和 的最高价氧化物对应的水化物可以发生反应,该反应的离子方程式是
的最高价氧化物对应的水化物可以发生反应,该反应的离子方程式是___________ 。

 和
和 形成的
形成的 分子的结构式是
分子的结构式是(2)元素
 的最简单气态氢化物的电子式是
的最简单气态氢化物的电子式是 和
和 中,最简单气态氢化物的沸点较高的是
中,最简单气态氢化物的沸点较高的是(3)元素
 和
和 形成的最简单化合物分子的空间结构是
形成的最简单化合物分子的空间结构是 、
、 、
、 中,简单离子半径从大到小的顺序是
中,简单离子半径从大到小的顺序是(4)元素
 的外围电子轨道表示式是
的外围电子轨道表示式是 、
、 、
、 中,第一电离能从大到小的顺序是
中,第一电离能从大到小的顺序是(5)元素
 的最简单气态氢化物和最高价氧化物对应的水化物可以发生反应,该反应的化学方程式是
的最简单气态氢化物和最高价氧化物对应的水化物可以发生反应,该反应的化学方程式是 和
和 的最高价氧化物对应的水化物可以发生反应,该反应的离子方程式是
的最高价氧化物对应的水化物可以发生反应,该反应的离子方程式是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】A、B、C、D、E代表前四周期原子序数依次增大的五种元素。A、D同主族且有两种常见化合物DA2和DA3;工业上电解熔融C2A3制取单质C;B、E除最外层均只有2个电子外,其余各层全充满,E位于元素周期表的ds区。回答下列问题:
(1)B、C中第一电离能较大的是_________ ,基态D原子价电子的轨道表达式为____________ 。
(2)DA2分子的VSEPR模型是____________ 。H2A比H2D熔沸点高得多的原因是____________ 。
(3)实验测得C与氯元素形成化合物的实际组成为C2Cl6,其球棍模型如图所示。已知C2Cl6 在加热时易升华,与过量的NaOH溶液反应可生成Na[C(OH)4]。
① C2Cl6属于____________ 晶体(填晶体类型),其中C原子的杂化轨道类型为____________ 杂化。
② [C(OH)4]-中存在的化学键有___________ 。
(4)工业上制备B的单质是电解熔融B的氯化物,而不是电解BA,原因是_____________ 。
(5)B、C的氟化物晶格能分别是2957 kJ·mol-1、5492 kJ·mol-1,二者相差很大的原因是____________ 。
(6)D与E所形成化合物晶体的晶胞如图所示。

① 在该晶胞中,E的配位数为______________ 。
② 已知该晶胞的密度为ρ g/cm3,则其中两个D原子之间的距离为_________ pm(列出计算式即可)。
(1)B、C中第一电离能较大的是
(2)DA2分子的VSEPR模型是
(3)实验测得C与氯元素形成化合物的实际组成为C2Cl6,其球棍模型如图所示。已知C2Cl6 在加热时易升华,与过量的NaOH溶液反应可生成Na[C(OH)4]。

① C2Cl6属于
② [C(OH)4]-中存在的化学键有
(4)工业上制备B的单质是电解熔融B的氯化物,而不是电解BA,原因是
(5)B、C的氟化物晶格能分别是2957 kJ·mol-1、5492 kJ·mol-1,二者相差很大的原因是
(6)D与E所形成化合物晶体的晶胞如图所示。

① 在该晶胞中,E的配位数为
② 已知该晶胞的密度为ρ g/cm3,则其中两个D原子之间的距离为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】近年来,我国航空航天事业成果显著,航空航天材料技术快速发展。
(1)“天宫二号”航天器使用了钛合金,质量轻,强度位于金属之首。基态钛原子的价层电子排布图为___________ 。
(2)“北斗三号”导航卫星使用的太阳能电池材料砷化镓是优良的化合物半导体,基态镓原子电子占据最高能级的电子云轮廓图为____________ 形。
(3)“C919”飞机机身使用复合材料——碳纤维和环氧树脂。
①下列电子排布图能表示碳原子的能量最低状态的是___________ (填字母)。
A.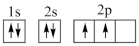 B.
B. 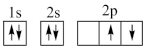 C.
C.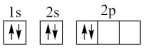 D.
D.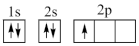
②氧原子的基态原子核外有___________ 个未成对电子。
(1)“天宫二号”航天器使用了钛合金,质量轻,强度位于金属之首。基态钛原子的价层电子排布图为
(2)“北斗三号”导航卫星使用的太阳能电池材料砷化镓是优良的化合物半导体,基态镓原子电子占据最高能级的电子云轮廓图为
(3)“C919”飞机机身使用复合材料——碳纤维和环氧树脂。
①下列电子排布图能表示碳原子的能量最低状态的是
A.
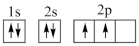 B.
B.  C.
C.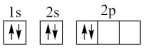 D.
D.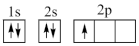
②氧原子的基态原子核外有
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】Cd位于第五周期ⅡB族,(CdSe)n小团簇(CdnSen,n=1~16)为Ⅱ-Ⅵ族化合物半导体材料,具有独特的光学和电学性质,常应用于发光二极管、生物系统成像与诊断等方面。回答下列问题:
(1)基态Se原子的价层电子排布式为___________ 。
(2)Cd的第一电离能大于同周期相邻元素,原因是___________ 。
(3)利用有机配体PH3、N(CH3)3等修饰(CdSe)2可改善其光致发光效率。其中PH3的空间构型是___________ 。N(CH3)3中N原子杂化轨道类型是___________ 。
(4)CdSe的一种晶体为立方ZnS型,晶胞结构如图所示。其中A原子坐标参数为( ,
, ,
, ),则B的原子坐标参数分别为
),则B的原子坐标参数分别为___________ 。该晶胞中CdSe键的键长为___________ cm。已知Cd和Se的原子半径分别为rCd nm和rSe nm,则该晶胞中原子的体积占晶胞体积的百分率为___________ 。

(1)基态Se原子的价层电子排布式为
(2)Cd的第一电离能大于同周期相邻元素,原因是
(3)利用有机配体PH3、N(CH3)3等修饰(CdSe)2可改善其光致发光效率。其中PH3的空间构型是
(4)CdSe的一种晶体为立方ZnS型,晶胞结构如图所示。其中A原子坐标参数为(
 ,
, ,
, ),则B的原子坐标参数分别为
),则B的原子坐标参数分别为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】2021年10月18日出版的《自然-化学》刊登了我国科学技术大学吴长征团队的研究新成果:AgCrS2在室温下具有超离子行为,该研究成果为未来新结构二维材料的合成和探索提供了新思路。
(1)基态铬原子电子排布式为_______ ,以顺时针方向自旋的电子最多有_______ 个,第一电离能P>S的原因是_______ 。
(2)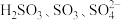 等微粒中,则H2S的中心原子杂化类型为
等微粒中,则H2S的中心原子杂化类型为_______ ,键角SO2________ SO3(填“>”、“=”、“<”), 的空间构型是
的空间构型是_______ 。
(3)CrF3、CrBr3的熔点分别为1100℃、79℃,其可能的主要原因是_______ 。
(4)氧铬酸钙是一种复合材料,可用于配制无机防锈颜料等,其晶胞结构如图
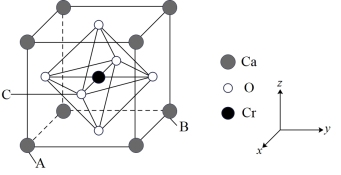
①已知A、B的原子坐标参数分别为(1,0,0)、(0,1,0),则C的原子坐标参数为_______ 。
②氧铬酸钙的化学式为_______ ,该晶体密度为ρg/cm3,钙和氧的最近距离为a nm,则代表阿伏加德罗常数NA=_________ mol-1
(1)基态铬原子电子排布式为
(2)
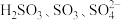 等微粒中,则H2S的中心原子杂化类型为
等微粒中,则H2S的中心原子杂化类型为 的空间构型是
的空间构型是(3)CrF3、CrBr3的熔点分别为1100℃、79℃,其可能的主要原因是
(4)氧铬酸钙是一种复合材料,可用于配制无机防锈颜料等,其晶胞结构如图

①已知A、B的原子坐标参数分别为(1,0,0)、(0,1,0),则C的原子坐标参数为
②氧铬酸钙的化学式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】I.表中列出了第三周期的几种元素的部分性质:
请按要求回答下列问题:
(1)写出基态a原子的价层电子排布式:____ 。
(2)表中元素原子半径最大的是(写元素符号)_____ 。
(3)a、b、c三种元素形成的氢化物中,其稳定性由强到弱的顺序是(用化学式表示)_____ 。
(4)d、e最高价氧化物对应水化物相互反应的离子方程式为_____ 。
(5)表中五种元素的第一电离能由大到小的顺序是(写元素符号)____ 。
II.硒(34Se)是动物和人体所必需的微量元素之一,也是重要的工业原料,与氧同族。
(6)Se原子结构示意图可表示为____ 。
(7)下列说法合理的是____ 。
a.SeO2既有氧化性又有还原性 b.沸点:H2O<H2S<H2Se
c.热稳定性:H2Se<HCl<H2S d.酸性:H2SeO4<HBrO4<HClO4
| 元素编号 | a | b | c | d | e |
| 电负性 | 3.0 | 2.5 | X | 1.5 | 0.9 |
| 主要化合价 | -1,+7 | -2,+6 | -3,+5 | +3 | +1 |
(1)写出基态a原子的价层电子排布式:
(2)表中元素原子半径最大的是(写元素符号)
(3)a、b、c三种元素形成的氢化物中,其稳定性由强到弱的顺序是(用化学式表示)
(4)d、e最高价氧化物对应水化物相互反应的离子方程式为
(5)表中五种元素的第一电离能由大到小的顺序是(写元素符号)
II.硒(34Se)是动物和人体所必需的微量元素之一,也是重要的工业原料,与氧同族。
(6)Se原子结构示意图可表示为
(7)下列说法合理的是
a.SeO2既有氧化性又有还原性 b.沸点:H2O<H2S<H2Se
c.热稳定性:H2Se<HCl<H2S d.酸性:H2SeO4<HBrO4<HClO4
您最近一年使用:0次
【推荐1】已知A、B、C、D、E、F是原子序数依次增大的前四周期元素。其中A是宇宙中含量最多的元素; B元素基态原子最高能级的不同轨道都有电子,并且自旋方向相同;C元素基态原子的价层电子排布是nsnnp2n; D元素基态原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;E与D的最高能层数相同,但其价层电子数等于其电子层数,且只有1个未成对电子。F元素基态原子的最外层只有一个电子,其次外层的所有轨道的电子均成对。
(1)请用元素符号完成下列空白:
①A、B、C、D四种元素的电负性:_______>_______>_______>_______;_______
②B、C、D、E四种元素的第一电离能:_______>_______>_______>_______。_______
(2)E元素的逐级电离能按照I1、I2、I3……的顺序,最先出现Ix>Ix-1时的x=_______ 。
(3)F元素基态原子的电子排布式为_______ 。与 其同周期基态原子未成对电子最多的元素符号为_______ ,该元素价电子层轨道表示式为_______ 。
(4)C与F形成的某晶体晶胞如图所示,则该晶体化学式为_______ 。

(1)请用元素符号完成下列空白:
①A、B、C、D四种元素的电负性:_______>_______>_______>_______;
②B、C、D、E四种元素的第一电离能:_______>_______>_______>_______。
(2)E元素的逐级电离能按照I1、I2、I3……的顺序,最先出现Ix>Ix-1时的x=
(3)F元素基态原子的电子排布式为
(4)C与F形成的某晶体晶胞如图所示,则该晶体化学式为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】化学物质在材料领域有着广泛用途:黄血盐 常用作颜料、染料,
常用作颜料、染料, 属于超导材料。
属于超导材料。
(1)上述涉及的元素中属于d区元素的有_______ 。电负性最大的元素的价层电子轨道表示式为_______ 。
(2)金属的熔点:K小于Fe,理由是_______ 。
(3)可溶性氰化物(如KCN)有剧毒,但黄血盐 的毒性极低,请从结构角度解释黄血盐毒性极低的原因是
的毒性极低,请从结构角度解释黄血盐毒性极低的原因是_______ 。
(4) 晶体的晶胞结构如图所示。与S原子距离最近且等距离的Ni原子数目为
晶体的晶胞结构如图所示。与S原子距离最近且等距离的Ni原子数目为_______ ,一个晶胞的质量为_______ g。

 常用作颜料、染料,
常用作颜料、染料, 属于超导材料。
属于超导材料。(1)上述涉及的元素中属于d区元素的有
(2)金属的熔点:K小于Fe,理由是
(3)可溶性氰化物(如KCN)有剧毒,但黄血盐
 的毒性极低,请从结构角度解释黄血盐毒性极低的原因是
的毒性极低,请从结构角度解释黄血盐毒性极低的原因是(4)
 晶体的晶胞结构如图所示。与S原子距离最近且等距离的Ni原子数目为
晶体的晶胞结构如图所示。与S原子距离最近且等距离的Ni原子数目为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】前36号元素A、B、C、D、E原子序数依次增大,A与B是同一周期紧邻元素,B与D同一主族,B元素氢化物的水溶液可用于玻璃的雕刻。C元素是同周期元素中第一电离能最小的元素,C与E的最外层电子数相同,E元素内层均排满电子。
(1)基态原子E的电子排布式为___________ ;依据电子排布周期表划分为5个区,该元素位于周期表的_________ 区。
(2)元素A、B、D电负性由大到小的顺序为___________ 。
(3)D2A分子中,中心原子的杂化方式为___________ 。分子键角大小关系,AB2分子_____ D2A分子(填“大于”,“小于”或“等于”),原因_________________________ 。
(4)单质C经常用于储氢,储氢后形成晶体结构如图所示:

该晶体中与C离子近邻的氢离子有_______ 个。这些氢离子,构成的空间构型为_______ 。已知C离子与氢离子之间最近的核间距为a pm,则该晶体的密度为_____ g·cm-3。
(1)基态原子E的电子排布式为
(2)元素A、B、D电负性由大到小的顺序为
(3)D2A分子中,中心原子的杂化方式为
(4)单质C经常用于储氢,储氢后形成晶体结构如图所示:

该晶体中与C离子近邻的氢离子有
您最近一年使用:0次



