“硫碘循环”法是分解水制氢气的研究热点,涉及下列三个反应:
反应I:SO2(g) + I2(aq) + 2H2O(l) = 2HI(aq) + H2SO4(aq)
反应II:2HI(g) H2(g) + I2(g)
H2(g) + I2(g)
反应III:2H2SO4(g) 2H2O(g) + 2SO2(g) + O2(g)
2H2O(g) + 2SO2(g) + O2(g)
(1)反应III实际上分两步进行:
H2SO4(g)=SO3(g) + H2O(g) ∆H1
2SO3(g) 2SO2(g) + O2(g) ∆H2
2SO2(g) + O2(g) ∆H2
则反应III的反应热∆H=_______ (用∆H1、∆H2表示)。
(2)某温度下将1mol HI充入密闭容器中发生反应II,达到第1次平衡后,用选择性膜完全分离出H2,达到第2次平衡后再次分离H2,重复多次,平衡时n(HI)如下表:
①第1次平衡时,HI的转化率为_______ %。
②归纳出分离H2的次数对HI转化率的影响:_______ 。
③计算第2次平衡时H2和I2的物质的量______ (写出计算过程)。
(3)反应I发生时,溶液中存在化学平衡:I2(aq) + I-(aq)
 (aq),其反应速率极快且平衡常数很大。现将1mol SO2缓缓通入含1 mol I2的水溶液中恰好完全反应。在答题卡中,画出溶液中I
(aq),其反应速率极快且平衡常数很大。现将1mol SO2缓缓通入含1 mol I2的水溶液中恰好完全反应。在答题卡中,画出溶液中I 的物质的量n( I
的物质的量n( I )随反应时间t变化的曲线图
)随反应时间t变化的曲线图______ 。
反应I:SO2(g) + I2(aq) + 2H2O(l) = 2HI(aq) + H2SO4(aq)
反应II:2HI(g)
 H2(g) + I2(g)
H2(g) + I2(g)反应III:2H2SO4(g)
 2H2O(g) + 2SO2(g) + O2(g)
2H2O(g) + 2SO2(g) + O2(g)(1)反应III实际上分两步进行:
H2SO4(g)=SO3(g) + H2O(g) ∆H1
2SO3(g)
 2SO2(g) + O2(g) ∆H2
2SO2(g) + O2(g) ∆H2则反应III的反应热∆H=
(2)某温度下将1mol HI充入密闭容器中发生反应II,达到第1次平衡后,用选择性膜完全分离出H2,达到第2次平衡后再次分离H2,重复多次,平衡时n(HI)如下表:
| 达到平衡的次数 | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 | …… |
| n(HI)/mol | 0.78 | 0.67 | 0.60 | 0.55 | 0.51 | …… |
①第1次平衡时,HI的转化率为
②归纳出分离H2的次数对HI转化率的影响:
③计算第2次平衡时H2和I2的物质的量
(3)反应I发生时,溶液中存在化学平衡:I2(aq) + I-(aq)

 (aq),其反应速率极快且平衡常数很大。现将1mol SO2缓缓通入含1 mol I2的水溶液中恰好完全反应。在答题卡中,画出溶液中I
(aq),其反应速率极快且平衡常数很大。现将1mol SO2缓缓通入含1 mol I2的水溶液中恰好完全反应。在答题卡中,画出溶液中I 的物质的量n( I
的物质的量n( I )随反应时间t变化的曲线图
)随反应时间t变化的曲线图
更新时间:2023-01-12 17:04:46
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
【推荐1】油气开采、石油化工、煤化工等行业废气普遍含有的硫化氢,需要回收处理并加以利用。
(1)已知下列反应的热化学方程式:
①2H2S(g) 2H2(g)+S2(g) ΔH1=+180 kJ/mol
2H2(g)+S2(g) ΔH1=+180 kJ/mol
②CS2(g)+2H2(g) S2(g)+CH4(g) ΔH2=-81 kJ/mol
S2(g)+CH4(g) ΔH2=-81 kJ/mol
则反应③CH4(g)+2H2S(g) 4H2(g)+CS2(g)的ΔH3=
4H2(g)+CS2(g)的ΔH3=_______ kJ/mol;下列叙述能说明反应③达到平衡状态的是_______ (填标号)。
a.断裂2mol C-H键的同时生成1mol C=S键 b.恒容条件下,体系压强不再变化
c.恒容条件下,气体的密度不再变化 d.v正(H2S)=2 v逆(CS2)
(2)在不同温度、反应压强为100kPa,进料H2S的摩尔分数(可看成体积分数)为0.1%~20%(其余为N2)的条件下,对于反应①,H2S分解平衡转化率的结果如图1所示。则T1、T2和T3由大到小的顺序为_______ ;H2S的摩尔分数越大,H2S分解平衡转化率越小的原因是_______ 。

(3)反应①和③的ΔG随温度的影响如图2所示,已知ΔG=-RTlnK(R为常数,T为温度,K为平衡常数),则在1000℃时,反应的自发趋势①_______ ③(填“>”、“<”或“=”)。在1000℃、100kPa反应条件下,将n(H2S):n(CH4):n(N2)=3:2:15的混合气进行反应,达到平衡时n(CS2):n(H2)约为1:4,n(S2)微乎其微,其原因是_______ 。
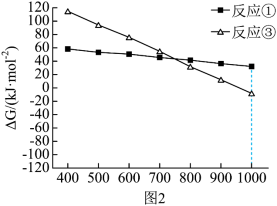
(4)在1000℃、100kPa反应条件下,将n(H2S):n(CH4):n(N2)=3:3:2的混合气进行反应③,达到平衡时,CS2分压与H2S的分压相同。则反应③的Kp=_______ (不用写单位)。
(5)工业废液中含有Zn2+,排放前需处理。向废液中加入由CH3COOH和CH3COONa组成的缓冲溶液调节pH,通入H2S发生反应:Zn2+(aq)+H2S(g)=ZnS(s)+2H+(aq)。处理后的废液中部分微粒浓度如下,则处理后的废液中c(Zn2+)=_______ mol/L。已知Ksp(ZnS)=1.0×10-23,Ka1(H2S)=1.0×10-7,Ka2(H2S)=1.0×10-14,Ka(CH3COOH)=2.0×10-5]
(1)已知下列反应的热化学方程式:
①2H2S(g)
 2H2(g)+S2(g) ΔH1=+180 kJ/mol
2H2(g)+S2(g) ΔH1=+180 kJ/mol②CS2(g)+2H2(g)
 S2(g)+CH4(g) ΔH2=-81 kJ/mol
S2(g)+CH4(g) ΔH2=-81 kJ/mol则反应③CH4(g)+2H2S(g)
 4H2(g)+CS2(g)的ΔH3=
4H2(g)+CS2(g)的ΔH3=a.断裂2mol C-H键的同时生成1mol C=S键 b.恒容条件下,体系压强不再变化
c.恒容条件下,气体的密度不再变化 d.v正(H2S)=2 v逆(CS2)
(2)在不同温度、反应压强为100kPa,进料H2S的摩尔分数(可看成体积分数)为0.1%~20%(其余为N2)的条件下,对于反应①,H2S分解平衡转化率的结果如图1所示。则T1、T2和T3由大到小的顺序为

(3)反应①和③的ΔG随温度的影响如图2所示,已知ΔG=-RTlnK(R为常数,T为温度,K为平衡常数),则在1000℃时,反应的自发趋势①

(4)在1000℃、100kPa反应条件下,将n(H2S):n(CH4):n(N2)=3:3:2的混合气进行反应③,达到平衡时,CS2分压与H2S的分压相同。则反应③的Kp=
(5)工业废液中含有Zn2+,排放前需处理。向废液中加入由CH3COOH和CH3COONa组成的缓冲溶液调节pH,通入H2S发生反应:Zn2+(aq)+H2S(g)=ZnS(s)+2H+(aq)。处理后的废液中部分微粒浓度如下,则处理后的废液中c(Zn2+)=
| 微粒 | H2S | CH3COOH | CH3COO- |
| 浓度/mol/L | 0.20 | 0.10 | 0.20 |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】探究CH3OH合成反应化学平衡的影响因素,有利于提高CH3OH的产率。以CO2、H2为原料合成CH3OH涉及的主要反应如下:
I.CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) △H1=-49.5 kJ•mol-1
II.CO(g)+2H2(g)⇌CH3OH(g) △H2
III.CO2(g)+H2(g)⇌CO(g)+H2O(g) △H3>0
已知CO(g)、H2(g)、CH3OH(g)的标准燃烧热分别为-285.8 kJ•mol-1,-283.0 kJ•mol-1,-761.0 kJ•mol-1
回答下列问题:
(1)△H2=___________ kJ•mol-1。
(2)一定条件下,向体积一定的恒容密闭容器中通入1molCO2和3molH2发生上述反应,达到平衡时,容器中CH3OH(g)为amol,CO为bmol,此时H2O(g)的物质的量为___________ mol(用含a,b的代数式表示,下同),反应III的平衡常数为___________ 。
(3)不同压强下,按照n(CO2):n(H2)=1:3投料,实验测定CH3OH的平衡产率(图1)和CO2的平衡转化率(图2)随温度的变化关系如图所示。

已知:CO2的平衡转化率=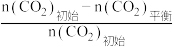 ×100%
×100%
CH3OH的平衡产率=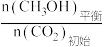 ×100%
×100%
①图1中,一定压强下,CH3OH的平衡产率随温度升高而下降的原因是___________ 。
②图1中,压强p1、p2、p3由大到小的顺序为___________ 。
③图2中T1温度时,三条曲线几乎交于一点的原因是___________ 。
I.CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) △H1=-49.5 kJ•mol-1
II.CO(g)+2H2(g)⇌CH3OH(g) △H2
III.CO2(g)+H2(g)⇌CO(g)+H2O(g) △H3>0
已知CO(g)、H2(g)、CH3OH(g)的标准燃烧热分别为-285.8 kJ•mol-1,-283.0 kJ•mol-1,-761.0 kJ•mol-1
回答下列问题:
(1)△H2=
(2)一定条件下,向体积一定的恒容密闭容器中通入1molCO2和3molH2发生上述反应,达到平衡时,容器中CH3OH(g)为amol,CO为bmol,此时H2O(g)的物质的量为
(3)不同压强下,按照n(CO2):n(H2)=1:3投料,实验测定CH3OH的平衡产率(图1)和CO2的平衡转化率(图2)随温度的变化关系如图所示。

已知:CO2的平衡转化率=
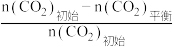 ×100%
×100%CH3OH的平衡产率=
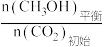 ×100%
×100%①图1中,一定压强下,CH3OH的平衡产率随温度升高而下降的原因是
②图1中,压强p1、p2、p3由大到小的顺序为
③图2中T1温度时,三条曲线几乎交于一点的原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】化学反应中的能量变化,通常表现为热量的变化,研究化学反应中的热量变化具有重要的意义。
(1)下列变化属于吸热反应的是_______ (填序号)。
①液态水气化;②胆矾加热变成白色粉末;③浓硫酸稀释;④氢气还原氧化铜;⑤盐酸和碳酸氢钠反应;⑥氢氧化钾和稀硫酸反应;⑦灼热的木炭与 的反应;⑧
的反应;⑧ 晶体与
晶体与 晶体的反应;⑨甲烷在空气中燃烧的反应
晶体的反应;⑨甲烷在空气中燃烧的反应
(2)已知:
 ;
;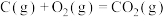
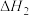
则
_______ 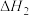 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(3)若
 ,则
,则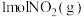 置于密闭容器中充分反应放出的热量
置于密闭容器中充分反应放出的热量_______ 28.45kJ(填“>”、“<”或“=”)。
(4)①已知:
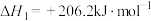

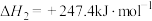
则 与
与 反应生成
反应生成 和
和 的热化学方程式为
的热化学方程式为_______ 。
(5)用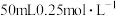 稀
稀 与
与 溶液在如图所示的装置中进行反应。通过测定反应过程中所放出的热量可计算出中和反应反应热。回答下列问题:
溶液在如图所示的装置中进行反应。通过测定反应过程中所放出的热量可计算出中和反应反应热。回答下列问题:_______ 。
②实验中若用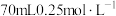 稀
稀 与
与 溶液进行反应,与上述实验相比,所放出的热量
溶液进行反应,与上述实验相比,所放出的热量_______ (填“相等”或“不相等”)。
③已知:中和反应后生成的溶液的比热容 为
为 ,溶液的密度均为
,溶液的密度均为 ,某学习小组三次实验测得温度平均升高3.4℃。则生成
,某学习小组三次实验测得温度平均升高3.4℃。则生成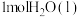 时放出的热量为
时放出的热量为_______ kJ。(结果保留一位小数)
④若上述实验所测中和热数值偏小,产生偏差的原因可能是_______ 。
a.实验装置保温、隔热效果差
b.量筒量取溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定 溶液的温度
溶液的温度
(1)下列变化属于吸热反应的是
①液态水气化;②胆矾加热变成白色粉末;③浓硫酸稀释;④氢气还原氧化铜;⑤盐酸和碳酸氢钠反应;⑥氢氧化钾和稀硫酸反应;⑦灼热的木炭与
 的反应;⑧
的反应;⑧ 晶体与
晶体与 晶体的反应;⑨甲烷在空气中燃烧的反应
晶体的反应;⑨甲烷在空气中燃烧的反应(2)已知:

 ;
;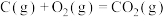
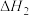
则

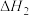 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。(3)若

 ,则
,则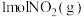 置于密闭容器中充分反应放出的热量
置于密闭容器中充分反应放出的热量(4)①已知:

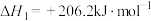

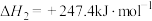
则
 与
与 反应生成
反应生成 和
和 的热化学方程式为
的热化学方程式为(5)用
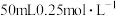 稀
稀 与
与 溶液在如图所示的装置中进行反应。通过测定反应过程中所放出的热量可计算出中和反应反应热。回答下列问题:
溶液在如图所示的装置中进行反应。通过测定反应过程中所放出的热量可计算出中和反应反应热。回答下列问题: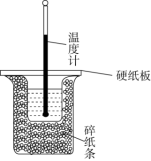
②实验中若用
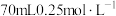 稀
稀 与
与 溶液进行反应,与上述实验相比,所放出的热量
溶液进行反应,与上述实验相比,所放出的热量③已知:中和反应后生成的溶液的比热容
 为
为 ,溶液的密度均为
,溶液的密度均为 ,某学习小组三次实验测得温度平均升高3.4℃。则生成
,某学习小组三次实验测得温度平均升高3.4℃。则生成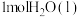 时放出的热量为
时放出的热量为④若上述实验所测中和热数值偏小,产生偏差的原因可能是
a.实验装置保温、隔热效果差
b.量筒量取溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定
 溶液的温度
溶液的温度
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】工业上常用 作还原剂还原铁矿石制得铁单质,实验室中可以用
作还原剂还原铁矿石制得铁单质,实验室中可以用 还原
还原 制得铁粉。
制得铁粉。
已知:①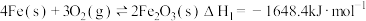
②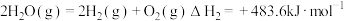
③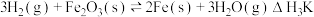
(1)
___________
(2) 可以用碳和水蒸气反应制取,反应的热化学方程式为
可以用碳和水蒸气反应制取,反应的热化学方程式为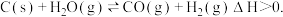 一定条件下该反应达到平衡时,温度、压强对
一定条件下该反应达到平衡时,温度、压强对 产率的影响如图
产率的影响如图 所示。
所示。
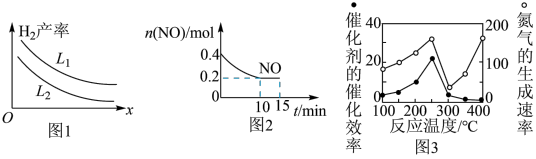
① 表示
表示 ___________ (填“温度”或“压强”); L1___________ L2 (填“ ”、“
”、“ ”或“
”或“ ”)。
”)。
②在一恒容绝热容器中加入一定量的C(s)和 发生反应:
发生反应: ,下列物理量不再改变时一定能说明反应达到平衡状态的是
,下列物理量不再改变时一定能说明反应达到平衡状态的是 ___________ 。(填标号)
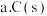 的质量
的质量 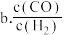
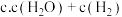
(3)实验证明用活性炭还原法能处理氮的氧化物,有关反应为 。某研究小组向某
。某研究小组向某 密闭容器中加入足量的活性炭和一定量的
密闭容器中加入足量的活性炭和一定量的 ,保持温度和体积不变,反应过程
,保持温度和体积不变,反应过程 中
中 的物质的量随时间的变化如图
的物质的量随时间的变化如图 所示。
所示。
①从反应开始到 时,以
时,以 表示的平均反应速率
表示的平均反应速率
___________ 。该温度时反应的平衡常数
___________ 。
②固定压强为 ,在不同温度下催化剂的催化效率与氮气的生成速率的关系如图
,在不同温度下催化剂的催化效率与氮气的生成速率的关系如图 所示。当氮气的生成速率主要取决于温度时,其影响范围是
所示。当氮气的生成速率主要取决于温度时,其影响范围是 ___________ 。
 作还原剂还原铁矿石制得铁单质,实验室中可以用
作还原剂还原铁矿石制得铁单质,实验室中可以用 还原
还原 制得铁粉。
制得铁粉。已知:①
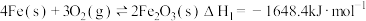
②
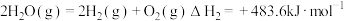
③
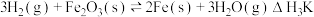
(1)

(2)
 可以用碳和水蒸气反应制取,反应的热化学方程式为
可以用碳和水蒸气反应制取,反应的热化学方程式为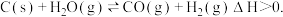 一定条件下该反应达到平衡时,温度、压强对
一定条件下该反应达到平衡时,温度、压强对 产率的影响如图
产率的影响如图 所示。
所示。
①
 表示
表示  ”、“
”、“ ”或“
”或“ ”)。
”)。②在一恒容绝热容器中加入一定量的C(s)和
 发生反应:
发生反应: ,下列物理量不再改变时一定能说明反应达到平衡状态的是
,下列物理量不再改变时一定能说明反应达到平衡状态的是 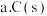 的质量
的质量 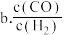
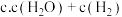
(3)实验证明用活性炭还原法能处理氮的氧化物,有关反应为
 。某研究小组向某
。某研究小组向某 密闭容器中加入足量的活性炭和一定量的
密闭容器中加入足量的活性炭和一定量的 ,保持温度和体积不变,反应过程
,保持温度和体积不变,反应过程 中
中 的物质的量随时间的变化如图
的物质的量随时间的变化如图 所示。
所示。①从反应开始到
 时,以
时,以 表示的平均反应速率
表示的平均反应速率

②固定压强为
 ,在不同温度下催化剂的催化效率与氮气的生成速率的关系如图
,在不同温度下催化剂的催化效率与氮气的生成速率的关系如图 所示。当氮气的生成速率主要取决于温度时,其影响范围是
所示。当氮气的生成速率主要取决于温度时,其影响范围是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】 催化重整不仅可以得到合成气(CO和
催化重整不仅可以得到合成气(CO和 ),还对温室气体的减排具有重要意义。回答下列问题:
),还对温室气体的减排具有重要意义。回答下列问题:
(1) 催化重整反应为
催化重整反应为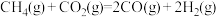 。
。
已知: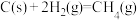 ∆H=-75
∆H=-75
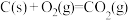 ∆H=-394
∆H=-394
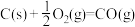 ∆H=-111
∆H=-111
该催化重整反应的∆H________  。有利于提高
。有利于提高 平衡转化率的条件是
平衡转化率的条件是________ (填标号)。
A.高温低压B.低温高压C.高温高压D.低温低压
某温度下,在体积为2L的容器中加入2mol 、1mol
、1mol 以及催化剂进行重整反应,达到平衡时
以及催化剂进行重整反应,达到平衡时 的转化率是50%,其平衡常数为
的转化率是50%,其平衡常数为__________ 。
(2)反应中催化剂活性会因积碳反应而降低,同时存在的消碳反应则使积碳量减少。相关数据如下表:
由上表判断,催化剂X________ Y(填“优于”或“劣于”),理由是__________________ 。在反应进料气组成、压强及反应时间相同的情况下,某催化剂表面的积碳量随温度的变化关系如图所示,升高温度时,下列关于积碳反应、消碳反应的平衡常数(K)和速率(v)的叙述正确的是__________ (填标号)。
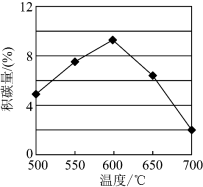
A.K积、K消均增加B.v消减小、v积增加
C.K积减小、K消增加D.v消增加的倍数比v积增加的倍数大
 催化重整不仅可以得到合成气(CO和
催化重整不仅可以得到合成气(CO和 ),还对温室气体的减排具有重要意义。回答下列问题:
),还对温室气体的减排具有重要意义。回答下列问题:(1)
 催化重整反应为
催化重整反应为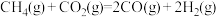 。
。已知:
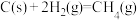 ∆H=-75
∆H=-75
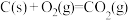 ∆H=-394
∆H=-394
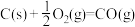 ∆H=-111
∆H=-111
该催化重整反应的∆H
 。有利于提高
。有利于提高 平衡转化率的条件是
平衡转化率的条件是A.高温低压B.低温高压C.高温高压D.低温低压
某温度下,在体积为2L的容器中加入2mol
 、1mol
、1mol 以及催化剂进行重整反应,达到平衡时
以及催化剂进行重整反应,达到平衡时 的转化率是50%,其平衡常数为
的转化率是50%,其平衡常数为(2)反应中催化剂活性会因积碳反应而降低,同时存在的消碳反应则使积碳量减少。相关数据如下表:
积碳反应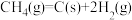 | 消碳反应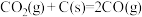 | ||
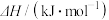 | 75 | 172 | |
活化能/( ) ) | 催化剂X | 33 | 91 |
| 催化剂Y | 43 | 72 | |
由上表判断,催化剂X

A.K积、K消均增加B.v消减小、v积增加
C.K积减小、K消增加D.v消增加的倍数比v积增加的倍数大
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】CH4既是重要的清洁能源也是一种重要的化工原料。以CO2、H2为原料合成CH4涉及的主要反应如下:
Ⅰ:CO2(g)+4H2(g) CH4(g)+2H2O(g) △H1
CH4(g)+2H2O(g) △H1
Ⅱ: CO2(g)+H2(g) CO(g)+H2O(g) △H2=+41.2 kJ/mol
CO(g)+H2O(g) △H2=+41.2 kJ/mol
常温常压下,H2(g)和CH4(g)的摩尔燃烧焓分别为-285.8 kJ/mol和-890.3 kJ/mol;H2O(l)=H2O(g)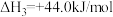
(1)△H1=___________ kJ/mol。
(2)一定条件下,向恒容密闭容器中通入1 mol CO2和3 mol H2发生上述反应,达到平衡时,容器中CH4(g)为a mol,H2O(g)为b mol,则反应Ⅱ的平衡常数为___________ (用含a、b的代数式表示)。
(3)为探究CO2(g)+4H2(g) CH4(g)+2H2O(g)的反应速率与浓度的关系,起始时,向恒容密闭容器中通入浓度均为1.0 mol/L CO2与H2。平衡时,根据相关数据绘制出两条反应速率-浓度关系曲线:v正-c(CO2)和v逆-c(H2O)。
CH4(g)+2H2O(g)的反应速率与浓度的关系,起始时,向恒容密闭容器中通入浓度均为1.0 mol/L CO2与H2。平衡时,根据相关数据绘制出两条反应速率-浓度关系曲线:v正-c(CO2)和v逆-c(H2O)。

则与曲线v正-c(CO2)相对应的是上图中曲线___________ (填“甲”或“乙”);该反应达到平衡后,某一时刻降低温度,重新达到平衡,平衡常数___________ (填“增大”或“减小”),则此时曲线甲对应的平衡点可能为___________ (填字母,下同),曲线乙对应的平衡点可能为___________ 。
Ⅰ:CO2(g)+4H2(g)
 CH4(g)+2H2O(g) △H1
CH4(g)+2H2O(g) △H1Ⅱ: CO2(g)+H2(g)
 CO(g)+H2O(g) △H2=+41.2 kJ/mol
CO(g)+H2O(g) △H2=+41.2 kJ/mol常温常压下,H2(g)和CH4(g)的摩尔燃烧焓分别为-285.8 kJ/mol和-890.3 kJ/mol;H2O(l)=H2O(g)
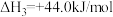
(1)△H1=
(2)一定条件下,向恒容密闭容器中通入1 mol CO2和3 mol H2发生上述反应,达到平衡时,容器中CH4(g)为a mol,H2O(g)为b mol,则反应Ⅱ的平衡常数为
(3)为探究CO2(g)+4H2(g)
 CH4(g)+2H2O(g)的反应速率与浓度的关系,起始时,向恒容密闭容器中通入浓度均为1.0 mol/L CO2与H2。平衡时,根据相关数据绘制出两条反应速率-浓度关系曲线:v正-c(CO2)和v逆-c(H2O)。
CH4(g)+2H2O(g)的反应速率与浓度的关系,起始时,向恒容密闭容器中通入浓度均为1.0 mol/L CO2与H2。平衡时,根据相关数据绘制出两条反应速率-浓度关系曲线:v正-c(CO2)和v逆-c(H2O)。
则与曲线v正-c(CO2)相对应的是上图中曲线
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】甲醇是重要的化工原料。利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主要反应如下:
① CO(g)+2H2(g)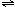 CH3OH(g) ΔH1 =-99kJ·mol-1
CH3OH(g) ΔH1 =-99kJ·mol-1
② CO2(g)+3H2(g)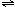 CH3OH(g)+H2O(g) ΔH2
CH3OH(g)+H2O(g) ΔH2
③ CO2(g)+H2(g)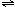 CO(g)+H2O(g) ΔH3=+ 41 kJ·mol-1
CO(g)+H2O(g) ΔH3=+ 41 kJ·mol-1
(1)ΔH2=______ kJ·mol-1,②反应正向的熵变ΔS______ 0(填“>”“<”或“=”)。
(2)在容积为2 L的密闭容器中,充入一定量CO2和H2合成甲醇(上述②反应),在其他条件不变时,温度T1、T2对反应的影响图象如图。
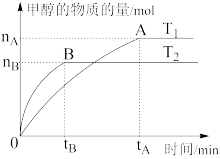
①温度为T1时,从反应到平衡,生成甲醇的平均速率为v(CH3OH)=_____ mol·L-1·min-1。
②图示的温度T1______ T2(填写“>”、“<”或“=”)
(3)T1温度时,将2 mol CO2和6 mol H2充入2 L密闭容器中,充分反应(上述②反应)达到平衡后,若CO2转化率为50%,此时容器内的压强与起始压强之比为________ 。欲提高CO2转化率,可采取的措施是_________________ (填一种即可)
① CO(g)+2H2(g)
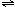 CH3OH(g) ΔH1 =-99kJ·mol-1
CH3OH(g) ΔH1 =-99kJ·mol-1② CO2(g)+3H2(g)
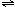 CH3OH(g)+H2O(g) ΔH2
CH3OH(g)+H2O(g) ΔH2③ CO2(g)+H2(g)
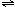 CO(g)+H2O(g) ΔH3=+ 41 kJ·mol-1
CO(g)+H2O(g) ΔH3=+ 41 kJ·mol-1(1)ΔH2=
(2)在容积为2 L的密闭容器中,充入一定量CO2和H2合成甲醇(上述②反应),在其他条件不变时,温度T1、T2对反应的影响图象如图。

①温度为T1时,从反应到平衡,生成甲醇的平均速率为v(CH3OH)=
②图示的温度T1
(3)T1温度时,将2 mol CO2和6 mol H2充入2 L密闭容器中,充分反应(上述②反应)达到平衡后,若CO2转化率为50%,此时容器内的压强与起始压强之比为
您最近一年使用:0次
【推荐2】已知化学反应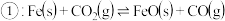 ,其平衡常数为
,其平衡常数为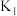 ,化学反应
,化学反应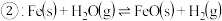 ,其平衡常数为
,其平衡常数为 ,在温度
,在温度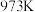 和
和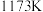 情况下,
情况下,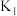 、
、 的值分别如下:
的值分别如下:
请完成下列问题:
(1)通过表格中的数值可以推断:反应 是
是_______  填“吸热”或“放热”
填“吸热”或“放热” 反应。
反应。
(2)现有反应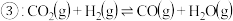 ,请你写出该反应的平衡常数
,请你写出该反应的平衡常数 的表达式:
的表达式: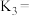
_______ 。
(3)在相同温度下,根据反应 与
与 可推导出
可推导出 与
与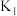 、
、 之间的关系式
之间的关系式_______ ,据此关系式及上表数据,也能推断出反应 是
是_______ (填“吸热”或“放热”)反应。
(4)要使反应 在一定条件下建立的平衡向正反应方向移动,可采取的措施有_______(填写字母序号,下同)。
在一定条件下建立的平衡向正反应方向移动,可采取的措施有_______(填写字母序号,下同)。
(5)已知 的可逆反应
的可逆反应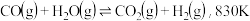 时,若起始时:
时,若起始时: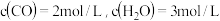 ,平衡时
,平衡时 的转化率为
的转化率为 ,水蒸气的转化率为
,水蒸气的转化率为_______ ; 的数值为
的数值为_______ 。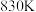 ,若只将起始时
,若只将起始时 改为
改为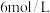 ,则水蒸气的转化率为
,则水蒸气的转化率为_______ 。
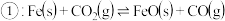 ,其平衡常数为
,其平衡常数为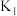 ,化学反应
,化学反应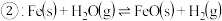 ,其平衡常数为
,其平衡常数为 ,在温度
,在温度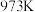 和
和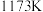 情况下,
情况下,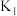 、
、 的值分别如下:
的值分别如下:| 温度 | 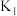 |  |
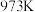 | 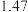 | 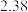 |
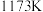 |  | 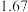 |
(1)通过表格中的数值可以推断:反应
 是
是 填“吸热”或“放热”
填“吸热”或“放热” 反应。
反应。(2)现有反应
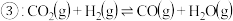 ,请你写出该反应的平衡常数
,请你写出该反应的平衡常数 的表达式:
的表达式: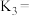
(3)在相同温度下,根据反应
 与
与 可推导出
可推导出 与
与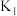 、
、 之间的关系式
之间的关系式 是
是(4)要使反应
 在一定条件下建立的平衡向正反应方向移动,可采取的措施有_______(填写字母序号,下同)。
在一定条件下建立的平衡向正反应方向移动,可采取的措施有_______(填写字母序号,下同)。| A.增大压强 | B.体积不变时充入稀有气体 | C.升高温度 | D.使用合适的催化剂 |
 的可逆反应
的可逆反应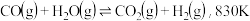 时,若起始时:
时,若起始时: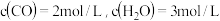 ,平衡时
,平衡时 的转化率为
的转化率为 ,水蒸气的转化率为
,水蒸气的转化率为 的数值为
的数值为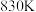 ,若只将起始时
,若只将起始时 改为
改为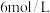 ,则水蒸气的转化率为
,则水蒸气的转化率为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】I.已知在常温常压下:
①2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(g) △H=_1275.6kJ•mol-1
②H2O(l)═H2O(g) △H=+44.0kJ•mol-1
写出表示甲醇燃烧热的热化学方程式:___________________ 。
Ⅱ.甲醇可以与水蒸气反应生成氢气,反应方程式如下:
CH3OH(g) + H2O(g) CO2(g) + 3H2(g) ;△H>0
CO2(g) + 3H2(g) ;△H>0
(1)一定条件下,向体积为2L的恒容密闭容器中充入1molCH3OH(g)和3molH2O(g),20s后,测得混合气体的压强是反应前的1.2倍,则用甲醇表示该反应的速率为__ 。
(2)判断⑴中可逆反应达到平衡状态的依据是(填序号)_____________ 。
①v正(CH3OH) = 3v逆(H2) ②混合气体的密度不变
③混合气体的平均相对分子质量不变
④CH3OH、H2O、CO2、H2的浓度都不再发生变化
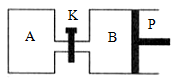
(3)右图中P是可自由平行滑动的活塞,关闭K,在相同温度时,向A容器中充入
1molCH3OH(g)和2molH2O(g),向B容器中充入1.2molCH3OH(g) 和2.4molH2O(g),两容器分别发生上述反应。已知起始时容器A和B的体积均为aL,反应达到平衡时容器B的体积为1.5aL,容器B中CH3OH
转化率为________ ;维持其他条件不变,若打开K一段时间后重新达到平衡,容器B的体积为________ L(连通管中气体体积忽略不计,且不考虑温度的影响)。
Ⅲ.如图甲、乙是电化学实验装置。请回答下列问题:
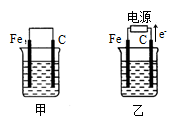
(1)若两池中均盛放CuSO4溶液,甲池中石墨棒上的电极反应式为_______________ .
(2)若乙池中盛放饱和NaCl溶液,则乙池中发生反应的化学方程式为___________ .
①2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(g) △H=_1275.6kJ•mol-1
②H2O(l)═H2O(g) △H=+44.0kJ•mol-1
写出表示甲醇燃烧热的热化学方程式:
Ⅱ.甲醇可以与水蒸气反应生成氢气,反应方程式如下:
CH3OH(g) + H2O(g)
 CO2(g) + 3H2(g) ;△H>0
CO2(g) + 3H2(g) ;△H>0(1)一定条件下,向体积为2L的恒容密闭容器中充入1molCH3OH(g)和3molH2O(g),20s后,测得混合气体的压强是反应前的1.2倍,则用甲醇表示该反应的速率为
(2)判断⑴中可逆反应达到平衡状态的依据是(填序号)
①v正(CH3OH) = 3v逆(H2) ②混合气体的密度不变
③混合气体的平均相对分子质量不变
④CH3OH、H2O、CO2、H2的浓度都不再发生变化
(3)右图中P是可自由平行滑动的活塞,关闭K,在相同温度时,向A容器中充入
1molCH3OH(g)和2molH2O(g),向B容器中充入1.2molCH3OH(g) 和2.4molH2O(g),两容器分别发生上述反应。已知起始时容器A和B的体积均为aL,反应达到平衡时容器B的体积为1.5aL,容器B中CH3OH
转化率为

Ⅲ.如图甲、乙是电化学实验装置。请回答下列问题:

(1)若两池中均盛放CuSO4溶液,甲池中石墨棒上的电极反应式为
(2)若乙池中盛放饱和NaCl溶液,则乙池中发生反应的化学方程式为
您最近一年使用:0次



