固体化合物X由三种元素组成,是具有良好前景的储氢材料,为了研究它的组成与性质,设计并完成了如图实验:
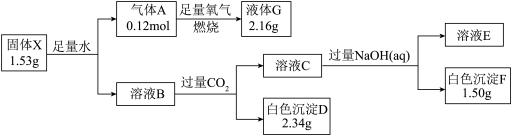
已知: ① X的焰色反应为砖红色 ② 溶液B中只有一种溶质
(1)X所含的三种元素为H、___ 、___ ,X化学是为___ 。
(2)固体X与足量水反应的化学方程式是____________________________________________________ 。

已知: ① X的焰色反应为砖红色 ② 溶液B中只有一种溶质
(1)X所含的三种元素为H、
(2)固体X与足量水反应的化学方程式是
更新时间:2023-01-12 14:36:15
|
相似题推荐
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐1】12-钨磷酸(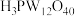 ,分子量:2880)是杂多化合物的代表物之一,实验室可通过乙醚萃取法合成。涉及的部分物质性质见下表:
,分子量:2880)是杂多化合物的代表物之一,实验室可通过乙醚萃取法合成。涉及的部分物质性质见下表:
【制备步骤】
Ⅰ.12-钨磷酸钠(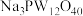 )溶液的制备
)溶液的制备
取 (分子量:330)和
(分子量:330)和 (分子量:178)于烧杯中,溶于80mL热水,边加热边搅拌下,向溶液中以细流加入14 mL浓盐酸,继续加热30 s。
(分子量:178)于烧杯中,溶于80mL热水,边加热边搅拌下,向溶液中以细流加入14 mL浓盐酸,继续加热30 s。
Ⅱ.12-钨磷酸的制备
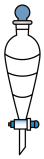
将烧杯中液体一并转移至分液漏斗中,加入205 mL乙醚及6 mL 6 mol/L的盐酸(均过量),振荡后静置,液体分三层,分出最下层液体于仪器 X 中,在通风橱内,置于热水浴中加热蒸除少量乙醚,得白色12-钨磷酸固体8.64 g。
(1)请用离子方程式表示步骤Ⅰ中12-钨磷酸钠的制备原理___________ ;
(2)“仪器X”为___________ ;
(3)步骤Ⅱ中,振荡分液漏斗制备12-钨磷酸时,需不时拧开分液漏斗活塞进行放气,这样操作的目的是___________ ;
(4)步骤Ⅱ中“液体分为三层”,最上层液体的主要成分为___________ (填代号);
a.乙醚 b.12-钨磷酸钠溶液 c.水 d.NaCl溶液
(5)步骤Ⅱ蒸除乙醚时,采用水浴加热而不采用明火加热的目的是___________ ;
(6)制备出的12-钨磷酸常因有灰尘、纸屑等有机纤维杂质落入而形成蓝色的“杂多蓝”,出现这一现象时,加入适量过氧化氢或溴水可使其恢复。上述实验现象可体现出12-钨磷酸常温下具有较强的___________ (填“氧化性”或“还原性”);
(7)根据上述实验数据计算,该实验的产率为___________ (设所得白色固体均为无水12-钨磷酸,结果保留两位有效数字);
(8)通过对X-射线衍射结果分析,得到12-钨磷酸根离子结构如下图,请回答:___________ ;
②12-钨磷酸根离子中存在___________ 种处于不同化学环境的氧原子。
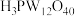 ,分子量:2880)是杂多化合物的代表物之一,实验室可通过乙醚萃取法合成。涉及的部分物质性质见下表:
,分子量:2880)是杂多化合物的代表物之一,实验室可通过乙醚萃取法合成。涉及的部分物质性质见下表:| 物质 | 性质 |
| 乙醚 | 无色液体,密度比水小且难溶于水,沸点34.5℃ |
| 12-钨磷酸 | 白色固体,能溶于水,常温下极易与乙醚形成密度大于水且难溶于水的油状醚合物 |
Ⅰ.12-钨磷酸钠(
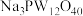 )溶液的制备
)溶液的制备取
 (分子量:330)和
(分子量:330)和 (分子量:178)于烧杯中,溶于80mL热水,边加热边搅拌下,向溶液中以细流加入14 mL浓盐酸,继续加热30 s。
(分子量:178)于烧杯中,溶于80mL热水,边加热边搅拌下,向溶液中以细流加入14 mL浓盐酸,继续加热30 s。Ⅱ.12-钨磷酸的制备
将烧杯中液体一并转移至分液漏斗中,加入205 mL乙醚及6 mL 6 mol/L的盐酸(均过量),振荡后静置,液体分三层,分出最下层液体于
(1)请用离子方程式表示步骤Ⅰ中12-钨磷酸钠的制备原理
(2)“仪器X”为
(3)步骤Ⅱ中,振荡分液漏斗制备12-钨磷酸时,需不时拧开分液漏斗活塞进行放气,这样操作的目的是
(4)步骤Ⅱ中“液体分为三层”,最上层液体的主要成分为
a.乙醚 b.12-钨磷酸钠溶液 c.水 d.NaCl溶液
(5)步骤Ⅱ蒸除乙醚时,采用水浴加热而不采用明火加热的目的是
(6)制备出的12-钨磷酸常因有灰尘、纸屑等有机纤维杂质落入而形成蓝色的“杂多蓝”,出现这一现象时,加入适量过氧化氢或溴水可使其恢复。上述实验现象可体现出12-钨磷酸常温下具有较强的
(7)根据上述实验数据计算,该实验的产率为
(8)通过对X-射线衍射结果分析,得到12-钨磷酸根离子结构如下图,请回答:
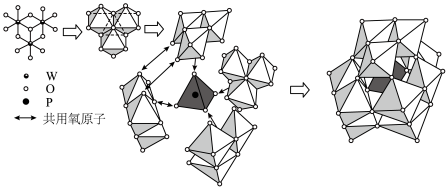
②12-钨磷酸根离子中存在
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐2】研究小组以 (绿色固体)、
(绿色固体)、 、THF(四氯呋喃,液体)等物质为原料制备固体配合物
、THF(四氯呋喃,液体)等物质为原料制备固体配合物 ,该配合物可作为有机反应的催化剂
,该配合物可作为有机反应的催化剂
(1)无水 (紫色固体,易升华)的制备装置如图所示(夹持装置略)。
(紫色固体,易升华)的制备装置如图所示(夹持装置略)。

①仪器a的名称为________ 。
②本实验持续通入 的目的有赶走体系中原有的空气、
的目的有赶走体系中原有的空气、________ 。
③反应管的温度升到660℃时发生反应,生成 和
和 (光气),其化学方程式为
(光气),其化学方程式为________ 。 有剧毒,与水反应生成两种酸性气体,b装置中生成的盐是
有剧毒,与水反应生成两种酸性气体,b装置中生成的盐是________ (填化学式)。
④反应管右端有15cm在加热炉外,其作用是________________ 。
(2) 的合成装置如图所示(搅拌和夹持装置咯)
的合成装置如图所示(搅拌和夹持装置咯)

将制备的无水 和极少量锌粉放入滤纸套筒内,双颈烧瓶中加入足量无水THF。制备反应的原理为
和极少量锌粉放入滤纸套筒内,双颈烧瓶中加入足量无水THF。制备反应的原理为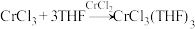 。
。
实验时烧瓶中THF受热蒸发,蒸汽沿蒸汽导管2上升至球形冷凝管,冷凝后滴入滤纸套筒1中,与滤纸套筒内的物质接触。当液面达到虹吸管3顶端时,经虹吸管3返回双颈烧瓶.从而实现了THF与 的连续反应及产物的连续萃取。
的连续反应及产物的连续萃取。
①锌粉的作用是________________ (用化学方程式表示)。
② 和
和 在THF的溶解性分别为
在THF的溶解性分别为________ 、________ (填“溶”或“不溶”)。
③合成反应完成后,取下双颈烧瓶,蒸发THF得到固体产品6.7410g。则该实验的产率为________ %。[已知: 的摩尔质量为152g/mol;
的摩尔质量为152g/mol; 的摩尔质量为374.5g/mol]
的摩尔质量为374.5g/mol]
 (绿色固体)、
(绿色固体)、 、THF(四氯呋喃,液体)等物质为原料制备固体配合物
、THF(四氯呋喃,液体)等物质为原料制备固体配合物 ,该配合物可作为有机反应的催化剂
,该配合物可作为有机反应的催化剂(1)无水
 (紫色固体,易升华)的制备装置如图所示(夹持装置略)。
(紫色固体,易升华)的制备装置如图所示(夹持装置略)。
①仪器a的名称为
②本实验持续通入
 的目的有赶走体系中原有的空气、
的目的有赶走体系中原有的空气、③反应管的温度升到660℃时发生反应,生成
 和
和 (光气),其化学方程式为
(光气),其化学方程式为 有剧毒,与水反应生成两种酸性气体,b装置中生成的盐是
有剧毒,与水反应生成两种酸性气体,b装置中生成的盐是④反应管右端有15cm在加热炉外,其作用是
(2)
 的合成装置如图所示(搅拌和夹持装置咯)
的合成装置如图所示(搅拌和夹持装置咯)
将制备的无水
 和极少量锌粉放入滤纸套筒内,双颈烧瓶中加入足量无水THF。制备反应的原理为
和极少量锌粉放入滤纸套筒内,双颈烧瓶中加入足量无水THF。制备反应的原理为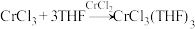 。
。实验时烧瓶中THF受热蒸发,蒸汽沿蒸汽导管2上升至球形冷凝管,冷凝后滴入滤纸套筒1中,与滤纸套筒内的物质接触。当液面达到虹吸管3顶端时,经虹吸管3返回双颈烧瓶.从而实现了THF与
 的连续反应及产物的连续萃取。
的连续反应及产物的连续萃取。①锌粉的作用是
②
 和
和 在THF的溶解性分别为
在THF的溶解性分别为③合成反应完成后,取下双颈烧瓶,蒸发THF得到固体产品6.7410g。则该实验的产率为
 的摩尔质量为152g/mol;
的摩尔质量为152g/mol; 的摩尔质量为374.5g/mol]
的摩尔质量为374.5g/mol]
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
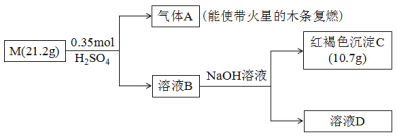
【推荐3】X通常状况下是一种红黄色气体,相对分子质量小于100,含有三种常见短周期元素。为研究X的组成,5.895g的X分三等份进行实验,过程如下(气体体积已折算至标准状况):

请回答:
(1)X的化学式为_______ 。溶液A的成分为_______ 。
(2)X与 反应的化学方程式为
反应的化学方程式为_______ 。
(3)金(Au)可溶于浓B溶液生成C和金的一价配离子(与 具有相同的空间结构),写出该反应的化学方程式:
具有相同的空间结构),写出该反应的化学方程式:_______ 。
(4)设计一个实验方案,探究溶液F中溶质的阳离子成分:_______ 。

请回答:
(1)X的化学式为
(2)X与
 反应的化学方程式为
反应的化学方程式为(3)金(Au)可溶于浓B溶液生成C和金的一价配离子(与
 具有相同的空间结构),写出该反应的化学方程式:
具有相同的空间结构),写出该反应的化学方程式:(4)设计一个实验方案,探究溶液F中溶质的阳离子成分:
您最近一年使用:0次
【推荐1】下图表示各物质之间的转化关系。已知:常温下B、D、F、G、I、J是气体,F、G是空气中的主要成分,D是一种碱性气体;A中阴、阳离子个数比是 ,E是一种黑色氧化物,H是紫红色金属单质(部分生成物和反应条件省略)
,E是一种黑色氧化物,H是紫红色金属单质(部分生成物和反应条件省略)

请按要求回答下列问题:
(1)A物质是_______ ;X物质是_______ ;K物质是_______ (均写化学式)。
(2)反应③的化学方程式是_______ 。
(3)反应①中产生标准状况下1.12L气体F,则转移的电子数目是_______ 。
(4)反应②的化学反应方程式为_______ ;作氧化剂的是_______ 。
(5)某小组同学用如图所示装置制取氨,并探究其性质。

①大试管中发生的反应的化学方程式是_______ 。
②请将方框中的收集装置补充完整_______ ,解释采用这种收集方法的原因是_______ 。
③甲同学用如图所示的装置进行尾气处理,乙同学认为不合理,其理由是:_______ 。

 ,E是一种黑色氧化物,H是紫红色金属单质(部分生成物和反应条件省略)
,E是一种黑色氧化物,H是紫红色金属单质(部分生成物和反应条件省略)
请按要求回答下列问题:
(1)A物质是
(2)反应③的化学方程式是
(3)反应①中产生标准状况下1.12L气体F,则转移的电子数目是
(4)反应②的化学反应方程式为
(5)某小组同学用如图所示装置制取氨,并探究其性质。

①大试管中发生的反应的化学方程式是
②请将方框中的收集装置补充完整
③甲同学用如图所示的装置进行尾气处理,乙同学认为不合理,其理由是:

您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
【推荐2】原子序数依次增大的A、B、C、D、E五种短周期元素,可以两两形成多种原子个数比为1:1的化合物,其中的甲、乙、丙、丁4种化合物有两种属于离子化合物。A、B的原子序数之和是元素D的一半。B既是组成蛋白质的必要元素,也是某些化肥的组成元素。只有C为金属元素,焰色反应呈黄色。请回答下列问题:
(1)元素E 的原子结构示意图为 。
(2)B和D形成的化合物甲,其相对分子质量在170~190之间,且D的质量分数约为70%,则该化合物的化学式为 。
(3)A和B形成的化合物乙为B4A4,在一定条件下可以电离出两种离子,其中一种为10e-的离子,该物质一定条件下的电离方程式为 。
(4)化合物C2D溶液在空气中长期放置会变质生成丙C2D2,用化学方程式表示该过程 。
(5)D和E形成的化合物丁中所有原子均满足8电子稳定结构,该化合物的电子式为 ;该物质遇水剧烈反应,产生有刺激性气味的混合气体X和Y,同时还有固体单质产生,已知X是能使品红褪色的气体,Y在标准状态下的密度为1.63g/L,该混合气体相对于H2的密度为21,上述过程对应的化学方程式为 。
某研究小组同学为确定干燥的X和Y混合气体中Y 的存在,设计方案如下:把干燥的X和Y与干燥的NH3混合,出现白烟,则证明有Y气体,你认为此方案 (填“正确”或“不正确”),理由是 。
(1)元素E 的原子结构示意图为 。
(2)B和D形成的化合物甲,其相对分子质量在170~190之间,且D的质量分数约为70%,则该化合物的化学式为 。
(3)A和B形成的化合物乙为B4A4,在一定条件下可以电离出两种离子,其中一种为10e-的离子,该物质一定条件下的电离方程式为 。
(4)化合物C2D溶液在空气中长期放置会变质生成丙C2D2,用化学方程式表示该过程 。
(5)D和E形成的化合物丁中所有原子均满足8电子稳定结构,该化合物的电子式为 ;该物质遇水剧烈反应,产生有刺激性气味的混合气体X和Y,同时还有固体单质产生,已知X是能使品红褪色的气体,Y在标准状态下的密度为1.63g/L,该混合气体相对于H2的密度为21,上述过程对应的化学方程式为 。
某研究小组同学为确定干燥的X和Y混合气体中Y 的存在,设计方案如下:把干燥的X和Y与干燥的NH3混合,出现白烟,则证明有Y气体,你认为此方案 (填“正确”或“不正确”),理由是 。
您最近一年使用:0次
【推荐3】将黑色固体单质甲加热至红热,投入黄色的溶液乙中,反应后产生混合气体A,A在常温下不与空气反应,根据图中转化关系回答下列问题:

(1)甲是_______ ,乙是_______ ,丙是_______ 。
(2)混合气体A的主要成分是_______ 。
(3)丙与溶液C反应的化学方程式是_______ 。
(4)若32.0 g丙与一定量的溶液乙反应,当丙反应完时,共产生13.44 L(标准状况下)气体,则消耗的溶液乙中溶质的物质的量为_______ 。

(1)甲是
(2)混合气体A的主要成分是
(3)丙与溶液C反应的化学方程式是
(4)若32.0 g丙与一定量的溶液乙反应,当丙反应完时,共产生13.44 L(标准状况下)气体,则消耗的溶液乙中溶质的物质的量为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】二氧化氯(ClO2,黄绿色易溶于水的气体)是高效、低毒的消毒剂,答下列问题:
(1)工业上可用KC1O3与Na2SO3在H2SO4存在下制得ClO2,该反应氧化剂与还原剂物质的量之比为________________________ ;
(2)实验室用NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料,通过以下过程制备ClO2:
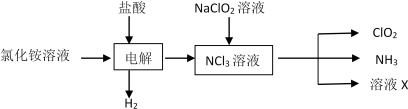
①电解时发生反应的化学方程式为________________________ ;
②设计实验来确定溶液X的成分,请补充完成实验步骤和现象
③除去ClO2中的NH3可选用的试剂是_______ (填标号);
a.水 b.碱石灰 C.浓硫酸 d.饱和食盐水
(3)O2处理过的饮用水会含有一定量的亚氯酸盐。若要除去超标的亚氯酸盐,下列物质最适宜的是_______ 填标号)。
a.明矾b.碘化钾c.盐酸d.硫酸亚铁
(1)工业上可用KC1O3与Na2SO3在H2SO4存在下制得ClO2,该反应氧化剂与还原剂物质的量之比为
(2)实验室用NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料,通过以下过程制备ClO2:

①电解时发生反应的化学方程式为
②设计实验来确定溶液X的成分,请补充完成实验步骤和现象
| 实验步骤 | 实验现象 | 实验结论 |
| I: 取一根铂丝 | 溶液X中含有钠离子 | |
| II: 取少许溶液X于一支试管中,滴加 | 溶液X中含有氯离子 |
a.水 b.碱石灰 C.浓硫酸 d.饱和食盐水
(3)O2处理过的饮用水会含有一定量的亚氯酸盐。若要除去超标的亚氯酸盐,下列物质最适宜的是
a.明矾b.碘化钾c.盐酸d.硫酸亚铁
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐2】有关物质的转化关系如下图所示,部分物质与条件已略去。已知A由两种元素组成,且其式量为65,B是由两种元素组成的黑色粉末,C是空气中含量最多的气体,D是白色粉末,且其焰色反应呈黄色,E是一种紫红色金属,H是一种红棕色气体,I是最常见的液体,K是一种强碱。

(1)A的化学式为____________ 。
(2)C的结构式为____________ 。
(3)D的电子式为____________ 。
(4)K中含有的化学键类型有____________ ,属于____________ (填离子化合物或者共价化合物)。
(5)写出反应①的化学方程式:______________________ 。
(6)写出反应②的离子方程式:_________________________ 。

(1)A的化学式为
(2)C的结构式为
(3)D的电子式为
(4)K中含有的化学键类型有
(5)写出反应①的化学方程式:
(6)写出反应②的离子方程式:
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐1】工业制得的氮化铝(AlN)产品中常含有少量Al4C3、Al2O3、C等杂质。某同学设计如下实验分别测定氮化铝(AlN)样品中AlN和Al4C3的质量分数。已知①Al4C3与硫酸反应可生成CH4;②AlN溶于强酸产生铵盐,溶于强碱生成氨气(忽略NH3在强碱性溶液中的溶解);③该实验条件下的气体摩尔体积为VmL/mol,实验装置如下(量气管为碱式滴定管改装)
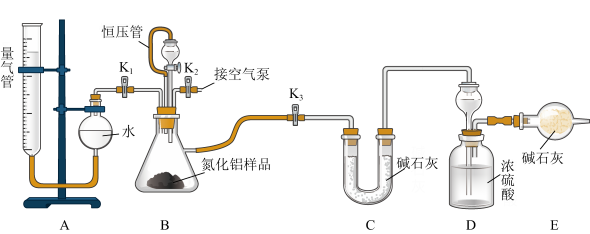
实验过程:连好装置后,检验装置的气密性;称得装置D的初始质量为ag;称取bg AlN样品置于装置B的锥形瓶中,各装置中加入相应药品,重新连好装置;读取量气管中液面的初始读数为x mL(量气装置左右液面相平)。
(1)①若先测量Al4C3质量分数,对K1、K2、K3三个活塞的操作是关闭活塞______ ,打开活塞______ 。
②当_____ 时,说明反应已经结束。读取读数之前,应对量气管进行的操作为____________ ;若量气管中的液面高于右侧球形容器中的液面,所测气体体积______ (填“偏大”、“偏小”或“无影响”)。
③记录滴定管的读数为y mL,则Al4C3的质量分数为_________ (用可能含a、b、x、y、Vm的代数式表示)。
④若无恒压管,对所测Al4C3质量分数的影响是______ (填“偏大”、“偏小”或“无影响”)。
(2)若先测量AlN质量分数:首先关闭活塞K1,打开活塞K3,通过分液漏斗加入过量的某物质,写出AlN与过量的某物质发生反应的离子方程式为__________ ;反应完成后,__________ (填该步应进行的操作),最后称得装置D的质量为cg,进而测量AlN的质量分数。

实验过程:连好装置后,检验装置的气密性;称得装置D的初始质量为ag;称取bg AlN样品置于装置B的锥形瓶中,各装置中加入相应药品,重新连好装置;读取量气管中液面的初始读数为x mL(量气装置左右液面相平)。
(1)①若先测量Al4C3质量分数,对K1、K2、K3三个活塞的操作是关闭活塞
②当
③记录滴定管的读数为y mL,则Al4C3的质量分数为
④若无恒压管,对所测Al4C3质量分数的影响是
(2)若先测量AlN质量分数:首先关闭活塞K1,打开活塞K3,通过分液漏斗加入过量的某物质,写出AlN与过量的某物质发生反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】A是一种红棕色金属氧化物;B、D是金属单质;J是一种难溶于水的白色化合物,受热易分解。
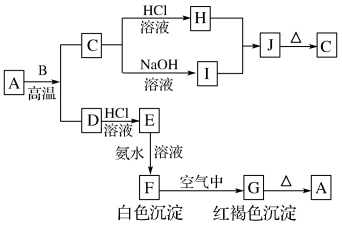
回答下列问题:
(1)A、E、J、G的化学式分别为___ 、___ 、___ 、___ 。
(2)C转化为I的离子方程式为___ 。
(3)H和I反应生成J的离子方程式为___ 。
(4)如何检验E溶液中大量存在的阳离子?___ 。

回答下列问题:
(1)A、E、J、G的化学式分别为
(2)C转化为I的离子方程式为
(3)H和I反应生成J的离子方程式为
(4)如何检验E溶液中大量存在的阳离子?
您最近一年使用:0次
解答题-有机推断题
|
较难
(0.4)
解题方法
【推荐3】已知A~K均为中学化学中的常见物质。它们之间的转化关系如下图所示,其中A、D为金属单质,反应过程中生成的水及其它部分产物已略去。
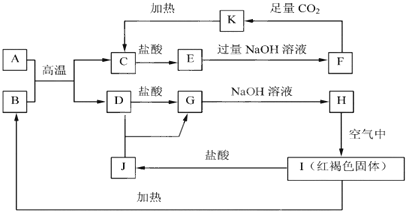
请回答以下问题:
(1)E中阳离子的结构示意图为__________ 。
(2)写出A与B反应生成C和D的化学方程式__________________ 。
(3)写出H在空气中生成I的化学方程式__________________ 。
(4)检验J中阳离子的方法是_____________________ 。

请回答以下问题:
(1)E中阳离子的结构示意图为
(2)写出A与B反应生成C和D的化学方程式
(3)写出H在空气中生成I的化学方程式
(4)检验J中阳离子的方法是
您最近一年使用:0次