鲍林提出杂化轨道理论能解释分子的空间结构,下列关于粒子的描述正确的是
| 选项 | 粒子 | 空间结构 | 解释 |
| A | SO3 | 正三角形 | S原子采取sp3杂化 |
| B | BF3 | 正三角形 | B原子采取sp2杂化 |
| C | C2H4 | 平面三角形 | C原子采取sp2杂化 |
| D |  | 四面体形 | Cl原子采取sp3杂化 |
| A.A | B.B | C.C | D.D |
更新时间:2023-01-13 20:53:36
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列有关说法正确的是
A. 分子的VSEPR模型与其空间立体构型一致 分子的VSEPR模型与其空间立体构型一致 |
B. 与 与 的中心原子杂化轨道类型相同 的中心原子杂化轨道类型相同 |
C. 分子中的键角为 分子中的键角为 |
D. 的熔沸点比 的熔沸点比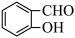 的熔沸点高 的熔沸点高 |
您最近一年使用:0次
【推荐2】下列说法不正确的是
| A.激光、焰色试验、原子光谱等与电子跃迁有关 |
| B.硫化氢晶体中,一个硫化氢分子周围有12个紧邻分子 |
| C.某元素基态原子的最外层电子排布式为4s1,则该元素为IA族元素 |
D.CO 与SO 与SO 中,O-C-O键角大于O-S-O键角 中,O-C-O键角大于O-S-O键角 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列说法中正确的是
| A.离子晶体中可能存在共价键 |
| B.金属晶体熔点都很高 |
C. 空间结构为正四面体形,和VSEPR模型不一致 空间结构为正四面体形,和VSEPR模型不一致 |
| D.通过X射线衍射实验难以区分石英玻璃和水晶 |
您最近一年使用:0次
【推荐2】在化学工业中,氮是非常重要的非金属元素。氨、铵盐、硝酸都是在化工生产中广泛使用的物质,水合肼(N2H4·H2O)是重要的氢能源稳定剂,其制备的反应原理为NaClO+2NH3=N2H4·H2O+NaCl。与此同时,氮的化合物如果处理不当也会造成环境污染。硝基胍是固体火箭推进剂的重要组分,其结构如图所示。下列说法中正确的是
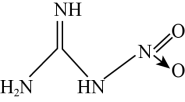

| A.硝基胍具有碱性 |
| B.硝基胍分子中只存在极性键 |
| C.硝基胍分子中所有原子均满足8电子稳定结构 |
| D.硝基胍分子中所有原子一定在同一平面内 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】2021年9月24日《科学》杂志发表了我国科学家的原创性重大突破,首次在实验室实现从CO2到淀粉的全合成。其合成路线如下:
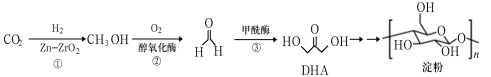
下列说法错误的是

下列说法错误的是
| A.电负性:O > C > H >Zn |
| B.CO2、HCHO、CH3OH分子中碳原子杂化方式分别是sp、sp2、sp3 |
| C.DHA分子间存在氢键 |
| D.甲醇分子中H-C-O键角大于甲醛分子中H-C-O键角 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】磷元素可组成多种物质。白磷化学性质活泼,需要放在水中保存,图a为1个白磷分子的结构示意图。黑磷在微电子和光探测领域有独特的应用价值,其晶体是与石墨类似的层状结构,图b为相邻两层的结构示意图。

下列说法不正确 的是

下列说法
A.1mol白磷中有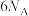 非极性键 非极性键 |
| B.白磷不溶于水与分子极性有关 |
| C.黑磷结构中层与层之间的作用力是共价键 |
| D.白磷与黑磷结构不同造成性质不同 |
您最近一年使用:0次

 和
和
 和
和
 和
和
 和
和

 键
键

