 。
。上述反应中,氧化剂是
 发生
发生 发生
发生 时转移电子数目为
时转移电子数目为 的物质的量是
的物质的量是 。
。
更新时间:2023-02-08 09:37:13
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】某汽车安全气囊的产气药剂主要含有NaN3、Fe2O3、KClO4、NaHCO3等物质。当汽车发生碰撞时,产气药剂产生大量气体使气囊迅速膨胀,从而起到保护作用。
(1)KClO4是助氧化剂,含有化学键的类型为___________ ;其中Cl的化合价是___________ 。
(2)NaHCO3是冷却剂,吸收产气过程中释放的热量而发生分解,其化学方程式为___________ 。
(3)Fe2O3是主氧化剂,与Na发生置换反应生成的还原产物为___________ (填化学式)。
(4)NaN3是气体发生剂,受热分解产生N2和Na。取130 g上述产气药剂,分解产生的气体通过碱石灰后的体积为33.6 L(标准状况),该产气药剂中NaN3的质量分数为___________ 。
(1)KClO4是助氧化剂,含有化学键的类型为
(2)NaHCO3是冷却剂,吸收产气过程中释放的热量而发生分解,其化学方程式为
(3)Fe2O3是主氧化剂,与Na发生置换反应生成的还原产物为
(4)NaN3是气体发生剂,受热分解产生N2和Na。取130 g上述产气药剂,分解产生的气体通过碱石灰后的体积为33.6 L(标准状况),该产气药剂中NaN3的质量分数为
您最近半年使用:0次
【推荐2】回答下列问题:
(1)在S2-、Fe3+、Fe2+、Mg2+、S、I-、H+中,只有氧化性的是___________ ,只有还原性的是___________ ,既有氧化性又有还原性的是___________ 。
(2)某同学写出以下三个化学方程式(未配平):
①NO+HNO3 N2O3+H2O
N2O3+H2O
②N2O4+H2O HNO3+HNO2
HNO3+HNO2
③NH3+NO HNO2+H2O
HNO2+H2O
其中你认为一定不可能实现的是___________ (填序号)。
(3)下列三个氧化还原反应中:
①2FeCl3+2KI=2FeCl2+2KCl+I2
②2FeCl2+Cl2=2FeCl3
③2NaClO3+4HCl(浓)=2NaCl+2ClO2↑+Cl2↑+2H2O
双线桥标出反应②的电子转移方向和数目:___________ ;反应③中的还原产物___________ ;
若溶质中Cl-与I-共存,为了氧化I-而Cl-不被氧化,除单质外,还可选用上述反应中的___________ 做氧化剂。
(1)在S2-、Fe3+、Fe2+、Mg2+、S、I-、H+中,只有氧化性的是
(2)某同学写出以下三个化学方程式(未配平):
①NO+HNO3
 N2O3+H2O
N2O3+H2O②N2O4+H2O
 HNO3+HNO2
HNO3+HNO2③NH3+NO
 HNO2+H2O
HNO2+H2O其中你认为一定不可能实现的是
(3)下列三个氧化还原反应中:
①2FeCl3+2KI=2FeCl2+2KCl+I2
②2FeCl2+Cl2=2FeCl3
③2NaClO3+4HCl(浓)=2NaCl+2ClO2↑+Cl2↑+2H2O
双线桥标出反应②的电子转移方向和数目:
若溶质中Cl-与I-共存,为了氧化I-而Cl-不被氧化,除单质外,还可选用上述反应中的
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】氧化还原反应在生产、生活中具有广泛的用途。
(1)下列生产、生活中的事例中没有发生氧化还原反应的是_____ (选填编号)。
a. 海水提溴 b. 工业制氯碱 c. 海水晒盐 d. 海带提碘
(2)水是人体的重要组成部分,是人体中含量最多的一种物质。“四种基本反应类型与氧化还原反应的关”可用下图表示。
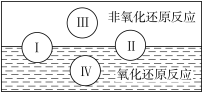
试写出有水参加且符合反应类型 IV 的一个化学方程式:___________________ 。
(3)工业上利用 NaIO3和 NaHSO3反应来制取单质 I2。
①配平下列化学方程式并标明电子转移的方向和数目:
_____ NaIO3+ NaHSO3→ I2+ Na2SO4+ H2SO4+ H2O
②该反应还原剂是_____ ,_____ 元素被还原,若生成 1mol 氧化产物则转移电子数目为_____ NA。
(4)已知:HSO3-、I2、I-、SO42-和一些未知物组成的一个氧化还原反应,其中SO42-是氧化产物,该反应中还原性HSO3-_____ I-(填“>”或“<”),完成该反应_____________________________________ 。
(1)下列生产、生活中的事例中没有发生氧化还原反应的是
a. 海水提溴 b. 工业制氯碱 c. 海水晒盐 d. 海带提碘
(2)水是人体的重要组成部分,是人体中含量最多的一种物质。“四种基本反应类型与氧化还原反应的关”可用下图表示。

试写出有水参加且符合反应类型 IV 的一个化学方程式:
(3)工业上利用 NaIO3和 NaHSO3反应来制取单质 I2。
①配平下列化学方程式并标明电子转移的方向和数目:
②该反应还原剂是
(4)已知:HSO3-、I2、I-、SO42-和一些未知物组成的一个氧化还原反应,其中SO42-是氧化产物,该反应中还原性HSO3-
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】某体系中存在如下反应: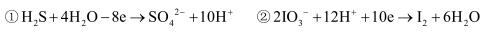
(1)反应①中 H2S 做___________ 剂,反应②属于___________ 反应(填“氧化”或“还原”)。
(2)若在反应①中失去 0.2mol 电子,则反应②中可生成___________ g 碘。
(3)由上述反应可推知___________ 。
a.氧化性K2SO4 KIO3 b.酸性: HIO3 H2SO4
c. 还原性 H2S I2 d. 反应过程中溶液的酸性逐渐减弱
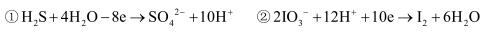
(1)反应①中 H2S 做
(2)若在反应①中失去 0.2mol 电子,则反应②中可生成
(3)由上述反应可推知
a.氧化性K2SO4 KIO3 b.酸性: HIO3 H2SO4
c. 还原性 H2S I2 d. 反应过程中溶液的酸性逐渐减弱
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】(1)147 g H2SO4的物质的量是________ ;0.5 mol H2SO4的质量是________ g;
(2)氧化铜在高温下发生分解反应:4CuO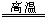 2Cu2O+O2↑,若反应过程中生成1molO2分子,则转移电子数为
2Cu2O+O2↑,若反应过程中生成1molO2分子,则转移电子数为____________ mol。
(3)反应:2FeCl3+2KI=2FeCl2+2KCl+I2,其中_____ 元素化合价升高,则该元素被_______ ,_____ 元素化合价降低;__________ 做还原剂,_______ 发生还原反应。
(4)钠在空气中燃烧的化学方程式:________________________________ ,1mol钠完全燃烧转移电子的个数为____________ 。
(2)氧化铜在高温下发生分解反应:4CuO
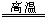 2Cu2O+O2↑,若反应过程中生成1molO2分子,则转移电子数为
2Cu2O+O2↑,若反应过程中生成1molO2分子,则转移电子数为(3)反应:2FeCl3+2KI=2FeCl2+2KCl+I2,其中
(4)钠在空气中燃烧的化学方程式:
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】元素周期表一百多种化学元素中,非金属元素占了23种,绝大部分非金属元素在社会中占有十分重要的位置,如C、N、O、Si、Cl等。
(1)氯元素原子在元素周期表中的位置是_______ ,最外电子层上有_______ 种能量不同的电子,该元素的简单阴离子核外电子排布式是_______ 。
(2)由氮元素与硅元素组成的物质,可用于制造发动机的耐热部件。推测:它属于_______ 晶体,请写出该化合物的化学式_______ 。
(3)下列事实能说明氯与氧两元素非金属性相对强弱的有_______ 。(选填编号)
a.Cl原子最外层电子数比O原子多
b.酸性:HCl>H2O
c.ClO2中氯元素为+4价,氧元素为−2价
d.沸点:H2O>HCl
有些国家自来水常用二氧化氯(ClO2)来杀菌消毒。工业上可用亚氯酸钠NaClO2和稀盐酸为原料制备ClO2,同时NaClO2被还原成Cl-,反应如下:NaClO2+HCl→ClO2↑+_______(没有配平)
(4)完成并配平上述方程式_______ 。该反应中氧化剂和还原剂的物质的量之比是_______ 。生成0.2molClO2转移电子的物质的量为_______ mol。
(1)氯元素原子在元素周期表中的位置是
(2)由氮元素与硅元素组成的物质,可用于制造发动机的耐热部件。推测:它属于
(3)下列事实能说明氯与氧两元素非金属性相对强弱的有
a.Cl原子最外层电子数比O原子多
b.酸性:HCl>H2O
c.ClO2中氯元素为+4价,氧元素为−2价
d.沸点:H2O>HCl
有些国家自来水常用二氧化氯(ClO2)来杀菌消毒。工业上可用亚氯酸钠NaClO2和稀盐酸为原料制备ClO2,同时NaClO2被还原成Cl-,反应如下:NaClO2+HCl→ClO2↑+_______(没有配平)
(4)完成并配平上述方程式
您最近半年使用:0次



