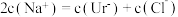室温下,向20 mL含有0.10 mol/L 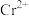 和0.10 mol/L
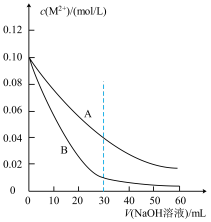
和0.10 mol/L  的溶液中滴加0.10 mol/L NaOH溶液,金属阳离子的浓度与滴入NaOH溶液体积的关系如图所示。已知:若溶液中金属阳离子浓度小于
的溶液中滴加0.10 mol/L NaOH溶液,金属阳离子的浓度与滴入NaOH溶液体积的关系如图所示。已知:若溶液中金属阳离子浓度小于 mol/L可视为沉淀完全;
mol/L可视为沉淀完全;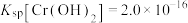 ,
,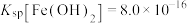 。则下列说法错误的是
。则下列说法错误的是
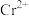 和0.10 mol/L
和0.10 mol/L  的溶液中滴加0.10 mol/L NaOH溶液,金属阳离子的浓度与滴入NaOH溶液体积的关系如图所示。已知:若溶液中金属阳离子浓度小于
的溶液中滴加0.10 mol/L NaOH溶液,金属阳离子的浓度与滴入NaOH溶液体积的关系如图所示。已知:若溶液中金属阳离子浓度小于 mol/L可视为沉淀完全;
mol/L可视为沉淀完全;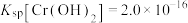 ,
,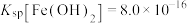 。则下列说法错误的是
。则下列说法错误的是
A.曲线A表示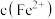 与V(NaOH溶液)的关系 与V(NaOH溶液)的关系 |
B.当pH=7时,溶液中 、 、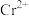 均沉淀完全 均沉淀完全 |
C.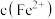 减小,并不能说明 减小,并不能说明 沉淀一定已开始生成 沉淀一定已开始生成 |
D.当两种离子均沉淀完全后,溶液中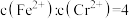 |
更新时间:2023-02-10 09:17:41
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列根据实验操作和现象能得出结论的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向含有 的 的 溶液中通气体 溶液中通气体 | 产生白色沉淀 |  一定体现氧化性 一定体现氧化性 |
| B | 向 溶液中加入足量氯水再加 溶液中加入足量氯水再加 萃取 萃取 |  层呈橙红色 层呈橙红色 |  的还原性强于 的还原性强于 |
| C | 向等浓度的 与 与 混合溶液中滴加少量 混合溶液中滴加少量 溶液 溶液 | 先生成黄色沉淀 | 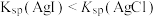 |
| D |  缓慢通入滴有酚酞的 缓慢通入滴有酚酞的 溶液中 溶液中 | 溶液红色褪去 |  具有漂白性 具有漂白性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】常温下,下列有关电解质溶液的说法正确的是
A.含有AgCl固体的饱和溶液,加少量水稀释, 和 和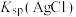 均保持不变 均保持不变 |
B.向饱和AgCl溶液中通入HCl,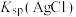 减小 减小 |
C.反应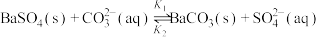 的 的 ( ( 、 、 ) ) |
D.向CH3COOH溶液中加入冰醋酸, 、 、 均增大 均增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】常温下,向 、
、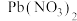 和
和 的混合液中滴加
的混合液中滴加 溶液,
溶液, 与
与 的关系如下图所示,已知:
的关系如下图所示,已知: ,
,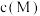 代表
代表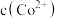 、
、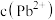 或
或 ;
; ;当被沉淀的离子的物质的量浓度小于
;当被沉淀的离子的物质的量浓度小于 时,认为该离子已沉淀完全。下列叙述正确的是
时,认为该离子已沉淀完全。下列叙述正确的是
 、
、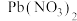 和
和 的混合液中滴加
的混合液中滴加 溶液,
溶液, 与
与 的关系如下图所示,已知:
的关系如下图所示,已知: ,
,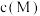 代表
代表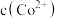 、
、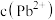 或
或 ;
; ;当被沉淀的离子的物质的量浓度小于
;当被沉淀的离子的物质的量浓度小于 时,认为该离子已沉淀完全。下列叙述正确的是
时,认为该离子已沉淀完全。下列叙述正确的是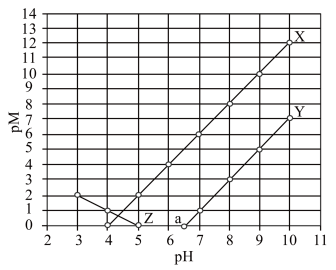
A.常温下,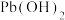 的 的 |
B. 、 、 分别代表 分别代表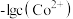 、 、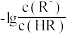 与 与 的关系 的关系 |
C.图中 点对应溶液的 点对应溶液的 为6.5,此时溶液中 为6.5,此时溶液中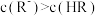 |
D.通过调节溶液 无法分离浓度均为 无法分离浓度均为 的 的 、 、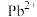 混合溶液 混合溶液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】用0.5mol/LNaHCO3溶液滴定25mL0.25mol/LCaCl2溶液,加入的碳酸氢钠溶液体积与溶液pH变化曲线如图所示,其中V=4.54mL时溶液中无沉淀,之后出现白色浑浊且逐渐增多,当滴加的NaHCO3溶液体积为25.00mL时,溶液的pH稳定在7.20左右,整个滴定过程中未见气泡产生。下列叙述正确的是

已知:Ksp(CaCO3)=3.36×10-9,Ka2(H2CO3)=4.7×10-11,100.8≈6.3

已知:Ksp(CaCO3)=3.36×10-9,Ka2(H2CO3)=4.7×10-11,100.8≈6.3
| A.总反应的化学方程式:CaCl2+2NaHCO3=2NaCl+CaCO3↓+H2CO3 |
B.a点的混合溶液,c(Na+)+c( )+c(H2CO3)+c( )+c(H2CO3)+c( )+c(Ca2+)>c(Cl-) )+c(Ca2+)>c(Cl-) |
| C.a→b的过程中,水的电离程度不断增大 |
D.b点的混合溶液,c( )•c(Ca2+)≈6.3×10-8 )•c(Ca2+)≈6.3×10-8 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】室温下:Ka1(H2C2O4)=5×10-2、Ka2(H2C2O4)=1×10-4、Ksp(CaC2O4)=2.5×10-9.通过下列实验探究某些草酸盐的性质。
实验①:用pH计测得0.100 mol·L-1K2C2O4溶液的pH=8。
实验②:向0.10 mol·L-1KHC2O4溶液中滴入少量酸性高锰酸钾溶液,振荡后溶液紫色褪去。
实验③:向0.10 mol·L-1K2C2O4溶液中滴加一定浓度的稀盐酸后,混合溶液的pH=7。
实验④:向0.10 mol·L-1KHC2O4溶液加入一定体积的等浓度CaCl2溶液产生白色沉淀,测得上层清液pH=4,c(Ca2+)=10-4 mol·L-1。
下列说法正确的是
实验①:用pH计测得0.100 mol·L-1K2C2O4溶液的pH=8。
实验②:向0.10 mol·L-1KHC2O4溶液中滴入少量酸性高锰酸钾溶液,振荡后溶液紫色褪去。
实验③:向0.10 mol·L-1K2C2O4溶液中滴加一定浓度的稀盐酸后,混合溶液的pH=7。
实验④:向0.10 mol·L-1KHC2O4溶液加入一定体积的等浓度CaCl2溶液产生白色沉淀,测得上层清液pH=4,c(Ca2+)=10-4 mol·L-1。
下列说法正确的是
A.实验①溶液中:  =2×10-3 =2×10-3 |
| B.实验②说明KHC2O4溶液具有漂白性 |
C.实验③反应所得溶液中存在:c(K+)=2c(C2O )+c(HC2O )+c(HC2O ) ) |
D.实验④所得上层清液中的c(HC2O )=2.5×10-5 mol·L-1 )=2.5×10-5 mol·L-1 |
您最近一年使用:0次

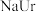 )悬浊液静置,取上层清液,再通入
)悬浊液静置,取上层清液,再通入 ,溶液中尿酸的浓度
,溶液中尿酸的浓度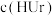 与
与 的关系如图所示。已知:
的关系如图所示。已知: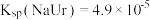 ,
,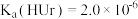 ,下列说法正确的是
,下列说法正确的是
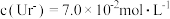
 时,
时,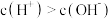
 的变化过程中,c(Na+) c(Ur-)的值将逐渐减小
的变化过程中,c(Na+) c(Ur-)的值将逐渐减小 时,
时,