实验室用 燃料电池作电源探究氯碱工业原理和粗铜的精炼原理,其中乙装置中的X为阳离子交换膜。
燃料电池作电源探究氯碱工业原理和粗铜的精炼原理,其中乙装置中的X为阳离子交换膜。
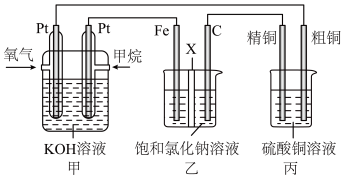
(1)甲装置中,负极的电极反应式为___________ 。
(2)乙装置中,石墨(C)极的电极反应式为___________ 。
(3)若在标准状况下,有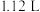 氧气参加反应,则理论上通过乙装置中X交换膜的电量为
氧气参加反应,则理论上通过乙装置中X交换膜的电量为___________ C(已知:法拉第常数代表每摩尔电子所携带的电荷,数值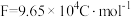 )。一段时间后,丙装置中
)。一段时间后,丙装置中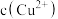
___________ (填“增大”“减小”或“不变”)。
(4)若以该 燃料电池为电源,用石墨作电极电解
燃料电池为电源,用石墨作电极电解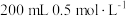 的
的 溶液,电解一段时间后,两极收集到的气体的体积相同(相同条件下测定),则整个电解过程转移电子的物质的量是
溶液,电解一段时间后,两极收集到的气体的体积相同(相同条件下测定),则整个电解过程转移电子的物质的量是___________ 。
 燃料电池作电源探究氯碱工业原理和粗铜的精炼原理,其中乙装置中的X为阳离子交换膜。
燃料电池作电源探究氯碱工业原理和粗铜的精炼原理,其中乙装置中的X为阳离子交换膜。
(1)甲装置中,负极的电极反应式为
(2)乙装置中,石墨(C)极的电极反应式为
(3)若在标准状况下,有
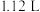 氧气参加反应,则理论上通过乙装置中X交换膜的电量为
氧气参加反应,则理论上通过乙装置中X交换膜的电量为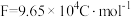 )。一段时间后,丙装置中
)。一段时间后,丙装置中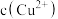
(4)若以该
 燃料电池为电源,用石墨作电极电解
燃料电池为电源,用石墨作电极电解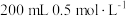 的
的 溶液,电解一段时间后,两极收集到的气体的体积相同(相同条件下测定),则整个电解过程转移电子的物质的量是
溶液,电解一段时间后,两极收集到的气体的体积相同(相同条件下测定),则整个电解过程转移电子的物质的量是
更新时间:2023-02-12 08:09:57
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】我国是最早发现并使用青铜器的国家,后母戊鼎是我国的一级文物,是世界上出土的最大最重的青铜礼器。现代社会中铜的应用常广泛,铜的回收再利用是化工生产的一个重要领域。实验室利用废旧电池的铜帽(Cu、Zn总含量约为99%)回收Cu并制备ZnO的部分实验过程如下:

请回答下列问题:
(1)请写出一种加快铜帽溶解的方法:__________________ 。铜帽溶解时通入空气的作用是___________________________ (用化学方程式表示)。
(2)调节溶液pH时,是将溶液的pH调_________ (填“大”或“小”)到2~3。
(3)电解精炼粗铜时,阴极的电极反应式为___________________________ 。工业上常采用甲醇燃料电池作为电解精炼铜旳电源,写出碱性甲醇燃料电池的负极反应式:___________________________ 。
(4)已知:pH>11时,Zn(OH)2能溶于NaOH溶液生成ZnO22-。室温下,几种离子生成氢氧化物沉淀的pH如下表所小(开始沉淀的pH按金属离子浓度为0.01mol·L-1计算):
①上表中Fe3+沉淀完全的pH为__________________ 。
②由过滤粗铜的滤液制备ZnO的实验步骤依次为(可选用的试剂:30%H2O2、稀硝酸、1.0mol·L-1NaOH溶液):
a.___________________________ ;b.___________________________ ;c.过滤;
d.___________________________ ;e.过滤、洗涤、干燥;f.900℃煅烧。

请回答下列问题:
(1)请写出一种加快铜帽溶解的方法:
(2)调节溶液pH时,是将溶液的pH调
(3)电解精炼粗铜时,阴极的电极反应式为
(4)已知:pH>11时,Zn(OH)2能溶于NaOH溶液生成ZnO22-。室温下,几种离子生成氢氧化物沉淀的pH如下表所小(开始沉淀的pH按金属离子浓度为0.01mol·L-1计算):
| Fe3+ | Fe2+ | Zn2+ | Al3+ | |
| 开始沉淀的pH | 2 | 7.3 | 7.2 | 3.9 |
| 沉淀完全的pH | 8.3 | 8.2 | 5.2 |
②由过滤粗铜的滤液制备ZnO的实验步骤依次为(可选用的试剂:30%H2O2、稀硝酸、1.0mol·L-1NaOH溶液):
a.
d.
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】高磷镍铁是生产钙镁磷肥的副产品。以高磷镍铁(主要含Ni、Fe、P,还含有少量Fe、Cu、Zn的磷化物)为原料生产硫酸镍晶体 的工艺流程如图。
的工艺流程如图。

(1)“电解”时,选用 硫酸溶液为电解液。将高磷镍铁制成电极板,则该电极板作
硫酸溶液为电解液。将高磷镍铁制成电极板,则该电极板作_______ (填“阳极”或“阴极”);另一极的产物主要为_______ (填化学式),电极反应式为_______ 。此外,溶液中的 有部分在阴极放电。
有部分在阴极放电。
(2)“沉镍”时,离子方程式为_______ ,为确保镍沉淀完全,理论上应调节溶液
_______ (已知:在该工业环境下,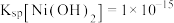 (近似值);当溶液中离子浓度
(近似值);当溶液中离子浓度 时,可认为该离子沉淀完全)。
时,可认为该离子沉淀完全)。
(3)已知:25℃时,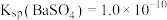 、
、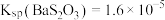 。向上述流程制得的
。向上述流程制得的 溶液中加入
溶液中加入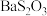 固体,充分反应后,过滤可得到
固体,充分反应后,过滤可得到 溶液。生成
溶液。生成 的化学方程式为
的化学方程式为_______ 。
 的工艺流程如图。
的工艺流程如图。
(1)“电解”时,选用
 硫酸溶液为电解液。将高磷镍铁制成电极板,则该电极板作
硫酸溶液为电解液。将高磷镍铁制成电极板,则该电极板作 有部分在阴极放电。
有部分在阴极放电。(2)“沉镍”时,离子方程式为

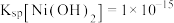 (近似值);当溶液中离子浓度
(近似值);当溶液中离子浓度 时,可认为该离子沉淀完全)。
时,可认为该离子沉淀完全)。(3)已知:25℃时,
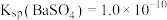 、
、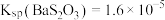 。向上述流程制得的
。向上述流程制得的 溶液中加入
溶液中加入 固体,充分反应后,过滤可得到
固体,充分反应后,过滤可得到 溶液。生成
溶液。生成 的化学方程式为
的化学方程式为
您最近一年使用:0次
【推荐3】我国科学家首次实现甲烷在温和条件下高选择性氧化制甲醇。
反应Ⅰ: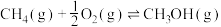

反应Ⅱ: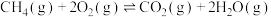
(1)已知:①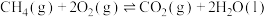
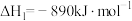
②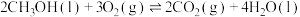
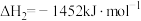
③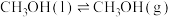
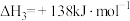
上述反应Ⅰ的
_______  。
。
(2)在密闭容器中投入2mol 和1mol
和1mol 发生反应Ⅰ、Ⅱ,保持起始投料量不变,在不同温度、压强下做平行实验,测得
发生反应Ⅰ、Ⅱ,保持起始投料量不变,在不同温度、压强下做平行实验,测得 的平衡体积分数
的平衡体积分数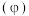 与温度、压强的关系如图所示。
与温度、压强的关系如图所示。
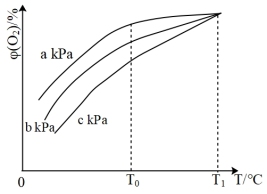
①a、b、c由大到小排序为_______ 。
②由图可知,当 时,以反应
时,以反应_______ (填“Ⅰ”或“Ⅱ”)为主,理由是_______ 。
③ ℃时,三条曲线几乎相交的原因可能是
℃时,三条曲线几乎相交的原因可能是_______ 。
(3)在恒温的刚性(恒容)密闭容器中,分别按照(a) 、
、 的体积比为2:1以及(b)
的体积比为2:1以及(b) 、
、 、
、 [
[ 的作用是活化催化剂]的体积比为2:1:8充入并发生反应Ⅰ、Ⅱ,相同的时间内(都加入相同催化剂),测得产物的选择性[如甲醇的选择性
的作用是活化催化剂]的体积比为2:1:8充入并发生反应Ⅰ、Ⅱ,相同的时间内(都加入相同催化剂),测得产物的选择性[如甲醇的选择性 ]如表所示。
]如表所示。
①b投料方式能显著提高甲醇选择性的原因是_______ 。
②向上述刚性密闭容器中按照体积比2:1:8充入 、
、 和
和 ,在450K下反应达到平衡时,
,在450K下反应达到平衡时, 的转化率为50%,
的转化率为50%, 的选择性为90%,则反应Ⅱ的压强平衡常数
的选择性为90%,则反应Ⅱ的压强平衡常数
_______ 。(计算结果保留2位小数)
(4)我国科学家研发出新型催化剂,利用电催化法实现将甲烷转化成甲醇,装置如图所示。

交换膜M是_______ (填“阳离子”或“阴离子”)交换膜。阳极的电极反应式为_______ 。
反应Ⅰ:
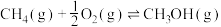

反应Ⅱ:
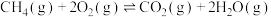
(1)已知:①
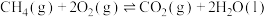
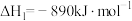
②
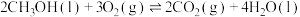
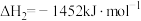
③
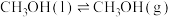
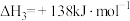
上述反应Ⅰ的

 。
。(2)在密闭容器中投入2mol
 和1mol
和1mol 发生反应Ⅰ、Ⅱ,保持起始投料量不变,在不同温度、压强下做平行实验,测得
发生反应Ⅰ、Ⅱ,保持起始投料量不变,在不同温度、压强下做平行实验,测得 的平衡体积分数
的平衡体积分数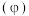 与温度、压强的关系如图所示。
与温度、压强的关系如图所示。
①a、b、c由大到小排序为
②由图可知,当
 时,以反应
时,以反应③
 ℃时,三条曲线几乎相交的原因可能是
℃时,三条曲线几乎相交的原因可能是(3)在恒温的刚性(恒容)密闭容器中,分别按照(a)
 、
、 的体积比为2:1以及(b)
的体积比为2:1以及(b) 、
、 、
、 [
[ 的作用是活化催化剂]的体积比为2:1:8充入并发生反应Ⅰ、Ⅱ,相同的时间内(都加入相同催化剂),测得产物的选择性[如甲醇的选择性
的作用是活化催化剂]的体积比为2:1:8充入并发生反应Ⅰ、Ⅱ,相同的时间内(都加入相同催化剂),测得产物的选择性[如甲醇的选择性 ]如表所示。
]如表所示。| 投料方式 | a | b |
 的选择性/% 的选择性/% | 90 | 15 |
 的选择性/% 的选择性/% | 10 | 85 |
②向上述刚性密闭容器中按照体积比2:1:8充入
 、
、 和
和 ,在450K下反应达到平衡时,
,在450K下反应达到平衡时, 的转化率为50%,
的转化率为50%, 的选择性为90%,则反应Ⅱ的压强平衡常数
的选择性为90%,则反应Ⅱ的压强平衡常数
(4)我国科学家研发出新型催化剂,利用电催化法实现将甲烷转化成甲醇,装置如图所示。

交换膜M是
您最近一年使用:0次
【推荐1】NiOOH可用作碱性镍镉电池的电极材料,用含镍废料(主要成分是Ni,杂质有Al、Fe、SiO2)制取NiOOH的流程如图。
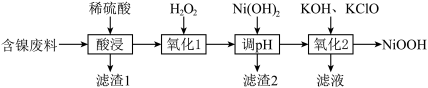
已知:i.镍、铁同族,但Ni2+的性质较稳定;
ii.常温下,该工艺条件下金属阳离子生成氢氧化物沉淀时的pH范围如表所示。
回答下列问题:
(1)“酸浸”前将废料粉碎的目的是___________ ,“滤渣2”的主要成分是___________ 。
(2)加入 的目的是
的目的是___________ ,实际生产中发现 的实际用量比理论用量多,原因是
的实际用量比理论用量多,原因是___________ 。
(3)“调pH”时pH的范围是___________ ,当溶液中离子浓度小于或等于 时认为该离子沉淀完全,则常温下
时认为该离子沉淀完全,则常温下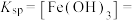
___________ ,“氧化2”中反应的离子方程式为___________ 。
(4)锌镍电池是一种可充电电池,其充电时总反应为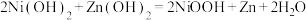 ,则放电时正极的电极反应式为
,则放电时正极的电极反应式为___________ ,充电时阴极周围溶液pH___________ (填“增大”“减小”或“不变”)。

已知:i.镍、铁同族,但Ni2+的性质较稳定;
ii.常温下,该工艺条件下金属阳离子生成氢氧化物沉淀时的pH范围如表所示。
| 沉淀物 |  |  |  |  |
| 开始沉淀时pH | 3.0 | 1.5 | 5.9 | 7.1 |
| 完全沉淀时pH | 4.7 | 3.2 | 9.0 | 9.2 |
(1)“酸浸”前将废料粉碎的目的是
(2)加入
 的目的是
的目的是 的实际用量比理论用量多,原因是
的实际用量比理论用量多,原因是(3)“调pH”时pH的范围是
 时认为该离子沉淀完全,则常温下
时认为该离子沉淀完全,则常温下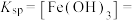
(4)锌镍电池是一种可充电电池,其充电时总反应为
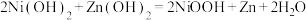 ,则放电时正极的电极反应式为
,则放电时正极的电极反应式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储。过程如下:
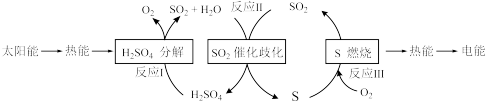
(1)反应Ⅰ: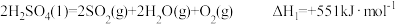
反应Ⅲ:
反应Ⅱ的化学方程式为___________ ,标准状况下每有 的
的 发生反应,释放的能量为
发生反应,释放的能量为___________  。
。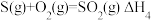 ,则
,则
___________  (填“>”、“<”或“=”)
(填“>”、“<”或“=”)
(2)利用下图所示装置可实现 的吸收,同时获得了硫黄、
的吸收,同时获得了硫黄、 消毒液。
消毒液。
①甲池中碳纳米管上的电极反应式是___________ 。
②乙池中的Y极可否改为与 电极相连,其理由是什么?
电极相连,其理由是什么?___________ 。


(1)反应Ⅰ:
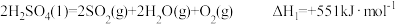
反应Ⅲ:

反应Ⅱ的化学方程式为
 的
的 发生反应,释放的能量为
发生反应,释放的能量为 。
。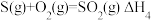 ,则
,则
 (填“>”、“<”或“=”)
(填“>”、“<”或“=”)(2)利用下图所示装置可实现
 的吸收,同时获得了硫黄、
的吸收,同时获得了硫黄、 消毒液。
消毒液。①甲池中碳纳米管上的电极反应式是
②乙池中的Y极可否改为与
 电极相连,其理由是什么?
电极相连,其理由是什么?
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】Ⅰ.某实验小组同学利用下图装置对电化学原理进行了一系列探究活动.回答下列问题:
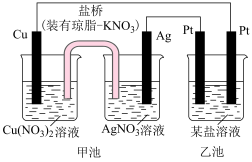
(1))甲池为___________ (填“原电池”或“电解池”)装置.甲池反应前,两电极质量相等,一段时间后,若Ag极的质量增加21.6g,则两电极质量相差_____________ g.
(2)若乙池中的某盐溶液是足量 溶液,则乙池中总反应的化学方程式
溶液,则乙池中总反应的化学方程式_________________ ,工作一段时间后,若要使乙池溶液恢复至原来浓度,可向溶液中加入___________ (填化学式).
Ⅱ.利用电化学原理,将、 和熔融
和熔融 制成燃料电池,模拟工业电解法来处理含
制成燃料电池,模拟工业电解法来处理含 废水,如下图所示;电解过程中溶液发生反应:
废水,如下图所示;电解过程中溶液发生反应: .
.
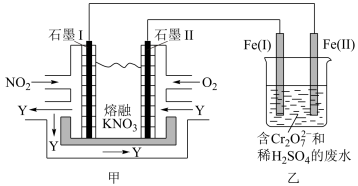
(3)甲池工作时, 转变成绿色硝化剂Y,Y是
转变成绿色硝化剂Y,Y是 ,可循环使用.则石墨Ⅰ附近发生的电极反应式为
,可循环使用.则石墨Ⅰ附近发生的电极反应式为____________________________________ .
(4)乙池中Fe(Ⅰ)棒上发生的电极反应为___________________________ ,若溶液中减少了 ,则电路中至少转移了
,则电路中至少转移了_________________ mol电子.
(5)向完全还原为 的乙池工业废水中滴加
的乙池工业废水中滴加 溶液,可将铬以
溶液,可将铬以 沉淀的形式除去,常温下
沉淀的形式除去,常温下 的溶度积
的溶度积 ,要使
,要使 降至
降至 ,溶液的pH应调至
,溶液的pH应调至___________ .

(1))甲池为
(2)若乙池中的某盐溶液是足量
 溶液,则乙池中总反应的化学方程式
溶液,则乙池中总反应的化学方程式Ⅱ.利用电化学原理,将、
 和熔融
和熔融 制成燃料电池,模拟工业电解法来处理含
制成燃料电池,模拟工业电解法来处理含 废水,如下图所示;电解过程中溶液发生反应:
废水,如下图所示;电解过程中溶液发生反应: .
.
(3)甲池工作时,
 转变成绿色硝化剂Y,Y是
转变成绿色硝化剂Y,Y是 ,可循环使用.则石墨Ⅰ附近发生的电极反应式为
,可循环使用.则石墨Ⅰ附近发生的电极反应式为(4)乙池中Fe(Ⅰ)棒上发生的电极反应为
 ,则电路中至少转移了
,则电路中至少转移了(5)向完全还原为
 的乙池工业废水中滴加
的乙池工业废水中滴加 溶液,可将铬以
溶液,可将铬以 沉淀的形式除去,常温下
沉淀的形式除去,常温下 的溶度积
的溶度积 ,要使
,要使 降至
降至 ,溶液的pH应调至
,溶液的pH应调至
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】如图是乙醇燃料电池工作时的示意图,乙池中M、N两个电极的材料是石墨和铁中的一种,工作时M、N两个电极的质量都不减少,请回答:
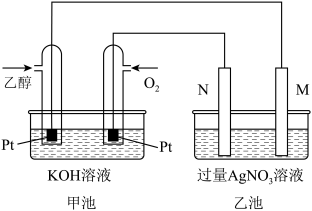
(1)甲池中通入乙醇的铂电极名称是___________ (选填“正极”、“负极”、“阴极”、“阳极”),通入O2的铂电极反应式为___________ 。
(2)乙池属于___________ (填“原电池”或“电解池”),工作时,乙池中电子流出的电极是___________ (选填“M”或N”);
(3)若乙池中某电极析出金属银4.32g时,甲池中理论上消耗氧气为___________ L(标况下);
(4)若用电解方法精炼粗铜,乙池电解液选用CuSO4溶液,则N电极的材料是___________ (选填“粗铜”或“精铜”),反应一段时间以后,电解液溶液的浓度___________ 。(选填“增大”、“减小”“不变”)

(1)甲池中通入乙醇的铂电极名称是
(2)乙池属于
(3)若乙池中某电极析出金属银4.32g时,甲池中理论上消耗氧气为
(4)若用电解方法精炼粗铜,乙池电解液选用CuSO4溶液,则N电极的材料是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】Ⅰ、工业上利用 和
和 在催化剂作用下合成甲醇
在催化剂作用下合成甲醇 。
。
已知相关物质的摩尔燃烧焓(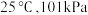 ):数据如下表所示:
):数据如下表所示:
(1)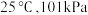 时,由
时,由 和
和 合成
合成 的热化学方程式为
的热化学方程式为___ 。
Ⅱ、某研究小组以甲醇—空气燃料电池为电源,用石墨电极持续电解 溶液,装置如下图所示。
溶液,装置如下图所示。
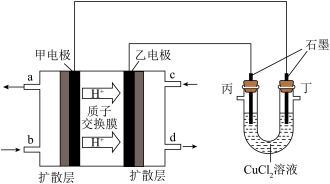
实验现象记录如下:
(2)甲电极的电极反应式为___________ ;当通入 (折算为标准状况下)甲醇蒸汽,测得电路中转移
(折算为标准状况下)甲醇蒸汽,测得电路中转移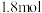 电子,则甲醇的利用率为
电子,则甲醇的利用率为___________ 。
(3)通电前 溶液呈酸性的原因:
溶液呈酸性的原因:___________ (用离子方程式表示)。
(4) 时丁电极的电极反应式为
时丁电极的电极反应式为___________ 。
(5)从丁电极刮取白色固体(含少量红色固体),经检验含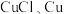 。针对
。针对 固体是如何产生的,某兴趣小组提出两种假设。
固体是如何产生的,某兴趣小组提出两种假设。
假设1:由电极反应产生: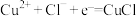
假设2:由反应___________ 产生(用离子方程式表示)。
(6)镀铜工业中,电镀液以 、
、 为主,同时含
为主,同时含 和添加剂。过多的
和添加剂。过多的 会使镀层出现白色胶状薄膜,电镀前向电镀液中加入适量
会使镀层出现白色胶状薄膜,电镀前向电镀液中加入适量 (微溶)固体能有效解决该问题,反应的离子方程式为
(微溶)固体能有效解决该问题,反应的离子方程式为___________ 。
 和
和 在催化剂作用下合成甲醇
在催化剂作用下合成甲醇 。
。已知相关物质的摩尔燃烧焓(
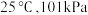 ):数据如下表所示:
):数据如下表所示:| 物质 |  |  | 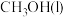 |
摩尔燃烧焓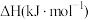 |  |  |  |
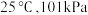 时,由
时,由 和
和 合成
合成 的热化学方程式为
的热化学方程式为Ⅱ、某研究小组以甲醇—空气燃料电池为电源,用石墨电极持续电解
 溶液,装置如下图所示。
溶液,装置如下图所示。
实验现象记录如下:
| 时刻 | 实验现象 | |
| 通电前 |  溶液呈绿色,显酸性 溶液呈绿色,显酸性 | |
 | 丙电极产生气体 | 丁电极底部出现少量红色固体,电极周围溶液变棕黑色 |
 | 丙电极产生气体 | 丁电极产生白色固体 |
| … | …… | |
 | 丙电极产生气体 | 丁电极产生气体 |
 (折算为标准状况下)甲醇蒸汽,测得电路中转移
(折算为标准状况下)甲醇蒸汽,测得电路中转移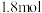 电子,则甲醇的利用率为
电子,则甲醇的利用率为(3)通电前
 溶液呈酸性的原因:
溶液呈酸性的原因:(4)
 时丁电极的电极反应式为
时丁电极的电极反应式为(5)从丁电极刮取白色固体(含少量红色固体),经检验含
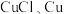 。针对
。针对 固体是如何产生的,某兴趣小组提出两种假设。
固体是如何产生的,某兴趣小组提出两种假设。假设1:由电极反应产生:
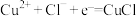
假设2:由反应
(6)镀铜工业中,电镀液以
 、
、 为主,同时含
为主,同时含 和添加剂。过多的
和添加剂。过多的 会使镀层出现白色胶状薄膜,电镀前向电镀液中加入适量
会使镀层出现白色胶状薄膜,电镀前向电镀液中加入适量 (微溶)固体能有效解决该问题,反应的离子方程式为
(微溶)固体能有效解决该问题,反应的离子方程式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】下图为相互串联的三个装置,试回答:
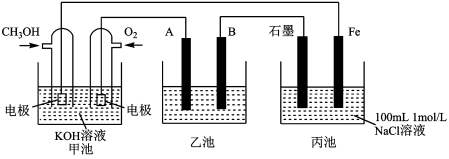
(1)写出甲池负极的电极反应式:_______ 。
(2)若利用乙池在铁片上镀银,则B电极反应式是_______ 。
(3)若利用乙池进行粗铜的电解精炼,则_______ 极(填“A”或“B”)是粗铜。
(4)向丙池溶液中滴加几滴酚酞试液,_______ 电极(填“石墨”或“Fe”)周围先出现红色,若甲池消耗3.2 gCH3OH气体,则丙池中阳极上产生气体的物质的量为_______ mol。
(5)工业冶炼铝的化学方程式是_______ 。
(6)工业级氢氧化钾的溶液中含有某些含氧酸根杂质,可用离子交换法膜法电解提纯。电解槽内装有阳离子交换膜(只允许阳离子通过),其工作原理如图所示。除去杂质后的氢氧化钾溶液从液体出口_______ (填写“A”或“B”)导出。


(1)写出甲池负极的电极反应式:
(2)若利用乙池在铁片上镀银,则B电极反应式是
(3)若利用乙池进行粗铜的电解精炼,则
(4)向丙池溶液中滴加几滴酚酞试液,
(5)工业冶炼铝的化学方程式是
(6)工业级氢氧化钾的溶液中含有某些含氧酸根杂质,可用离子交换法膜法电解提纯。电解槽内装有阳离子交换膜(只允许阳离子通过),其工作原理如图所示。除去杂质后的氢氧化钾溶液从液体出口

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】新能源汽车所用蓄电池分为铅酸蓄电池、二次锂电池、空气电池等。铅酸蓄电池是常见的二次电池,应用非常广泛。电池反应式为: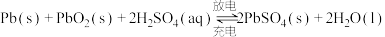 。用铅酸蓄电池作电源,可以进行粗铜(含
。用铅酸蓄电池作电源,可以进行粗铜(含 、
、 等杂质)的电解精炼,也可以电解饱和食盐水制烧碱和氯气。其装置如图所示:
等杂质)的电解精炼,也可以电解饱和食盐水制烧碱和氯气。其装置如图所示:

(1)铅酸蓄电池负极的电极反应式为___________ ;电池工作时, 向
向___________ (填“ ”或“
”或“ ”)极移动,放电一段时间后,溶液的
”)极移动,放电一段时间后,溶液的
___________ (填“增大”“减小”或“不变”);若外电路通过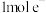 ,理论上负极板的质量增加
,理论上负极板的质量增加___________ g。
(2)电解精炼铜时,X极的电极材料是___________ ;U形管中的电解质溶液为___________ ;阴极发生的电极反应式为___________ 。
(3)如果X、Y都为石墨,U形管中装的是饱和 溶液,电解的总反应式为
溶液,电解的总反应式为___________ ;如果消耗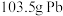 ,理论上产生的
,理论上产生的 在标准状态下的体积为
在标准状态下的体积为___________ L。
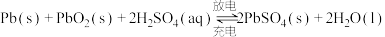 。用铅酸蓄电池作电源,可以进行粗铜(含
。用铅酸蓄电池作电源,可以进行粗铜(含 、
、 等杂质)的电解精炼,也可以电解饱和食盐水制烧碱和氯气。其装置如图所示:
等杂质)的电解精炼,也可以电解饱和食盐水制烧碱和氯气。其装置如图所示:
(1)铅酸蓄电池负极的电极反应式为
 向
向 ”或“
”或“ ”)极移动,放电一段时间后,溶液的
”)极移动,放电一段时间后,溶液的
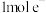 ,理论上负极板的质量增加
,理论上负极板的质量增加(2)电解精炼铜时,X极的电极材料是
(3)如果X、Y都为石墨,U形管中装的是饱和
 溶液,电解的总反应式为
溶液,电解的总反应式为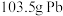 ,理论上产生的
,理论上产生的 在标准状态下的体积为
在标准状态下的体积为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】如图所示,某同学设计了一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜(甲醚具有可燃性,是一种常用的燃料)。
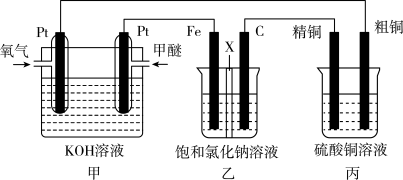
根据要求回答相关问题
(1)装置甲中通入燃料甲醚的一极是________ (填“正极”或“负极”),写出正极的电极反应式:________ 。
(2)装置乙中Fe为________ 极(填“阳极”或“阴极”),石墨电极(C)的电极反应式为:________ 。
(3)如果粗铜中含有锌、银等杂质,丙装置的阳极泥中含有________ ,反应一段时间后,硫酸铜溶液浓度将________ (填“增大”、“减小”或“不变”)。
(4)当装置甲中消耗0.05mol O2时,装置乙中溶液的pH为________ (溶液体积为200mL不变)。

根据要求回答相关问题
(1)装置甲中通入燃料甲醚的一极是
(2)装置乙中Fe为
(3)如果粗铜中含有锌、银等杂质,丙装置的阳极泥中含有
(4)当装置甲中消耗0.05mol O2时,装置乙中溶液的pH为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】如图所示,某化学兴趣小组设计了一个燃料电池,并探究氯碱工业原理和粗铜精炼原理,其中乙装置中X为阳离子交换膜。根据要求回答相关问题:
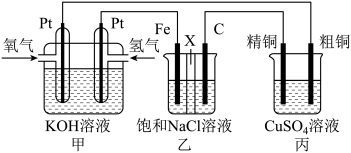
(1)通入氧气的电极为_____ (填“正极”或“负极”),此电极反应式为_________ 。
(2)铁电极为_______ (填“阳极”或“阴极”),乙装置中电解反应的化学方程式为_________________ 。
(3)某粗铜中含有铁、金、银和铂等杂质,通过电解精制后,为从电解液中制得硫酸铜晶体(CuSO4·5H2O),设计了如下工艺流程:

已知:几种金属阳离子开始沉淀和沉淀完全的pH。
①步骤I中加入试剂A的目的是_____________________________ ,试剂A应选择______ (填序号);
a.氯气 b.过氧化氢 C.酸性高锰酸钾溶液
②步骤II中试剂B为_________ (答出一种即可),调节pH的范围是___________ ;
③步骤III的操作是加热浓缩、___________ 、过滤。

(1)通入氧气的电极为
(2)铁电极为
(3)某粗铜中含有铁、金、银和铂等杂质,通过电解精制后,为从电解液中制得硫酸铜晶体(CuSO4·5H2O),设计了如下工艺流程:

已知:几种金属阳离子开始沉淀和沉淀完全的pH。
| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
| Fe3+ | 1.9 | 3.2 |
| Fe2+ | 7.6 | 9.6 |
| Cu2+ | 4.7 | 6.7 |
a.氯气 b.过氧化氢 C.酸性高锰酸钾溶液
②步骤II中试剂B为
③步骤III的操作是加热浓缩、
您最近一年使用:0次



