现有部分元素的性质与原子或分子结构的相关信息如表所示:
(1)T、X、Y、Z形成的简单离子半径由大到小的顺序是_______ 。(用离子符号表示)
(2)元素Y与元素Z相比,金属性较强的是_______ (用元素符号表示),下列表述中能证明这一事实的是_______ 填字母序号。
a.Y单质的熔点比Z单质的低
b.Y的化合价比Z的低
c.常温下Y单质与水反应很剧烈,而Z单质与水很难反应
d.Y最高价氧化物对应的水化物的碱性比Z的强
(3)T、X、Y、Z中有两种元素能形成既含离子键又含非极性共价键的常见化合物,写出该化合物的化学式_______ 。请指出元素T在周期表中的位置_______ 。
(4)元素X与氢元素以原子个数比1∶2化合时,形成可用于火箭燃料的化合物W(W的相对分子质量为32)。元素T和氢元素以原子个数比1:1化合形成化合物Q。Q与W发生氧化还原反应生成X的单质和的T另一种氢化物,请写出Q与W反应的化学方程式_______ 。
| 元素编号 | 元素性质与原子(或分子)结构的相关信息 |
| T | 最外层电子数是次外层电子数的3倍 |
| X | 常温下单质分子为双原子分子,分子中含有3对共用电子对 |
| Y | M层比K层少1个电子 |
| Z | 其离子是第三周期金属元素的离子中半径最小的 |
(2)元素Y与元素Z相比,金属性较强的是
a.Y单质的熔点比Z单质的低
b.Y的化合价比Z的低
c.常温下Y单质与水反应很剧烈,而Z单质与水很难反应
d.Y最高价氧化物对应的水化物的碱性比Z的强
(3)T、X、Y、Z中有两种元素能形成既含离子键又含非极性共价键的常见化合物,写出该化合物的化学式
(4)元素X与氢元素以原子个数比1∶2化合时,形成可用于火箭燃料的化合物W(W的相对分子质量为32)。元素T和氢元素以原子个数比1:1化合形成化合物Q。Q与W发生氧化还原反应生成X的单质和的T另一种氢化物,请写出Q与W反应的化学方程式
更新时间:2023-02-17 07:29:22
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】铜器在空气中久置会和空气中的水蒸气、 、
、 作用产生绿锈,该绿锈俗称铜绿,又称孔雀石[主要成分为
作用产生绿锈,该绿锈俗称铜绿,又称孔雀石[主要成分为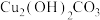 ],铜绿能与酸反应生成铜盐、
],铜绿能与酸反应生成铜盐、 和
和 。某同学实现了
。某同学实现了 的转化。
的转化。
回答下列问题:
(1)“铜→铜绿”的化学方程式为___________ 。
(2)若“铜绿→M”时,加入足量的稀硫酸,紧接着“ ”时,加入足量的
”时,加入足量的 ,经过上述操作,
,经过上述操作,___________ (填“能”或“不能”)得到纯净的 ,理由为
,理由为___________ 。
(3)“ ”的过程中,过滤时主要用到的玻璃仪器有
”的过程中,过滤时主要用到的玻璃仪器有___________ 。“P→Cu”的反应过程中观察到的现象为___________ 。
(4)取mg铜绿投入足量的稀硫酸中,产生的 的质量为
的质量为___________ g。
 、
、 作用产生绿锈,该绿锈俗称铜绿,又称孔雀石[主要成分为
作用产生绿锈,该绿锈俗称铜绿,又称孔雀石[主要成分为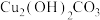 ],铜绿能与酸反应生成铜盐、
],铜绿能与酸反应生成铜盐、 和
和 。某同学实现了
。某同学实现了 的转化。
的转化。回答下列问题:
(1)“铜→铜绿”的化学方程式为
(2)若“铜绿→M”时,加入足量的稀硫酸,紧接着“
 ”时,加入足量的
”时,加入足量的 ,经过上述操作,
,经过上述操作, ,理由为
,理由为(3)“
 ”的过程中,过滤时主要用到的玻璃仪器有
”的过程中,过滤时主要用到的玻璃仪器有(4)取mg铜绿投入足量的稀硫酸中,产生的
 的质量为
的质量为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】某科研小组采用如图所示方案回收一种光盘金属层中的少量Ag(金属层中其他金属含量过低,对实验的影响可忽略)。

已知:①NaClO溶液在受热或酸性条件下易分解,如:3NaClO=2NaCl+NaClO3
②AgCl可溶于氨水:AgCl+2NH3•H2O Ag(NH3)
Ag(NH3) +Cl-+2H2O
+Cl-+2H2O
③常温时N2H4•H2O(水合肼)在碱性条件下能还原Ag(NH3) :4Ag(NH3)
:4Ag(NH3) +N2H4•H2O=4Ag↓+N2↑+4NH
+N2H4•H2O=4Ag↓+N2↑+4NH +4NH3↑+H2O
+4NH3↑+H2O
(1)“氧化”阶段需在80℃条件下进行,适宜的加热方式为___ 。
(2)NaClO溶液与Ag反应的产物为AgCl、NaOH和O2,该反应的化学方程式为__ 。HNO3也能氧化Ag,从反应产物的角度分析,以HNO3代替NaClO的缺点是__ 。
(3)为提高Ag的回收率,需对“过滤Ⅱ”的滤渣进行洗涤,并__ 。
(4)请设计从“过滤Ⅱ”后的滤液中获取单质Ag的实验方案:__ (实验中须使用的试剂有:2mol•L-1水合肼溶液,1mol•L-1H2SO4)。

已知:①NaClO溶液在受热或酸性条件下易分解,如:3NaClO=2NaCl+NaClO3
②AgCl可溶于氨水:AgCl+2NH3•H2O
 Ag(NH3)
Ag(NH3) +Cl-+2H2O
+Cl-+2H2O③常温时N2H4•H2O(水合肼)在碱性条件下能还原Ag(NH3)
 :4Ag(NH3)
:4Ag(NH3) +N2H4•H2O=4Ag↓+N2↑+4NH
+N2H4•H2O=4Ag↓+N2↑+4NH +4NH3↑+H2O
+4NH3↑+H2O(1)“氧化”阶段需在80℃条件下进行,适宜的加热方式为
(2)NaClO溶液与Ag反应的产物为AgCl、NaOH和O2,该反应的化学方程式为
(3)为提高Ag的回收率,需对“过滤Ⅱ”的滤渣进行洗涤,并
(4)请设计从“过滤Ⅱ”后的滤液中获取单质Ag的实验方案:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】工业以软锰矿(主要成分 ,含
,含 、
、 、
、 等杂质)和硫铁矿(主要成分为
等杂质)和硫铁矿(主要成分为 )为原料制备高纯
)为原料制备高纯 的流程如下。
的流程如下。
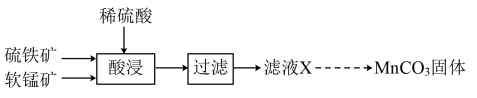
已知:
ⅰ.滤液X中的金属阳离子主要为 、
、 ,还含有少量的
,还含有少量的 和
和 。
。
ⅱ.常温下,溶液中部分金属离子开始沉淀时的pH见下表(金属离子浓度以1mol/L计算)。
(1)基态锰原子的核外电子排布式为___________ 。
(2)“过滤”所得滤渣中含有S、等,生成硫单质的离子方程式为___________ 。
(3)为获得高纯 (除杂时杂质离子浓度不大于
(除杂时杂质离子浓度不大于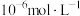 ),请补充完整由滤液X制备高纯
),请补充完整由滤液X制备高纯 的实验方案:取滤液X,
的实验方案:取滤液X,___________ ,低温干燥,得高纯 。(实验中须使用的试剂:氨水、
。(实验中须使用的试剂:氨水、 固体、
固体、 、
、 溶液、蒸馏水)
溶液、蒸馏水)
(4)利用 制备
制备 过程中发生如下反应:
过程中发生如下反应: ,
,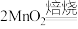
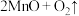 。为测定焙烧后所得氧化物的成分,设计如下实验:
。为测定焙烧后所得氧化物的成分,设计如下实验:
步骤1:取一定量固体,加入10.00mL 0.5000
 溶液,在酸性条件下充分反应。
溶液,在酸性条件下充分反应。
步骤2:用0.05000 的
的 滴定溶液中的
滴定溶液中的 ,滴定至终点时,消耗
,滴定至终点时,消耗 10.00mL。(
10.00mL。( 未配平)。
未配平)。
步骤3:加热条件下,加入适量 将溶液中
将溶液中 氧化为Mn(Ⅲ)。持续加热一段时间后冷却,用0.1500
氧化为Mn(Ⅲ)。持续加热一段时间后冷却,用0.1500 的
的 标准液滴定生成的Mn(Ⅲ),滴定至终点时,消耗标准溶液20.00mL。
标准液滴定生成的Mn(Ⅲ),滴定至终点时,消耗标准溶液20.00mL。
计算焙烧后产物中Mn和O的物质的量之比。(写出计算过程)________
 ,含
,含 、
、 、
、 等杂质)和硫铁矿(主要成分为
等杂质)和硫铁矿(主要成分为 )为原料制备高纯
)为原料制备高纯 的流程如下。
的流程如下。
已知:
ⅰ.滤液X中的金属阳离子主要为
 、
、 ,还含有少量的
,还含有少量的 和
和 。
。ⅱ.常温下,溶液中部分金属离子开始沉淀时的pH见下表(金属离子浓度以1mol/L计算)。
| 金属离子 |  |  |  |  |
| 开始沉淀pH | 1.5 | 3.3 | 6.5 | 8.3 |
(2)“过滤”所得滤渣中含有S、等,生成硫单质的离子方程式为
(3)为获得高纯
 (除杂时杂质离子浓度不大于
(除杂时杂质离子浓度不大于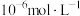 ),请补充完整由滤液X制备高纯
),请补充完整由滤液X制备高纯 的实验方案:取滤液X,
的实验方案:取滤液X, 。(实验中须使用的试剂:氨水、
。(实验中须使用的试剂:氨水、 固体、
固体、 、
、 溶液、蒸馏水)
溶液、蒸馏水)(4)利用
 制备
制备 过程中发生如下反应:
过程中发生如下反应: ,
,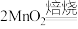
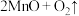 。为测定焙烧后所得氧化物的成分,设计如下实验:
。为测定焙烧后所得氧化物的成分,设计如下实验:步骤1:取一定量固体,加入10.00mL 0.5000

 溶液,在酸性条件下充分反应。
溶液,在酸性条件下充分反应。步骤2:用0.05000
 的
的 滴定溶液中的
滴定溶液中的 ,滴定至终点时,消耗
,滴定至终点时,消耗 10.00mL。(
10.00mL。( 未配平)。
未配平)。步骤3:加热条件下,加入适量
 将溶液中
将溶液中 氧化为Mn(Ⅲ)。持续加热一段时间后冷却,用0.1500
氧化为Mn(Ⅲ)。持续加热一段时间后冷却,用0.1500 的
的 标准液滴定生成的Mn(Ⅲ),滴定至终点时,消耗标准溶液20.00mL。
标准液滴定生成的Mn(Ⅲ),滴定至终点时,消耗标准溶液20.00mL。计算焙烧后产物中Mn和O的物质的量之比。(写出计算过程)
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】A、B、C、D四种元素都是短周期元素。A元素的离子具有黄色的焰色反应。B元素的离子结构和Ne具有相同的电子层排布;5.8gB的氢氧化物恰好能与100mL2mol/L盐酸完全反应;B原子核中质子数和中子数相等。H2在C单质中燃烧产生苍白色火焰。D元素原子的电子层结构里,最外层电子数是次外层电子数的3倍。根据上述条件,回答:
(1)元素C位于第_____ 周期______ 族,它的最高价氧化物的化学式为_______ 。
(2)A是________ 元素,B是___________ 元素,D是___________ 元素。(填元素符号)
(3)A与D形成稳定化合物的化学式为________ ,该化合物是由____________ 键形成的。写出该化合物与CO2反应的化学方程式_______________________________________ 。
(4)C元素的单质有毒,可用A的最高价氧化物对应的水化物的溶液吸收,其离子方程式为_______________________________________________________________ 。
(1)元素C位于第
(2)A是
(3)A与D形成稳定化合物的化学式为
(4)C元素的单质有毒,可用A的最高价氧化物对应的水化物的溶液吸收,其离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】已知X、Y、Z都是短周期主族元素,它们的原子序数依次递增,X原子的电子层数与它的核外电子总数相同,而Z原子的最外层电子数是次外层电子数的三倍,Y和Z可以形成两种以上气态化合物。
(1)写出X2Z2的电子式_________ ,Y单质分子的结构式____________ 。
(2)由Y和Z组成,且Y和Z质量比为7∶20的化合物的分子式是_____________ 。
(3)写出由X、Y、Z中的两种元素组成,且与X2Z分子具有相同电子数的两种离子,阳离子_____ 阴离子______ 。
(4)X、Y、Z可以形成一种盐,此盐中X、Y、Z元素的原子个数比为4∶2∶3,该盐的化学式是_____ 。X、Y也能形成一种盐,X、Y元素的原子个数比为5∶1,则该盐的化学式为 ______________________________
(5)下列说法正确的是( )
a.氢化物热稳定性:Y>Z
b.氢化物的熔沸点:Y>Z
c.原子半径:Y>Z
d.Z的氢化物的熔沸点比同主族其他物质的高,是因为分子内形成了氢键
(1)写出X2Z2的电子式
(2)由Y和Z组成,且Y和Z质量比为7∶20的化合物的分子式是
(3)写出由X、Y、Z中的两种元素组成,且与X2Z分子具有相同电子数的两种离子,阳离子
(4)X、Y、Z可以形成一种盐,此盐中X、Y、Z元素的原子个数比为4∶2∶3,该盐的化学式是
(5)下列说法正确的是
a.氢化物热稳定性:Y>Z
b.氢化物的熔沸点:Y>Z
c.原子半径:Y>Z
d.Z的氢化物的熔沸点比同主族其他物质的高,是因为分子内形成了氢键
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】W、X、Y、Z、M、N六种元素的原子序数依次递增,其中W、X、Y、Z为短周期元素,六种元素的元素性质或原子结构特征如下表,回答下列问题。
(1)写出元素Z元素周期表中的位置___________ 。
(2)W、X、Y三种元素的电负性数值由大到小的顺序为___________ (用元素符号作答,下同),这三种元素的第一电离能由大到小的顺序为___________ 。
(3)写出元素M的价层电子排布式___________ 。
(4)写出元素N的N3+最外层电子排布式___________ 。
| 元素 | 元素性质或原子结构特征 |
| W | 原子p轨道的电子数为2 |
| X | 原子中最高能级的不同轨道都有电子,且自旋方向相同 |
| Y | 最外能层电子数是最内能层电子数的3倍 |
| Z | 原子核外s能级上的电子总数与p能级上的电子总数相等,但第一电离能都高于同周期相邻元素 |
| M | 第24号元素 |
| N | 一种常见的金属元素,正三价离子遇硫氰化钾显红色 |
(2)W、X、Y三种元素的电负性数值由大到小的顺序为
(3)写出元素M的价层电子排布式
(4)写出元素N的N3+最外层电子排布式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】元素是构成我们生活的世界中一切物质的“原材料”。
(1)1869年,门捷列夫在前人研究的基础上制出了第一张元素周期表,随着化学科学的不断发展,门捷列夫在周期表中为未知元素留下的空位逐渐被填满。而且,随着对原子结构的揭秘,科学家们发现了元素性质不是随着相对原子质量的递增呈现周期性变化,而是随着原子序数(核电荷数)的递增呈现周期性变化。其本质原因是_______ (填序号)。
A.随着核电荷数的递增,原子核外电子排布呈现周期性变化
B.随着核电荷数的递增,原子半径呈现周期性变化
C.随着核电荷数的递增,元素最高正化合价呈现周期性变化
(2)有A、B、D、E、X、Y、Z七种短周期主族元素。X、Y、Z处于同一周期,Y的最高价氧化物对应的水化物与强酸、强碱均能反应,Z的单质常温下为气态,相同条件下相对于氢气的密度为35.5,其余元素的信息如图所示。

①上述七种元素中,处于第二周期的有_______ (填元素符号),X在周期表中的位置是_______ 。
②E的原子结构示意图为_______ 。
③Y的最高价氧化物对应水化物与X的最高价氧化物对应水化物反应的离子方程式为_______ 。
④B和D的最高价氧化物对应的水化物的化学式分别为_______ 、_______ ,二者酸性前者_______ (填“强于”或“弱于”)后者,原因是B和D的非金属性有差异,利用原子结构解释产生差异的原因:_______ 。
(1)1869年,门捷列夫在前人研究的基础上制出了第一张元素周期表,随着化学科学的不断发展,门捷列夫在周期表中为未知元素留下的空位逐渐被填满。而且,随着对原子结构的揭秘,科学家们发现了元素性质不是随着相对原子质量的递增呈现周期性变化,而是随着原子序数(核电荷数)的递增呈现周期性变化。其本质原因是
A.随着核电荷数的递增,原子核外电子排布呈现周期性变化
B.随着核电荷数的递增,原子半径呈现周期性变化
C.随着核电荷数的递增,元素最高正化合价呈现周期性变化
(2)有A、B、D、E、X、Y、Z七种短周期主族元素。X、Y、Z处于同一周期,Y的最高价氧化物对应的水化物与强酸、强碱均能反应,Z的单质常温下为气态,相同条件下相对于氢气的密度为35.5,其余元素的信息如图所示。

①上述七种元素中,处于第二周期的有
②E的原子结构示意图为
③Y的最高价氧化物对应水化物与X的最高价氧化物对应水化物反应的离子方程式为
④B和D的最高价氧化物对应的水化物的化学式分别为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】下列为元素周期表中的一部分,用化学式或元素符号回答下列问题。
(1)10种元素中,化学性质最不活泼的是_______ (填元素符号);
(2)①②⑤中,最高价氧化物的水化物,碱性最强的是_______ (填化学式):
(3)元素⑦形成的双原子分子的电子式为_______ 。
(4)元素⑥和⑦分别形成的氢化物稳定性强弱关系为_______ 。(填化学式,下同)
(5)10种元素中,最高价氧化物对应水化物酸性最强的是_______ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | O |
| 2 | ⑥ | ⑦ | ||||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 4 | ② | ④ | ⑨ |
(2)①②⑤中,最高价氧化物的水化物,碱性最强的是
(3)元素⑦形成的双原子分子的电子式为
(4)元素⑥和⑦分别形成的氢化物稳定性强弱关系为
(5)10种元素中,最高价氧化物对应水化物酸性最强的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】下表列出了①-⑪元素在元素周期表中的部分位置:
请回答下列问题。
(1)元素⑩在周期表中的位置:____________________ 。
(2)⑤、⑨元素的碱性强弱顺序的是______________ (用化学式表示)。
(3)写出一种含②元素的10电子化合物_______________ (填化学式)。
(4)写出元素⑨的单质与水反应的离子方程式_______________________________ 。
(5)写出元素⑦的最高价氧化物跟氢氧化钠溶液反应的离子方程式_____________ 。
(6)写出由⑧元素形成的单质与水反应的离子方程式_____________________ 。
(7)能比较⑧和⑪的非金属性强弱的依据是_____________ (填字母)
a.氢化物酸性⑧弱于⑪
b.⑧的单质与氢气化合比⑪的单质容易
c .最高价氧化物的水化物的酸性⑧强于⑪
| ① | |||||||||||||||||
| ② | ③ | ④ | |||||||||||||||
| ⑤ | ⑥ | ⑦ | ⑧ | ||||||||||||||
| ⑨ | ⑩ | ⑪ | |||||||||||||||
(1)元素⑩在周期表中的位置:
(2)⑤、⑨元素的碱性强弱顺序的是
(3)写出一种含②元素的10电子化合物
(4)写出元素⑨的单质与水反应的离子方程式
(5)写出元素⑦的最高价氧化物跟氢氧化钠溶液反应的离子方程式
(6)写出由⑧元素形成的单质与水反应的离子方程式
(7)能比较⑧和⑪的非金属性强弱的依据是
a.氢化物酸性⑧弱于⑪
b.⑧的单质与氢气化合比⑪的单质容易
c .最高价氧化物的水化物的酸性⑧强于⑪
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】现有A、B、C、D四种短周期主族元素,其中原子序数依次增大。已知B和D同主族。A元素的最高正价和最低负价的绝对值之差为2;1molC单质能与冷水反应,在标准状况下生成11.2LH2;D-的电子层结构与Ar原子相同。请回答下列问题:
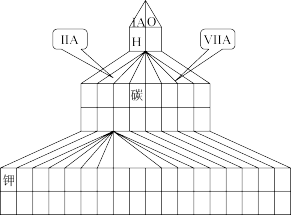
⑴在下图塔式周期表相应位置标出A、B、C、D四种元素的元素符号。同时在图中将过渡元素涂黑。
_____________
⑵用电子式表示B与C形成化合物的过程___________ 。
⑶图中“钾”和D形成的简单离子的半径大小为________________ (用离子符号和“>”、“=”或“<”表示)。
⑷元素非金属性强弱比较有很多方法,其中A和D的非金属性强弱的研究方案中比较可行的是_______ (填序号)。
①比较两种单质的颜色②比较氢化物的稳定性
③比较原子半径大小④比较最高价氧化物对应水化物的酸性
⑸A元素能与另外三种元素中的一种元素形成共价化合物,分子中的原子个数比为1:3,相对分子质量为120.5。则该物质的结构式为____________ 。
⑴在下图塔式周期表相应位置标出A、B、C、D四种元素的元素符号。同时在图中将过渡元素涂黑。

⑵用电子式表示B与C形成化合物的过程
⑶图中“钾”和D形成的简单离子的半径大小为
⑷元素非金属性强弱比较有很多方法,其中A和D的非金属性强弱的研究方案中比较可行的是
①比较两种单质的颜色②比较氢化物的稳定性
③比较原子半径大小④比较最高价氧化物对应水化物的酸性
⑸A元素能与另外三种元素中的一种元素形成共价化合物,分子中的原子个数比为1:3,相对分子质量为120.5。则该物质的结构式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】随原子序数递增,八种短周期元素(用字母x等表示)原子半径的相对大小、最高正价或最低负价的变化如图所示。

根据判断出的元素回答问题:
(1)f在周期表中的位置是____ 。
(2)比较d、e常见离子的半径大小(用化学式表示,下同):____ >____ ;比较g、h的最高价氧化物对应水化物的酸性强弱:____ >____ 。
(3)任选上述元素组成一种四原子共价化合物,写出其电子式:_________ 。
(4)已知1 mol e的单质在足量d2中燃烧,恢复至室温,放出255.5 kJ热量,写出该反应的热化学方程式:_________________ 。
(5)上述元素可组成盐R:zx4f(gd4)2。向盛有10 mL 1 mol·L-1 R溶液的烧杯中滴加1 mol·L-1 NaOH溶液,沉淀物质的量随NaOH溶液体积的变化示意图如图:
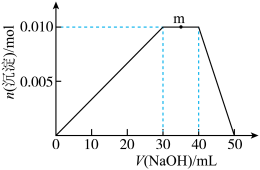
①R化学式为:________ ,其物质的量为________ 。
②写出m点反应的离子方程式:_________ 。
③若在R溶液中改加20 mL 1.1 mol·L-1 Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为_____ mol。

根据判断出的元素回答问题:
(1)f在周期表中的位置是
(2)比较d、e常见离子的半径大小(用化学式表示,下同):
(3)任选上述元素组成一种四原子共价化合物,写出其电子式:
(4)已知1 mol e的单质在足量d2中燃烧,恢复至室温,放出255.5 kJ热量,写出该反应的热化学方程式:
(5)上述元素可组成盐R:zx4f(gd4)2。向盛有10 mL 1 mol·L-1 R溶液的烧杯中滴加1 mol·L-1 NaOH溶液,沉淀物质的量随NaOH溶液体积的变化示意图如图:

①R化学式为:
②写出m点反应的离子方程式:
③若在R溶液中改加20 mL 1.1 mol·L-1 Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大。A与D同主族;C与E同主族;B、C同周期;B原子最外层电子数比其次外层电子数多2;B、A两元素的核电荷数之差等于它们的原子最外层电子数之和;F元素是同周期元素中原子半径最小的主族元素。A、B、C、D、E、F形成的化合物甲、乙、丙、丁、戊、己的组成如下表所示。
回答下列问题
(1)元素B的元素符号是:____________ 化合物丙的电子式为________________ 。化合物丁存在的化学键类型是_________ 。
(2)化合物甲的沸点比戊____________ (填“高”或“低”),B、C、D原子半径从大到小依次为_______________ (用元素符号)
(3)向含有0.2 mol乙的水溶液中加入少量MnO2,使乙完全反应,发生转移的电子数为_________ NA (NA代表阿伏加德罗常数)
(4)A单质与C单质在KOH溶液中可以组成燃料电池,则正极附近溶液的pH将_____________ ;放电一段时间KOH的物质的量_________ (填“变大”“变小”“不变”)
(5)用电子式表示己的形成过程:__________________________________ 。
| 化合物 | 甲 | 乙 | 丙 | 丁 | 戊 | 己 |
| 化学式 | A2C | A2C2 | B2A2 | D2C2 | A2E | DF |
(1)元素B的元素符号是:
(2)化合物甲的沸点比戊
(3)向含有0.2 mol乙的水溶液中加入少量MnO2,使乙完全反应,发生转移的电子数为
(4)A单质与C单质在KOH溶液中可以组成燃料电池,则正极附近溶液的pH将
(5)用电子式表示己的形成过程:
您最近一年使用:0次



