亚硝酸钠( ,外观极像食盐,一样有咸味)是一种重要的化工原料,酸性条件下能氧化碘离子等还原性物质。已知亚硝酸(
,外观极像食盐,一样有咸味)是一种重要的化工原料,酸性条件下能氧化碘离子等还原性物质。已知亚硝酸( )是一种弱酸,不稳定,易分解生成NO(无色)气体和
)是一种弱酸,不稳定,易分解生成NO(无色)气体和 (红棕色)气体;
(红棕色)气体; 是一种难溶于水(白色)、易溶于酸的化合物。回答下列问题:
是一种难溶于水(白色)、易溶于酸的化合物。回答下列问题:
(1)人体正常的血红蛋白含有 ,若误食亚硝酸钠会把
,若误食亚硝酸钠会把 转换为
转换为 而中毒,应立即注射美蓝溶液进行治疗。上述过程中
而中毒,应立即注射美蓝溶液进行治疗。上述过程中 表现出
表现出_______ 性(填“氧化”或“还原”下同),亚硝酸钠作_______ 剂,美蓝溶液被_______ 。
(2)下列有关检验工业食盐中是否混有亚硝酸钠的说法错误的是_______ 。
A.取样品,加碘化钾淀粉溶液,酸化后溶液变蓝,说明样品中含有亚硝酸钠
B.取样品,加稀硫酸,若观察到产生红棕色气体,证明样品中含有亚硝酸钠
C.取样品,加水溶解后,向其中加入 溶液,若观察到出现白色沉淀,则证明有亚硝酸钠
溶液,若观察到出现白色沉淀,则证明有亚硝酸钠
(3)可用适量二氧化氯( )处理鱼塘中过量的亚硝酸钠,
)处理鱼塘中过量的亚硝酸钠, 被还原为
被还原为 ,该反应氧化剂与还原剂的物质的量之比为
,该反应氧化剂与还原剂的物质的量之比为_______ ;若有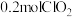 参与反应,则转移电子的数目是
参与反应,则转移电子的数目是_______ 。
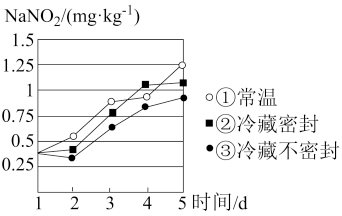
(4)某腌制品中亚硝酸钠含量随时间变化如图所示,若要保证在亚硝酸钠含量低于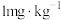 时食用,则三种条件下保存时间最长的是
时食用,则三种条件下保存时间最长的是_______ (填序号)。
 ,外观极像食盐,一样有咸味)是一种重要的化工原料,酸性条件下能氧化碘离子等还原性物质。已知亚硝酸(
,外观极像食盐,一样有咸味)是一种重要的化工原料,酸性条件下能氧化碘离子等还原性物质。已知亚硝酸( )是一种弱酸,不稳定,易分解生成NO(无色)气体和
)是一种弱酸,不稳定,易分解生成NO(无色)气体和 (红棕色)气体;
(红棕色)气体; 是一种难溶于水(白色)、易溶于酸的化合物。回答下列问题:
是一种难溶于水(白色)、易溶于酸的化合物。回答下列问题:(1)人体正常的血红蛋白含有
 ,若误食亚硝酸钠会把
,若误食亚硝酸钠会把 转换为
转换为 而中毒,应立即注射美蓝溶液进行治疗。上述过程中
而中毒,应立即注射美蓝溶液进行治疗。上述过程中 表现出
表现出(2)下列有关检验工业食盐中是否混有亚硝酸钠的说法错误的是
A.取样品,加碘化钾淀粉溶液,酸化后溶液变蓝,说明样品中含有亚硝酸钠
B.取样品,加稀硫酸,若观察到产生红棕色气体,证明样品中含有亚硝酸钠
C.取样品,加水溶解后,向其中加入
 溶液,若观察到出现白色沉淀,则证明有亚硝酸钠
溶液,若观察到出现白色沉淀,则证明有亚硝酸钠(3)可用适量二氧化氯(
 )处理鱼塘中过量的亚硝酸钠,
)处理鱼塘中过量的亚硝酸钠, 被还原为
被还原为 ,该反应氧化剂与还原剂的物质的量之比为
,该反应氧化剂与还原剂的物质的量之比为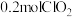 参与反应,则转移电子的数目是
参与反应,则转移电子的数目是(4)某腌制品中亚硝酸钠含量随时间变化如图所示,若要保证在亚硝酸钠含量低于
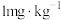 时食用,则三种条件下保存时间最长的是
时食用,则三种条件下保存时间最长的是
更新时间:2023-02-24 10:42:47
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】氧化还原反应的学习,为我们研究化学物质和化学反应提供了新的视角:
(1)吸入人体内的氧有2%转化为氧化性极强的“活性氧”,它能加速人体衰老,被称为“生命杀手”,服用维生素C能消除人体内的活性氧,由此推断维生素C的作用是_______ 。
(2)高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,湿法制备高铁酸钠的原理为: 。该反应中氧化剂是
。该反应中氧化剂是_______ ;被氧化的元素是_______
(3)配平下列方程式:_______ 。
_______ _______
_______ _______
_______ _______
_______ _______
_______ _______
_______
(4)已知反应:①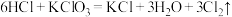
②
③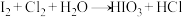 (未配平)
(未配平)
a)使用单线桥法标出反应①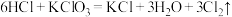 的电子转移方向和数目
的电子转移方向和数目_______ 。
b)根据以上三个方程式判断,下列说法正确的是_______
A.还原性由强到弱顺序:
B.氧化性由强到弱顺序: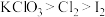
C.反应③中氧化剂和还原剂的系数之比为1∶5
D.结合反应②③,将足量 通入含有淀粉的
通入含有淀粉的 溶液中,可能会观察到先变蓝后褪色
溶液中,可能会观察到先变蓝后褪色
(1)吸入人体内的氧有2%转化为氧化性极强的“活性氧”,它能加速人体衰老,被称为“生命杀手”,服用维生素C能消除人体内的活性氧,由此推断维生素C的作用是
(2)高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,湿法制备高铁酸钠的原理为:
 。该反应中氧化剂是
。该反应中氧化剂是(3)配平下列方程式:
_______
 _______
_______ _______
_______ _______
_______ _______
_______ _______
_______
(4)已知反应:①
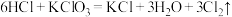
②

③
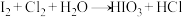 (未配平)
(未配平)a)使用单线桥法标出反应①
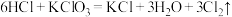 的电子转移方向和数目
的电子转移方向和数目b)根据以上三个方程式判断,下列说法正确的是
A.还原性由强到弱顺序:

B.氧化性由强到弱顺序:
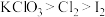
C.反应③中氧化剂和还原剂的系数之比为1∶5
D.结合反应②③,将足量
 通入含有淀粉的
通入含有淀粉的 溶液中,可能会观察到先变蓝后褪色
溶液中,可能会观察到先变蓝后褪色
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】已知铜和浓硫酸可以在加热条件下发生反应,化学方程式如下(已配平):Cu+2H2SO4(浓) CuSO4+A↑+2H2O,试通过计算和推理完成下面的填空:
CuSO4+A↑+2H2O,试通过计算和推理完成下面的填空:
(1)在参加反应的硫酸中,被还原的硫酸与未被还原的硫酸的物质的量之比为___________ 。
(2)一定量的铜片与 的浓硫酸充分反应(浓硫酸过量),如果该反应过程中转移了0.6mol电子,生成的A气体在标准状况下的体积为
的浓硫酸充分反应(浓硫酸过量),如果该反应过程中转移了0.6mol电子,生成的A气体在标准状况下的体积为___________ L(假设气体全部逸出)。
(3)将(2)中反应后所得的溶液稀释后与足量的 溶液反应,所得沉淀的质量为
溶液反应,所得沉淀的质量为___________ g。
 CuSO4+A↑+2H2O,试通过计算和推理完成下面的填空:
CuSO4+A↑+2H2O,试通过计算和推理完成下面的填空:(1)在参加反应的硫酸中,被还原的硫酸与未被还原的硫酸的物质的量之比为
(2)一定量的铜片与
 的浓硫酸充分反应(浓硫酸过量),如果该反应过程中转移了0.6mol电子,生成的A气体在标准状况下的体积为
的浓硫酸充分反应(浓硫酸过量),如果该反应过程中转移了0.6mol电子,生成的A气体在标准状况下的体积为(3)将(2)中反应后所得的溶液稀释后与足量的
 溶液反应,所得沉淀的质量为
溶液反应,所得沉淀的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】完成下列问题。
(1)有下列反应:
①SO3+H2O=H2SO4
②Cl2+H2O=HCl+HClO
③2F2+2H2O=4HF+O2
④CO2+2NaOH=Na2CO3+H2O
上述反应中不属于氧化还原反应的是_______ (填序号,下同);H2O只作还原剂的是_______ ;属于氧化还原反应,但其中的H2O既不被氧化,又不被还原的是_______ 。
(2)为治理汽车尾气中的NO和CO对环境的污染,可在汽车排气管上安装催化转化器,发生如下反应:2NO+2CO N2+2CO2。
N2+2CO2。
①用双线桥标出电子转移的方向和数目_______ 。
②若消耗30 g的NO得到还原产物的质量为_______ g。
(1)有下列反应:
①SO3+H2O=H2SO4
②Cl2+H2O=HCl+HClO
③2F2+2H2O=4HF+O2
④CO2+2NaOH=Na2CO3+H2O
上述反应中不属于氧化还原反应的是
(2)为治理汽车尾气中的NO和CO对环境的污染,可在汽车排气管上安装催化转化器,发生如下反应:2NO+2CO
 N2+2CO2。
N2+2CO2。①用双线桥标出电子转移的方向和数目
②若消耗30 g的NO得到还原产物的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】按要求回答下列问题:
(1)标准状况下,1.12LCH4的质量为_______ g。
(2)与3.2gSO2所含的O 原子 数相等的NO2 的质量为_______ g。
(3)配制500mL1.0mol·L-1CuSO4溶液时,在移液洗涤后,摇动容量瓶有少量液体溅出,则所配溶液物质的量浓变会_______ (选填“偏高”、“偏低”、“无影响”)。
(4)把2.0mol·L-1Na2SO4溶液和1.0mol·L-1H2SO4溶液等体积混合(假设混合后溶液的体积为两者体积之和),则SO42-的物质的量浓度为_______ mol·L-1。
(5)浓氨水可用于检验氯气管道是否漏气,其原理是8NH3+3Cl2=6NH4Cl+N2。该反应中氧化剂与还原剂的物质的最之比为_______ 。
(1)标准状况下,1.12LCH4的质量为
(2)与3.2gSO2所含的O 原子 数相等的NO2 的质量为
(3)配制500mL1.0mol·L-1CuSO4溶液时,在移液洗涤后,摇动容量瓶有少量液体溅出,则所配溶液物质的量浓变会
(4)把2.0mol·L-1Na2SO4溶液和1.0mol·L-1H2SO4溶液等体积混合(假设混合后溶液的体积为两者体积之和),则SO42-的物质的量浓度为
(5)浓氨水可用于检验氯气管道是否漏气,其原理是8NH3+3Cl2=6NH4Cl+N2。该反应中氧化剂与还原剂的物质的最之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】高锰酸钾(KMnO4)是一种广泛使用的氧化剂和消毒剂。
(1)用酸性KMnO4溶液测定室内甲醛含量,产物中含有Mn2+和CO2,请推测该反应的离子方程式_______ 。
(2)将室内气体通入50 mL1×10-3 mol/L酸性KMnO4溶液中,通入5 L时,溶液颜色恰好变为无色,计算室内甲醛的浓度为_______ mg/L;
(3)上述酸性KMnO4是指用硫酸酸化的KMnO4溶液,请说明不使用盐酸酸化的理由_______ ,离子方程式为_______ 。
(4)配制KMnO4溶液,定容操作的方法为_______ 。
(5)KMnO4溶液与明矾溶液混合后,发生复分解反应,生成深紫色沉淀,写出该反应的化学方程式_______ 。
(6)KMnO4溶液与双氧水混合后,会产生气泡,这说明双氧水具有_______ 性。
(7)某种烃的相对分子质量为92,易使酸性KMnO4溶液褪色,但不能使溴水因发生化学变化而褪色,则该烃的结构简式为_______ 。
(1)用酸性KMnO4溶液测定室内甲醛含量,产物中含有Mn2+和CO2,请推测该反应的离子方程式
(2)将室内气体通入50 mL1×10-3 mol/L酸性KMnO4溶液中,通入5 L时,溶液颜色恰好变为无色,计算室内甲醛的浓度为
(3)上述酸性KMnO4是指用硫酸酸化的KMnO4溶液,请说明不使用盐酸酸化的理由
(4)配制KMnO4溶液,定容操作的方法为
(5)KMnO4溶液与明矾溶液混合后,发生复分解反应,生成深紫色沉淀,写出该反应的化学方程式
(6)KMnO4溶液与双氧水混合后,会产生气泡,这说明双氧水具有
(7)某种烃的相对分子质量为92,易使酸性KMnO4溶液褪色,但不能使溴水因发生化学变化而褪色,则该烃的结构简式为
您最近一年使用:0次
【推荐3】KClO3和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯。其变化可表述为:2KClO3+4HCl(浓)===2KCl+2ClO2↑+Cl2↑+2H2O。
(1)请分析该反应中电子转移的情况(用双线桥法表示)___________________________ 。
(2)浓盐酸在反应中显示出来的性质是________
(3)若产生0.1 mol Cl2,则被氧化的HCl的物质的量为________ mol。
(1)请分析该反应中电子转移的情况(用双线桥法表示)
(2)浓盐酸在反应中显示出来的性质是
(3)若产生0.1 mol Cl2,则被氧化的HCl的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】消毒剂在生活中应用广泛,Na2FeO 4、Cl2、ClO2、H2O2、NaClO 是生活中不同领域的消毒剂。根据下列反应回答问题
A.2H2O2 =2H2O+O2 ↑
B.16HCl+2KMnO4 =5Cl2↑+2MnCl2 +2KCl+8H2O
C.2Fe(OH)3 +3KClO+4KOH=2K2FeO4+3KCl+5H2O
D.2KClO3 +4HCl=2ClO2 ↑+2KCl+Cl2 ↑+2H2O
(1)储存过氧化氢的试剂瓶上最适合贴上的一个标签是_______(填序号)。
(2)反应 A 中,氧化产物是_______ ;反应 B 中,做还原剂的HCl与做酸性介质的HCl物质的量之比为_______ ,0.4mol KMnO4 参加反应,做酸性介质的 HCl的物质的量为_______ 。
(3)用双线桥表示反应C电子转移的方向和数目:_______
2Fe(OH)3 +3KClO+4KOH=2K2 FeO4 +3KCl+5H2O
(4)反应 D中0.2mol HCl参加反应,转移的电子数为_______ 。
(5)某强酸反应体系中发生的一个氧化还原的离子反应,反应物和生成物共六种微粒:H2O、ClO-、NH 、H+、N2、Cl-。其中c(Cl-)随反应进行逐渐增加。
、H+、N2、Cl-。其中c(Cl-)随反应进行逐渐增加。
①氧化产物与还原产物的物质的量之比为_______ 。
②反应后溶液的酸性_______ (填“增强”或“减弱”)。
(6)对于反应14CuSO4+5FeS2+12H2O=7Cu2S+5FeSO4+12H2SO4,1 mol硫酸铜可以氧化_______ mol的硫。
A.2H2O2 =2H2O+O2 ↑
B.16HCl+2KMnO4 =5Cl2↑+2MnCl2 +2KCl+8H2O
C.2Fe(OH)3 +3KClO+4KOH=2K2FeO4+3KCl+5H2O
D.2KClO3 +4HCl=2ClO2 ↑+2KCl+Cl2 ↑+2H2O
(1)储存过氧化氢的试剂瓶上最适合贴上的一个标签是_______(填序号)。
A. | B. | C. | D. |
(3)用双线桥表示反应C电子转移的方向和数目:
2Fe(OH)3 +3KClO+4KOH=2K2 FeO4 +3KCl+5H2O
(4)反应 D中0.2mol HCl参加反应,转移的电子数为
(5)某强酸反应体系中发生的一个氧化还原的离子反应,反应物和生成物共六种微粒:H2O、ClO-、NH
 、H+、N2、Cl-。其中c(Cl-)随反应进行逐渐增加。
、H+、N2、Cl-。其中c(Cl-)随反应进行逐渐增加。①氧化产物与还原产物的物质的量之比为
②反应后溶液的酸性
(6)对于反应14CuSO4+5FeS2+12H2O=7Cu2S+5FeSO4+12H2SO4,1 mol硫酸铜可以氧化
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】2021年12月13日从天津市疫情防控指挥部获悉,中国内地首次发现新冠病毒“奥密克戎”变异株。当下疫情对生产生活仍然影响极大,人们认识到日常杀菌消毒的重要性,其中含氯消毒剂在生产生活中有着广泛的用途。回答下列问题:
(1)写出实验室中制取氯气的离子方程式:___________ 。
(2)已知 与浓盐酸反应的化学方程式:
与浓盐酸反应的化学方程式: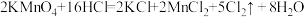 ,该反应也可以用来制取氯气,
,该反应也可以用来制取氯气,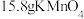 能和
能和___________ 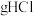 发生上述反应,其中有
发生上述反应,其中有___________ 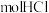 被氧化,产生的
被氧化,产生的 在标准状况下的体积为
在标准状况下的体积为___________ L。
(3)实验室还可以利用如下反应制取氯气: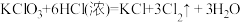 。若制取标准状况下
。若制取标准状况下 氯气,反应过程中转移电子的物质的量为
氯气,反应过程中转移电子的物质的量为___________ 。
(1)写出实验室中制取氯气的离子方程式:
(2)已知
 与浓盐酸反应的化学方程式:
与浓盐酸反应的化学方程式: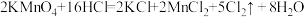 ,该反应也可以用来制取氯气,
,该反应也可以用来制取氯气,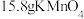 能和
能和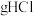 发生上述反应,其中有
发生上述反应,其中有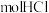 被氧化,产生的
被氧化,产生的 在标准状况下的体积为
在标准状况下的体积为(3)实验室还可以利用如下反应制取氯气:
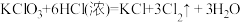 。若制取标准状况下
。若制取标准状况下 氯气,反应过程中转移电子的物质的量为
氯气,反应过程中转移电子的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】建筑工地常用的 因外观和食盐相似,又有咸味,容易使人误食中毒。已知
因外观和食盐相似,又有咸味,容易使人误食中毒。已知 能发生如下反应:__NaNO2+__HI →__NO↑+__I2+__NaI+ __H2O
能发生如下反应:__NaNO2+__HI →__NO↑+__I2+__NaI+ __H2O
(1)配平上述化学方程式,并用双线桥表示电子转移情况____ 。
(2)上述反应的氧化剂是____ ;若有1mol的还原剂被氧化,则反应中转移电子的数目是_______ 。
(3)根据上述反应,可用试纸和生活中常见的物质进行实验,以鉴别 和
和 ,可选用的物质有:①水、②淀粉-碘化钾试纸、③淀粉、④白酒、⑤食醋,选取上述物质进行实验,下列组合合适的是______(填字母)。
,可选用的物质有:①水、②淀粉-碘化钾试纸、③淀粉、④白酒、⑤食醋,选取上述物质进行实验,下列组合合适的是______(填字母)。
(4)某厂废液中,含有2%~5%的 ,直接排放会造成污染,使用
,直接排放会造成污染,使用 处理,能使
处理,能使 转化为不引起二次污染的
转化为不引起二次污染的 ,反应的化学方程式为
,反应的化学方程式为______ 。
(5)以过氧化氢作还原剂,在硫酸介质中还原NaClO3制备ClO2,并将制得的ClO2处理含CN-废水。ClO2处理含CN-废水的离子方程式为______ 。
 因外观和食盐相似,又有咸味,容易使人误食中毒。已知
因外观和食盐相似,又有咸味,容易使人误食中毒。已知 能发生如下反应:__NaNO2+__HI →__NO↑+__I2+__NaI+ __H2O
能发生如下反应:__NaNO2+__HI →__NO↑+__I2+__NaI+ __H2O(1)配平上述化学方程式,并用双线桥表示电子转移情况
(2)上述反应的氧化剂是
(3)根据上述反应,可用试纸和生活中常见的物质进行实验,以鉴别
 和
和 ,可选用的物质有:①水、②淀粉-碘化钾试纸、③淀粉、④白酒、⑤食醋,选取上述物质进行实验,下列组合合适的是______(填字母)。
,可选用的物质有:①水、②淀粉-碘化钾试纸、③淀粉、④白酒、⑤食醋,选取上述物质进行实验,下列组合合适的是______(填字母)。| A.③⑤ | B.②④ | C.②⑤ | D.①②③⑤ |
 ,直接排放会造成污染,使用
,直接排放会造成污染,使用 处理,能使
处理,能使 转化为不引起二次污染的
转化为不引起二次污染的 ,反应的化学方程式为
,反应的化学方程式为(5)以过氧化氢作还原剂,在硫酸介质中还原NaClO3制备ClO2,并将制得的ClO2处理含CN-废水。ClO2处理含CN-废水的离子方程式为
您最近一年使用:0次



