常温下,在溶液中可以发生以下反应
① ;
;
② ;
;
③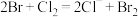 ,
,
由此判断下列说法错误的是
①
 ;
;②
 ;
;③
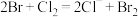 ,
,由此判断下列说法错误的是
A.氧化性强弱顺序为: |
B.若反应①中转移1mol电子,则产生的 在标准状况下的体积约为11.2L 在标准状况下的体积约为11.2L |
| C.溴元素在反应②中被还原,在③中被氧化 |
| D.反应①中作还原剂与表现酸性的HCl的分子数之比为3:5 |
更新时间:2023-02-20 21:57:05
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】CuSO4溶液中加入过量KI溶液,产生白色CuI沉淀,溶液变成棕色(产生I2)。向反应后的溶液中通入过量SO2,溶液变成无色(生成SO )。下列说法正确的是
)。下列说法正确的是
 )。下列说法正确的是
)。下列说法正确的是| A.滴加KI溶液时,CuSO4被氧化,I2是还原反应的产物 |
| B.通入SO2后,溶液变成无色,SO2体现氧化性 |
| C.整个过程发生了复分解反应和氧化还原反应 |
| D.上述实验条件下,物质的氧化性:Cu2+>I2>SO2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】向铜屑、稀盐酸和铁盐的混合溶液中持续通入空气可制备氯化铜,其反应过程如图所示。下列说法不正确 的是
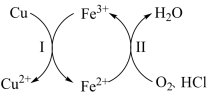

A.制备 的总反应为 的总反应为 |
B.反应Ⅰ中 作氧化剂 作氧化剂 |
C.反应Ⅱ中 作还原剂 作还原剂 |
D.还原性: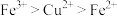 |
您最近一年使用:0次
【推荐3】2021年10月16日,神舟十三号载人飞船在酒泉卫星发射中心由长征二号F遥十三运载火箭送入太空,并和中国太空站组合体成功对接,这是中国建设航天强国最新里程碑。以下说法错误的是
| A.长征二号F遥十三运载火箭使用“偏二甲肼和二氧化氮”作推进剂,二氧化氮起氧化剂作用 |
| B.太空站组合体的“太阳翼”及光伏发电系统能将太阳能变为化学能 |
| C.太空站组合体、神舟返回舱和长征二号火箭均使用了高强度碳纤维,碳纤维属于新型无机高分子材料 |
| D.太空站组合体中最常见的保温隔热材料采用镀铝聚亚酰胺(PI)薄膜,聚亚酰胺是有机高分子材料 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】已知BrF3在常温常压下为无色或淡黄色液体,可通过下列反应制备:①2K+[BrF4]-+[BrF2] [SnF6]2-=K2SnF6+4BrF3②Br2+2ClF3=2BrF3+Cl2。下列说法错误的是
[SnF6]2-=K2SnF6+4BrF3②Br2+2ClF3=2BrF3+Cl2。下列说法错误的是
 [SnF6]2-=K2SnF6+4BrF3②Br2+2ClF3=2BrF3+Cl2。下列说法错误的是
[SnF6]2-=K2SnF6+4BrF3②Br2+2ClF3=2BrF3+Cl2。下列说法错误的是| A.反应①无电子转移 |
| B.由反应②可推知,氧化性:ClF3>BrF3 |
C.20℃时BrF3具有很强的导电性,可能原因是液体中存在2BrF3 BrF BrF +BrF +BrF |
D.反应3BrF3+5H2O=HBrO3+Br2+9HF+O2↑中,每生成1molO2有 molBrF3被还原 molBrF3被还原 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】根据下列实验操作和现象所得到的结论正确的是
| 选项 | 实验操作和现象 | 实验结论 |
| A | 向包有足量Na2O2粉末的脱脂棉上滴加几滴水,脱脂棉燃烧 | Na2O2与水反应放热 |
| B | 将Fe片分别插入盛有CuSO4溶液和AgNO3溶液的试管中,Fe片表面均有固体析出 | 金属性:Fe>Cu>Ag |
| C | 向某溶液中先滴加稀盐酸,无现象后滴加AgNO3溶液,有白色沉淀生成 | 原溶液中一定含有C1- |
| D | 将有色鲜花放入盛有干燥氯气的集气瓶中,盖上玻璃片,鲜花褪色 | Cl2具有漂白性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】已知反应H2SO3+Br2+H2O=H2SO4+2HBr。将0.1mol Cl2通入100mL含等物质的量的HBr和H2SO3的混合液中,有一半的HBr被氧化。则下列说法正确的是
| A.物质的还原性强弱:HBr>H2SO3>HCl |
| B.HBr和H2SO3的物质的量浓度为0.8mol·L-1 |
| C.通入0.1molCl2发生的离子反应:4H2SO3+5Cl2+2Br-=Br2+10Cl-+4H2SO4 |
| D.若再通入0.05molCl2恰好能将HBr和H2SO3完全氧化 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】化学需氧量(Chemial Oxygen Demand)是在一定条件下,用强氧化剂氧化一定体积水中的还原性物质时所消耗氧化剂的量,折算成氧气的量(单位为mg/L)来表示。我国地表水可采用标准 法测定水中化学需氧量(COD),即水体中还原性物质每消耗
法测定水中化学需氧量(COD),即水体中还原性物质每消耗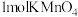 折算为
折算为 的消耗量。其操作步骤如下:
的消耗量。其操作步骤如下:
①取水样 ,先加入足量稀硫酸酸化,再加入
,先加入足量稀硫酸酸化,再加入 的
的 标准液,煮沸30min(充分氧化水中的还原性物质),溶液呈稳定的红色,冷却至室温。
标准液,煮沸30min(充分氧化水中的还原性物质),溶液呈稳定的红色,冷却至室温。
②向①中溶液中加入 的
的 标准液(过量)。
标准液(过量)。
③用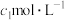 的
的 标准液滴定②中溶液至滴定终点,消耗
标准液滴定②中溶液至滴定终点,消耗 标准液
标准液 。
。
计算水样中COD含量(mg/L)表达式正确的是
 法测定水中化学需氧量(COD),即水体中还原性物质每消耗
法测定水中化学需氧量(COD),即水体中还原性物质每消耗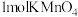 折算为
折算为 的消耗量。其操作步骤如下:
的消耗量。其操作步骤如下:①取水样
 ,先加入足量稀硫酸酸化,再加入
,先加入足量稀硫酸酸化,再加入 的
的 标准液,煮沸30min(充分氧化水中的还原性物质),溶液呈稳定的红色,冷却至室温。
标准液,煮沸30min(充分氧化水中的还原性物质),溶液呈稳定的红色,冷却至室温。②向①中溶液中加入
 的
的 标准液(过量)。
标准液(过量)。③用
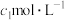 的
的 标准液滴定②中溶液至滴定终点,消耗
标准液滴定②中溶液至滴定终点,消耗 标准液
标准液 。
。计算水样中COD含量(mg/L)表达式正确的是
A. | B.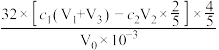 |
C.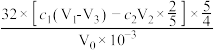 | D.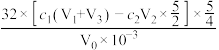 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】将50mL 18mol/L的浓硫酸与铜共热一段时间后,待反应混合物冷却后,滤去多余的铜,将滤液加水稀释至200mL,滤液中 的浓度为3mol/L,则下列说法正确的是
的浓度为3mol/L,则下列说法正确的是
 的浓度为3mol/L,则下列说法正确的是
的浓度为3mol/L,则下列说法正确的是A.稀释后的溶液中 的物质的量浓度为3mol/L 的物质的量浓度为3mol/L |
B.生成的 在标况下的体积为6.72L 在标况下的体积为6.72L |
| C.溶解的铜的质量为38.4g |
| D.反应中消耗的硫酸为0.3mol |
您最近一年使用:0次



