下列关于化学反应的方向叙述中不正确的是
A.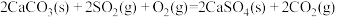 该反应 该反应 |
B.反应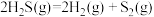 其化学平衡常数表达式为 其化学平衡常数表达式为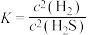 |
C.若 , , ,化学反应在任何温度下都能自发进行 ,化学反应在任何温度下都能自发进行 |
D.合成甲醇的反应: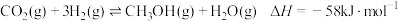 ,加入催化剂对化学平衡常数无影响 ,加入催化剂对化学平衡常数无影响 |
更新时间:2023-03-02 23:04:10
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】某温度下,某反应达平衡时平衡常数K=c(C)·c(D)/c(A)·c(B)。恒容时,温度升高,C的物质的量浓度减小。下列说法正确的是( )
| A.该反应的焓变ΔH>0 |
| B.恒温恒容时,增大体系压强,c(D)一定增大 |
| C.升高温度,逆反应速率减小 |
D.该反应的化学方程式可能为A(g)+B(g) C(g)+D(g) C(g)+D(g) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法正确的是
| A.常温下,某AgCl溶液有未溶AgCl固体剩余,向其上层清液中通入少量HCl,无沉淀生成 |
B.常温下,10 mL  的NH4Cl溶液中由水电离出的 的NH4Cl溶液中由水电离出的 物质的量浓度为 物质的量浓度为 mol·L mol·L |
C.某温度下,反应 达平衡,压缩体积后达新平衡时容器中的 达平衡,压缩体积后达新平衡时容器中的 浓度比原平衡大 浓度比原平衡大 |
D.将 的强酸溶液稀释100倍,则 的强酸溶液稀释100倍,则 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表,说法错误的是
| 物质 | X | Y | Z |
| 初始浓度/mol·L-1 | 0.1 | 0.2 | 0 |
| 平衡浓度/mol·L-1 | 0.05 | 0.05 | 0.1 |
| A.反应达到平衡时,X的转化率为50% |
| B.方程式为X+3Y⇌2Z,平衡常数为1600 |
| C.增大压强使平衡正向方向移动,平衡常数增大 |
| D.改变温度可以改变此反应的平衡常数 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】在密闭容器中,一定量的N2和H2发生反应: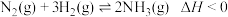 ,某实验小组测得N2的转化率(
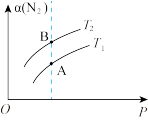
,某实验小组测得N2的转化率( )在不同温度(T)与压强(p)下的实验数据,三者之间的关系如图所示。下列有关说法正确的是
)在不同温度(T)与压强(p)下的实验数据,三者之间的关系如图所示。下列有关说法正确的是
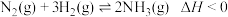 ,某实验小组测得N2的转化率(
,某实验小组测得N2的转化率( )在不同温度(T)与压强(p)下的实验数据,三者之间的关系如图所示。下列有关说法正确的是
)在不同温度(T)与压强(p)下的实验数据,三者之间的关系如图所示。下列有关说法正确的是
| A.升高温度,平衡向正反应方向移动 |
| B.达到平衡后,缩小容器体积,H2的转化率提高 |
| C.图中A、B两点对应的平衡常数相等 |
D.温度: 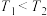 |
您最近一年使用:0次
【推荐1】反应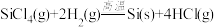 可用于纯硅的制备。下列有关该反应的说法正确的是
可用于纯硅的制备。下列有关该反应的说法正确的是
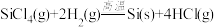 可用于纯硅的制备。下列有关该反应的说法正确的是
可用于纯硅的制备。下列有关该反应的说法正确的是A.该反应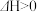 、 、 |
B.该反应的平衡常数 |
C.高温下反应每生成1 mol Si需消耗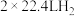 |
D.用E表示键能,该反应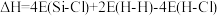 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法中正确的是
A.若  ,该化学反应在任何温度下都不能自发进行 ,该化学反应在任何温度下都不能自发进行 |
| B.知道了某过程有自发性之后,就能确定该过程是否一定会发生 |
C.一定温度下,反应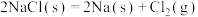 的 的  |
| D.某反应在低温条件下能自发进行,那么该反应在高温条件下也一定能自发进行 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】温度 时,向容积为2L的密闭容器中加入活性炭(足量)和A,发生反应
时,向容积为2L的密闭容器中加入活性炭(足量)和A,发生反应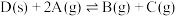 ,第15min时,温度调整到
,第15min时,温度调整到 ,测得下列各时刻A的物质的量如下表所示。反应中没有使用催化剂,下列说法不正确的是
,测得下列各时刻A的物质的量如下表所示。反应中没有使用催化剂,下列说法不正确的是
 时,向容积为2L的密闭容器中加入活性炭(足量)和A,发生反应
时,向容积为2L的密闭容器中加入活性炭(足量)和A,发生反应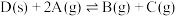 ,第15min时,温度调整到
,第15min时,温度调整到 ,测得下列各时刻A的物质的量如下表所示。反应中没有使用催化剂,下列说法不正确的是
,测得下列各时刻A的物质的量如下表所示。反应中没有使用催化剂,下列说法不正确的是 /℃ /℃ |  /℃ /℃ | ||||||
 | 0 | 5min | 10min | 15min | 20min | 25min | 30min |
 | 2.00 | 1.50 | 1.20 | 1.20 | 0.60 | 0.40 | 0.40 |
A.0~5min,生成B的平均速率为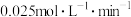 |
B.由表中数据可知 ,且该反应的 ,且该反应的 |
C.其他条件不变,30min时加入B、C各 ,达到新平衡后,A的体积分数不变 ,达到新平衡后,A的体积分数不变 |
D. 、 、 温度下,该反应对应的平衡常数为 温度下,该反应对应的平衡常数为 、 、 ,其大小顺序为 ,其大小顺序为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】橡皮筋在拉伸和收缩状态时结构如图:在其拉伸过程中有放热现象,反之吸热。25℃、101kPa时,下列化学反应的焓变、熵变和自发性与橡皮筋从拉伸状态到收缩状态一致的是


| A.2Na+2H2O=2NaOH+H2↑ |
| B.Ba(OH)2·8H2O+2NH4Cl=BaCl2+2NH3↑+10H2O |
| C.2H2+O2=2H2O |
| D.CaCO3=CaO+CO2↑ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】化学反应速率、化学平衡是化学反应的重要原理,下列说法正确的是
A.在恒容恒温条件下,当 达到平衡后,再充入一定量的Ar后,活化分子百分数减少,反应速率减慢 达到平衡后,再充入一定量的Ar后,活化分子百分数减少,反应速率减慢 |
B.25℃时将 的HA溶液加水稀释至 的HA溶液加水稀释至 ,稀释后溶液的体积大于等于原溶液体积的1000倍 ,稀释后溶液的体积大于等于原溶液体积的1000倍 |
C.反应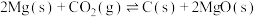  ,则该反应能在高温自发进行 ,则该反应能在高温自发进行 |
D.保持温度不变,向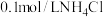 溶液中加入 溶液中加入 固体,容液中 固体,容液中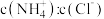 的比值变小 的比值变小 |
您最近一年使用:0次

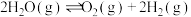
 ;(2)
;(2)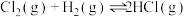
 ;(3)
;(3)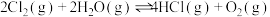
 ,则
,则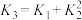
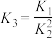
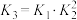
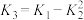
 和
和 重整技术可获得合成气(主要成分为CO、
重整技术可获得合成气(主要成分为CO、 ),重整过程中部分反应的热化学方程式:
),重整过程中部分反应的热化学方程式: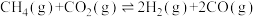
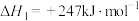


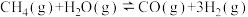

 配比随温度变化对出口合成气中
配比随温度变化对出口合成气中 的影响如图所示。
的影响如图所示。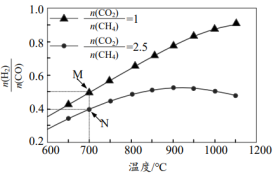
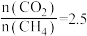 时,温度高于900℃后
时,温度高于900℃后 的说法正确的是
的说法正确的是

