设NA为阿伏加德罗常数的值。下列说法不正确的是
| A.标准状况下,22.4 L CCl4中,原子数大于5NA |
| B.71g Cl2与足量烧碱溶液反应制备漂白液,转移的电子数为NA |
| C.1 L 0.1 mol/L Na[Ag(CN)2]溶液中CN-的数目为0.2 NA |
| D.1 mol C2H6O中含碳氢单键数可能为5NA |
更新时间:2023-03-07 19:56:02
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】设 为阿伏加德罗常数的值,下列说法中正确的是
为阿伏加德罗常数的值,下列说法中正确的是
 为阿伏加德罗常数的值,下列说法中正确的是
为阿伏加德罗常数的值,下列说法中正确的是A. 的摩尔质量是 的摩尔质量是 |
B.标准状况下,过氧化氢分解制得1.12L ,转移电子数为0.2 ,转移电子数为0.2 |
C.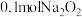 中阴离子数为 中阴离子数为 |
D.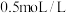 的 的 溶液中含有氯离子数为 溶液中含有氯离子数为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】用NA表示阿伏加德罗常数的值,下列说法正确的是
| A.1mol·L-1的AlCl3溶液中,Cl-离子的数目为3NA |
| B.常温常压下,1.06gNa2CO3,含有的Na+离子数为0.02NA |
| C.标准状况下,11.2LH2O含有的分子数为0.5NA |
| D.5.6g铁分别与足量的盐酸或氯气反应,电子转移总数均为0.3NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】设NA为阿伏加 德罗常数,下列说法中正确的是( )
| A.含有1mol Na2SO4的溶液中,含有的Na+个数为NA |
| B.18g水中含有电子数为8NA |
| C.标准状况下,22.4LH2含有氢原子个数为2NA |
| D.1.2L H2一定含有NA个氢原子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】设 为阿伏加 德罗常数的值,下列叙述正确的是
为阿伏加 德罗常数的值,下列叙述正确的是
 为阿伏加 德罗常数的值,下列叙述正确的是
为阿伏加 德罗常数的值,下列叙述正确的是A.标准状况下, 一氧化氮和 一氧化氮和 氧气混合后的分子总数小于 氧气混合后的分子总数小于 |
B.常温下,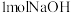 固体含有的分子总数为 固体含有的分子总数为 |
C. 时, 时, 的 的 ,则饱和 ,则饱和 溶液中 溶液中 的数目为 的数目为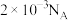 |
D. 时, 时,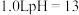 的 的 溶液中含有的 溶液中含有的 数目为 数目为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】设 NA 为阿伏加德罗常数的值,下列说法正确的是
| A.1 mol O2 和 N2 的混合气体中的含有的原子数为 2NA |
| B.含有 1 mol 硅原子的晶体硅和二氧化硅中,共价键的数目均为 2 NA |
| C.常温下,pH=2的硫酸溶液中,氢离子的数目为 0.01 NA |
| D.7.8 g Na2O2 与足量水反应,转移的电子数为 0.2 NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】设NA为阿伏加 德罗常数的值。下列说法正确的是( )
| A.在标准状况下,2.24 LSO3中含氧原子数为0.3NA |
| B.0.1 mol O2完全反应时,转移的电子数一定为0.4NA |
| C.含0.1 mol FeCl3的饱和溶液最多可形成的胶体粒子数为0.1NA |
| D.常温常压下,1.8 g甲基(-CD3)中含有的中子数为0.9NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】NA表示阿伏加德罗常数,下列判断正确的是
| A.1.00 mol NaCl中含有6.02×1023个NaCl分子 |
| B.标准状况下,22.4L HF含有NA个HF分子 |
| C.在密闭容器中加入H2和N2,充分反应后得到1mol NH3时转移的电子数为3NA |
| D.常温常压下,46g的NO2和N2O4混合气体含有的原子数为6NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】用NA表示阿伏加德罗常数的值,下列说法中正确的是
| A.1mol N2所含有的原子数为NA |
| B.标准状况下,1.7g NH3所含有的电子数为NA |
| C.标准状况下,22.4L氢气所含的原子数为NA |
| D.1.0mol/L碳酸钠溶液中所含有的钠离子数为2NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】用 NA表示阿伏加德罗常数的值,下列叙述正确的是
| A.13.2gCO2和N2O形成的混合物含有的原子数目为0.9NA |
| B.0.5mol/LBa(OH)2溶液中含有 OH-的数目为NA |
| C.标准状况下,5.6LH2O 有的原子数目为 0.75NA |
| D.100g质量分数为46%的乙醇(C2H5OH)溶液中,含有的氢原子数为 6NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】中国“天宫”号空间站的成功建设显示了我国科技发展的巨大成就,其使用的“柔性砷化镓太阳能电池”能量转化效率超30%,电池性能远超其他空间站。下列相关叙述不正确的是
| A.基态砷原子有3个单电子 |
B.三氯化砷( )分子中 )分子中 的杂化方式是 的杂化方式是 |
| C.砷化镓熔点很高,但低于硅晶体 |
D.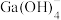 中含有配位键 中含有配位键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】铁与镁组成的储氢合金的立方晶胞结构如图所示。铁原子位于顶角和面心的位置,镁原子位于将晶胞平分为8个立方单位的体心位置。下列说法正确的是
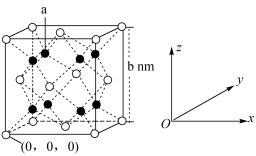

| A.a位置原子的分数坐标为(0.25,0.75,0.75) |
| B.Fe原子的配位数为4 |
C.Fe原子与Mg原子间最短距离为 |
| D.[Fe(CN)5(NO)]2-的中心离子为Fe2+,配位数为6,配位原子有C和O |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】已知[Co(H2O)6]2+呈粉红色,[CoCl4]2-呈蓝色,[ZnCl4]2-为无色。现将CoCl2溶于水,加入浓盐酸后,溶液由粉红色变为蓝色,存在以下平衡:[Co(H2O)6]2++4Cl- [CoCl4]2-+6H2O ΔH,用该溶液做实验,溶液的颜色变化如图:
[CoCl4]2-+6H2O ΔH,用该溶液做实验,溶液的颜色变化如图:
 [CoCl4]2-+6H2O ΔH,用该溶液做实验,溶液的颜色变化如图:
[CoCl4]2-+6H2O ΔH,用该溶液做实验,溶液的颜色变化如图: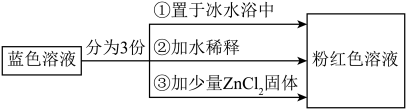
| A.由实验①可推知ΔH>0 |
| B.等物质的量的[Co(H2O)6]2+和[CoCl4]2-中,所含配位键数目不同 |
| C.实验②是由于加水稀释,使得Q<K,导致平衡逆向移动 |
| D.由实验③可知该实验条件下配离子的稳定性:[ZnCl4]2->[CoCl4]2- |
您最近一年使用:0次



