298K时,BaSO4与BaCO3在水中的沉淀溶解平衡曲线如图所示,下列说法错误的是

已知101.4=25

已知101.4=25
| A.298K时,BaSO4的溶解度小于BaCO3的溶解度 |
| B.U点坐标为(4,4.8) |
| C.作为分散质BaSO4,W点v(沉淀)<v(溶解) |
D.对于沉淀溶解平衡BaSO4(s)+CO (aq) (aq) BaCO3(s)+SO BaCO3(s)+SO (aq),其平衡常数K=0.04 (aq),其平衡常数K=0.04 |
更新时间:2023-03-15 09:52:15
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】一定温度下,在2L恒容密闭容器中加入1molN2和3molH2发生反应:N2(g)+3H2(g)⇌2NH3(g) ∆H<0,NH3的物质的量与时间的关系如表所示:
下列说法正确的是
| 时间/min | 0 | 2 | 4 | 6 |
| n(NH3)/mol | 0 | 0.2 | 0.3 | 0.3 |
| A.该反应可以在高温下自发进行 |
| B.在6min末再加入1mol N2和3mol H2,反应达新平衡时,N2的转化率大于15% |
| C.正反应合成氨的活化能大于逆反应氨分解的活化能 |
| D.升高温度,可使正反应速率减小,逆反应速率增大,故平衡逆向移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】常温下将盐酸溶液滴加到联氨 的水溶液中,混合溶液中的微粒的物质的量分数
的水溶液中,混合溶液中的微粒的物质的量分数 随
随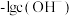 变化的关系如图所示。下列叙述错误的是
变化的关系如图所示。下列叙述错误的是
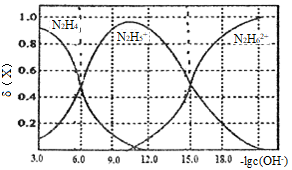
 的水溶液中,混合溶液中的微粒的物质的量分数
的水溶液中,混合溶液中的微粒的物质的量分数 随
随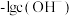 变化的关系如图所示。下列叙述错误的是
变化的关系如图所示。下列叙述错误的是
A.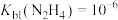 |
B.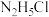 溶液中 溶液中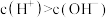 |
C.反应 的 的 |
D.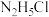 溶液中存在 溶液中存在 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列实验、现象与结论正确且相符的是
| 选项 | 实验 | 现象 | 结论 |
| A | 向盛有 溶液的试管中加入几滴酸化的硫酸亚铁溶液 溶液的试管中加入几滴酸化的硫酸亚铁溶液 | 溶液变成棕黄色,一段时间后,溶液中出现气泡,随后有红褐色沉淀生成 |  催化 催化 分解产生 分解产生 ; ; 分解反应放热,促进 分解反应放热,促进 的水解平衡正向移动 的水解平衡正向移动 |
| B | 将充满 的密闭玻璃球浸泡在热水中 的密闭玻璃球浸泡在热水中 | 红棕色变深 | 反应:  |
| C | 白铁皮(镀锌铁)出现刮痕后浸泡在饱和食盐水中,一段时间后滴入几滴 溶液 溶液 | 无明显现象 | 该过程未发生氧化还原反应 |
| D | 向2支盛有 相同浓度硝酸银溶液的试管中,分别加入2滴相同浓度的 相同浓度硝酸银溶液的试管中,分别加入2滴相同浓度的 和 和 溶液 溶液 | 一支无明显现象,另一支产生黄色沉淀 | 相同条件下, 比 比 的溶解度大 的溶解度大 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列选项正确的是( )
| A.25℃时,AgBr在0.0lmol/L的MgBr2溶液和NaBr溶液中的溶解度相同 |
B.53℃时,将0.01mol/L的醋酸溶液加水不断稀释, 减小 减小 |
| C.Na2CO3、NaHCO3溶液等浓度等体积混合后:3c(Na+)=2[c(CO32-)+c(HCO3-)+c(H2CO3)] |
| D.NaCN溶液和盐酸混合呈中性的溶液中:c(Na+)>c(Cl-)=c(HCN) |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列实验方案中,不能达到相应实验目的的是
| 选项 | A | B | C | D |
| 实验方案 |  |  |  | 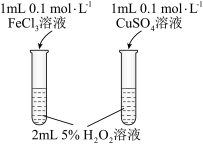 |
| 目的 | 研究温度对化学平衡的影响 | 验证锌与硫酸铜反应过程中有电子转移 | 证明溶解度:AgCl>Ag2S | 比较不同催化剂对化学反应速率的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法正确的是( )
A.用坩埚灼烧MgCl2·6H2O的化学方程式为:MgCl2·6H2O MgCl2+6H2O MgCl2+6H2O | |||||||
B.根据表中提供的数据,等物质的量浓度的NaClO、NaHCO3混合溶液中,有c(HCO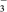 )>c(ClO-)>c(OH-) )>c(ClO-)>c(OH-)
| |||||||
| C.常温下,将pH=2的稀硫酸稀释10倍,其中各离子的物质的量浓度都变为原来的十分之一 | |||||||
D.某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示,溶度积常数Ksp=c(Ba2+)·c(SO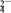 ),则加入Na2SO4可使溶液由a点变到b点;通过蒸发可以使溶液由d点变到c点 ),则加入Na2SO4可使溶液由a点变到b点;通过蒸发可以使溶液由d点变到c点 . . |
您最近一年使用:0次

 3Z(g),平衡时X、Y、Z的体积分数分别为30%、60%、10%。向平衡体系中再加入1molZ,重新建立平衡时X、Y、Z的体积分数不变。下列叙述不正确的是
3Z(g),平衡时X、Y、Z的体积分数分别为30%、60%、10%。向平衡体系中再加入1molZ,重新建立平衡时X、Y、Z的体积分数不变。下列叙述不正确的是 的溶解平衡曲线如图,下列说法错误的是
的溶解平衡曲线如图,下列说法错误的是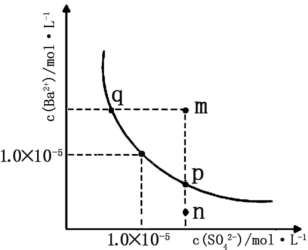
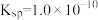
 固体可使n点移动到p点
固体可使n点移动到p点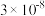
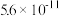

 溶液除去锅炉水垢中的
溶液除去锅炉水垢中的 :
: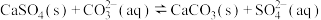
 作抗胃酸药:
作抗胃酸药:


