在硫酸铜溶液中加入过量浓氨水,可形成[Cu(NH3)4 (H2O)2]2+。下列有关说法错误的是
| A.配离子中两种配体的中心原子杂化方式和VSEPR模型均相同 |
| B.基态原子第一电离能:N>O>S |
| C.键角:BF3>H2O>NH3 |
| D.配离子[Cu(NH3)4 (H2O)2]2+的空间结构是八面体形 |
更新时间:2023-03-18 20:33:26
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】四氯化锗(GeCl4)是光导纤维的常用掺杂剂,锗与硅同族。下列说法正确的是
| A.基态Ge原子价层电子轨道表达式为4s24p2 | B.GeCl4的熔点比SiCl4低 |
| C.GeCl4的空间构型为正四面体 | D.第一电离能大小:Cl>Ge>Si |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列分子或离子的VSEPR模型与空间结构一致的是
A. | B. | C. | D. |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】叠氮酸钠(NaN3)是重要的化工原料。以甲醇、亚硝酸钠等为原料制备NaN3流程如图。已知水合肼(N2H4·H2O)不稳定,具有强还原性。下列描述正确的是
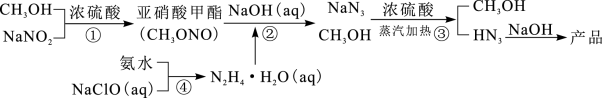

| A.反应①和反应③中浓硫酸作用不同 |
| B.反应④应将氨水逐滴滴入NaClO溶液中制备水合肼 |
| C.反应②中,消耗3molN2H4·H2O时,反应中转移5mol电子 |
D.N 的空间构型为V形 的空间构型为V形 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】以下关于PH3的叙述正确 的是
| A.PH3分子中无未成键的孤电子对 | B.PH3是非极性分子 |
| C.它的分子空间结构是三角锥形 | D.磷原子采用sp2杂化 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】短周期主族元素X、Y、Z、W的原子序数依次增大,基态X原子核外未成对电子数为3,基态Y原子核外s轨道的电子数与p轨道的电子数相同,Z元素在短周期中金属性最强,基态W原子核外最高能级含有5个电子。下列说法正确的是
A.原子半径: |
| B.化合物ZW中阴阳离子最外层均满足8电子稳定结构 |
C.基态原子的第一电离能: |
D. 与 与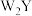 分子的空间结构相同 分子的空间结构相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】某教授团队研究发现,稀土铈基低温耐硫脱硝催化剂的反应历程如图所示(“□”代表空位)。下列叙述正确的是
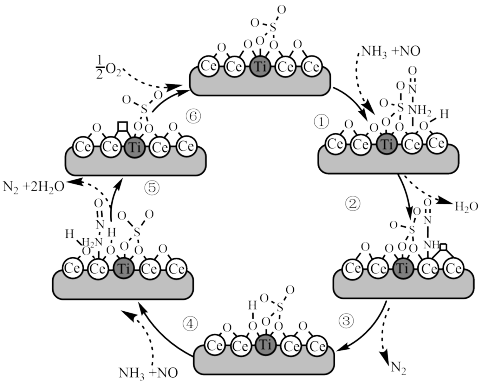

A.上述循环中S都采用 杂化 杂化 |
| B.上述循环中Ce、Ti形成的共价键数目都发生了变化 |
| C.该历程的总反应中氧化产物与还原产物的物质的量之比为1:2 |
| D.每形成1mol氢氧键,形成1mol“空位” |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】证实证伪是化学学科需要的重要证据推理意识。已知:正高碘酸(结构如图所示)是一种五元弱酸,具有强氧化性,脱水可得偏高碘酸(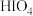 ),下列说法一定正确的是
),下列说法一定正确的是
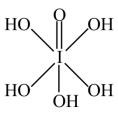
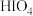 ),下列说法一定正确的是
),下列说法一定正确的是
A. 溶液一定显碱性 溶液一定显碱性 |
| B.正高碘酸中心原子的杂化方式为sp3杂化 |
C.正高碘酸与 反应后溶液呈紫红色,反应如下: 反应后溶液呈紫红色,反应如下: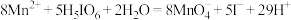 |
D.正高碘酸隔绝空气加热分解仅生成 、 、 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】氟利昂 破坏臭氧层的反应过程如图所示。设
破坏臭氧层的反应过程如图所示。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 破坏臭氧层的反应过程如图所示。设
破坏臭氧层的反应过程如图所示。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
A.0.5mol由 、 、 组成的混合物中共价键的数目为 组成的混合物中共价键的数目为 |
B.1.6g由 和 和 组成的混合气体中含有的原子总数为 组成的混合气体中含有的原子总数为 |
C.标准状况下,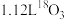 中含有的中子总数为 中含有的中子总数为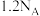 |
D.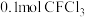 的中心原子的孤电子对数为 的中心原子的孤电子对数为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】关于配合物[TiCl(H2O)5]Cl2·H2O的下列说法错误的是
| A.配位体是Cl-和H2O,Cl-和H2O提供孤对电子 |
| B.Ti元素位于元素周期表的d区 |
| C.配离子是[TiCl(H2O)5]2+,配位数是6 |
| D.含0.1mol该配合物的溶液与足量AgNO3溶液反应,生成0.3molAgCl沉淀 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】设NA为阿伏加 德罗常数的值,下列说法中正确的是
| A.标准状况下,1mol金刚石中含有的C–C键数目为4NA |
| B.1mol SiO2晶体中含有的Si–O键数目为2NA |
| C.63g HNO3,中心原子N的价层电子对中,孤电子对数为NA |
| D.常温常压下,1mol配合物[Cu(NH3)4]SO4中,含有的σ键数目为20NA |
您最近一年使用:0次




