下列三个化学反应焓变、平衡常数与温度的关系分别如下表所示。下列说法正确的是
| 化学反应 | 平衡常数 | 温度 | |
| 973K | 1173K | ||
①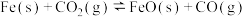  |  | 1.47 | 2.15 |
②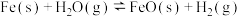  |  | 2.38 | 1.67 |
③  |  | a | b |
A.1173K时,反应①起始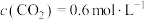 ,平衡时 ,平衡时 约为0.4 约为0.4 |
B.反应②是吸热反应, |
| C.反应③达平衡后,升高温度或缩小反应容器的容积平衡逆向移动 |
D.相同温度下, ; ;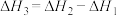 |
2023·北京丰台·一模 查看更多[7]
北京市顺义区第二中学2023-2024学年高三下学期3月月考化学试题(已下线)题型13 化学平衡常数的计算及应用-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)北京市第一六一中学2023-2024学年高三上学期12月月考化学试题湖北省黄冈市重点校2022-2023学年高一下学期期末综合选拔性联考化学试题海南省海南中学2023届高三下学期第三次模拟考试化学试题(已下线)专题15 化学反应速率和化学平衡北京市丰台区2022-2023学年高三下学期第一次模拟练习化学试题
更新时间:2023-03-24 13:16:38
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】用CaSO4代替O2与燃料CO反应是一种高效、清洁的新型燃烧技术,发生如下反应:
① CaSO4(s)+CO(g) ⇌
CaSO4(s)+CO(g) ⇌  CaS(s)+CO2(g) ΔH1=-47.3 kJ·mol-1
CaS(s)+CO2(g) ΔH1=-47.3 kJ·mol-1
②CaSO4(s)+CO(g) ⇌ CaO(s)+CO2(g)+SO2(g) ΔH2=+210.5 kJ·mol-1
③CO(g) ⇌ C(s)+
C(s)+ CO2(g) ΔH3=-86.2 kJ·mol-1
CO2(g) ΔH3=-86.2 kJ·mol-1
下列说法错误 的是 ( )
①
 CaSO4(s)+CO(g) ⇌
CaSO4(s)+CO(g) ⇌  CaS(s)+CO2(g) ΔH1=-47.3 kJ·mol-1
CaS(s)+CO2(g) ΔH1=-47.3 kJ·mol-1②CaSO4(s)+CO(g) ⇌ CaO(s)+CO2(g)+SO2(g) ΔH2=+210.5 kJ·mol-1
③CO(g) ⇌
 C(s)+
C(s)+ CO2(g) ΔH3=-86.2 kJ·mol-1
CO2(g) ΔH3=-86.2 kJ·mol-1下列说法
| A.反应①达到平衡时,增大压强平衡不移动 |
B.反应②的平衡常数表达式为K= |
| C.反应①和②是主反应,反应③是副反应 |
D.2CaSO4(s)+7CO(g)  CaS(s)+CaO(s)+6CO2(g)+C(s)+SO2(g)是放热反应 CaS(s)+CaO(s)+6CO2(g)+C(s)+SO2(g)是放热反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】已知:①lmolH 分子中化学键断裂时需要吸收436 kJ的能量②1 mol C1
分子中化学键断裂时需要吸收436 kJ的能量②1 mol C1 分子中化学键断裂时需要吸收243 kJ的能量③由H原子和C1原子形成l mol HCl分子时释放431 kJ的能量下列叙述中正确的是
分子中化学键断裂时需要吸收243 kJ的能量③由H原子和C1原子形成l mol HCl分子时释放431 kJ的能量下列叙述中正确的是
 分子中化学键断裂时需要吸收436 kJ的能量②1 mol C1
分子中化学键断裂时需要吸收436 kJ的能量②1 mol C1 分子中化学键断裂时需要吸收243 kJ的能量③由H原子和C1原子形成l mol HCl分子时释放431 kJ的能量下列叙述中正确的是
分子中化学键断裂时需要吸收243 kJ的能量③由H原子和C1原子形成l mol HCl分子时释放431 kJ的能量下列叙述中正确的是 A.氢气和氯气反应生成氯化氢气体的热化学方程式是: H2( g)+Cl2(g)="2HCl(g)" 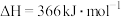 |
B.氢气和氯气反应生成2 mol氯化氢气体,反应的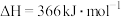 |
C.氢气和氯气反应生成2mol氯化氢气体,反应的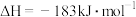 |
D.氢气和氯气反应生成1 mol氯化氢气气体,反应的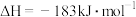 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】现代火法炼锌过程中发生了以下三个主要反应。下列说法正确的是
① 2ZnS(s) + 3O2(g)=2ZnO(s)+2SO2(g) △H1=a kJ·mol-1
② 2C(s) +O2(g)=2CO(g) △H2=b kJ·mol-1
③ ZnO(s) +CO(g)=Zn(g) +CO2(g) △H3=c kJ·mol-1
① 2ZnS(s) + 3O2(g)=2ZnO(s)+2SO2(g) △H1=a kJ·mol-1
② 2C(s) +O2(g)=2CO(g) △H2=b kJ·mol-1
③ ZnO(s) +CO(g)=Zn(g) +CO2(g) △H3=c kJ·mol-1
| A.以上三个反应中,只有①是放热反应 |
| B.反应②的作用是仅为反应③提供还原剂 |
C.反应 ZnS(s)+C(s)+2O2(g)=Zn(g)+SO2(g)+CO2(g)的△H= (a+b+2c) kJ·mol-1 (a+b+2c) kJ·mol-1 |
D.碳的燃烧热为 b kJ·mol-1 b kJ·mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】将一定量纯净的氨基甲酸铵固体置于恒容的密闭真空容器中,在恒定温度下使其达到分解平衡:NH2COONH4(s)  2NH3(g)+CO2(g),实验测得不同温度下的平衡数据列于下表:
2NH3(g)+CO2(g),实验测得不同温度下的平衡数据列于下表:
下列说法正确的是
 2NH3(g)+CO2(g),实验测得不同温度下的平衡数据列于下表:
2NH3(g)+CO2(g),实验测得不同温度下的平衡数据列于下表:| 温度/℃ | 15 | 20 | 25 | 30 | 35 |
| 平衡总压强/kPa | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
| 平衡气体总浓度/ 10-3mol·L-1 | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
| A.该反应在低温下可以自发进行 |
| B.当体系中气体的平均相对分子质量不变时,说明该反应达到了平衡状态 |
| C.恒温条件下,向容器中再充入2mol NH3和1molCO2,平衡向左移动,平衡后,NH3的浓度减小 |
| D.15℃时,该反应的平衡常数约为2.05×10-9 |
您最近一年使用:0次
【推荐2】已知C2H4(g)+H2(g) C2H6(g) △H<0,在3个体积相等的恒容容器发生反应,结果如下表。下列说法正确的是
C2H6(g) △H<0,在3个体积相等的恒容容器发生反应,结果如下表。下列说法正确的是
 C2H6(g) △H<0,在3个体积相等的恒容容器发生反应,结果如下表。下列说法正确的是
C2H6(g) △H<0,在3个体积相等的恒容容器发生反应,结果如下表。下列说法正确的是| 容器编号 | 温度/K | 起始物质的量/ mol | 平衡物质的量/ mol | ||
| H2(g) | C2H4(g) | C2H6(g) | C2H6(g) | ||
| Ⅰ | T1 | 0.10 | 0.10 | 0 | 0.05 |
| Ⅱ | T1 | 0.10 | 0.10 | 0.10 | |
| Ⅲ | T2 | 0 | 0 | 0.10 | 0.06 |
| A.T1<T2 |
| B.容器II达平衡时C2H4(g)物质的量约为0. 078 mol |
| C.T1时,容器I的平衡常数K=20 |
| D.容器II中起始反应速率:v(正)<v(逆) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】在2L密闭容器中充入气体A和B,发生A(g)+B(g)  C(g)+2D(g) ΔH,所得实验数据如下表。下列说法正确的是
C(g)+2D(g) ΔH,所得实验数据如下表。下列说法正确的是
 C(g)+2D(g) ΔH,所得实验数据如下表。下列说法正确的是
C(g)+2D(g) ΔH,所得实验数据如下表。下列说法正确的是| 实验编号 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | |
| n(A) | n(B) | n(C) | ||
| ① | 300 | 0.40 | 0.10 | 0.090 |
| ② | 500 | 0.40 | 0.10 | 0.080 |
| ③ | 500 | 0.20 | 0.05 | a |
| A.ΔH>0 |
| B.500℃该反应的平衡常数K=0.32 mol·L-1 |
| C.③中达到平衡时,a >0.040 |
| D.5min末测得①中n(C)=0.050 mol,则0到5min内v(D)=0.02 mol·L-1·min-1 |
您最近一年使用:0次



