实验小组设计实验除去粗盐溶液中的Ca2+、Mg2+、SO 并进行定性检验。
并进行定性检验。
已知:Ksp[Mg(OH)2]=5.6×10-12,Ksp(BaSO4)=1.1×10-10,Ksp(BaCO3)=2.6×10-9。不正确 的是
 并进行定性检验。
并进行定性检验。已知:Ksp[Mg(OH)2]=5.6×10-12,Ksp(BaSO4)=1.1×10-10,Ksp(BaCO3)=2.6×10-9。

| A.调节溶液的pH>12,可使滤液中c(Mg2+)<1×10-5mol/L |
B.加入Na2CO3溶液发生的反应是Ba2++CO =BaCO3↓、Ca2++CO =BaCO3↓、Ca2++CO =CaCO3↓ =CaCO3↓ |
C.加入盐酸发生的反应是2H++CO =CO2↑+H2O、H++OH-=H2O =CO2↑+H2O、H++OH-=H2O |
| D.若步骤①加入BaCl2溶液后进行过滤,可以避免白色沉淀M的生成 |
更新时间:2023-03-31 15:05:37
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】粉末X中可能含有Fe、FeO、CuO、 、NaCl和
、NaCl和 中的若干种。为确定该固体粉末的成分,某同学依次进行了以下实验:
中的若干种。为确定该固体粉末的成分,某同学依次进行了以下实验:
①将X加入足量水,得到不溶物Y和溶液Z
②取少量Y加入足量浓盐酸,加热,产生黄绿色气体,并有少量红色不溶物
③用玻璃棒蘸取溶液Z滴于广泛pH试纸上,试纸呈蓝色
④向Z溶液中滴加 溶液,生成白色沉淀
溶液,生成白色沉淀
分析以上实验现象,下列结论正确的是
 、NaCl和
、NaCl和 中的若干种。为确定该固体粉末的成分,某同学依次进行了以下实验:
中的若干种。为确定该固体粉末的成分,某同学依次进行了以下实验:①将X加入足量水,得到不溶物Y和溶液Z
②取少量Y加入足量浓盐酸,加热,产生黄绿色气体,并有少量红色不溶物
③用玻璃棒蘸取溶液Z滴于广泛pH试纸上,试纸呈蓝色
④向Z溶液中滴加
 溶液,生成白色沉淀
溶液,生成白色沉淀分析以上实验现象,下列结论正确的是
| A.X中一定不存在FeO |
B.不溶物Y中一定含有Fe、 和CuO 和CuO |
C.Z溶液中一定不含有 |
| D.向④中所生成的白色沉淀中滴加盐酸,若沉淀不完全溶解,则粉末X中含有NaCl |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】某溶液中只可能含有下列离子中的几种(不考虑溶液中含的较少的 和
和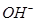 、
、 、
、 、
、 、
、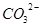 、
、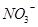 。取200mL该溶液,分为等体积的两份分别做下列实验。
。取200mL该溶液,分为等体积的两份分别做下列实验。
实验1:第一份加入足量的烧碱并加热,产生的气体在标准状况下为224mL
实验2:第二份先加入足量的盐酸,无现象,再加足量的 溶液,得固体2.33克。
溶液,得固体2.33克。
下列说法正确的是
 和
和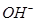 、
、 、
、 、
、 、
、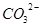 、
、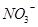 。取200mL该溶液,分为等体积的两份分别做下列实验。
。取200mL该溶液,分为等体积的两份分别做下列实验。实验1:第一份加入足量的烧碱并加热,产生的气体在标准状况下为224mL
实验2:第二份先加入足量的盐酸,无现象,再加足量的
 溶液,得固体2.33克。
溶液,得固体2.33克。下列说法正确的是
A.该溶液中可能含有 |
B.该溶液中肯定含有 、 、 、 、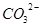 、 、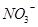 |
C.该溶液中一定不含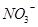 |
D.该溶液中一定含 ,且 ,且 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】水溶液中的离子平衡在生产生活中有广泛的应用,下列说法不正确的是
| A.蒸干硫酸镁溶液并灼烧得到干燥的硫酸镁固体,则蒸干氯化镁溶液并灼烧也可得到干燥的氯化镁固体 |
| B.用氯化铵溶液除去铁器表面的铁锈是利用了铵根离子水解生成的氢离子 |
| C.向2ml0.lmol/L的硝酸银(AgNO3)溶液中滴入2ml同浓度的氯化钾(KCl溶液,生成白色沉淀,再向该体系中滴入同浓度的硫化钠(Na2S)溶液,白色沉淀变成黑色沉淀,由此证明硫化银的溶度积常数小于氯化银的溶度积常数即Ksp(Ag2S)<Ksp(AgCl) |
| D.pH=6的盐酸和pH=8的碳酸钠溶液中,二者由水电离出的氢离子浓度不同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】以菱锶矿(含80~90% SrCO3,少量MgCO3、CaCO3、BaCO3等)制备高纯碳酸锶的工艺流程如下:
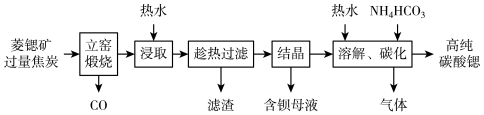
下列说法错误的是

下列说法错误的是
| A.“立窑煅烧”的立窑衬里可以选择石英砂砖 |
| B.用热水浸取有利于除去Ca(OH)2 |
| C.结晶除钡的原理是利用Ba(OH)2和Sr(OH)2的溶解度差异 |
D.“碳化”的反应方程式为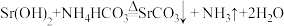 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列实验操作、现象及根据现象得出的结论,都正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 用食醋浸泡水垢,[水垢主要成分:CaCO3与Mg(OH)2] | 水垢溶解,有无色气泡产生 | 碱性:CH3COONa>Na2CO3 |
| B | 向浓度均为0.1mol/L的NaCl和NaI混合溶液中滴加少量AgNO3溶液 | 先出现黄色沉淀 | Ksp(AgI)>Ksp(AgCl) |
| C | 向CH3COONa溶液中滴加酚酞,加热 | 溶液红色加深 | 水解是吸热过程 |
| D | 用广范pH试纸测定新制氯水的pH | pH=3.0 | 氯水呈酸性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
【推荐1】一定温度下,AgCl及Ag2CrO4的沉淀溶解平衡曲线如图所示,p(X)表示离子浓度的负对数,如p(Ag+)表示-lgc(Ag+)(已知当离子浓度≤1×10-5mol·L-1时认为该离子完全沉淀;lg2=0.3)。下列说法错误的是
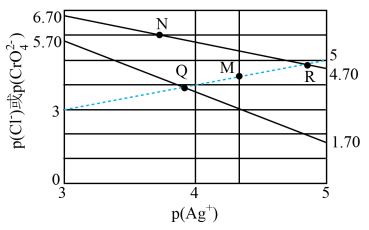

| A.处于M点的Ag2CrO4溶液会产生沉淀 |
| B.R点的溶液可能是AgCl固体溶于水形成的饱和溶液 |
| C.该温度下Ag2CrO4的Ksp=2×10-12 |
D.用AgNO3标准溶液确定NaCl溶液中的c(Cl-),可以用Na2CrO4作指示剂,当Cl-完全沉淀时,c( )=5×10-3mol·L-1 )=5×10-3mol·L-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】25 ℃时,用Na2S沉淀Cu2+、Zn2+两种金属阳离子(M2+),所需S2-最低浓度的对数值lgc(S2-)与lgc(M2+)的关系如图所示。下列说法不正确的是( )


| A.向Cu2+浓度为1×10-5 mol·L-1的工业废水中加入ZnS粉末,会有CuS沉淀析出 |
| B.25 ℃时,Ksp(CuS)约为1×10-35 |
| C.向100 mL Zn2+、Cu2+浓度均为1×10-5 mol·L-1的混合溶液中逐滴加入1×10-4 mol·L-1的Na2S溶液,Cu2+先沉淀 |
| D.Na2S溶液中:c(S2-)+c(HS-)+c(H2S)=2c(Na+) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】常温下,将11.65 g BaSO4粉末置于盛有250mL蒸馏水的烧杯中,然后向烧杯中加入Na2CO3固体(忽视溶液体积的变化)并充分搅拌,加入Na2CO3固体的过程中,溶液中几种离子的浓度变化曲线如图所示,下列说法中不正确的是


| A.相同温度时,Ksp(BaSO4)<Ksp(BaCO3) |
| B.若使0.05 mol BaSO4全部转化为BaCO3,至少加入1.3 mol Na2CO3 |
| C.BaSO4恰好全部转化为BaCO3时,溶液中离子浓度大小为:c(CO32-)>c(SO42-)>c(OH-)>c(Ba2+) |
| D.BaSO4在水中的溶解度、Ksp均比在BaCl2溶液中的大 |
您最近一年使用:0次



