按要求回答下列问题:
Ⅰ.在下列物质中:①CO2 ②KCl ③Ne ④金刚石 ⑤NH4Cl ⑥Ca(OH)2 ⑦N2H4 ⑧SiO2
⑨液氨 ⑩SO3 ⑪NaCl,其中(1)~(4)题填写序号。
(1)既有离子键,又有极性键的是_______ 。
(2)含有非极性键的分子晶体是_______ 。
(3)①、②、④、⑨、⑪中,熔点由高到低的顺序为_______ 。
(4)①、④、⑨、⑩键角由大到小的顺序为_______ 。
(5)平均1molSiO2中,含有共价键数目为_______ 。
Ⅱ.
(6)金红石型TiO2的晶胞为长方体,晶胞参数如图所示。
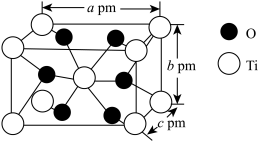
TiO2的摩尔质量为Mg/mol,阿伏加德罗常数为NA,该晶体的密度为_______ g/cm3。
(7)(CN)2是一种与Cl2性质相似的气体,分子中每个原子都达到了8电子稳定结构,写出(CN)2的电子式_______ ,分子中σ键与π键数目之比为_______ ,(CN)2分子为_______ (填“极性分子”或“非极性分子”)。
(8)乙二胺(H2N-CH2-CH2-NH2)和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高得多,原因是_______ 。
(9)布洛芬具有抗炎、镇痛、解热作用,但口服该药对胃、肠道有刺激性,可以对该分子进行如图所示的成酯修饰以减轻副作用:
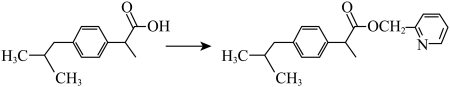
请用“*”标出以上两种分子中的所有手性碳原子_______ 。
Ⅰ.在下列物质中:①CO2 ②KCl ③Ne ④金刚石 ⑤NH4Cl ⑥Ca(OH)2 ⑦N2H4 ⑧SiO2
⑨液氨 ⑩SO3 ⑪NaCl,其中(1)~(4)题填写序号。
(1)既有离子键,又有极性键的是
(2)含有非极性键的分子晶体是
(3)①、②、④、⑨、⑪中,熔点由高到低的顺序为
(4)①、④、⑨、⑩键角由大到小的顺序为
(5)平均1molSiO2中,含有共价键数目为
Ⅱ.
(6)金红石型TiO2的晶胞为长方体,晶胞参数如图所示。

TiO2的摩尔质量为Mg/mol,阿伏加德罗常数为NA,该晶体的密度为
(7)(CN)2是一种与Cl2性质相似的气体,分子中每个原子都达到了8电子稳定结构,写出(CN)2的电子式
(8)乙二胺(H2N-CH2-CH2-NH2)和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高得多,原因是
(9)布洛芬具有抗炎、镇痛、解热作用,但口服该药对胃、肠道有刺激性,可以对该分子进行如图所示的成酯修饰以减轻副作用:

请用“*”标出以上两种分子中的所有手性碳原子
23-24高二上·浙江·期末 查看更多[1]
(已下线)高二上期末考化学190
更新时间:2023-04-07 12:44:27
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】下图表示几种无机物之间的转化关系.其中A 、B 均为黑色粉末,B为非金属单质,C 为无色无毒气体,D为金属单质,E 是红棕色气体,G 是具有漂白性的气体,H 的水溶液呈蓝色.
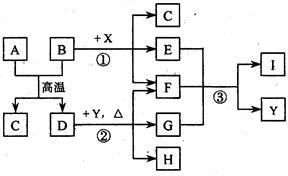
请回答下列问题:
(l)A的化学式是_____________ ,C 的电子式是_______________ ,Y 的名称是_______________ .
(2)反应① 的化学方程式为______________________________________ .
(3)实验室测定气体E 的相对分子质量时,得到的实验值总是比理论值偏大,其原因是(用化学方程式表示)___________________________________________________ .
(4)用石墨作电极电解H 的水溶液,电解总反应的离子方程式是_____________________________ .
(5)推测反应③ 的还原产物可能是______________________ .
(6)19.2 g的D与足量的一定浓度X的溶液反应,将所得的气体与_______ LO2(标准状况下)混合,恰好能被水完全吸收.

请回答下列问题:
(l)A的化学式是
(2)反应① 的化学方程式为
(3)实验室测定气体E 的相对分子质量时,得到的实验值总是比理论值偏大,其原因是(用化学方程式表示)
(4)用石墨作电极电解H 的水溶液,电解总反应的离子方程式是
(5)推测反应③ 的还原产物可能是
(6)19.2 g的D与足量的一定浓度X的溶液反应,将所得的气体与
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】如图是元素周期表中短周期元素的一部分,表中所列字母分别代表一种元素。
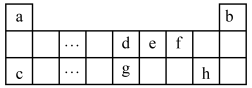
(1)上述____ (填字母)元素原子半径最小。
(2)“神舟”九号飞船内需要有一种化合物来吸收宇航员呼出的CO2,其结构式为____ 。你认为该物质应该是由图中的____ 和____ (均填字母)元素组成的。飞船中需要制造一种适合宇航员生存的人工生态环境,应该在氧气中充入一种气体,用于稀释氧气,该气体分子的电子式是____ 。
(3)在一定条件下,a与h可形成一种18电子化合物,其分子中所含化学键的类型为____ (填“极性键”或“非极性键”);该物质的电子式是____ 。
(4)现有另一种元素X,其原子获得一个电子的能力比图中所列元素都要强,则X是____ (填名称)元素,用电子式表示其氢化物分子的形成过程____ 。

(1)上述
(2)“神舟”九号飞船内需要有一种化合物来吸收宇航员呼出的CO2,其结构式为
(3)在一定条件下,a与h可形成一种18电子化合物,其分子中所含化学键的类型为
(4)现有另一种元素X,其原子获得一个电子的能力比图中所列元素都要强,则X是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】原子序数由小到大排列的四种短周期元素X、Y、Z、W,其中X、Z、W与氢元素可形成XH3、H2Z和HW三种分子:Y与氧元素可形成Y2O和Y2O2两种离子化合物。
(1)Y与Z形成的化合物电子式为_______ ,含有的化学键是_______ 。
(2)用电子式表示Y2O的形成过程:_______ 。
(3)X、Z、W三种元素的最高价氧化物对应的水化物中,酸性最强的是_______ (填化学式)。
(4)XH3与W2发生置换反应,生成的化合物属于离子化合物,该离子化合物是_______ (填化学式)。
(5)W2与NaOH溶液反应生成的三种物质中,属于离子化合物的是_______ 。
(1)Y与Z形成的化合物电子式为
(2)用电子式表示Y2O的形成过程:
(3)X、Z、W三种元素的最高价氧化物对应的水化物中,酸性最强的是
(4)XH3与W2发生置换反应,生成的化合物属于离子化合物,该离子化合物是
(5)W2与NaOH溶液反应生成的三种物质中,属于离子化合物的是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】某温度下,在体积为5 L的密闭容器内发生如下反应: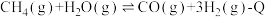
(1)在上述反应的反应物与生成物中,非极性分子为:_______ 。
(2)若反应20 min后气体总物质的量增加了10 mol,则甲烷的平均反应速率为_______ 。
(3)下列选项中的物理量不变时,一定可以判断反应达到平衡的是_______。
(4)在某一时刻,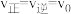 ,反应若改变某一条件,可使得
,反应若改变某一条件,可使得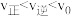 ,指出可以改变的条件,并说明理由:
,指出可以改变的条件,并说明理由:_______ 。
已知CO与合成 是可逆反应:
是可逆反应: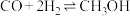 。
。
(5)若上述反应达到平衡时CO与 的转化率相同,则投料比
的转化率相同,则投料比
_______ 。
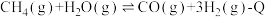
(1)在上述反应的反应物与生成物中,非极性分子为:
(2)若反应20 min后气体总物质的量增加了10 mol,则甲烷的平均反应速率为
(3)下列选项中的物理量不变时,一定可以判断反应达到平衡的是_______。
| A.容器内氢元素的质量分数 | B.容器内的压强 |
| C.反应的平衡常数 | D.容器内气体的平均相对分子质量 |
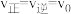 ,反应若改变某一条件,可使得
,反应若改变某一条件,可使得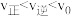 ,指出可以改变的条件,并说明理由:
,指出可以改变的条件,并说明理由:已知CO与合成
 是可逆反应:
是可逆反应: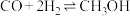 。
。(5)若上述反应达到平衡时CO与
 的转化率相同,则投料比
的转化率相同,则投料比
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】按要求回答下列问题。
(1)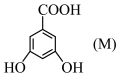 和
和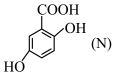 熔点:M
熔点:M_______ N(填“高于”或“低于”)。
(2) 是
是_______ 分子(填“极性”或“非极性”),其中As的基态原子简化电子排布式为:_______ 。
(3)向 溶液中滴加氨水会生成蓝色沉淀,再滴加氨水到沉淀刚好全部溶解可得深蓝色溶液,请写出蓝色沉淀溶解时发生的化学方程式:
溶液中滴加氨水会生成蓝色沉淀,再滴加氨水到沉淀刚好全部溶解可得深蓝色溶液,请写出蓝色沉淀溶解时发生的化学方程式:_______ 。
(4)根据价层电子对互斥模型,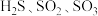 的气态分子中,中心原子价层电子对数不同于其他分子的是
的气态分子中,中心原子价层电子对数不同于其他分子的是_______ 。
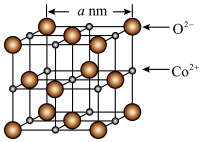
(5)CoO的面心立方晶胞如下图所示。设阿伏加德罗常数的值为NA,则CoO晶体的密度为_______  。
。 、
、 、
、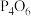 和
和 的熔点由大到小的顺序为:
的熔点由大到小的顺序为:_______ 。
(1)
 和
和 熔点:M
熔点:M(2)
 是
是(3)向
 溶液中滴加氨水会生成蓝色沉淀,再滴加氨水到沉淀刚好全部溶解可得深蓝色溶液,请写出蓝色沉淀溶解时发生的化学方程式:
溶液中滴加氨水会生成蓝色沉淀,再滴加氨水到沉淀刚好全部溶解可得深蓝色溶液,请写出蓝色沉淀溶解时发生的化学方程式:(4)根据价层电子对互斥模型,
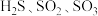 的气态分子中,中心原子价层电子对数不同于其他分子的是
的气态分子中,中心原子价层电子对数不同于其他分子的是(5)CoO的面心立方晶胞如下图所示。设阿伏加德罗常数的值为NA,则CoO晶体的密度为
 。
。
 、
、 、
、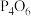 和
和 的熔点由大到小的顺序为:
的熔点由大到小的顺序为:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】硫代乙醇酸( )可用作毛毯整理剂及冷烫液的原料,工业上可利用反应
)可用作毛毯整理剂及冷烫液的原料,工业上可利用反应 制备,实验室设计如图装置进行相关模拟实验(夹持装置省略)。
制备,实验室设计如图装置进行相关模拟实验(夹持装置省略)。 (熔点-16.5℃、沸点123℃)在空气中迅速被氧化,在较高温度下受热分解产生有毒的硫化物烟气。
(熔点-16.5℃、沸点123℃)在空气中迅速被氧化,在较高温度下受热分解产生有毒的硫化物烟气。
回答下列问题:
(1) 可通过以下反应制备:
可通过以下反应制备: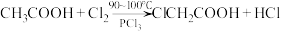 。
。
①简述 小于
小于 的原因:
的原因:___________ 。
② 属于
属于___________ (填“极性”或“非极性”)分子。
(2)该实验需要250mL 10mol/L NaOH溶液,配制该溶液时,下列操作正确的是___________ (填标号)。
(3)检查完气密性后,关闭 、
、 、
、 ,添加实验药品,先制备NaHS。
,添加实验药品,先制备NaHS。
①制备 时,打开
时,打开 ,使25%磷酸缓缓滴入
,使25%磷酸缓缓滴入 浓溶液中,缓缓滴加的优点是
浓溶液中,缓缓滴加的优点是___________ 。
②实验时不能用25%硝酸代替装置A中25%磷酸的原因是___________ 。
③装置C的作用是___________ 。
④装置D中多孔球泡的作用是___________ ;写出装置D中刚开始反应的离子方程式:___________ 。
⑤经过一系列分离提纯可获得 粗品,提纯
粗品,提纯 需要采取减压精馏的原因是
需要采取减压精馏的原因是___________ 。
 )可用作毛毯整理剂及冷烫液的原料,工业上可利用反应
)可用作毛毯整理剂及冷烫液的原料,工业上可利用反应 制备,实验室设计如图装置进行相关模拟实验(夹持装置省略)。
制备,实验室设计如图装置进行相关模拟实验(夹持装置省略)。
 (熔点-16.5℃、沸点123℃)在空气中迅速被氧化,在较高温度下受热分解产生有毒的硫化物烟气。
(熔点-16.5℃、沸点123℃)在空气中迅速被氧化,在较高温度下受热分解产生有毒的硫化物烟气。回答下列问题:
(1)
 可通过以下反应制备:
可通过以下反应制备: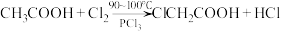 。
。①简述
 小于
小于 的原因:
的原因:②
 属于
属于(2)该实验需要250mL 10mol/L NaOH溶液,配制该溶液时,下列操作正确的是
| 操作 |
|
|
|
|
| 选项 | a | b | c | d |
(3)检查完气密性后,关闭
 、
、 、
、 ,添加实验药品,先制备NaHS。
,添加实验药品,先制备NaHS。①制备
 时,打开
时,打开 ,使25%磷酸缓缓滴入
,使25%磷酸缓缓滴入 浓溶液中,缓缓滴加的优点是
浓溶液中,缓缓滴加的优点是②实验时不能用25%硝酸代替装置A中25%磷酸的原因是
③装置C的作用是
④装置D中多孔球泡的作用是
⑤经过一系列分离提纯可获得
 粗品,提纯
粗品,提纯 需要采取减压精馏的原因是
需要采取减压精馏的原因是
您最近一年使用:0次
【推荐1】物质结构的多样性使人类使用的材料精彩纷呈,请回答下列问题。
(1)氧化锆(ZrO2)材料具有高硬度,高强度,高韧性,极高的耐磨性及耐化学腐蚀性,氧化锆陶瓷在许多领域获得广泛应用。锆是与钛同族的第五周期元素,则锆原子的价电子排布式为____ 。
(2)同主族元素所形成的物质具有性质相似的特点,H2O的熔沸点均比H2S高,其原因是____ 。
(3)Mn和Fe的部分电离能数据如表:
气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难,其原因是____ 。
(4)电镀厂排放的废水中常含有剧毒的CN-,可在TiO2的催化下,先用NaClO将CN-氧化成CNO-,再在酸性条件下将CNO-继续氧化成N2和CO2。请回答:
①H、C、N、O四种元素的电负性由小到大的顺序为____ 。
②与CNO-互为等电子体的微粒的化学式为___ (写出一种即可)。
(5)硒化锌是一种重要的半导体材料,其晶胞结构如图所示(Se位于晶胞的顶点和面心),已知该晶胞中硒原子的配位数为____ ;若该晶胞密度为ρg•cm-3,硒化锌的摩尔质量为Mg•mol-1。NA代表阿伏加德罗常数,则晶胞参数a为____ pm(写出表达式即可)。

(1)氧化锆(ZrO2)材料具有高硬度,高强度,高韧性,极高的耐磨性及耐化学腐蚀性,氧化锆陶瓷在许多领域获得广泛应用。锆是与钛同族的第五周期元素,则锆原子的价电子排布式为
(2)同主族元素所形成的物质具有性质相似的特点,H2O的熔沸点均比H2S高,其原因是
(3)Mn和Fe的部分电离能数据如表:
| 元素 | Mn | Fe | |
| 电离能(kJ·mol-1) | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难,其原因是
(4)电镀厂排放的废水中常含有剧毒的CN-,可在TiO2的催化下,先用NaClO将CN-氧化成CNO-,再在酸性条件下将CNO-继续氧化成N2和CO2。请回答:
①H、C、N、O四种元素的电负性由小到大的顺序为
②与CNO-互为等电子体的微粒的化学式为
(5)硒化锌是一种重要的半导体材料,其晶胞结构如图所示(Se位于晶胞的顶点和面心),已知该晶胞中硒原子的配位数为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】材料是生物医疗、国防军事以及航空航天等领域发展提供支撑。
(1)磷酸亚铁锂( )常用作锂离子电池正极材料,周期表中与Li的化学性质最相似的邻族元素是
)常用作锂离子电池正极材料,周期表中与Li的化学性质最相似的邻族元素是_______ (填元素符号),该元素基态原子核外M层电子自旋状态_______ (填“相同”或“相反”);
(2)苯胺(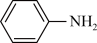 )常作为合成原料,与甲苯(
)常作为合成原料,与甲苯(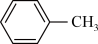 )相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是
)相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是_______ ;
(3)反应 的产物分子中采取
的产物分子中采取 杂化的原子是
杂化的原子是_______ (填元素名称):
(4) 是制备氟磺酸类化合物的常用原料,分子结构如图所示:
是制备氟磺酸类化合物的常用原料,分子结构如图所示:
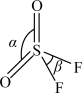
已知键角α为124°,β为96°,则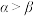 的原因主要是
的原因主要是_______ ;
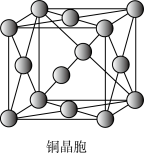
(5)第三代硅太阳能电池以铜钢镓硒CiGs(CIS中掺入Ga)等化合物为主要材料。Cu晶体的晶胞如图,其配位数为_______ ;
往 溶液中加入过量氨水,可生成
溶液中加入过量氨水,可生成 ,下列说法正确的是
,下列说法正确的是_______ ;
A. 中所含的化学键有离子键、极性键和配位键
中所含的化学键有离子键、极性键和配位键
B.在 中
中 给出孤电子对,
给出孤电子对, 提供空轨道
提供空轨道
C. 组成元素中第一电离能最大的是氧元素
组成元素中第一电离能最大的是氧元素
D. 与
与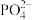 互为等电子体,空间构型均为正四面体形
互为等电子体,空间构型均为正四面体形
(6) 和
和 属于简单磷酸盐,而直链的多磷酸盐则是一种复杂磷酸盐,如:焦磷酸钠、三磷酸钠等。焦磷酸根离子、三磷酸根离子如下图所示:
属于简单磷酸盐,而直链的多磷酸盐则是一种复杂磷酸盐,如:焦磷酸钠、三磷酸钠等。焦磷酸根离子、三磷酸根离子如下图所示:
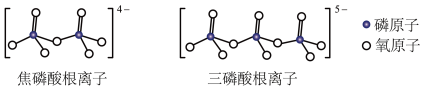
这类磷酸根离子的化学式可用通式表示为_______ (用n代表P原子数)。
(1)磷酸亚铁锂(
 )常用作锂离子电池正极材料,周期表中与Li的化学性质最相似的邻族元素是
)常用作锂离子电池正极材料,周期表中与Li的化学性质最相似的邻族元素是(2)苯胺(
 )常作为合成原料,与甲苯(
)常作为合成原料,与甲苯( )相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是
)相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是(3)反应
 的产物分子中采取
的产物分子中采取 杂化的原子是
杂化的原子是(4)
 是制备氟磺酸类化合物的常用原料,分子结构如图所示:
是制备氟磺酸类化合物的常用原料,分子结构如图所示:
已知键角α为124°,β为96°,则
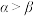 的原因主要是
的原因主要是(5)第三代硅太阳能电池以铜钢镓硒CiGs(CIS中掺入Ga)等化合物为主要材料。Cu晶体的晶胞如图,其配位数为

往
 溶液中加入过量氨水,可生成
溶液中加入过量氨水,可生成 ,下列说法正确的是
,下列说法正确的是A.
 中所含的化学键有离子键、极性键和配位键
中所含的化学键有离子键、极性键和配位键B.在
 中
中 给出孤电子对,
给出孤电子对, 提供空轨道
提供空轨道C.
 组成元素中第一电离能最大的是氧元素
组成元素中第一电离能最大的是氧元素D.
 与
与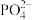 互为等电子体,空间构型均为正四面体形
互为等电子体,空间构型均为正四面体形(6)
 和
和 属于简单磷酸盐,而直链的多磷酸盐则是一种复杂磷酸盐,如:焦磷酸钠、三磷酸钠等。焦磷酸根离子、三磷酸根离子如下图所示:
属于简单磷酸盐,而直链的多磷酸盐则是一种复杂磷酸盐,如:焦磷酸钠、三磷酸钠等。焦磷酸根离子、三磷酸根离子如下图所示:
这类磷酸根离子的化学式可用通式表示为
您最近一年使用:0次
【推荐3】二氧化碳化学资源化利用已经显示出越来越重要的科技与经济价值,如用铜锌氧化物催化二氧化碳加氢生成 ,合成碳酸乙烯酯(
,合成碳酸乙烯酯(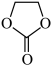 )等。回答下列问题:
)等。回答下列问题:
(1)基态铜原子价电子排布式为_______ ;第二电离能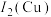
_______ 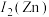 。
。
(2)碳酸乙烯酯中碳原子杂化方式为_______ ,每个分子中含_______ 个 键。
键。
(3) 加氢得到
加氢得到 ,
, 的沸点比
的沸点比 的高,原因是
的高,原因是_______ 。
(4)高温时,太阳能反应器中的 失去部分氧,温度稍低时,从
失去部分氧,温度稍低时,从 中重新夺取氧。
中重新夺取氧。 的晶胞结构如图所示:
的晶胞结构如图所示:
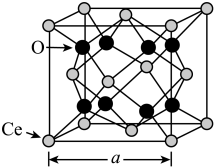
①Ce的配位数为_______ 。
②若高温下该晶胞中1个氧原子变为空位,_______ 个面心上的Ce由 价变为
价变为 价(顶点上的Ce化合价不变)。
价(顶点上的Ce化合价不变)。
③已知 的密度为
的密度为 ,设
,设 为阿伏加德罗常数的值,则晶胞边长
为阿伏加德罗常数的值,则晶胞边长
_______ pm(列出计算式即可)。
 ,合成碳酸乙烯酯(
,合成碳酸乙烯酯( )等。回答下列问题:
)等。回答下列问题:(1)基态铜原子价电子排布式为
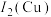
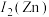 。
。(2)碳酸乙烯酯中碳原子杂化方式为
 键。
键。(3)
 加氢得到
加氢得到 ,
, 的沸点比
的沸点比 的高,原因是
的高,原因是(4)高温时,太阳能反应器中的
 失去部分氧,温度稍低时,从
失去部分氧,温度稍低时,从 中重新夺取氧。
中重新夺取氧。 的晶胞结构如图所示:
的晶胞结构如图所示:
①Ce的配位数为
②若高温下该晶胞中1个氧原子变为空位,
 价变为
价变为 价(顶点上的Ce化合价不变)。
价(顶点上的Ce化合价不变)。③已知
 的密度为
的密度为 ,设
,设 为阿伏加德罗常数的值,则晶胞边长
为阿伏加德罗常数的值,则晶胞边长
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】过渡金属硫化物因其独特的光电催化性能及相对稳定的化学性质而受到广泛的研究,三元金属硫化物ZnIn2S4是一种层状结构的可见光响应光催化剂。回答下列问题:
(1)基态Zn的价电子排布式为_______ 。Gn与In同主族,第一电离能:Zn_______ Ga (填“<”、“>”或“=”)。
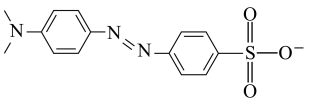
(2)指示剂甲基橙阴离子的结构如图,其中硫原子的杂化类型为_______ ,该结构中含有孤电子对的原子有_______ 。
(3) 的空间构型为
的空间构型为_______ , 、
、 、SO3按键角从小到大的顺序排列为
、SO3按键角从小到大的顺序排列为_______ ,试解释原因_______ 。
(4)Zn2+容易形成配合物,[Zn(CN)4]2-中Zn2+与CN - 的碳原子形成配位键。 [Zn(CN)4]2-中σ 键与π键的个数之比为_______ 。
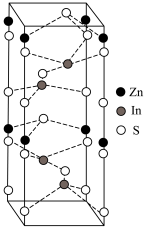
(5)ZnIn2S4晶胞结构如图,其边长为a nm,高为b nm,阿伏加德罗常数的值为NA,该晶体的密度为_______ g·cm-3(列出计算式)。
(1)基态Zn的价电子排布式为
(2)指示剂甲基橙阴离子的结构如图,其中硫原子的杂化类型为

(3)
 的空间构型为
的空间构型为 、
、 、SO3按键角从小到大的顺序排列为
、SO3按键角从小到大的顺序排列为(4)Zn2+容易形成配合物,[Zn(CN)4]2-中Zn2+与CN - 的碳原子形成配位键。 [Zn(CN)4]2-中σ 键与π键的个数之比为
(5)ZnIn2S4晶胞结构如图,其边长为a nm,高为b nm,阿伏加德罗常数的值为NA,该晶体的密度为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】氮族元素包括氮(N)、磷(P)、砷(As)、锑(Sb)、铋(Bi),在性质上表现出从典型非金属元素到典型金属元素的完整过渡。回管下列问题:
(1)羟胺(NH2OH)的水溶液呈碱性,其碱性原理与氨水相似,同浓度两种溶液的碱性较强的是_____ (填“NH2OH”或“NH3”),原因是_____ 。
(2)氢键的形成对物质的密度、熔沸点、粘稠性等产生影响。市售82%磷酸是粘稠状的液体,黏度较大的原因是_____ 。
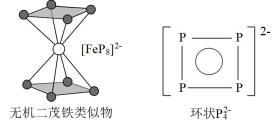
(3)南开大学某课题组成功合成无机二茂铁的类似物[FeP8]2-,结构如图所示,环状 结构与苯相似,
结构与苯相似, 中的大
中的大 键表示为
键表示为_____ 。(分子中的大π键可用 表示,其中m代表形成大π键的原子数,n代表形成大π键的电子数)
表示,其中m代表形成大π键的原子数,n代表形成大π键的电子数)
(4)超盐晶体PH4AlBr4由超碱 和超卤素
和超卤素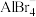 组成。比较
组成。比较 与PH3键角大小:
与PH3键角大小:
_____ PH3(填“ ”、“<”或“=”),原因是
”、“<”或“=”),原因是_____ 。
(5)钼酸铋(Bi2MoO6)可用于光催化水的分解,其立方晶胞结构(未画出氧原子)如图所示,晶胞参数为a pm、a pm、c pm。
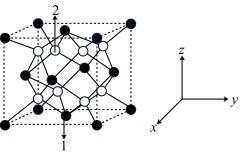
①若原子1的分数坐标为( ,
, ,0),原子2的分数坐标为
,0),原子2的分数坐标为_____ 。
②设NA为阿伏加德罗常数的值,Bi2MoO6的摩尔质量为M。Bi2MoO6晶体的密度为_____ g/cm3 (列计算式)。
(1)羟胺(NH2OH)的水溶液呈碱性,其碱性原理与氨水相似,同浓度两种溶液的碱性较强的是
(2)氢键的形成对物质的密度、熔沸点、粘稠性等产生影响。市售82%磷酸是粘稠状的液体,黏度较大的原因是
(3)南开大学某课题组成功合成无机二茂铁的类似物[FeP8]2-,结构如图所示,环状
 结构与苯相似,
结构与苯相似, 中的大
中的大 键表示为
键表示为 表示,其中m代表形成大π键的原子数,n代表形成大π键的电子数)
表示,其中m代表形成大π键的原子数,n代表形成大π键的电子数)
(4)超盐晶体PH4AlBr4由超碱
 和超卤素
和超卤素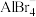 组成。比较
组成。比较 与PH3键角大小:
与PH3键角大小:
 ”、“<”或“=”),原因是
”、“<”或“=”),原因是(5)钼酸铋(Bi2MoO6)可用于光催化水的分解,其立方晶胞结构(未画出氧原子)如图所示,晶胞参数为a pm、a pm、c pm。

①若原子1的分数坐标为(
 ,
, ,0),原子2的分数坐标为
,0),原子2的分数坐标为②设NA为阿伏加德罗常数的值,Bi2MoO6的摩尔质量为M。Bi2MoO6晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】Ni2+与丁二酮肟生成鲜红色丁二酮肟镍沉淀,该反应可用于检验Ni2+。
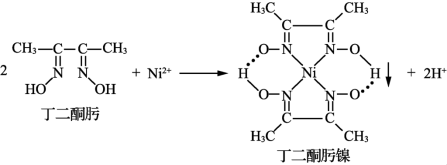
(1)Ni2+基态核外电子排布式为___________ 。
(2)1mol丁二酮肟分子中含有σ键的数目为______ mol。
(3)丁二酮肟镍分子中碳原子的杂化轨道类型为_____ 。
(4)Ni(CO)4是一种无色液体,沸点为43℃,熔点为-19.3 ℃。Ni(CO)4的晶体类型是_ 。
(5)与CO互为等电子体的二价阴离子为_____ ,Ni(CO)4中Ni与CO的C原子形成配位键,不考虑空间构型,Ni(CO)4的结构可用示意图表示为_____ 。
(6)下列离子的VSEPR模型与离子的空间立体构型一致的是_______ 。
A.SO32- B.ClO4- C.NO2- D.ClO3-
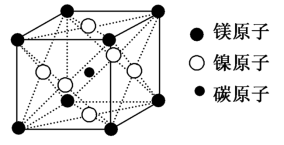
(7)最近发现,只含镁、镍和碳三种元素的晶体竟然也具有超导性。鉴于这三种元素都是常见元素,从而引起广泛关注。该新型超导晶体的一个晶胞如图所示,则该晶体的化学式为______

(1)Ni2+基态核外电子排布式为
(2)1mol丁二酮肟分子中含有σ键的数目为
(3)丁二酮肟镍分子中碳原子的杂化轨道类型为
(4)Ni(CO)4是一种无色液体,沸点为43℃,熔点为-19.3 ℃。Ni(CO)4的晶体类型是
(5)与CO互为等电子体的二价阴离子为
(6)下列离子的VSEPR模型与离子的空间立体构型一致的是
A.SO32- B.ClO4- C.NO2- D.ClO3-
(7)最近发现,只含镁、镍和碳三种元素的晶体竟然也具有超导性。鉴于这三种元素都是常见元素,从而引起广泛关注。该新型超导晶体的一个晶胞如图所示,则该晶体的化学式为

您最近一年使用:0次