I、吡啶(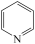 )是类似于苯的芳香化合物,工业上用作合成药品、消毒剂、染料等的原料。2-乙烯基吡啶(VPy)是合成治疗矽肺病药物的原料,可由如图路线合成。
)是类似于苯的芳香化合物,工业上用作合成药品、消毒剂、染料等的原料。2-乙烯基吡啶(VPy)是合成治疗矽肺病药物的原料,可由如图路线合成。
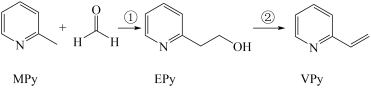
请回答下列问题:
(1)MPy分子中碳原子的杂化方式为_______
(2)EPy晶体中微粒间的作用力类型有_______ (填标号)。
a.离子键b.金属键c.极性键d.非极性键e.配位键f.氢键
(3)反应①中每生成1molEPy,断裂_______ 个π键,形成_______ 个σ键。
(4)吡啶、 与
与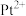 形成二氯二吡啶合铂配合物,有顺式和反式两种同分异构体。科学研究表明,顺式分子具有抗癌活性。
形成二氯二吡啶合铂配合物,有顺式和反式两种同分异构体。科学研究表明,顺式分子具有抗癌活性。
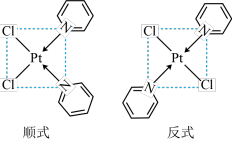
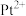 的配位数为
的配位数为_______ 。顺式二氯二吡啶合铂分子能否溶于水_______ (填“能”或“否”),
Ⅱ、有下列实验:
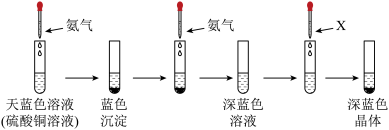
(5)该深蓝色晶体的化学式为_______ ,溶剂X可以是_______ (填名称),继续添加氨水,沉淀溶解,写出沉淀溶解的离子方程式为_______ 。
(6)该实验能说明 、
、 与
与 结合能力的强到弱的顺序是
结合能力的强到弱的顺序是_______ 。
(7)下列有关化学实验“操作→现象→解释”均正确的是_______ 。
 )是类似于苯的芳香化合物,工业上用作合成药品、消毒剂、染料等的原料。2-乙烯基吡啶(VPy)是合成治疗矽肺病药物的原料,可由如图路线合成。
)是类似于苯的芳香化合物,工业上用作合成药品、消毒剂、染料等的原料。2-乙烯基吡啶(VPy)是合成治疗矽肺病药物的原料,可由如图路线合成。
请回答下列问题:
(1)MPy分子中碳原子的杂化方式为
(2)EPy晶体中微粒间的作用力类型有
a.离子键b.金属键c.极性键d.非极性键e.配位键f.氢键
(3)反应①中每生成1molEPy,断裂
(4)吡啶、
 与
与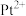 形成二氯二吡啶合铂配合物,有顺式和反式两种同分异构体。科学研究表明,顺式分子具有抗癌活性。
形成二氯二吡啶合铂配合物,有顺式和反式两种同分异构体。科学研究表明,顺式分子具有抗癌活性。
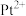 的配位数为
的配位数为Ⅱ、有下列实验:

(5)该深蓝色晶体的化学式为
(6)该实验能说明
 、
、 与
与 结合能力的强到弱的顺序是
结合能力的强到弱的顺序是(7)下列有关化学实验“操作→现象→解释”均正确的是
| 选项 | 操作 | 现象 | 解释 |
| A | 向某溶液中滴加KSCN溶液 | 产生红色沉淀 | 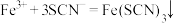 |
| B | 向由0.1molCrCl3·6H2O配成的溶液加入足量AgNO3溶液 | 产生0.2mol沉淀 | 已知 的配位数为6.则CrCl3·6H2O的化学式可表示为 的配位数为6.则CrCl3·6H2O的化学式可表示为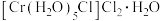 |
| C | 向K2Cr2O7溶液中先滴加3滴浓硫酸,再改加l0滴浓NaOH | 溶液先橙色加深,后变为黄色 | 溶液中存在: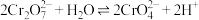 |
| D | 向AgCl悬浊液中滴加氨水 | 沉淀溶解 | AgCl不溶于水,但溶于氨水,重新电离成Ag+和Cl- |
更新时间:2023-04-11 15:37:19
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】已知:W、X、Y、Z、T 均为短周期元素,且原子半径依次增大。请填空:
(1)W、Z 是形成化合物种类最多的两种元素,写出 Z 的核外电子的轨道表示式______________ 。
(2)化合物 YW3 溶于水能使酚酞变红,用方程式表示酚酞变红的原因____ 。
(3)元素 T 的原子中电子占据 7 根轨道,则 T 在元素周期表____ 周期___ 族; T 的化合物 TY 熔融时不导电,常用作砂轮与耐高温材料,由此推知,它属于____ 。
a 离子晶体 b 原子晶体 c 分子晶体 d 无法判断
(4)YX3 与 YW3 具有相同的分子空间构型,YX3 属于______ (填“极性”、“非极性”)分子,其中 Y 的化合价为____ 。
(1)W、Z 是形成化合物种类最多的两种元素,写出 Z 的核外电子的轨道表示式
(2)化合物 YW3 溶于水能使酚酞变红,用方程式表示酚酞变红的原因
(3)元素 T 的原子中电子占据 7 根轨道,则 T 在元素周期表
a 离子晶体 b 原子晶体 c 分子晶体 d 无法判断
(4)YX3 与 YW3 具有相同的分子空间构型,YX3 属于
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】下图是元素周期表的一部分:
Ⅰ.用化学用语 回答下列问题:
(1)①、②、⑥形成的化合物中存在的化学键类型有________ 。
(2)④、⑦、⑧的最高价含氧酸的酸性由强到弱的顺序是_______ 。
(3)写出②的离子结构示意图为__________ 。
(4)Y由②⑥⑧三种元素组成,它的水溶液是生活中常见的消毒剂。Y的水溶液与洁厕灵混合使用会产生一种有毒气体,该反应的离子方程式为_______ 。
Ⅱ.A、B、C、D都是中学化学中常见的物质,其中A、B、C均含有同一种元素,在一定条件下相互转化关系如下(部分反应中的水已略去)。根据题意回答下列问题:
(1)若A是一种金属单质,C是淡黄色固体,写出C的一种用途_____ ;
(2)若A、B、C均为化合物且含有同一种金属元素,D是会造成温室效应的一种气体,请写出D的电子式_____ ,A和C反应的离子方程式 ___ 。
(3)若D是一种常见的过渡金属单质,原子核内有26个质子,向C的水溶液中滴加AgNO3溶液,产生不溶于稀HNO3的白色沉淀,检验此C溶液中金属离子的方法是________ ;又知在酸性溶液中该金属离子能被双氧水氧化,写出该反应的离子方程式_________ 。
| ① | |||||||||||||||||
| ④ | ⑤ | ⑥ | |||||||||||||||
| ② | ③ | ⑦ | ⑧ | ||||||||||||||
| Fe | |||||||||||||||||
(1)①、②、⑥形成的化合物中存在的化学键类型有
(2)④、⑦、⑧的最高价含氧酸的酸性由强到弱的顺序是
(3)写出②的离子结构示意图为
(4)Y由②⑥⑧三种元素组成,它的水溶液是生活中常见的消毒剂。Y的水溶液与洁厕灵混合使用会产生一种有毒气体,该反应的离子方程式为
Ⅱ.A、B、C、D都是中学化学中常见的物质,其中A、B、C均含有同一种元素,在一定条件下相互转化关系如下(部分反应中的水已略去)。根据题意回答下列问题:
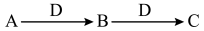
(1)若A是一种金属单质,C是淡黄色固体,写出C的一种用途
(2)若A、B、C均为化合物且含有同一种金属元素,D是会造成温室效应的一种气体,请写出D的电子式
(3)若D是一种常见的过渡金属单质,原子核内有26个质子,向C的水溶液中滴加AgNO3溶液,产生不溶于稀HNO3的白色沉淀,检验此C溶液中金属离子的方法是
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
解题方法
【推荐3】有机物A、B、C、D有如下转化关系。回答下列问题:

(1)乙烯的电子式为____________ ,分子中含有的共价键类型有________ (填极性键或非极性键)。
(2)写出反应的化学方程式和有机反应类型:
④__________________________________________ ,反应类型:________ 。
⑤__________________________________________ ,反应类型:________ 。

(1)乙烯的电子式为
(2)写出反应的化学方程式和有机反应类型:
④
⑤
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】西瓜膨大剂别名氯吡苯脲,是经过国家批准的植物生长调节剂,实践证明长期使用对人体无害。已知其相关性质如表所示:
(1)氯吡苯脲晶体中,氮原子的杂化轨道类型为_______ 。
(2)氯吡苯脲晶体中,微粒间的作用力不包括_______ 。(填序号)
A.离子键 B.金属键 C.极性键 D.非极性键 E.配位键 F.氢键
(3)氯吡苯脲易溶于水的原因是_______ 。
(4)查文献可知,可用2-氯-4-氨基吡啶与异氰酸苯酯反应,生成氯吡苯脲。

1mol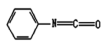 中含有的键数目为
中含有的键数目为_______ 。
(5)已知苯环上的-OH能电离出H+,(苯酚)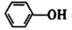 ⇌H++
⇌H++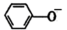 ,苯酚的酸性大于
,苯酚的酸性大于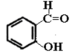 (邻羟基苯甲醛),其原因是
(邻羟基苯甲醛),其原因是_______ 。
| 分子式 | 结构简式 | 外观 | 熔点 | 溶解性 |
| C12H10ClN3O |  | 白色结晶粉末 | 170~172°C | 易溶于水 |
(2)氯吡苯脲晶体中,微粒间的作用力不包括
A.离子键 B.金属键 C.极性键 D.非极性键 E.配位键 F.氢键
(3)氯吡苯脲易溶于水的原因是
(4)查文献可知,可用2-氯-4-氨基吡啶与异氰酸苯酯反应,生成氯吡苯脲。

1mol
 中含有的键数目为
中含有的键数目为(5)已知苯环上的-OH能电离出H+,(苯酚)
 ⇌H++
⇌H++ ,苯酚的酸性大于
,苯酚的酸性大于 (邻羟基苯甲醛),其原因是
(邻羟基苯甲醛),其原因是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】生产生活中处处有化学,结合物质与结构的相关知识,回答下列问题:
(1)维生素B1可作为辅酶参与糖的代谢,并有保护神经系统的作用,该物质的结构简式如图所示:
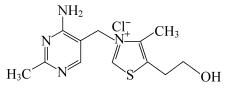
①维生素B1晶体溶于水的过程中要克服的微粒间的作用力有___________ 。
a.离子键、共价键
b.离子键、氢键、共价键
c.氢键、范德华力
d.离子键、氢键、范德华力
②维生素B1燃烧可生成N2、NH3、CO2、SO2、H2O、HCl等物质,这些物质中属于非极性分子的化合物有___________ 。
(2)液氨常被用作制冷剂,若不断地升高温度,实现“液氨 氨气
氨气 氮气和氢气
氮气和氢气 氮原子和氢原子”的变化,在变化的各阶段被破坏的粒子间的相互作用是①
氮原子和氢原子”的变化,在变化的各阶段被破坏的粒子间的相互作用是①___________ ;②极性键;③___________ 。
(3)F2与其他卤素单质反应可以形成卤素互化物,例如ClF3、BrF3等。已知反应Cl2(g)+3F2(g)=2ClF3(g) ΔH=-313 kJ·mol-1,F—F键的键能为159 kJ·mol-1,Cl-Cl键的键能为242 kJ·mol-1,则ClF3中Cl-F键的平均键能为___________ kJ·mol-1。ClF3的熔、沸点比BrF3的___________ (填“高”或“低”)。
(4)TiCl4稳定性比CCl4差,极易水解,试从结构分析其原因___________ 。
(5)氯丙烯分子( )中碳原子轨道杂化类型是
)中碳原子轨道杂化类型是___________ 。
(6)铁能与三氮唑(Bipy,结构如图)形成多种化合物。
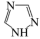
1 mol Bipy中含有σ键___________ mol,Bipy中碳原子杂化方式为___________ 。
(1)维生素B1可作为辅酶参与糖的代谢,并有保护神经系统的作用,该物质的结构简式如图所示:

①维生素B1晶体溶于水的过程中要克服的微粒间的作用力有
a.离子键、共价键
b.离子键、氢键、共价键
c.氢键、范德华力
d.离子键、氢键、范德华力
②维生素B1燃烧可生成N2、NH3、CO2、SO2、H2O、HCl等物质,这些物质中属于非极性分子的化合物有
(2)液氨常被用作制冷剂,若不断地升高温度,实现“液氨
 氨气
氨气 氮气和氢气
氮气和氢气 氮原子和氢原子”的变化,在变化的各阶段被破坏的粒子间的相互作用是①
氮原子和氢原子”的变化,在变化的各阶段被破坏的粒子间的相互作用是①(3)F2与其他卤素单质反应可以形成卤素互化物,例如ClF3、BrF3等。已知反应Cl2(g)+3F2(g)=2ClF3(g) ΔH=-313 kJ·mol-1,F—F键的键能为159 kJ·mol-1,Cl-Cl键的键能为242 kJ·mol-1,则ClF3中Cl-F键的平均键能为
(4)TiCl4稳定性比CCl4差,极易水解,试从结构分析其原因
(5)氯丙烯分子(
 )中碳原子轨道杂化类型是
)中碳原子轨道杂化类型是(6)铁能与三氮唑(Bipy,结构如图)形成多种化合物。

1 mol Bipy中含有σ键
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】氮元素可以形成多种化合物,回答以下问题;
(1)基态氮原子的轨道表示式是___________ 。
(2)肼( )分子可视为
)分子可视为 分子中的一个氢原子被
分子中的一个氢原子被 (氨基)取代形成的另一种氮的氢化物。
(氨基)取代形成的另一种氮的氢化物。
①写出与 分子互为等电子体的一种离于的化学式
分子互为等电子体的一种离于的化学式___________ 。
②肼( )是
)是___________ 分子(填极性分子或非极性分子)。
③肼可用作火箭燃料,燃烧时发生的反应是: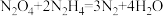
若该反应中有4mol N-H键断裂,则形成的 键有
键有___________ mol。
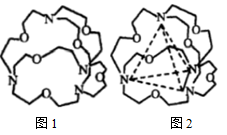
(3)图1表示某种含氮有机化合物的结构,其分子内4个氮原子分别位于正四面体的4个顶点(见图2),分子内存在空腔,能嵌入某离子或分子并形成4个氢键予以识别。下列分子或离子中,能被该有机化合物识别的是___________ (填标号)。
a. b.
b. c.
c. d.
d.
(1)基态氮原子的轨道表示式是
(2)肼(
 )分子可视为
)分子可视为 分子中的一个氢原子被
分子中的一个氢原子被 (氨基)取代形成的另一种氮的氢化物。
(氨基)取代形成的另一种氮的氢化物。①写出与
 分子互为等电子体的一种离于的化学式
分子互为等电子体的一种离于的化学式②肼(
 )是
)是③肼可用作火箭燃料,燃烧时发生的反应是:
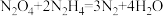
若该反应中有4mol N-H键断裂,则形成的
 键有
键有(3)图1表示某种含氮有机化合物的结构,其分子内4个氮原子分别位于正四面体的4个顶点(见图2),分子内存在空腔,能嵌入某离子或分子并形成4个氢键予以识别。下列分子或离子中,能被该有机化合物识别的是

a.
 b.
b. c.
c. d.
d.
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】铜、锌及其化合物用途广泛。回答下列问题:
(1)Zn2+的价层电子轨道表达式为__ 。
(2)元素第二电离能(I2):Zn_ Cu(填“>”“<”或“=”)。
(3)卤化锌的熔点如表所示:
①ZnCl2、ZnBr2、ZnI2的熔点呈表中变化规律的原因___ 。
②ZnF2的熔点远高于其它三种卤化锌,其原因为___ 。
(4)邻氨基吡啶(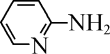 )的铜配合物在有机不对称合成中起催化诱导效应,其结构简式如图所示。
)的铜配合物在有机不对称合成中起催化诱导效应,其结构简式如图所示。

①邻氨基吡啶的铜配合物中,C原子杂化类型为__ 。
②1mol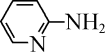 中σ键和π键的数目之比为
中σ键和π键的数目之比为__ 。
(5)铜的晶胞为面心立方(如图所示),已知晶胞参数为a,则该晶胞的空间利用率为__ 。(圆周率为π)。

(1)Zn2+的价层电子轨道表达式为
(2)元素第二电离能(I2):Zn
(3)卤化锌的熔点如表所示:
| ZnF2 | ZnCl2 | ZnBr2 | ZnI2 | |
| 熔点/℃ | 872 | 275 | 394 | 446 |
②ZnF2的熔点远高于其它三种卤化锌,其原因为
(4)邻氨基吡啶(
 )的铜配合物在有机不对称合成中起催化诱导效应,其结构简式如图所示。
)的铜配合物在有机不对称合成中起催化诱导效应,其结构简式如图所示。
①邻氨基吡啶的铜配合物中,C原子杂化类型为
②1mol
 中σ键和π键的数目之比为
中σ键和π键的数目之比为(5)铜的晶胞为面心立方(如图所示),已知晶胞参数为a,则该晶胞的空间利用率为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题:
(1)已知:
分析表中四种物质的相关数据,请回答:
①CH4和SiH4比较,NH3和PH3比较,沸点高低的各自原因是____ 。
②结合上述数据和规律判断,一定压强下HF和HCl的混合气体降温时____ 先液化。
(2)SO2与CO2分子的空间结构分别是____ 和___ ,相同条件下两者在水中的溶解度较大的是___ (写分子式),理由是什么?___ 。
(3)醋酸的球棍模型如图1所示。
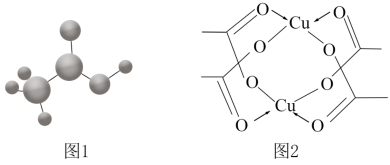
①在醋酸中,碳原子的轨道杂化类型有____ 。
②Cu的水合醋酸盐晶体局部结构如图2所示,该晶体中含有的化学键是___ (填选项字母)。
A.极性键 B.非极性键 C.金属键 D.配位键
(1)已知:
| CH4 | SiH4 | NH3 | PH3 | |
| 沸点/K | 101.7 | 161.2 | 239.7 | 185.4 |
| 分解温度/K | 873 | 773 | 1073 | 713.2 |
分析表中四种物质的相关数据,请回答:
①CH4和SiH4比较,NH3和PH3比较,沸点高低的各自原因是
②结合上述数据和规律判断,一定压强下HF和HCl的混合气体降温时
(2)SO2与CO2分子的空间结构分别是
(3)醋酸的球棍模型如图1所示。

①在醋酸中,碳原子的轨道杂化类型有
②Cu的水合醋酸盐晶体局部结构如图2所示,该晶体中含有的化学键是
A.极性键 B.非极性键 C.金属键 D.配位键
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】钴的合金及其配合物用途非常广泛。已知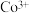 比
比 的氧化性更强,在水溶液中不能大量存在.
的氧化性更强,在水溶液中不能大量存在.
(1)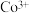 的核外电子排布式为
的核外电子排布式为_____________ 。
(2)无水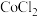 的熔点为
的熔点为 、沸点为
、沸点为 ,
, 熔点为
熔点为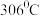 、沸点为
、沸点为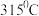 .
.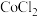 属于
属于_______ 晶体, 属于
属于_____ 晶体。
(3) 可用于激光起爆器等,可由
可用于激光起爆器等,可由 、
、 、
、 共反应制备.
共反应制备.
① 的空间构型为
的空间构型为______________________ 。
② 的化学式为
的化学式为 ,与
,与 (III)形成配位键的原子是
(III)形成配位键的原子是_____
已知 的结构式是
的结构式是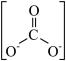
③ 可以
可以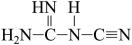 (双聚氰胺)为原料制备,
(双聚氰胺)为原料制备, 双聚氯胺分子中含
双聚氯胺分子中含 键的数目为
键的数目为___________ 。
(4) 与
与 作用可生成
作用可生成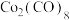 ,其结构如图所示,该分子中
,其结构如图所示,该分子中 原子的杂化方式为
原子的杂化方式为_____________________________ 。

(5)钴酸锂是常见锂电池的电极材料,其晶胞结构如图所示。该晶胞中氧原子的数目为______ 。已知 为阿伏伽德罗常数的数值,则该晶胞的密度为
为阿伏伽德罗常数的数值,则该晶胞的密度为______ (用含 、
、 、
、 的代数式表示)
的代数式表示)
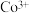 比
比 的氧化性更强,在水溶液中不能大量存在.
的氧化性更强,在水溶液中不能大量存在.(1)
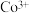 的核外电子排布式为
的核外电子排布式为(2)无水
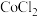 的熔点为
的熔点为 、沸点为
、沸点为 ,
, 熔点为
熔点为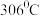 、沸点为
、沸点为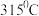 .
.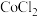 属于
属于 属于
属于(3)
 可用于激光起爆器等,可由
可用于激光起爆器等,可由 、
、 、
、 共反应制备.
共反应制备.①
 的空间构型为
的空间构型为②
 的化学式为
的化学式为 ,与
,与 (III)形成配位键的原子是
(III)形成配位键的原子是已知
 的结构式是
的结构式是
③
 可以
可以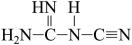 (双聚氰胺)为原料制备,
(双聚氰胺)为原料制备, 双聚氯胺分子中含
双聚氯胺分子中含 键的数目为
键的数目为(4)
 与
与 作用可生成
作用可生成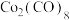 ,其结构如图所示,该分子中
,其结构如图所示,该分子中 原子的杂化方式为
原子的杂化方式为
(5)钴酸锂是常见锂电池的电极材料,其晶胞结构如图所示。该晶胞中氧原子的数目为
 为阿伏伽德罗常数的数值,则该晶胞的密度为
为阿伏伽德罗常数的数值,则该晶胞的密度为 、
、 、
、 的代数式表示)
的代数式表示)
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】铁及其化合物在生活中有广泛应用。
(1)Fe2+基态的外围电子排布式为___ 。
(2)实验室用Fe3+检验苯酚。苯酚分子中碳原子的杂化方式为___ 。
(3)以Fe和BN为原料合成的铁氮化合物在光电子器材领域有广泛应用。
①以氨硼烷(NH3·BH3)为原料可以获得BN。氨硼烷的结构式为___ (配位键用“→”表示),氨硼烷易溶于水,其主要原因是___ 。
②氨气是合成氨硼烷原料之一。NH3属于___ 分子(填“极性”或“非极性”)。
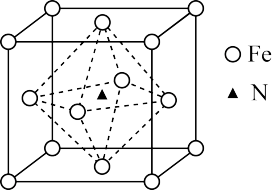
③如图为Fe与N所形成的一种化合物的基本结构单元,该化合物的化学式为___ 。
(1)Fe2+基态的外围电子排布式为
(2)实验室用Fe3+检验苯酚。苯酚分子中碳原子的杂化方式为
(3)以Fe和BN为原料合成的铁氮化合物在光电子器材领域有广泛应用。
①以氨硼烷(NH3·BH3)为原料可以获得BN。氨硼烷的结构式为
②氨气是合成氨硼烷原料之一。NH3属于
③如图为Fe与N所形成的一种化合物的基本结构单元,该化合物的化学式为

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】已知A、B、C、D、E、F都是元素周期表中前四周期的元素,它们的原子序数依次增大。A是宇宙中含量最丰富的元素,B、D原子的L层有2个未成对电子。E3+离子M层3d轨道电子为半满状态,F比E原子序数大1且位于同一族。请根据以上情况,回答下列问题:(答题时,用所对应的元素符号表示)
(1)写出F的价电子排布图_______ ,E位于周期表____ 区。
(2)B、C、D的电负性由小到大的顺序为___________ 。
(3)A、B、D三种元素可以形成组成为A2BD、A4BD、A2BD2的分子,其中B原子采取sp3 杂化的是_______ (填结构简式)
(4)F可形成分子式均为F(NH3)5BrSO4的两种配合物,往其中一种配合物的溶液中加入BaCl2溶液时,无明显现象,若加入AgNO3溶液时产生淡黄色沉淀,则这种配合物的化学式为_______
(5)B元素在自然界有多种同素异形体,硬度最大晶体中每个晶胞平均含有___ 个B原子。
(1)写出F的价电子排布图
(2)B、C、D的电负性由小到大的顺序为
(3)A、B、D三种元素可以形成组成为A2BD、A4BD、A2BD2的分子,其中B原子采取sp3 杂化的是
(4)F可形成分子式均为F(NH3)5BrSO4的两种配合物,往其中一种配合物的溶液中加入BaCl2溶液时,无明显现象,若加入AgNO3溶液时产生淡黄色沉淀,则这种配合物的化学式为
(5)B元素在自然界有多种同素异形体,硬度最大晶体中每个晶胞平均含有
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
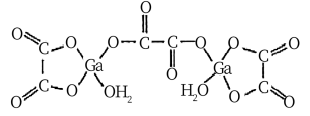
【推荐3】(1)二水合草酸镓的结构如图所示,其中镓原子在周期表中的位置为__________ ,草酸根中碳原子的杂化方式为__________ 。
(2)琥珀酸亚铁片是用于缺铁性贫血的预防和治疗的常见药物,其中“亚铁”是关键成分,K3[Fe(CN)6]溶液是检验 Fe2+的试剂,1mol CN-中含π键的数目为______ ,临床建议服用维生素 C 促进“亚铁”的吸收,避免生成 Fe3+,从原子结构角度来看,Fe2+易被氧化成 Fe3+的原因是___________ 。
(3)化合物(CH3)3N 与盐酸反应生成[(CH3) 3NH]+,该过程新生成的化学键为______ (填序号)
a. 离子键 b. 配位键 c. 氢键 d. 非极性共价键
若化合物(CH3)3N 能溶于水,试解析其原因____________________ 。
(4)Cu2+等过渡元素水合离子是否有颜色与原子结构有关,且存在一定的规律。试推断 Ni2+的水合离子为__________ (填“有”或“无”)色离子,依据是_____________ 。
(5)元素铜与镍的第二电离能分别为:ICu=1959kJ·mol-1、INi=1753kJ·mol-1,ICu>INi的原因是_______ 。

(2)琥珀酸亚铁片是用于缺铁性贫血的预防和治疗的常见药物,其中“亚铁”是关键成分,K3[Fe(CN)6]溶液是检验 Fe2+的试剂,1mol CN-中含π键的数目为
(3)化合物(CH3)3N 与盐酸反应生成[(CH3) 3NH]+,该过程新生成的化学键为
a. 离子键 b. 配位键 c. 氢键 d. 非极性共价键
若化合物(CH3)3N 能溶于水,试解析其原因
(4)Cu2+等过渡元素水合离子是否有颜色与原子结构有关,且存在一定的规律。试推断 Ni2+的水合离子为
| 离子 | Sc3+ | Ti3+ | Fe2+ | Cu2+ | Zn2+ |
| 颜色 | 无色 | 紫红色 | 浅绿色 | 蓝色 | 无色 |
(5)元素铜与镍的第二电离能分别为:ICu=1959kJ·mol-1、INi=1753kJ·mol-1,ICu>INi的原因是
您最近一年使用:0次



