C、H、O、N是四种常见的非金属元素,其单质及化合物在诸多领域中都有广泛的应用。回答下列问题:
(1)基态碳原子的轨道表示式为___________ 。
(2)乙醇分子中碳原子的杂化方式为___________ ,1mol乙醇分子中含有 键的数目为
键的数目为___________ ( 为阿伏加德罗常数的值)。乙醇与水互溶,其原因是乙醇与水分子间形成氢键、
为阿伏加德罗常数的值)。乙醇与水互溶,其原因是乙醇与水分子间形成氢键、___________ 。
(3) 分子的空间构型为
分子的空间构型为___________ , 的键角
的键角___________ (填“>”或“<”) 的键角。
的键角。
(4)丙氨酸(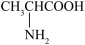 )是蛋白质中含量最高的α型氨基酸,该分子中含
)是蛋白质中含量最高的α型氨基酸,该分子中含___________ 个手性碳原子。
(1)基态碳原子的轨道表示式为
(2)乙醇分子中碳原子的杂化方式为
 键的数目为
键的数目为 为阿伏加德罗常数的值)。乙醇与水互溶,其原因是乙醇与水分子间形成氢键、
为阿伏加德罗常数的值)。乙醇与水互溶,其原因是乙醇与水分子间形成氢键、(3)
 分子的空间构型为
分子的空间构型为 的键角
的键角 的键角。
的键角。(4)丙氨酸(
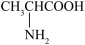 )是蛋白质中含量最高的α型氨基酸,该分子中含
)是蛋白质中含量最高的α型氨基酸,该分子中含
更新时间:2023-04-15 09:15:42
|
相似题推荐
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】硼及其化合物在工农业生产、新型材料等方面应用广泛。回答下列问题:
(1)B的基态原子核外电子排布式为_______ 。
(2)硼、铝同主族,晶体硼的熔点为 ,而金属铝的熔点为
,而金属铝的熔点为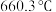 ,试从晶体结构解释其原因:
,试从晶体结构解释其原因:_______ .
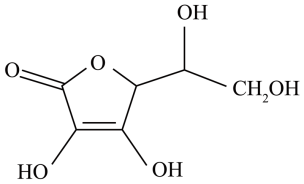
(3)抗坏血酸的分子结构如图所示,分子中碳原子的轨道杂化类型为_______ ;推测抗坏血酸在水中的溶解性:_______ (填“难溶”或“易溶”)于水;抗坏血酸分子中,含有_______ 个手性碳原子。
(4)
已知铁和镁形成的晶胞如图所示:

①图中a处原子坐标参数为_______ 。
②已知该晶胞密度为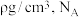 为阿伏加德罗常数的值。该晶胞中
为阿伏加德罗常数的值。该晶胞中 原子与
原子与 原子的最近距离是
原子的最近距离是_______  (用含
(用含 、
、 的代数式表示,
的代数式表示, 的相对原子质量为56,
的相对原子质量为56, 的相对原子质量为24)。
的相对原子质量为24)。
(1)B的基态原子核外电子排布式为
(2)硼、铝同主族,晶体硼的熔点为
 ,而金属铝的熔点为
,而金属铝的熔点为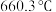 ,试从晶体结构解释其原因:
,试从晶体结构解释其原因:(3)抗坏血酸的分子结构如图所示,分子中碳原子的轨道杂化类型为

(4)
已知铁和镁形成的晶胞如图所示:

①图中a处原子坐标参数为
②已知该晶胞密度为
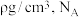 为阿伏加德罗常数的值。该晶胞中
为阿伏加德罗常数的值。该晶胞中 原子与
原子与 原子的最近距离是
原子的最近距离是 (用含
(用含 、
、 的代数式表示,
的代数式表示, 的相对原子质量为56,
的相对原子质量为56, 的相对原子质量为24)。
的相对原子质量为24)。
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
【推荐2】2015年10月,中国科学家屠呦呦因为发现了新型抗疟药——青蒿素,获得了诺贝尔生理学或医学奖,青蒿素的结构简式如图所示,回答下列问题:
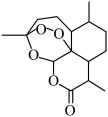
(1)青蒿素属于___________ (填“烃”或“烃的衍生物”)。
(2)青蒿素的分子式为___________ ;青蒿素分子中含有___________ 个手性碳原子。
(3)青蒿素分子中具有的官能团有___________。(填字母)
(4)青蒿素为无色针状晶体,可溶于乙醇、乙醚,在水中几乎不溶,熔点为156~157℃,是高效的抗疟药,高温下不稳定。已知:乙醚的沸点为34.5℃,乙醇的沸点为78℃。
实验室用有机溶剂A提取青蒿素的流程如下图所示。
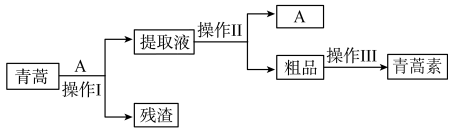
①实验前要对青蒿进行粉碎,其目的是___________ 。
②A是___________ (填“乙醇”或“乙醚”),操作Ⅱ的名称是___________ 。
③操作Ⅲ的主要过程可能是___________ 。(填字母)
A.加水溶解,蒸发浓缩、冷却结晶
B.加95%的乙醇,蒸发浓缩、冷却结晶、过滤
C.加入乙醚进行萃取分液

(1)青蒿素属于
(2)青蒿素的分子式为
(3)青蒿素分子中具有的官能团有___________。(填字母)
| A.羟基 | B.醚键 | C.羧基 | D.酯基 |
实验室用有机溶剂A提取青蒿素的流程如下图所示。

①实验前要对青蒿进行粉碎,其目的是
②A是
③操作Ⅲ的主要过程可能是
A.加水溶解,蒸发浓缩、冷却结晶
B.加95%的乙醇,蒸发浓缩、冷却结晶、过滤
C.加入乙醚进行萃取分液
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
【推荐3】水体中过量的抗生素会对环境造成极大危害,零价铁(Fe)及耦合技术在处理抗生素废水中应用广泛。
I.还原法
零价铁作为一种还原剂可以提供电子,水中的 得电子生成
得电子生成 (氢自由基),
(氢自由基), 通过双键加成、单电子还原与抗生素发生反应。
通过双键加成、单电子还原与抗生素发生反应。
(1)氧化反应:_______ 。
还原反应:(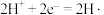 电中性)。
电中性)。
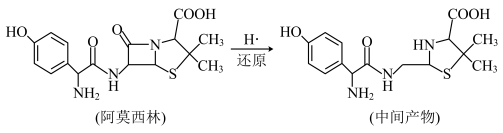
(2) 与阿莫西林(抗生素的一种)发生多步反应,第一步如下图所示,请在图中标出阿莫西林断裂的化学键(参考示例“
与阿莫西林(抗生素的一种)发生多步反应,第一步如下图所示,请在图中标出阿莫西林断裂的化学键(参考示例“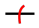 ”),用“O”在中间产物圈出一个手性碳原子
”),用“O”在中间产物圈出一个手性碳原子_______ 。
(3)纳米零价铁5分钟去除甲硝唑接近100%,相同条件下非纳米零价铁去除率约为0%,试解释原因_______ 。
Ⅱ.氧化法
(4)酸性条件Fe可与溶解氧生成 ,
, 和
和 作用生成羟基自由基
作用生成羟基自由基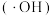 和
和 ,
, 氧化抗生素。
氧化抗生素。 和
和 生成
生成 的离子方程式是
的离子方程式是_______ 。
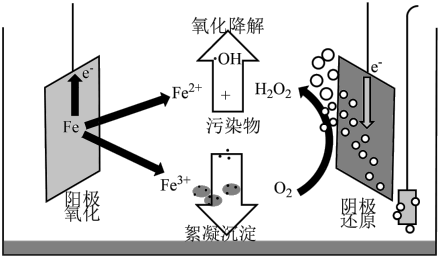
(5)下图为酸性条件零价铁−电芬顿耦合法(电化学氧化法)原理示意图的一部分,左侧连接电源_______ ,结合阴极电极反应说明该法生成 的原理
的原理_______ 。
I.还原法
零价铁作为一种还原剂可以提供电子,水中的
 得电子生成
得电子生成 (氢自由基),
(氢自由基), 通过双键加成、单电子还原与抗生素发生反应。
通过双键加成、单电子还原与抗生素发生反应。(1)氧化反应:
还原反应:(
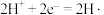 电中性)。
电中性)。(2)
 与阿莫西林(抗生素的一种)发生多步反应,第一步如下图所示,请在图中标出阿莫西林断裂的化学键(参考示例“
与阿莫西林(抗生素的一种)发生多步反应,第一步如下图所示,请在图中标出阿莫西林断裂的化学键(参考示例“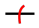 ”),用“O”在中间产物圈出一个手性碳原子
”),用“O”在中间产物圈出一个手性碳原子
(3)纳米零价铁5分钟去除甲硝唑接近100%,相同条件下非纳米零价铁去除率约为0%,试解释原因
Ⅱ.氧化法
(4)酸性条件Fe可与溶解氧生成
 ,
, 和
和 作用生成羟基自由基
作用生成羟基自由基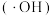 和
和 ,
, 氧化抗生素。
氧化抗生素。 和
和 生成
生成 的离子方程式是
的离子方程式是(5)下图为酸性条件零价铁−电芬顿耦合法(电化学氧化法)原理示意图的一部分,左侧连接电源
 的原理
的原理
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐1】如图是元素周期表的一部分,根据元素在周期表中的位置,回答下列问题:
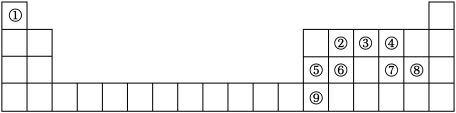
(1)⑤号元素基态原子最高能级的电子占据的原子轨道电子云轮廓为___________ 形。
(2)②③④号元素的第一电离能由大到小的顺序为___________ (用元素符号表示)。
(3)元素①②形成的一种化合物是石油化学工业重要的基本原料,写出该化合物中σ键与π键的数目之比为___________ 。
(4)元素⑦⑧可形成原子个数比为 的共价化合物,分子中各原子最外层均达到8电子的稳定结构,试写出其结构式:
的共价化合物,分子中各原子最外层均达到8电子的稳定结构,试写出其结构式:___________ 。
(5)元素③⑥形成的化合物是一种性质优良的无机非金属材料,具有熔点高,硬度大,电绝缘性好,化学性质稳定等性质,它的晶体类型是___________ 。
(6)元素⑨可形成的卤化物的熔点如表所示:
三种物质的熔点呈现以上规律的原因是___________ 。

(1)⑤号元素基态原子最高能级的电子占据的原子轨道电子云轮廓为
(2)②③④号元素的第一电离能由大到小的顺序为
(3)元素①②形成的一种化合物是石油化学工业重要的基本原料,写出该化合物中σ键与π键的数目之比为
(4)元素⑦⑧可形成原子个数比为
 的共价化合物,分子中各原子最外层均达到8电子的稳定结构,试写出其结构式:
的共价化合物,分子中各原子最外层均达到8电子的稳定结构,试写出其结构式:(5)元素③⑥形成的化合物是一种性质优良的无机非金属材料,具有熔点高,硬度大,电绝缘性好,化学性质稳定等性质,它的晶体类型是
(6)元素⑨可形成的卤化物的熔点如表所示:
| 卤化物 | 氟化物 | 氯化物 | 溴化物 |
| 熔点/℃ | 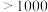 | 77.75 | 122.3 |
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】2019年的化学诺贝尔奖颁给了为锂电池研究作出贡献的三位科学家,其研究的是两种常见锂电池:一种是采用镍钴锰酸锂Li(NiCoMn)O2或镍钴铝酸锂为正极的“三元材料锂电池”;另一种是采用磷酸铁锂(LiFePO4)为正极的电池。请回答下列问题:
(1)Mn位于元素周期表的_______ 区(填“s”或“p”或“d”或“ds”或“f”),基态钴原子的未成对电子数为_______ ,1mol [CoCl (NH3)5] Cl2 中含σ键数目为_______ NA。
(2)磷元素的最高价氧化物的水化物H3PO4在工业上有诸多特殊的用途,其中PO 的空间构型是
的空间构型是_______ ,中心原子的杂化方式是_______ 。
(3)PH3是_______ 分子(填“极性”或“非极性”),其在水中的溶解性比NH3小,原因是_______ 。
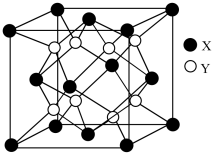
(4)硫化锂Li2S(摩尔质量M g∙mol-1)的纳米晶体是开发先进锂电池的关键材料,硫化锂的晶体为反萤石结构,其晶胞结构如图。若硫化锂晶体的密度为ρ g·cm-3,则距离最近的两个S2-的距离是_______ cm。(用含ρ、M、NA的计算式表示)
(1)Mn位于元素周期表的
(2)磷元素的最高价氧化物的水化物H3PO4在工业上有诸多特殊的用途,其中PO
 的空间构型是
的空间构型是(3)PH3是
(4)硫化锂Li2S(摩尔质量M g∙mol-1)的纳米晶体是开发先进锂电池的关键材料,硫化锂的晶体为反萤石结构,其晶胞结构如图。若硫化锂晶体的密度为ρ g·cm-3,则距离最近的两个S2-的距离是

您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐3】前四周期元素X、Y、Z、W核电荷数依次增大,核电荷数之和为58;Y原子的M层p轨道有3个未成对电子;Z与Y同周期,且在该周期中电负性最大;W原子的L层电子数与最外层电子数之比为4:1,其d轨道中的电子数与最外层电子数之比为5:2。
(1)写出Z元素在元素周期表中的位置:___________ 。
(2) 与X形成共价化合物A,Z与X形成共价化合物B,A与B还原性较强的是
与X形成共价化合物A,Z与X形成共价化合物B,A与B还原性较强的是___________  写分子式
写分子式 。
。
(3) 的最高价氧化物的水化物的化学式为
的最高价氧化物的水化物的化学式为___________ ;
(4) 单质
单质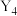 与
与 在一定条件下恰好完全反应生成
在一定条件下恰好完全反应生成 化合物C,一个C分子中所含有的σ键数目为
化合物C,一个C分子中所含有的σ键数目为___________ ;
(5)含W元素的最高化合价的含氧酸根离子是___________ ,该含氧酸根离子在分析化学中有重要作用,在酸性条件下该含氧酸根离子可将 氧化成
氧化成 ,请写出该反应的离子方程式
,请写出该反应的离子方程式___________ 。
(1)写出Z元素在元素周期表中的位置:
(2)
 与X形成共价化合物A,Z与X形成共价化合物B,A与B还原性较强的是
与X形成共价化合物A,Z与X形成共价化合物B,A与B还原性较强的是 写分子式
写分子式 。
。(3)
 的最高价氧化物的水化物的化学式为
的最高价氧化物的水化物的化学式为(4)
 单质
单质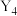 与
与 在一定条件下恰好完全反应生成
在一定条件下恰好完全反应生成 化合物C,一个C分子中所含有的σ键数目为
化合物C,一个C分子中所含有的σ键数目为(5)含W元素的最高化合价的含氧酸根离子是
 氧化成
氧化成 ,请写出该反应的离子方程式
,请写出该反应的离子方程式
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】VIA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种氧化态,含VIA族元素的化合物在研究和生产中有许多重要用途。请回答下列问题:
(1)S单质的常见形式为S8,其环状结构如图所示,S原子采用的轨道杂化方式是___ ;

(2)Se原子的原子序数为___ ,基态电子的排布式为[Ar]___ ;
(3)H2Se的稳定性比H2S___ (填“强”或“弱”)。SeO3分子的立体构型为___ 。
(4)下列分子中含手性碳的是___ 。
a. b.
b.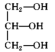 c.
c. d.CH3CHClCH2CHO
d.CH3CHClCH2CHO
(5)元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(E1)。第二周期部分元素的E1变化趋势如图(a)所示,其中除氮元素外,其他元素的E1自左而右依次增大的原因___ ;氮元素的E1呈现异常的原因是___ 。

(1)S单质的常见形式为S8,其环状结构如图所示,S原子采用的轨道杂化方式是

(2)Se原子的原子序数为
(3)H2Se的稳定性比H2S
(4)下列分子中含手性碳的是
a.
 b.
b. c.
c. d.CH3CHClCH2CHO
d.CH3CHClCH2CHO(5)元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(E1)。第二周期部分元素的E1变化趋势如图(a)所示,其中除氮元素外,其他元素的E1自左而右依次增大的原因

您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】A、B、C、D、E、F、G、W是原子序数依次增大的8种元素,A元素原子的2p原子轨道上有2个未成对的电子,B元素在同周期中原子半径最大,与A可形成原子个数比为1:1和2:1的两种化合物,C单质是一种常见的半导体材料,F有9个原子轨道,且只有一个未成对电子,没有空轨道,G的单质是一种常见金属,其+2价离子G2+有4个未成对电子,W能形成红色(或砖红色)的W2A和黑色的WA两种化合物。
(1)C元素在元素周期表中的位置___________ ,W位于元素周期表___________ 区,W的简化电子排布式___________ 。
(2)EF2中心原子杂化轨道类型___________ ,EA 的VSEPR模型
的VSEPR模型___________ ,EA 的空间构型
的空间构型___________ 。
(3)D、E、F三元素第一电离能从大到小的顺序是___________ (用元素符号及“ ”表示)。
”表示)。
(4)A、B、C、D四元素电负性由大到小顺序___________ (用元素符号及“ ”表示)。
”表示)。
(5)G3+比G2+稳定,原因是___________ 。
(1)C元素在元素周期表中的位置
(2)EF2中心原子杂化轨道类型
 的VSEPR模型
的VSEPR模型 的空间构型
的空间构型(3)D、E、F三元素第一电离能从大到小的顺序是
 ”表示)。
”表示)。(4)A、B、C、D四元素电负性由大到小顺序
 ”表示)。
”表示)。(5)G3+比G2+稳定,原因是
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐3】磷酸亚铁锂电池是新能源汽车的动力电池之一,采用湿法治金工艺回收处理废旧电池正极片(主要成分:LiFePO4、石墨、铝箔等),其流程如下:

已知:Li2CO3 为无色晶体,熔点 618℃,溶于硫酸,在水中的溶解度随温度升高而减小。
(1) 的空间构型为
的空间构型为_____ 。
(2)“碱浸”时主要发生反应的离子方程式为_____ ,为加快浸出速率, 除可以适当加热外,还可以采取的措施有_____ (至少答出两点)。
(3)“氧化浸出”时,当其他条件相同,选用不同的氧化剂,测得滤液 b 中Li+含量如下:
实际工业生产中氧化剂选用的是H2O2,请分析不能选用NaClO3的理由是_____ (用离子方程式回答),该步操作加热温度不宜过高的原因是_____ 。
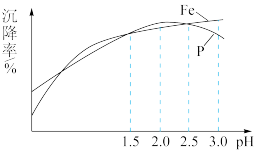
(4)“滤液b”中主要含有Li+、Fe3+、 及 Cl-等,在一定条件下,溶液 pH与 FePO4沉降率关系如图所示,综合考虑 Fe、P 两种元素沉降率,“沉降除杂”时选择的最佳 pH为
及 Cl-等,在一定条件下,溶液 pH与 FePO4沉降率关系如图所示,综合考虑 Fe、P 两种元素沉降率,“沉降除杂”时选择的最佳 pH为_____ (从 1.5、2.0、2.5 及 3.0 中选择)。
(5)最后一步“一系列操作”包括_____ 、洗涤、干燥。

已知:Li2CO3 为无色晶体,熔点 618℃,溶于硫酸,在水中的溶解度随温度升高而减小。
(1)
 的空间构型为
的空间构型为(2)“碱浸”时主要发生反应的离子方程式为
(3)“氧化浸出”时,当其他条件相同,选用不同的氧化剂,测得滤液 b 中Li+含量如下:
| 氧化剂 | NaClO3 | H2O2 | NaClO | O2 |
| Li+含量(g/L) | 9.55 | 8.92 | 8.75 | 7.05 |
实际工业生产中氧化剂选用的是H2O2,请分析不能选用NaClO3的理由是
(4)“滤液b”中主要含有Li+、Fe3+、
 及 Cl-等,在一定条件下,溶液 pH与 FePO4沉降率关系如图所示,综合考虑 Fe、P 两种元素沉降率,“沉降除杂”时选择的最佳 pH为
及 Cl-等,在一定条件下,溶液 pH与 FePO4沉降率关系如图所示,综合考虑 Fe、P 两种元素沉降率,“沉降除杂”时选择的最佳 pH为
(5)最后一步“一系列操作”包括
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐1】短周期元素A、D、E、F、W原子序数依次递增,已知:
①D元素的某种同位素通常用于地质年代的鉴定;
②F元素电负性在周期表所有元素中位列第二;
③W的各级电离能如图。
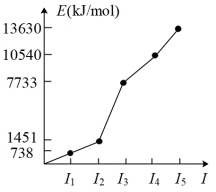
请回答:
(1)D、E、F三元素的第一电离能由大到小的顺序是___________ (用元素符号表示)。
(2)写出一种由上述元素形成氢键的表达式___________ 。
(3)元素W在周期表中的位置是___________ 。
①D元素的某种同位素通常用于地质年代的鉴定;
②F元素电负性在周期表所有元素中位列第二;
③W的各级电离能如图。

请回答:
(1)D、E、F三元素的第一电离能由大到小的顺序是
(2)写出一种由上述元素形成氢键的表达式
(3)元素W在周期表中的位置是
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】铁和硫及其化合物在日常生产、生活中有着广泛的应用。回答下列问题:
(1)基态 的价电子排布图为
的价电子排布图为______ 。
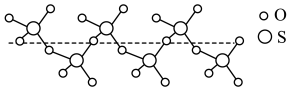
(2)某种硫的氧化物冷却到289.8K时凝固得到一种螺旋状单链结构的固体,其结构片段如图所示,从该结构片段分析可知该物质的化学式为______ ,两种原子的第一电离能大小关系是______ 。
(3)有机铁肥三硝酸六尿素合铁(Ⅲ)的化学式为 。尿素分子中C原子的杂化方式是
。尿素分子中C原子的杂化方式是______ , 中“
中“ ”与
”与 (Ⅲ)之间的作用力是
(Ⅲ)之间的作用力是______ ,根据价层电子对互斥理论推测 的空间构型为
的空间构型为____________ 。
(4) 可用
可用 检验,
检验, 对应的酸有两种,分别为硫氰酸
对应的酸有两种,分别为硫氰酸 和异硫氰酸
和异硫氰酸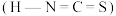 ,这两种酸中沸点较高的是
,这两种酸中沸点较高的是______ ,原因是_________________________________________ 。
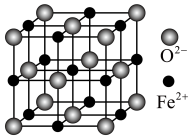
(5)立方 晶体的晶胞结构如图所示,其晶胞边长为
晶体的晶胞结构如图所示,其晶胞边长为 ,列式表示
,列式表示 晶体的密度:
晶体的密度:______  (用含
(用含 的代数式表示,阿伏加德罗常数的值为
的代数式表示,阿伏加德罗常数的值为 )。
)。
(1)基态
 的价电子排布图为
的价电子排布图为(2)某种硫的氧化物冷却到289.8K时凝固得到一种螺旋状单链结构的固体,其结构片段如图所示,从该结构片段分析可知该物质的化学式为

(3)有机铁肥三硝酸六尿素合铁(Ⅲ)的化学式为
 。尿素分子中C原子的杂化方式是
。尿素分子中C原子的杂化方式是 中“
中“ ”与
”与 (Ⅲ)之间的作用力是
(Ⅲ)之间的作用力是 的空间构型为
的空间构型为(4)
 可用
可用 检验,
检验, 对应的酸有两种,分别为硫氰酸
对应的酸有两种,分别为硫氰酸 和异硫氰酸
和异硫氰酸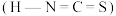 ,这两种酸中沸点较高的是
,这两种酸中沸点较高的是(5)立方
 晶体的晶胞结构如图所示,其晶胞边长为
晶体的晶胞结构如图所示,其晶胞边长为 ,列式表示
,列式表示 晶体的密度:
晶体的密度: (用含
(用含 的代数式表示,阿伏加德罗常数的值为
的代数式表示,阿伏加德罗常数的值为 )。
)。
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】回答下列问题:
(1)现有三种有机物 丙烷、
丙烷、 二甲醚
二甲醚 和
和 乙醇
乙醇 ,沸点数据如下
,沸点数据如下
(i)乙醇沸点高于二甲醚的原因是___________
(ii)二甲醚沸点高于丙烷的原因是___________
(2) 本草衍义
本草衍义 中对精制砒霜
中对精制砒霜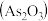 过程有如下叙述:“取砒之法,将生砒就置火上,以器覆之,令砒盐上飞着覆器,遂凝结累然下垂如乳尖,长者为胜,平短者次之。”
过程有如下叙述:“取砒之法,将生砒就置火上,以器覆之,令砒盐上飞着覆器,遂凝结累然下垂如乳尖,长者为胜,平短者次之。”
(i)文中涉及的操作方法是______
A.蒸馏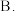 升华
升华  干馏
干馏 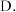 萃取
萃取 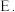 精馏
精馏  重结晶
重结晶
(ii)由以上工艺,砒霜最可能的晶体类型是______
A.原子晶体 分子晶体
分子晶体  离子晶体
离子晶体  金属晶体
金属晶体  混合晶体
混合晶体
(iii)砒霜是剧毒物质,法庭医学分析上常用马氏试砷法来证明是否砒霜中毒:把试样与锌和硫酸混和,若试样中含有砒霜,则生成砷化氢气体,反应的化学方程式为___________ 。
(1)现有三种有机物
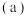 丙烷、
丙烷、 二甲醚
二甲醚 和
和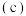 乙醇
乙醇 ,沸点数据如下
,沸点数据如下| 沸点 | 78℃ | -23℃ | -42.09℃ |
| 物质 | CH3CH2OH | H3COCH3 | CH3CH2CH3 |
(ii)二甲醚沸点高于丙烷的原因是
(2)
 本草衍义
本草衍义 中对精制砒霜
中对精制砒霜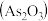 过程有如下叙述:“取砒之法,将生砒就置火上,以器覆之,令砒盐上飞着覆器,遂凝结累然下垂如乳尖,长者为胜,平短者次之。”
过程有如下叙述:“取砒之法,将生砒就置火上,以器覆之,令砒盐上飞着覆器,遂凝结累然下垂如乳尖,长者为胜,平短者次之。”(i)文中涉及的操作方法是
A.蒸馏
 升华
升华  干馏
干馏  萃取
萃取  精馏
精馏  重结晶
重结晶(ii)由以上工艺,砒霜最可能的晶体类型是
A.原子晶体
 分子晶体
分子晶体  离子晶体
离子晶体  金属晶体
金属晶体  混合晶体
混合晶体(iii)砒霜是剧毒物质,法庭医学分析上常用马氏试砷法来证明是否砒霜中毒:把试样与锌和硫酸混和,若试样中含有砒霜,则生成砷化氢气体,反应的化学方程式为
您最近一年使用:0次



