自然界中的氮元素以氮气、氮氧化物和硝酸盐等形式存在,人类对氮元素的利用,就是实现氮元素在不同物质之间的转化。
(1)下列有关物质的性质与用途具有对应关系的是_______。
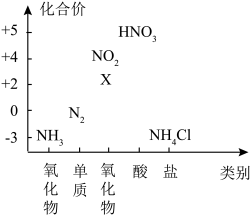
(2)下图为氮元素的价类二维图。下列说法正确的是_______。
(3)为了测定铁铜合金的组成,将15.2 g铁、铜合金加入200 mL某浓度的稀硝酸中,待合金完全溶解后,共收集到NO气体4.48 L(标准状况下),并测得反应后溶液中 的浓度为0.5 mol•L
的浓度为0.5 mol•L ,若反应前后溶液的体积变化忽略不计,则下列判断正确的是_______。
,若反应前后溶液的体积变化忽略不计,则下列判断正确的是_______。
(4)浓、稀硝酸的性质既相似又有差别,若要除去铁制品表面的铜镀层应选择_____ (填“浓”或“稀”)硝酸,原因是_______ 。
(5)①氨气是生产氮肥的主要原料,其电子式为_______ 。
②工业合成氨的化学方程式为_______ 。
③检验铵态氮肥中 的实验方案是
的实验方案是_______ 。
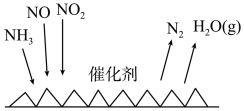
(6) 催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如下图所示。当
催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如下图所示。当 与NO的物质的量之比为1∶1时与足量氨气在一定条件下发生脱氮反应。该反应的化学方程式为
与NO的物质的量之比为1∶1时与足量氨气在一定条件下发生脱氮反应。该反应的化学方程式为_______ 。
(1)下列有关物质的性质与用途具有对应关系的是_______。
A. 易溶于水,可用作制冷剂 易溶于水,可用作制冷剂 | B. 具有强氧化性,可用于制 具有强氧化性,可用于制 |
C. 受热易分解,可用作化肥 受热易分解,可用作化肥 | D. 性质稳定,可用于食品保护 性质稳定,可用于食品保护 |

| A.X属于酸性氧化物 |
B. 转化为 转化为 一定需要加入氧化剂 一定需要加入氧化剂 |
C.一定条件下, 和 和 反应可以转化成 反应可以转化成 |
D.实验室采用加热分解 固体制取 固体制取 |
 的浓度为0.5 mol•L
的浓度为0.5 mol•L ,若反应前后溶液的体积变化忽略不计,则下列判断正确的是_______。
,若反应前后溶液的体积变化忽略不计,则下列判断正确的是_______。A.反应后溶液中可能存在的金属阳离子有: 、 、 和 和 |
B.上述合金中铁与铜物质的量之比为 |
| C.反应后的溶液中可继续溶解铁铜合金质量最多为1.9 g |
D.原硝酸的物质的量浓度为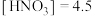 mol⋅L-1 mol⋅L-1 |
(5)①氨气是生产氮肥的主要原料,其电子式为
②工业合成氨的化学方程式为
③检验铵态氮肥中
 的实验方案是
的实验方案是(6)
 催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如下图所示。当
催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如下图所示。当 与NO的物质的量之比为1∶1时与足量氨气在一定条件下发生脱氮反应。该反应的化学方程式为
与NO的物质的量之比为1∶1时与足量氨气在一定条件下发生脱氮反应。该反应的化学方程式为
更新时间:2023-04-24 00:12:34
|
相似题推荐
【推荐1】下列四个反应
①2Na+2H2O=2NaOH+H2↑ ②2F2+2H2O=4HF+O2
③Cl2+H2O=HCl+HClO ④C+H2O(g) CO+H2
CO+H2
试从氧化还原的角度,回答下列问题:
(1)水只作还原剂的是__________________ (填序号)
(2)二氧化氯(ClO2)是一种在水处理方面有广泛应用的高效安全消毒剂,而且不会产生对人体有潜在危害的物质。工业上可以用如下方法制备ClO2:2NaClO3+H2O2+H2SO4=2ClO2↑+O2↑+Na2SO4+2H2O。反应中氧化剂是____________ ,生成1.25mol氧化产物共转移电子_________ mol。写出该反应的离子方程式_____________ 。
①2Na+2H2O=2NaOH+H2↑ ②2F2+2H2O=4HF+O2
③Cl2+H2O=HCl+HClO ④C+H2O(g)
 CO+H2
CO+H2试从氧化还原的角度,回答下列问题:
(1)水只作还原剂的是
(2)二氧化氯(ClO2)是一种在水处理方面有广泛应用的高效安全消毒剂,而且不会产生对人体有潜在危害的物质。工业上可以用如下方法制备ClO2:2NaClO3+H2O2+H2SO4=2ClO2↑+O2↑+Na2SO4+2H2O。反应中氧化剂是
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】大气污染物主要成分是SO2、NO2、NO、CO及可吸入颗粒等,主要来自于燃煤、机动车尾气和工业废气,会导致雾霾、酸雨等。
(1)大气污染物成分中属于酸性氧化物的是___ (填化学式)。
(2)工业上可以用NaOH溶液或氨水吸收污染物SO2,写出用氢氧化钠吸收过量SO2的离子方程式:___ 。
(3)汽车的三元催化转化器中,在催化剂作用下NO和CO转化为无毒气体,反应的化学方程式是:2CO+2NO 2CO2+N2。
2CO2+N2。
①该反应中,氧化剂是___ (填化学式),氧化产物是___ (填化学式)。
②当生成2molN2时,转移电子的物质的量是___ 。
(4)NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术,生成的产物都无毒。NH3还原NO2时,还原剂和氧化剂的物质的量之比是___ 。
(5)SO2通过下列过程既能制得H2SO4又能制得H2。
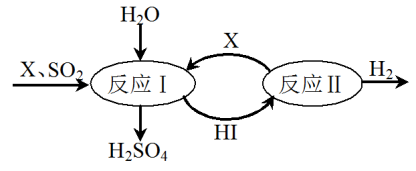
①可循环利用的物质是___ (填化学式)。
②制得H2SO4的化学方程式是___ 。
③制得H2的化学方程式是___ 。
(1)大气污染物成分中属于酸性氧化物的是
(2)工业上可以用NaOH溶液或氨水吸收污染物SO2,写出用氢氧化钠吸收过量SO2的离子方程式:
(3)汽车的三元催化转化器中,在催化剂作用下NO和CO转化为无毒气体,反应的化学方程式是:2CO+2NO
 2CO2+N2。
2CO2+N2。①该反应中,氧化剂是
②当生成2molN2时,转移电子的物质的量是
(4)NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术,生成的产物都无毒。NH3还原NO2时,还原剂和氧化剂的物质的量之比是
(5)SO2通过下列过程既能制得H2SO4又能制得H2。

①可循环利用的物质是
②制得H2SO4的化学方程式是
③制得H2的化学方程式是
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】2022年1月,南太平洋岛国汤加境内发生了“21世纪至今最剧烈的火山喷发”,科学家对喷发出的火山灰及气体进行分析测定,发现含有下列物质:①S ②SO2 ③CH4 ④SiO2 ⑤Fe3O4 ⑥MgCl2 ⑦CO ⑧Al2O3 ⑨CO2 ⑩H2SO4。
(1)上述物质中属于金属氧化物的是_______ (填序号,下同),属于酸性氧化物的是_______ ,属于非电解质的物质是_______ 。
(2)⑩的稀溶液能与①~⑨中的某些物质反应,请写出相应的离子反应方程式_______ 。
(3)16g S先转变成SO2,再转变成H2SO4,转移的电子数是_______ 。
(1)上述物质中属于金属氧化物的是
(2)⑩的稀溶液能与①~⑨中的某些物质反应,请写出相应的离子反应方程式
(3)16g S先转变成SO2,再转变成H2SO4,转移的电子数是
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题:
(1)生铁中含有一种铁碳化合物X(Fe3C)。X在足量的空气中高温煅烧,生成有磁性的固体Y,将Y溶于过量盐酸后,溶液中大量存在的阳离子有_______ (填离子符号)。
(2)某透明溶液仅含Na+、Fe2+、Ba2+、Al3+、 、Cl-、
、Cl-、 中的4种离子,且均为1mol。向该溶液中加入过量的稀硫酸,有气泡产生,且溶液中阴离子种类不变(不考虑水的电离和离子的水解)。则溶液中存在的离子是
中的4种离子,且均为1mol。向该溶液中加入过量的稀硫酸,有气泡产生,且溶液中阴离子种类不变(不考虑水的电离和离子的水解)。则溶液中存在的离子是_______ 。
(3)高铁酸钾 是一种既能杀菌消海、又能絮凝净水的水处理剂。其工业制备反应为
是一种既能杀菌消海、又能絮凝净水的水处理剂。其工业制备反应为 (未配平),每生成
(未配平),每生成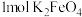 ,转移的电子数为
,转移的电子数为_______ 。
(4)自然界中Cr主要以 价和
价和 价形式存在。
价形式存在。 中的Cr能引起细胞的突变,在酸性条件下可用亚硫酸钠将
中的Cr能引起细胞的突变,在酸性条件下可用亚硫酸钠将 还原。其离子方程式为
还原。其离子方程式为_______ 。
(1)生铁中含有一种铁碳化合物X(Fe3C)。X在足量的空气中高温煅烧,生成有磁性的固体Y,将Y溶于过量盐酸后,溶液中大量存在的阳离子有
(2)某透明溶液仅含Na+、Fe2+、Ba2+、Al3+、
 、Cl-、
、Cl-、 中的4种离子,且均为1mol。向该溶液中加入过量的稀硫酸,有气泡产生,且溶液中阴离子种类不变(不考虑水的电离和离子的水解)。则溶液中存在的离子是
中的4种离子,且均为1mol。向该溶液中加入过量的稀硫酸,有气泡产生,且溶液中阴离子种类不变(不考虑水的电离和离子的水解)。则溶液中存在的离子是(3)高铁酸钾
 是一种既能杀菌消海、又能絮凝净水的水处理剂。其工业制备反应为
是一种既能杀菌消海、又能絮凝净水的水处理剂。其工业制备反应为 (未配平),每生成
(未配平),每生成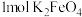 ,转移的电子数为
,转移的电子数为(4)自然界中Cr主要以
 价和
价和 价形式存在。
价形式存在。 中的Cr能引起细胞的突变,在酸性条件下可用亚硫酸钠将
中的Cr能引起细胞的突变,在酸性条件下可用亚硫酸钠将 还原。其离子方程式为
还原。其离子方程式为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
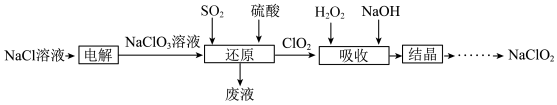
【推荐2】NaClO2是一种重要的含氯消毒剂,也常用来漂白织物等,其一种生产工艺如下图。
(1)NaClO2中氯元素的化合价是___________ 。
(2)“电解”时,所用的食盐水可由粗盐水精制而成。精制食盐时,需除去粗盐中的Ca2+、Mg2+,加入的试剂分别为___________ 、___________ (填化学式)。
(3)“还原”中,发生反应的离子方程式为___________ 。
(4)“废液”中的主要溶质是___________ (填化学式)。
(5)“吸收”反应中,氧化剂和还原剂的物质的量之比为___________ ,该反应中氧
化产物为___________ 。
(1)NaClO2中氯元素的化合价是
(2)“电解”时,所用的食盐水可由粗盐水精制而成。精制食盐时,需除去粗盐中的Ca2+、Mg2+,加入的试剂分别为
(3)“还原”中,发生反应的离子方程式为
(4)“废液”中的主要溶质是
(5)“吸收”反应中,氧化剂和还原剂的物质的量之比为
化产物为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】已知下列物质甲、乙、丙、丁分别由H、C、Na、O、Cl、Fe元素中的一种或几种组成。按要求填空。
(1)若甲物质为酸性氧化物,且固体甲可人工降雨。则甲的化学式为_____ (写一种),甲与足量的澄清石灰水反应的离子方程式__________ 。
(2)若乙物质是非电解质,且乙可做医用消毒剂。则乙的化学式为________ ,1分子的乙完全燃烧,转移电子数目为_______ 个
(3)实验室可用丙的饱和溶液制备Fe(OH)3(胶体),则丙的化学式为_______ ,胶体区别于其他分散系的本质特征是______ ,区分溶液和胶体的方法是________ 。
(4)酸性高锰酸钾溶液具有强氧化性,某反应中参加反应的离子为 、H+和一种未知离子。产物为Fe3+、Mn2+和H2O.该反应的离子方程式为
、H+和一种未知离子。产物为Fe3+、Mn2+和H2O.该反应的离子方程式为________ 。
(1)若甲物质为酸性氧化物,且固体甲可人工降雨。则甲的化学式为
(2)若乙物质是非电解质,且乙可做医用消毒剂。则乙的化学式为
(3)实验室可用丙的饱和溶液制备Fe(OH)3(胶体),则丙的化学式为
(4)酸性高锰酸钾溶液具有强氧化性,某反应中参加反应的离子为
 、H+和一种未知离子。产物为Fe3+、Mn2+和H2O.该反应的离子方程式为
、H+和一种未知离子。产物为Fe3+、Mn2+和H2O.该反应的离子方程式为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】氮元素的单质和常见化合物在工、农业生产中用途广泛。
(1)氮气的化学性质很稳定,可用作灯泡填充气。解释其原因是___________ 。
(2)___________ 实验证明氨气极易溶于水。通常用___________ (填名称)干燥氨气。
(3)铵盐大多在农业上用作化肥,固体 与固体
与固体 加热反应可生成氨气,其化学方程式为
加热反应可生成氨气,其化学方程式为___________ 。
(4)硝酸是一种重要的含氮酸,书写铜和稀硝酸反应的离子方程式___________ 。
(5)如图为合成氨以及氨氧化制硝酸的流程示意图。
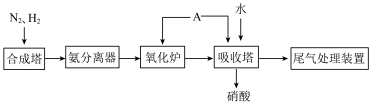
①写出合成塔中的化学反应方程式___________ 。向氧化炉和吸收塔中通入的A是___________ 。
②工业制硝酸的尾气是酸性气体,为防止环境污染,可以用___________ (填化学式)溶液吸收。
(1)氮气的化学性质很稳定,可用作灯泡填充气。解释其原因是
(2)
(3)铵盐大多在农业上用作化肥,固体
 与固体
与固体 加热反应可生成氨气,其化学方程式为
加热反应可生成氨气,其化学方程式为(4)硝酸是一种重要的含氮酸,书写铜和稀硝酸反应的离子方程式
(5)如图为合成氨以及氨氧化制硝酸的流程示意图。

①写出合成塔中的化学反应方程式
②工业制硝酸的尾气是酸性气体,为防止环境污染,可以用
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】硝酸是一种具有强氧化性、腐蚀性的强酸,其还原产物因硝酸浓度的不同而有变化,从总体上说,硝酸浓度越高,平均每分子硝酸得到的电子数越少,浓硝酸的还原产物主要为 、稀硝酸的还原产物为
、稀硝酸的还原产物为 。实验室中,常用
。实验室中,常用 与浓
与浓 反应制取
反应制取 ,用
,用 与稀
与稀 反应制取
反应制取 。
。
(1)浓硝酸具有以下性质:①强氧化性②酸性③还原性④不稳定性⑤挥发性,下列反应或者现象主要体现了硝酸的什么性质:
①久置浓硝酸显黄色___________ (填序号,下同),请写出反应的化学方程式___________ 。
②用稀硝酸清洗试管壁上的银___________ 。
(2) 与适量的浓
与适量的浓 反应,铜全部作用后,共收集到
反应,铜全部作用后,共收集到 气体(标准状况下),反应中消耗的
气体(标准状况下),反应中消耗的 的物质的量是___________(填字母代号)。
的物质的量是___________(填字母代号)。
(3)硝酸的还原产物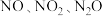 等对环境均有副作用,为了可持续发展,当今社会提出的一个新概念:“绿色化学”,它要求从经济、环保和技术上设计可行的化学反应,则下列由单质钢制取硝酸铜的方法可行且符合“绿色化学”的是_______ (填字母代号)。
等对环境均有副作用,为了可持续发展,当今社会提出的一个新概念:“绿色化学”,它要求从经济、环保和技术上设计可行的化学反应,则下列由单质钢制取硝酸铜的方法可行且符合“绿色化学”的是_______ (填字母代号)。
(4)实际上硝酸不仅可被还原为 或
或 ,浓度更稀时硝酸还可以被还原为
,浓度更稀时硝酸还可以被还原为 等,锌与很稀的硝酸反应生成硝酸锌、硝酸铵和水,写出该反应的化学方程式
等,锌与很稀的硝酸反应生成硝酸锌、硝酸铵和水,写出该反应的化学方程式___________ ,当生成 硝酸锌时,被还原的硝酸的物质的量为
硝酸锌时,被还原的硝酸的物质的量为___________ 。
(5)汽车彻底改变了我们生活,成为我们的不可成缺的交通工具之一,汽车尾气系统中的催化转化器,可有效降低尾气中的 和
和 等向大气的排放,在催化转化器的前半部发生的反应为
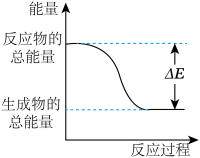
等向大气的排放,在催化转化器的前半部发生的反应为 ,已知汽车尾气处理反应能量过程如下图,下列说法正确的是___________。
,已知汽车尾气处理反应能量过程如下图,下列说法正确的是___________。
 、稀硝酸的还原产物为
、稀硝酸的还原产物为 。实验室中,常用
。实验室中,常用 与浓
与浓 反应制取
反应制取 ,用
,用 与稀
与稀 反应制取
反应制取 。
。(1)浓硝酸具有以下性质:①强氧化性②酸性③还原性④不稳定性⑤挥发性,下列反应或者现象主要体现了硝酸的什么性质:
①久置浓硝酸显黄色
②用稀硝酸清洗试管壁上的银
(2)
 与适量的浓
与适量的浓 反应,铜全部作用后,共收集到
反应,铜全部作用后,共收集到 气体(标准状况下),反应中消耗的
气体(标准状况下),反应中消耗的 的物质的量是___________(填字母代号)。
的物质的量是___________(填字母代号)。A. | B. | C. | D. |
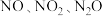 等对环境均有副作用,为了可持续发展,当今社会提出的一个新概念:“绿色化学”,它要求从经济、环保和技术上设计可行的化学反应,则下列由单质钢制取硝酸铜的方法可行且符合“绿色化学”的是_______ (填字母代号)。
等对环境均有副作用,为了可持续发展,当今社会提出的一个新概念:“绿色化学”,它要求从经济、环保和技术上设计可行的化学反应,则下列由单质钢制取硝酸铜的方法可行且符合“绿色化学”的是_______ (填字母代号)。A.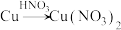 |
B. |
C.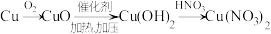 |
D.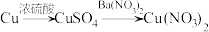 |
 或
或 ,浓度更稀时硝酸还可以被还原为
,浓度更稀时硝酸还可以被还原为 等,锌与很稀的硝酸反应生成硝酸锌、硝酸铵和水,写出该反应的化学方程式
等,锌与很稀的硝酸反应生成硝酸锌、硝酸铵和水,写出该反应的化学方程式 硝酸锌时,被还原的硝酸的物质的量为
硝酸锌时,被还原的硝酸的物质的量为(5)汽车彻底改变了我们生活,成为我们的不可成缺的交通工具之一,汽车尾气系统中的催化转化器,可有效降低尾气中的
 和
和 等向大气的排放,在催化转化器的前半部发生的反应为
等向大气的排放,在催化转化器的前半部发生的反应为 ,已知汽车尾气处理反应能量过程如下图,下列说法正确的是___________。
,已知汽车尾气处理反应能量过程如下图,下列说法正确的是___________。
| A.该反应为放热反应 | B.该反应为吸热反应 |
C.形成 化学键需要吸收热量 化学键需要吸收热量 | D.反应物的总能量小于生成物的总能量 |
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】氮元素在地球上含量丰富,是构成生命体的基本元素之一。回答下列问题:
(1)下列变化中,属于固氮的是_______ (填字母)。
A.豆科植物把空气中的氮气转化为化合态的氮
B.分离液态空气获得氮气
C.用NH4Cl和熟石灰制备氨气
D.NO2溶于水得到HNO3
E.土壤中的硝酸盐被细菌分解转化为氮气
(2)受到阳光照射浓硝酸会变黄的原因是_______ (用化学方程式表示)。
(3)近几年来关于氮污染的治理倍受关注,根据氮的性质回答以下问题:
①氮氧化物是空气的主要污染物,用碱液脱硝是目前研究的课题之一。将NO2通入氢氧化钠溶液中可得到NaNO3和NaNO2,写出其反应方程式:_______ 。
②向酸性工业废水中加入次氯酸钠溶液,可将其中的NH 完全转化为N2,而次氯酸钠被还原为NaCl。写出上述反应的离子方程式:
完全转化为N2,而次氯酸钠被还原为NaCl。写出上述反应的离子方程式:_______ 。
(4)潜艇中使用的液氨-液氧燃料电池工作原理如图所示:_______ (填“正极”或“负极”)。
②电极b的电极反应式为_______ 。
(1)下列变化中,属于固氮的是
A.豆科植物把空气中的氮气转化为化合态的氮
B.分离液态空气获得氮气
C.用NH4Cl和熟石灰制备氨气
D.NO2溶于水得到HNO3
E.土壤中的硝酸盐被细菌分解转化为氮气
(2)受到阳光照射浓硝酸会变黄的原因是
(3)近几年来关于氮污染的治理倍受关注,根据氮的性质回答以下问题:
①氮氧化物是空气的主要污染物,用碱液脱硝是目前研究的课题之一。将NO2通入氢氧化钠溶液中可得到NaNO3和NaNO2,写出其反应方程式:
②向酸性工业废水中加入次氯酸钠溶液,可将其中的NH
 完全转化为N2,而次氯酸钠被还原为NaCl。写出上述反应的离子方程式:
完全转化为N2,而次氯酸钠被还原为NaCl。写出上述反应的离子方程式:(4)潜艇中使用的液氨-液氧燃料电池工作原理如图所示:
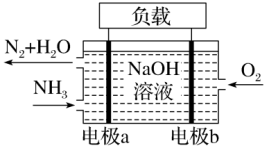
②电极b的电极反应式为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】细菌可以促使铁、氮两种元素进行氧化还原反应,并耦合两种元素的循环。耦合循环中的部分转化如图所示。
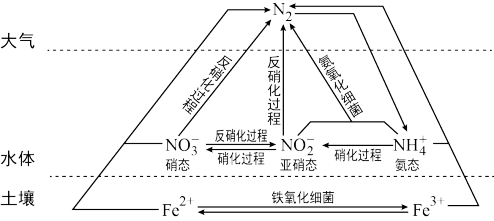
(1)如图所示氮循环中,属于氮的固定的有_____ (填字母序号)。
a.N2转化为氨态氮
b.硝化过程
c.反硝化过程
(2)氮肥是水体中 的主要来源之一,检验氮肥中
的主要来源之一,检验氮肥中 的实验方案是
的实验方案是_____ 。
(3)硝化过程中,含氮物质发生_____ (填“氧化”或“还原”)反应。
(4)氨态氮与亚硝态氮可以在氨氧化细菌的作用下转化为氮气。该反应中,当产生0.02mol氮气时,转移的电子的物质的量为_____ mol。
(5)土壤中的铁循环可用于水体脱氮(脱氮是指将氮元素从水体中除去),用离子方程式说明利用土壤中的铁循环脱除水体中氨态氮的原理_____ 。

(1)如图所示氮循环中,属于氮的固定的有
a.N2转化为氨态氮
b.硝化过程
c.反硝化过程
(2)氮肥是水体中
 的主要来源之一,检验氮肥中
的主要来源之一,检验氮肥中 的实验方案是
的实验方案是(3)硝化过程中,含氮物质发生
(4)氨态氮与亚硝态氮可以在氨氧化细菌的作用下转化为氮气。该反应中,当产生0.02mol氮气时,转移的电子的物质的量为
(5)土壤中的铁循环可用于水体脱氮(脱氮是指将氮元素从水体中除去),用离子方程式说明利用土壤中的铁循环脱除水体中氨态氮的原理
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】大气污染物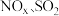 的脱除和利用可以保护大气环境。含氮废水中氨氮(以
的脱除和利用可以保护大气环境。含氮废水中氨氮(以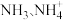 存在)和硝态氮(以
存在)和硝态氮(以 存在)会引起水体富营养化,需经处理后才能排放。
存在)会引起水体富营养化,需经处理后才能排放。
(1)空气中的 可在催化剂作用下被
可在催化剂作用下被 还原生成
还原生成 ,该反应的化学方程式是
,该反应的化学方程式是___________ 。
(2)工业上常在燃煤过程中加入 浆状物脱除
浆状物脱除 ,脱硫的产品
,脱硫的产品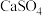 用于制造石膏,该脱硫反应的总化学方程式是
用于制造石膏,该脱硫反应的总化学方程式是___________ 。
(3)可以用天然海水吸收含硫烟气中 。根据如图所示的实验结果,为了提高一定浓度含硫烟气中
。根据如图所示的实验结果,为了提高一定浓度含硫烟气中 的吸收效率,下列措施正确的是
的吸收效率,下列措施正确的是___________ (填字母)。
B.减小通入含硫烟气的流速
C.减少天然海水的进入量
(4)利用微生物可对含氮废水进行处理,流程如图:___________ 。
②检验含氮废水中氨氮 是否除尽的实验操作是
是否除尽的实验操作是___________ 。
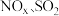 的脱除和利用可以保护大气环境。含氮废水中氨氮(以
的脱除和利用可以保护大气环境。含氮废水中氨氮(以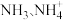 存在)和硝态氮(以
存在)和硝态氮(以 存在)会引起水体富营养化,需经处理后才能排放。
存在)会引起水体富营养化,需经处理后才能排放。(1)空气中的
 可在催化剂作用下被
可在催化剂作用下被 还原生成
还原生成 ,该反应的化学方程式是
,该反应的化学方程式是(2)工业上常在燃煤过程中加入
 浆状物脱除
浆状物脱除 ,脱硫的产品
,脱硫的产品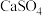 用于制造石膏,该脱硫反应的总化学方程式是
用于制造石膏,该脱硫反应的总化学方程式是(3)可以用天然海水吸收含硫烟气中
 。根据如图所示的实验结果,为了提高一定浓度含硫烟气中
。根据如图所示的实验结果,为了提高一定浓度含硫烟气中 的吸收效率,下列措施正确的是
的吸收效率,下列措施正确的是
B.减小通入含硫烟气的流速
C.减少天然海水的进入量
(4)利用微生物可对含氮废水进行处理,流程如图:
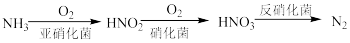
②检验含氮废水中氨氮
 是否除尽的实验操作是
是否除尽的实验操作是
您最近半年使用:0次

 )的生物法处理流程如图所示:
)的生物法处理流程如图所示:
 溶液调节pH至9充分反应后,升温至30℃,然后通入空气。以上操作能降低废水中氨氮含量的原因为
溶液调节pH至9充分反应后,升温至30℃,然后通入空气。以上操作能降低废水中氨氮含量的原因为 的转化,称为硝化过程。在碱性条件下实现上述硝化过程的总反应的离子方程式为
的转化,称为硝化过程。在碱性条件下实现上述硝化过程的总反应的离子方程式为

