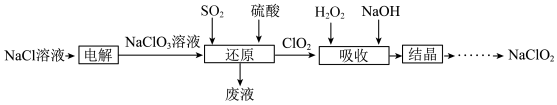
NaClO2是一种重要的含氯消毒剂,也常用来漂白织物等,其一种生产工艺如下图。
(1)NaClO2中氯元素的化合价是___________ 。
(2)“电解”时,所用的食盐水可由粗盐水精制而成。精制食盐时,需除去粗盐中的Ca2+、Mg2+,加入的试剂分别为___________ 、___________ (填化学式)。
(3)“还原”中,发生反应的离子方程式为___________ 。
(4)“废液”中的主要溶质是___________ (填化学式)。
(5)“吸收”反应中,氧化剂和还原剂的物质的量之比为___________ ,该反应中氧
化产物为___________ 。
(1)NaClO2中氯元素的化合价是
(2)“电解”时,所用的食盐水可由粗盐水精制而成。精制食盐时,需除去粗盐中的Ca2+、Mg2+,加入的试剂分别为
(3)“还原”中,发生反应的离子方程式为
(4)“废液”中的主要溶质是
(5)“吸收”反应中,氧化剂和还原剂的物质的量之比为
化产物为
更新时间:2024-05-06 18:45:31
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】请根据已知信息回答下列各问:
Ⅰ.已知H3PO2(次磷酸)是一元酸,H3PO2水溶液中存在H3PO2分子。
(1)写出 H3PO2溶液与足量NaOH溶液反应的离子方程式___________ 。
(2)磷酸(H3PO4)、亚磷酸(H3PO3)、次磷酸都是重要的化工产品。已知:1 mol磷酸、亚磷酸、次磷酸最多消耗NaOH的物质的量依次为3 mol、2 mol、1 mol。则NaH2PO4、NaH2PO2、NaH2PO3中属于正盐的是___________ (填化学式)。
Ⅱ. 可用作清洁剂、防腐剂等。
可用作清洁剂、防腐剂等。
(3)下列关于NaHSO4的说法正确的是___________ ;
a.NaHSO4固体不能导电 b.NaHSO4溶液的导电性一定强于CH3COOH溶液
c.NaHSO4属于电解质 d.NaHSO4溶液显中性
(4) 溶液与NaHCO3溶液反应的离子方程式为
溶液与NaHCO3溶液反应的离子方程式为___________ 。
Ⅲ.有以下物质:
①石墨、②铁、③蔗糖、④一氧化碳、⑤氯化铁固体、⑥碳酸氢钠固体、⑦氢氧化钡溶液、⑧纯醋酸、⑨熔融氯化钠、⑩液态氯化氢
(5)以上物质属于电解质的是___________ ;能导电的是___________
(6)写出用⑤的饱和溶液制备Fe(OH)3胶体的离子反应方程式:___________ 。
(7)将物质⑥配制成溶液,逐滴加入⑦溶液中至沉淀量最大,写出离子方程式:___________ 。
Ⅰ.已知H3PO2(次磷酸)是一元酸,H3PO2水溶液中存在H3PO2分子。
(1)写出 H3PO2溶液与足量NaOH溶液反应的离子方程式
(2)磷酸(H3PO4)、亚磷酸(H3PO3)、次磷酸都是重要的化工产品。已知:1 mol磷酸、亚磷酸、次磷酸最多消耗NaOH的物质的量依次为3 mol、2 mol、1 mol。则NaH2PO4、NaH2PO2、NaH2PO3中属于正盐的是
Ⅱ.
 可用作清洁剂、防腐剂等。
可用作清洁剂、防腐剂等。(3)下列关于NaHSO4的说法正确的是
a.NaHSO4固体不能导电 b.NaHSO4溶液的导电性一定强于CH3COOH溶液
c.NaHSO4属于电解质 d.NaHSO4溶液显中性
(4)
 溶液与NaHCO3溶液反应的离子方程式为
溶液与NaHCO3溶液反应的离子方程式为Ⅲ.有以下物质:
①石墨、②铁、③蔗糖、④一氧化碳、⑤氯化铁固体、⑥碳酸氢钠固体、⑦氢氧化钡溶液、⑧纯醋酸、⑨熔融氯化钠、⑩液态氯化氢
(5)以上物质属于电解质的是
(6)写出用⑤的饱和溶液制备Fe(OH)3胶体的离子反应方程式:
(7)将物质⑥配制成溶液,逐滴加入⑦溶液中至沉淀量最大,写出离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】盐酸、硫酸和硝酸是中学阶段常见的“三大酸”。现就三大酸与金属反应的情况,回答下列问题:
(1)稀盐酸不与Cu反应,若在稀盐酸中加入H2O2(常见氧化剂,作氧化剂时还原产物为水)后,则可使铜顺利溶解。该反应的化学方程式为:______________________ 。
(2)在一定体积的10 mol·L-1的浓硫酸中加入过量铜片,加热使之反应,被还原的硫酸为0.9 mol。则浓硫酸的实际体积________________ (填“大于”、“等于”或“小于”)180 mL。若使剩余的铜片继续溶解,可在其中加入硝酸盐溶液(如KNO3溶液),则该反应的离子方程式为__________________ 。
(3) 欲迅速除去铝壶底部的水垢,又不损坏铝壶,最好的方法是( )
(1)稀盐酸不与Cu反应,若在稀盐酸中加入H2O2(常见氧化剂,作氧化剂时还原产物为水)后,则可使铜顺利溶解。该反应的化学方程式为:
(2)在一定体积的10 mol·L-1的浓硫酸中加入过量铜片,加热使之反应,被还原的硫酸为0.9 mol。则浓硫酸的实际体积
(3) 欲迅速除去铝壶底部的水垢,又不损坏铝壶,最好的方法是
| A.浓盐酸 | B.稀硝酸 | C.冷的浓硝酸 | D.冷的浓硫酸 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】回答下列问题:
(1)在 、
、 、
、 、
、 、
、 、
、 、
、 中,只有氧化性的是
中,只有氧化性的是___________ ,只有还原性的是___________ ,既有氧化性又有还原性的是___________ 。
(2)高铁酸钠 是一种新型绿色消毒剂,主要用于饮用水处理,工业上有一种制备高铁酸钠的化学反应原理可用离子方程式表示为:
是一种新型绿色消毒剂,主要用于饮用水处理,工业上有一种制备高铁酸钠的化学反应原理可用离子方程式表示为:

①由上述反应可知,氧化性强弱:
___________  (填“>”或“<”);
(填“>”或“<”);
②请用单线桥法表示该反应中电子的转移情况:___________ 。
(3) 、
、 、
、 、
、 、
、 、
、 组成的一个氧化还原反应体系中,发生
组成的一个氧化还原反应体系中,发生 的反应过程。
的反应过程。
①该反应中,氧化剂是___________ , 氧化剂在反应过程中转移电子数是
氧化剂在反应过程中转移电子数是___________ ;
②将以上物质填入下面横线上,并配平该反应。
___________ 。
(1)在
 、
、 、
、 、
、 、
、 、
、 、
、 中,只有氧化性的是
中,只有氧化性的是(2)高铁酸钠
 是一种新型绿色消毒剂,主要用于饮用水处理,工业上有一种制备高铁酸钠的化学反应原理可用离子方程式表示为:
是一种新型绿色消毒剂,主要用于饮用水处理,工业上有一种制备高铁酸钠的化学反应原理可用离子方程式表示为:
①由上述反应可知,氧化性强弱:

 (填“>”或“<”);
(填“>”或“<”);②请用单线桥法表示该反应中电子的转移情况:
(3)
 、
、 、
、 、
、 、
、 、
、 组成的一个氧化还原反应体系中,发生
组成的一个氧化还原反应体系中,发生 的反应过程。
的反应过程。①该反应中,氧化剂是
 氧化剂在反应过程中转移电子数是
氧化剂在反应过程中转移电子数是②将以上物质填入下面横线上,并配平该反应。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】(2019 长兴中学)(氧化还原配平)配平下列方程式:
(1)_______ NH4NO3 = _______ HNO3+_______ N2↑+_______ H2O
(2)___ H2C2O4+___ KMnO4+ ___ H2SO4—____ CO2↑+___ K2SO4+___ MnSO4+___ H2O
(1)
(2)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】生产生活中的化学电源、金属冶炼、环境污染等都与氧化还原反应息息相关,研究氧化还原反应,对人类进步和社会发展都具有极其重要的意义。
(1)已知下列反应在一定条件下可以发生:H2O2+2Fe2++2H+=2Fe3++2H2O;H2O2+2Fe3+= 2Fe2++2H+ +O2↑
①通过观察以上两个反应,对其中Fe2+的认识是__________________ 。
②I2和Fe2+一样也能与H2O2发生上述类似反应,类比上述反应,在下面空格上填入合适的化学方程式:H2O2+I2= 2HIO;___________ 。总的化学方程式为_____________________________ 。
(2)2017年4月1日,中共中央、国务院印发通知,决定设立河北雄安新区。据报道周边污水渗坑给雄安新区的水环境带来隐患,目前采用多种方法对污水进行处理,改善水资源状况。
①碱性环境下,Cl2可将水中残存的CN-转化为两种无毒的气体,则该反应生成两种无毒气体的物质的量之比为_________________ 。
②酸性环境下,向含重铬酸根(Cr2O72-)的废水中加入FeSO4溶液,然后调节溶液pH,使生成的Cr3+转化为Cr(OH)3,写出第一步反应对应的离子方程式________________________________ 。
(1)已知下列反应在一定条件下可以发生:H2O2+2Fe2++2H+=2Fe3++2H2O;H2O2+2Fe3+= 2Fe2++2H+ +O2↑
①通过观察以上两个反应,对其中Fe2+的认识是
②I2和Fe2+一样也能与H2O2发生上述类似反应,类比上述反应,在下面空格上填入合适的化学方程式:H2O2+I2= 2HIO;
(2)2017年4月1日,中共中央、国务院印发通知,决定设立河北雄安新区。据报道周边污水渗坑给雄安新区的水环境带来隐患,目前采用多种方法对污水进行处理,改善水资源状况。
①碱性环境下,Cl2可将水中残存的CN-转化为两种无毒的气体,则该反应生成两种无毒气体的物质的量之比为
②酸性环境下,向含重铬酸根(Cr2O72-)的废水中加入FeSO4溶液,然后调节溶液pH,使生成的Cr3+转化为Cr(OH)3,写出第一步反应对应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】氧化还原反应是一类重要的反应。
(1)已知反应Cu+2Fe3+=Cu2++2Fe2+,氧化性Fe3+_____ Cu2+(填“ < ”或“ > ”) 。
(2)在2Na2O2+2CO2=2Na2CO3+O2反应中,若转移3mol电子,则所产生的氧气在标准状况下的体积为______ 。
(3)在xR2++yH++O2═mR3++nH2O的离子方程式中,对系数m和R2+、R3+判断正确的是___________ 。
A.m=y,R3+是还原剂 B.m=2y,R2+被氧化
C.m=2,R3+是氧化剂 D.m=4,R2+是还原剂
(4)实验室中所用少量氯气是用下列方法制取的:4HCl(浓)+MnO2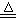 Cl2↑+MnCl2+2H2O其中氧化剂与还原剂的物质的量之比
Cl2↑+MnCl2+2H2O其中氧化剂与还原剂的物质的量之比_____________ ,写出该反应的离子方程式__________________________
(5)草酸能使酸性KMnO4溶液褪色,配平下面的化学方程式: KMnO4+ H2SO4+ H2C2O4 = MnSO4+ K2SO4 + CO2↑+ H2O,答案为:________________
(1)已知反应Cu+2Fe3+=Cu2++2Fe2+,氧化性Fe3+
(2)在2Na2O2+2CO2=2Na2CO3+O2反应中,若转移3mol电子,则所产生的氧气在标准状况下的体积为
(3)在xR2++yH++O2═mR3++nH2O的离子方程式中,对系数m和R2+、R3+判断正确的是
A.m=y,R3+是还原剂 B.m=2y,R2+被氧化
C.m=2,R3+是氧化剂 D.m=4,R2+是还原剂
(4)实验室中所用少量氯气是用下列方法制取的:4HCl(浓)+MnO2
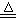 Cl2↑+MnCl2+2H2O其中氧化剂与还原剂的物质的量之比
Cl2↑+MnCl2+2H2O其中氧化剂与还原剂的物质的量之比(5)草酸能使酸性KMnO4溶液褪色,配平下面的化学方程式: KMnO4+ H2SO4+ H2C2O4 = MnSO4+ K2SO4 + CO2↑+ H2O,答案为:
您最近一年使用:0次
填空题
|
适中
(0.65)
真题
解题方法
【推荐1】(1)已知3种原子晶体的熔点数据如下表:
金刚石熔点比晶体硅熔点高的原因是_______ 。
(2)提纯含有少量氯化钠的甘氨酸样品:将样品溶于水,调节溶液的pH使甘氨酸结晶析出,可实现甘氨酸的提纯。其理由是_______ 。
| 金刚石 | 碳化硅 | 晶体硅 | |
| 熔点/℃ | >3550 | 2600 | 1415 |
(2)提纯含有少量氯化钠的甘氨酸样品:将样品溶于水,调节溶液的pH使甘氨酸结晶析出,可实现甘氨酸的提纯。其理由是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】用化学方法除去下列物质中混有的少量杂质,其中括号内为杂质,写出除杂需加入的试剂(用化学式表示)以及发生反应的离子方程式。
(1)固体Na2CO3(NaHCO3)除杂发生反应的化学方程式___ ;
(2)固体Fe(OH)3(Al(OH)3)除杂发生反应的离子方程式____ ;
(3)溶液FeCl2(CuCl2)除杂发生反应的离子方程式____ ;
(4)气体CO2(HCl)除杂发生反应的离子方程式___ 。
(1)固体Na2CO3(NaHCO3)除杂发生反应的化学方程式
(2)固体Fe(OH)3(Al(OH)3)除杂发生反应的离子方程式
(3)溶液FeCl2(CuCl2)除杂发生反应的离子方程式
(4)气体CO2(HCl)除杂发生反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】粗盐中可溶性杂质的除去方法(完成下表)。
硫酸盐:加入试剂___________________ 、反应的化学方程式为___________________
MgCl2:加入试剂___________________ 、反应的化学方程式为___________________
CaCl2:加入试剂___________________ 、反应的化学方程式为___________________
多余的NaOH、Na2CO3:加入试剂___________________ 、反应的化学方程式为___________________
杂质 | 加入的试剂 | 发生反应的化学方程式 |
硫酸盐 | ||
MgCl2 | ||
CaCl2 | ||
多余的NaOH、Na2CO3 |
硫酸盐:加入试剂
MgCl2:加入试剂
CaCl2:加入试剂
多余的NaOH、Na2CO3:加入试剂
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】实验室里用图所示装置制取并收集纯净的氯气.回答下列问题:

①写出烧瓶中发生反应的化学方程式:_________________________________ .
②C处盛有饱和食盐水,其作用是_________________ .
③D处盛放的试剂是_________ (填名称),其作用是_____________ .
④F处盛有__________ (填名称),发生反应的离子方程式为_______________ .

①写出烧瓶中发生反应的化学方程式:
②C处盛有饱和食盐水,其作用是
③D处盛放的试剂是
④F处盛有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】许多含氮物质会造成环境污染,硝酸工业的尾气(含 )会造成大气污染,通常用选择性非催化还原法或碱液吸收法。而废水中过量的氨氮(
)会造成大气污染,通常用选择性非催化还原法或碱液吸收法。而废水中过量的氨氮( 和
和 )会导致水体富营养化,则通常用强氧化剂或微生物法来吸收。
)会导致水体富营养化,则通常用强氧化剂或微生物法来吸收。
(1)废气中氮氧化物的吸收。
①在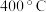 左右且有催化剂存在的情况下,
左右且有催化剂存在的情况下, 能把
能把 还原成无色无毒气体直接排入空气中,则发生反应的化学方程式为
还原成无色无毒气体直接排入空气中,则发生反应的化学方程式为___________ 。
②碱液吸收法。该工艺中采用气液逆流接触吸收(尾气从吸收塔底进入,石灰乳从吸收塔顶喷淋),得到的滤渣可循环使用,该滤渣的主要成分是___________ (填化学式)。工艺需控制 和
和 的物质的量之比接近
的物质的量之比接近___________ ,若小于这个比值,则会导致___________ 。
 溶液也可以吸收氮氧化物,写出
溶液也可以吸收氮氧化物,写出 溶液吸收
溶液吸收 混合气体得到亚硝酸钠的化学方程式
混合气体得到亚硝酸钠的化学方程式___________ 。
(2)废水中过量的氨氮(如 和
和 )处理,科研小组用
)处理,科研小组用 氧化法处理氨氮废水。
氧化法处理氨氮废水。
已知:
A. 的氧化性比
的氧化性比 强;
强;
B. 比
比 更易被氧化;
更易被氧化;
C.国家标准要求经处理过的氨氨废水 要控制在
要控制在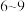 。
。
进水 对氨氨去除率的影响如下图所示。
对氨氨去除率的影响如下图所示。 为
为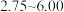 范围内,氨氮去除率随
范围内,氨氮去除率随 升高而上升的原因是
升高而上升的原因是___________ 。
写出酸性条件下 氧化
氧化 的离子方程式:
的离子方程式:___________ 。
已知:a. 的氧化性比
的氧化性比 弱;b.
弱;b. 氧化氨氮的速率比
氧化氨氮的速率比 小。
小。
在其他条件不变时,仅增加单位时间内通入空气的量,氨氮去除率___________ (填“显著变大”“显著变小”或“几乎不变”)。
(3)微生物脱氮氯法: 。
。
写出酸性条件下步骤a的离子方程式:___________ 。
 )会造成大气污染,通常用选择性非催化还原法或碱液吸收法。而废水中过量的氨氮(
)会造成大气污染,通常用选择性非催化还原法或碱液吸收法。而废水中过量的氨氮( 和
和 )会导致水体富营养化,则通常用强氧化剂或微生物法来吸收。
)会导致水体富营养化,则通常用强氧化剂或微生物法来吸收。(1)废气中氮氧化物的吸收。
①在
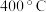 左右且有催化剂存在的情况下,
左右且有催化剂存在的情况下, 能把
能把 还原成无色无毒气体直接排入空气中,则发生反应的化学方程式为
还原成无色无毒气体直接排入空气中,则发生反应的化学方程式为②碱液吸收法。该工艺中采用气液逆流接触吸收(尾气从吸收塔底进入,石灰乳从吸收塔顶喷淋),得到的滤渣可循环使用,该滤渣的主要成分是
 和
和 的物质的量之比接近
的物质的量之比接近 溶液也可以吸收氮氧化物,写出
溶液也可以吸收氮氧化物,写出 溶液吸收
溶液吸收 混合气体得到亚硝酸钠的化学方程式
混合气体得到亚硝酸钠的化学方程式(2)废水中过量的氨氮(如
 和
和 )处理,科研小组用
)处理,科研小组用 氧化法处理氨氮废水。
氧化法处理氨氮废水。已知:
A.
 的氧化性比
的氧化性比 强;
强;B.
 比
比 更易被氧化;
更易被氧化;C.国家标准要求经处理过的氨氨废水
 要控制在
要控制在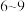 。
。进水
 对氨氨去除率的影响如下图所示。
对氨氨去除率的影响如下图所示。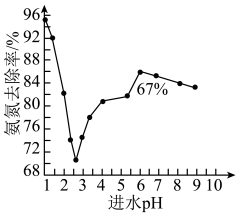
 为
为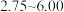 范围内,氨氮去除率随
范围内,氨氮去除率随 升高而上升的原因是
升高而上升的原因是写出酸性条件下
 氧化
氧化 的离子方程式:
的离子方程式:已知:a.
 的氧化性比
的氧化性比 弱;b.
弱;b. 氧化氨氮的速率比
氧化氨氮的速率比 小。
小。在其他条件不变时,仅增加单位时间内通入空气的量,氨氮去除率
(3)微生物脱氮氯法:
 。
。写出酸性条件下步骤a的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】将CaCl2投入过氧化氢(H2O2)溶液中,并通入适量气体,可得到CaO2·8H2O白色沉淀。
已知:①CaO2·8H2O属微溶性化合物;②过氧化物受热或在强酸性条件下比较容易分解;③由于大量水分子参与结晶,该反应放热;④H2O2是一种弱酸,具有微弱的酸性,CaO2可看作它对应的一种盐。
(1)制取上述过氧化钙晶体的反应条件应包括____ (选择填空)
a 适当低温 b 高温 c 强酸性 d 反应物浓度足够高
(2)通入的气体是______ 。
(3)写出该反应的化学方程式。___________
(4)产物被滤出后用蒸馏水淋洗。如何确定“洗净”____________
已知:①CaO2·8H2O属微溶性化合物;②过氧化物受热或在强酸性条件下比较容易分解;③由于大量水分子参与结晶,该反应放热;④H2O2是一种弱酸,具有微弱的酸性,CaO2可看作它对应的一种盐。
(1)制取上述过氧化钙晶体的反应条件应包括
a 适当低温 b 高温 c 强酸性 d 反应物浓度足够高
(2)通入的气体是
(3)写出该反应的化学方程式。
(4)产物被滤出后用蒸馏水淋洗。如何确定“洗净”
您最近一年使用:0次



