一定条件下,容积2L的密闭容器中,将1mol L气体和0.5mol M气体混合,发生如下反应: ,5s时反应达到平衡,生成0.2mol R,测得Q的浓度为
,5s时反应达到平衡,生成0.2mol R,测得Q的浓度为 。计算:
。计算:
(1)化学方程式中a的值为___________ 。
(2)前5s内用M表示的化学反应速率为___________ ,L的转化率为___________ 。
(3)一定能使该反应的速率增大的措施有___________(填字母)。
(4)可认定上述可逆反应在一定条件下已达到化学平衡状态的是___________ (填字母)。
A.体系压强不再变化
B.体系的密度不再变化
C.
D.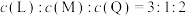
E.Q(g)的物质的量浓度不再发生变化
 ,5s时反应达到平衡,生成0.2mol R,测得Q的浓度为
,5s时反应达到平衡,生成0.2mol R,测得Q的浓度为 。计算:
。计算:(1)化学方程式中a的值为
(2)前5s内用M表示的化学反应速率为
(3)一定能使该反应的速率增大的措施有___________(填字母)。
| A.其他条件不变,充入一定量气体L | B.降低温度 |
| C.保持温度不变,将容器的体积压缩 | D.保持体积不变,充入无关惰性气体 |
A.体系压强不再变化
B.体系的密度不再变化
C.

D.
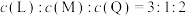
E.Q(g)的物质的量浓度不再发生变化
更新时间:2023-04-26 08:24:49
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】碳、硫的含量影响钢铁性能。某兴趣小组用如下流程对钢样进行探究。
(1)钢样中硫元素以FeS形式存在,FeS在足量氧气中灼烧,生成的固体产物中Fe、O两种元素的质量比为21:8,则该固体产物的化学式为_____________ 。
(2)检验钢样灼烧生成气体中的CO2,需要的试剂是____________ (填字母)。
a.酸性KMnO4溶液b.澄清石灰水c.饱和小苏打溶液d.浓H2SO4
(3)取10.00 g钢样在足量氧气中充分灼烧,将生成的气体用足量1%的H2O2溶液充分吸收,再用0.1000mol·L-1NaOH溶液滴定吸收液至终点,消耗NaOH溶液20.00mL;另取10.00g钢样在足量氧气中充分灼烧,将生成的气体通过盛有足量碱石灰的U形管(如下图),碱石灰增重0.614 g。
①用l%H2O2溶液吸收SO2,发生反应的离子方程式为___________________ 。
②分别计算该钢样中硫、碳元素的质量分数(写出计算过程)。
③实验测得的碳元素质量分数比真实值偏高,其可能的原因是______________ (填字母)
a.U型管中生成的亚硫酸盐吸收了O2
b.碱石灰吸收了空气中的CO2
c.气体通过碱石灰的流速过快,末被充分吸收

(1)钢样中硫元素以FeS形式存在,FeS在足量氧气中灼烧,生成的固体产物中Fe、O两种元素的质量比为21:8,则该固体产物的化学式为
(2)检验钢样灼烧生成气体中的CO2,需要的试剂是
a.酸性KMnO4溶液b.澄清石灰水c.饱和小苏打溶液d.浓H2SO4
(3)取10.00 g钢样在足量氧气中充分灼烧,将生成的气体用足量1%的H2O2溶液充分吸收,再用0.1000mol·L-1NaOH溶液滴定吸收液至终点,消耗NaOH溶液20.00mL;另取10.00g钢样在足量氧气中充分灼烧,将生成的气体通过盛有足量碱石灰的U形管(如下图),碱石灰增重0.614 g。

①用l%H2O2溶液吸收SO2,发生反应的离子方程式为
②分别计算该钢样中硫、碳元素的质量分数(写出计算过程)。
③实验测得的碳元素质量分数比真实值偏高,其可能的原因是
a.U型管中生成的亚硫酸盐吸收了O2
b.碱石灰吸收了空气中的CO2
c.气体通过碱石灰的流速过快,末被充分吸收
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】现有下列十种物质:①HCl ②NaCl ③纯碱 ④CO2 ⑤CH3COOH ⑥KOH ⑦氢氧化铁胶体 ⑧NH3 ⑨空气 ⑩Fe2(SO4)3
(1)上述十种物质中,属于电解质的有___________ ,属于非电解质的有___________ 。
(2)有两种物质在水溶液中可发生反应,离子方程式为H++OH-=H2O,该反应的化学方程式为___________ ;
(3)标准状况下,___________ L ④分子中含有0.2mol氧原子;
(4)现有100mL⑩溶液中含有Fe2(SO4)3 40.0g,则溶液中Fe2(SO4)3的物质的量浓度是___________ 。
(1)上述十种物质中,属于电解质的有
(2)有两种物质在水溶液中可发生反应,离子方程式为H++OH-=H2O,该反应的化学方程式为
(3)标准状况下,
(4)现有100mL⑩溶液中含有Fe2(SO4)3 40.0g,则溶液中Fe2(SO4)3的物质的量浓度是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】通过计算填写下列内容:
(1)在标准状况下,6.72L CO的物质的量为_______ mol,质量为_______ g。
(2)23g C2H5OH的氢原子数目为_______ 。
(3)100mLNa2SO4溶液中, SO 的物质的量浓度为1mol/L,则Na+的物质的量浓度为
的物质的量浓度为1mol/L,则Na+的物质的量浓度为_______ ,加水稀释至1L后,Na2SO4的物质的量浓度为 _______
(4)常用的干燥剂有:①生石灰;②氢氧化钠固体;③变色硅胶(主要成分是二氧化硅,在其中掺入少量的无水氯化钴作指示剂);④五氧化二磷;⑤无水氯化钙;⑥浓硫酸。
①上述物质中,属于非电解质的是_______ (填字母,下同)。
A. ④ B. ③④ C.③④⑤ D. ③④⑤⑥
②上述干燥剂中①,其主要化学成分所属的类别为_______ 。
A.酸 B.碱 C.盐 D.酸性氧化物 E.碱性氧化物
③硅胶中无水氯化钴(CoCl2)呈蓝色,吸水后变为粉红色的CoCl2·6H2O,该变化过程属于_______ (填“物理变化”或“化学变化”)。
(1)在标准状况下,6.72L CO的物质的量为
(2)23g C2H5OH的氢原子数目为
(3)100mLNa2SO4溶液中, SO
 的物质的量浓度为1mol/L,则Na+的物质的量浓度为
的物质的量浓度为1mol/L,则Na+的物质的量浓度为(4)常用的干燥剂有:①生石灰;②氢氧化钠固体;③变色硅胶(主要成分是二氧化硅,在其中掺入少量的无水氯化钴作指示剂);④五氧化二磷;⑤无水氯化钙;⑥浓硫酸。
①上述物质中,属于非电解质的是
A. ④ B. ③④ C.③④⑤ D. ③④⑤⑥
②上述干燥剂中①,其主要化学成分所属的类别为
A.酸 B.碱 C.盐 D.酸性氧化物 E.碱性氧化物
③硅胶中无水氯化钴(CoCl2)呈蓝色,吸水后变为粉红色的CoCl2·6H2O,该变化过程属于
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】研发CO2利用技术成为了研究热点,某科研团队采用一种类似“搭积木”的方式,在实验室中首次实现从二氧化碳到淀粉分子的全合成,“积木”中涉及如下两个反应:①CO2(g)+3H2(g) CH3OH(g)+H2O(g),②CH3OH(g)+O2(g)
CH3OH(g)+H2O(g),②CH3OH(g)+O2(g) HCHO(g)+H2O2(l)。一定温度下,往5L反应釜中充入1molCO2、3molH2,反应5min,气体总的物质的量减少了20%,则0~5min内,H2的平均反应速率v=
HCHO(g)+H2O2(l)。一定温度下,往5L反应釜中充入1molCO2、3molH2,反应5min,气体总的物质的量减少了20%,则0~5min内,H2的平均反应速率v=____ 。
 CH3OH(g)+H2O(g),②CH3OH(g)+O2(g)
CH3OH(g)+H2O(g),②CH3OH(g)+O2(g) HCHO(g)+H2O2(l)。一定温度下,往5L反应釜中充入1molCO2、3molH2,反应5min,气体总的物质的量减少了20%,则0~5min内,H2的平均反应速率v=
HCHO(g)+H2O2(l)。一定温度下,往5L反应釜中充入1molCO2、3molH2,反应5min,气体总的物质的量减少了20%,则0~5min内,H2的平均反应速率v=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】氮的化合物被广泛应用于工业、航天、医药等领域。请回答下列问题:
(1)氨气可作为脱硝剂。在恒温恒容的密闭容器中充入一定量的NO和 ,在一定条件下发生反应:
,在一定条件下发生反应: 。该反应达到平衡状态的标志是___________(填序号)。
。该反应达到平衡状态的标志是___________(填序号)。
(2)一定条件下,在5L密闭容器内,发生反应: ,
, 的物质的量随时间变化的情况如表:
的物质的量随时间变化的情况如表:
①0~2s内用 表示的该反应的平均反应速率为
表示的该反应的平均反应速率为___________  ;5s时,
;5s时, 的转化率为
的转化率为___________ 。
②为加快反应速率,可以采取的措施是___________ (填序号)。
a.恒容时充入He(g)
b.恒压时充入He(g)
c.恒容时充入 (g)
(g)
(3)已知: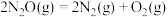 。不同温度
。不同温度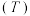 下,
下, 分解半衰期随起始压强的变化情况如图所示(图中半衰期指任一浓度
分解半衰期随起始压强的变化情况如图所示(图中半衰期指任一浓度 减小一半时所需的时间),则
减小一半时所需的时间),则
___________ (填“>”“=”或“<”) 。若温度为
。若温度为 、起始压强为
、起始压强为 ,则反应至
,则反应至 时,体系压强
时,体系压强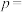
___________ kPa(用 表示)。
表示)。

(1)氨气可作为脱硝剂。在恒温恒容的密闭容器中充入一定量的NO和
 ,在一定条件下发生反应:
,在一定条件下发生反应: 。该反应达到平衡状态的标志是___________(填序号)。
。该反应达到平衡状态的标志是___________(填序号)。A.反应速率 |
| B.容器内压强不再变化 |
C.容器内 |
D.12molN—H键断裂的同时生成5molN N键 N键 |
 ,
, 的物质的量随时间变化的情况如表:
的物质的量随时间变化的情况如表:| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
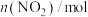 | 0.040 | 0.020 | 0.010 | 0.005 | 0.005 | 0.005 |
 表示的该反应的平均反应速率为
表示的该反应的平均反应速率为 ;5s时,
;5s时, 的转化率为
的转化率为②为加快反应速率,可以采取的措施是
a.恒容时充入He(g)
b.恒压时充入He(g)
c.恒容时充入
 (g)
(g)(3)已知:
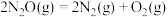 。不同温度
。不同温度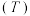 下,
下, 分解半衰期随起始压强的变化情况如图所示(图中半衰期指任一浓度
分解半衰期随起始压强的变化情况如图所示(图中半衰期指任一浓度 减小一半时所需的时间),则
减小一半时所需的时间),则
 。若温度为
。若温度为 、起始压强为
、起始压强为 ,则反应至
,则反应至 时,体系压强
时,体系压强
 表示)。
表示)。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】某温度时,在一个2L的恒容容器中,X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线如图所示。根据图中数据填空:
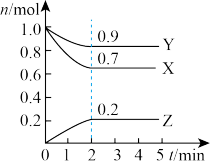
(1)该反应的化学方程式为_______ 。
(2)反应开始至 ,以气体Y表示的平均反应速率为
,以气体Y表示的平均反应速率为_______ ,X的转化率_______ , 时容器内压强是反应开始时的
时容器内压强是反应开始时的_______ 倍。
(3) 时,正反应速率
时,正反应速率_______ 逆反应速率(填“ ”“
”“ ”或“
”或“ ”)。
”)。
(4)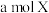 与
与 的混合气体发生上述反应,反应到某时刻各物质的量恰好满足:
的混合气体发生上述反应,反应到某时刻各物质的量恰好满足: ,则原混合气体中
,则原混合气体中
_______ 。

(1)该反应的化学方程式为
(2)反应开始至
 ,以气体Y表示的平均反应速率为
,以气体Y表示的平均反应速率为 时容器内压强是反应开始时的
时容器内压强是反应开始时的(3)
 时,正反应速率
时,正反应速率 ”“
”“ ”或“
”或“ ”)。
”)。(4)
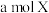 与
与 的混合气体发生上述反应,反应到某时刻各物质的量恰好满足:
的混合气体发生上述反应,反应到某时刻各物质的量恰好满足: ,则原混合气体中
,则原混合气体中
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】把在空气中久置的镁条7.2 g投入盛有500 mL 0.5 mol·L-1硫酸溶液的烧杯中,镁条与硫酸反应产生氢气的速率与反应时间如图所示,回答下列问题:

(1)曲线由0→a段不产生氢气的原因________ ,有关的离子方程式为______________ ;
(2)曲线由b→c段,产生氢气的速率逐渐增大的主要原因________________ ;
(3)曲线由c以后,产生氢气的速率逐渐下降的主要原因________________ 。
(4)在b到c这段时间内,收集到氢气V L(标准状况),则这段时间内用硫酸表示的平均速率为________ mol/(L·s)(假设反应前后溶液体积不变)。
(5)对于足量镁条和100 mL 2 mol/L硫酸生成氢气的反应,下列措施能减缓反应速率,但又不影响生成氢气的总量的是________ 。
①加NaOH固体;②加BaCl2溶液;③加KNO3溶液;④加H2O;⑤加CH3COONa固体;⑥加小苏打溶液;⑦加少量CuSO4溶液;⑧加Na2SO4溶液;⑨将2 mol/L硫酸换成160 mL 2.5 mol/L的盐酸;⑩将镁条换成镁粉。

(1)曲线由0→a段不产生氢气的原因
(2)曲线由b→c段,产生氢气的速率逐渐增大的主要原因
(3)曲线由c以后,产生氢气的速率逐渐下降的主要原因
(4)在b到c这段时间内,收集到氢气V L(标准状况),则这段时间内用硫酸表示的平均速率为
(5)对于足量镁条和100 mL 2 mol/L硫酸生成氢气的反应,下列措施能减缓反应速率,但又不影响生成氢气的总量的是
①加NaOH固体;②加BaCl2溶液;③加KNO3溶液;④加H2O;⑤加CH3COONa固体;⑥加小苏打溶液;⑦加少量CuSO4溶液;⑧加Na2SO4溶液;⑨将2 mol/L硫酸换成160 mL 2.5 mol/L的盐酸;⑩将镁条换成镁粉。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】某研究性学习小组利用 溶液和酸性
溶液和酸性 溶液的反应探究“外界条件的改变对化学反应速率的影响”,进行了如下实验:(说明:
溶液的反应探究“外界条件的改变对化学反应速率的影响”,进行了如下实验:(说明: 为二元弱酸,其水溶液无色)
为二元弱酸,其水溶液无色)
(1)已知酸性 溶液与
溶液与 溶液反应的离子方程式为:
溶液反应的离子方程式为: ,该反应中每转移
,该反应中每转移 电子,产生的
电子,产生的 在标况下的体积为
在标况下的体积为___________ 。
(2)其表格中
___________ 、
___________ ;通过实验___________ (只填a、b、c实验序号中的2个)可探究出温度变化对化学反应速率的影响,其表格中
___________ 。
(3)若 ,则由此实验可以得出的结论是
,则由此实验可以得出的结论是___________ ;忽略溶液体积的变化,利用实验b中数据计算, 内,用
内,用 的浓度变化表示的反应速率
的浓度变化表示的反应速率
___________ 。
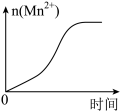
(4)该小组的一位同学通过查阅资料发现,上述实验过程中 随时间的变化情况如图所示,并认为造成这种变化的原因是反应体系中的某种粒子对
随时间的变化情况如图所示,并认为造成这种变化的原因是反应体系中的某种粒子对 与草酸之间的反应有某种特殊作用,则该作用是
与草酸之间的反应有某种特殊作用,则该作用是___________ 。
 溶液和酸性
溶液和酸性 溶液的反应探究“外界条件的改变对化学反应速率的影响”,进行了如下实验:(说明:
溶液的反应探究“外界条件的改变对化学反应速率的影响”,进行了如下实验:(说明: 为二元弱酸,其水溶液无色)
为二元弱酸,其水溶液无色)| 实验 序号 | 实验温度/K | 有关物质 | 溶液颜色褪至无 色所需时间/s | ||||
酸性 溶液 溶液 |  溶液 溶液 |  | |||||
 |  |  |  |  | |||
| a | 293 | 2 | 0.02 | 4 | 0.1 | 0 |  |
| b |  | 2 | 0.02 | 3 | 0.1 |  | 8 |
| c | 313 | 2 | 0.02 |  | 0.1 | 1 |  |
 溶液与
溶液与 溶液反应的离子方程式为:
溶液反应的离子方程式为: ,该反应中每转移
,该反应中每转移 电子,产生的
电子,产生的 在标况下的体积为
在标况下的体积为(2)其表格中



(3)若
 ,则由此实验可以得出的结论是
,则由此实验可以得出的结论是 内,用
内,用 的浓度变化表示的反应速率
的浓度变化表示的反应速率
(4)该小组的一位同学通过查阅资料发现,上述实验过程中
 随时间的变化情况如图所示,并认为造成这种变化的原因是反应体系中的某种粒子对
随时间的变化情况如图所示,并认为造成这种变化的原因是反应体系中的某种粒子对 与草酸之间的反应有某种特殊作用,则该作用是
与草酸之间的反应有某种特殊作用,则该作用是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】把在空气中久置的铝片5.0 g投入盛有500 mL 0.5 mol/L硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间的关系可用如图所示的坐标曲线来表示,请回答下列问题:

(1)曲线由O→a段不产生氢气的原因是___________________________ ,有关的化学方程式为___________________________________________ 。
(2)曲线由a→c段,产生氢气的速率增加较快的主要原因是_____________________ 。
(3)曲线由c以后,产生氢气的速率逐渐下降的主要原因是_________________________ 。

(1)曲线由O→a段不产生氢气的原因是
(2)曲线由a→c段,产生氢气的速率增加较快的主要原因是
(3)曲线由c以后,产生氢气的速率逐渐下降的主要原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题:
(1) 溶液常用于腐蚀印刷电路铜板,发生
溶液常用于腐蚀印刷电路铜板,发生 ,若将此反应设计成原电池,则负极所用电极材料为
,若将此反应设计成原电池,则负极所用电极材料为___________ ,当线路中转移 电子时,则被腐蚀铜的质量为
电子时,则被腐蚀铜的质量为___________ g.
(2)高铁电池是一种新型可充电电池,该电池能较长时间保持稳定的放电电压.高铁电池的总反应式为: .放电时,负极反应式充电为
.放电时,负极反应式充电为___________________ ,
(3)实验小组对可逆反应 进行探究。
进行探究。 时,起始向
时,起始向 恒容密闭容器中充入X、Y,测得反应过程中X、Y、Z三种气体的物质的量浓度
恒容密闭容器中充入X、Y,测得反应过程中X、Y、Z三种气体的物质的量浓度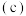 与时间
与时间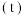 的关系如图所示.
的关系如图所示. 内的反应速率
内的反应速率
____________________ ;
②为提高此反应的速率,下列措施可行的是_________ (填字母代号);
A.移出Z B.使用适合催化剂 C.降低温度 D.增大压强
③该反应达③最大限度时Y的体积分数为_____________________ ;
④下列描述能表示该反应达平衡状态的是_____________________ ;
A.容器内的混合气体的平均相对分子质量不再改变 B.容器内压强不再发生变化
C. D.X的体积分数不再改变
D.X的体积分数不再改变
(1)
 溶液常用于腐蚀印刷电路铜板,发生
溶液常用于腐蚀印刷电路铜板,发生 ,若将此反应设计成原电池,则负极所用电极材料为
,若将此反应设计成原电池,则负极所用电极材料为 电子时,则被腐蚀铜的质量为
电子时,则被腐蚀铜的质量为(2)高铁电池是一种新型可充电电池,该电池能较长时间保持稳定的放电电压.高铁电池的总反应式为:
 .放电时,负极反应式充电为
.放电时,负极反应式充电为(3)实验小组对可逆反应
 进行探究。
进行探究。 时,起始向
时,起始向 恒容密闭容器中充入X、Y,测得反应过程中X、Y、Z三种气体的物质的量浓度
恒容密闭容器中充入X、Y,测得反应过程中X、Y、Z三种气体的物质的量浓度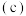 与时间
与时间 的关系如图所示.
的关系如图所示.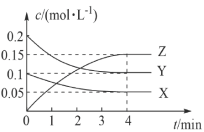
 内的反应速率
内的反应速率
②为提高此反应的速率,下列措施可行的是
A.移出Z B.使用适合催化剂 C.降低温度 D.增大压强
③该反应达③最大限度时Y的体积分数为
④下列描述能表示该反应达平衡状态的是
A.容器内的混合气体的平均相对分子质量不再改变 B.容器内压强不再发生变化
C.
 D.X的体积分数不再改变
D.X的体积分数不再改变
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】在10L的密闭容器中,进行如下化学反应:CO2(g)+H2(g)⇌CO(g)+H2O(g),其化学平衡常数K与温度t的关系如下表:
请回答:
(1)该反应为___________ (填“吸热”或“放热”)反应。
(2)该反应的化学平衡常数表达式为K=___________ 。保持温度和体积不变,充入一定量的CO2,则平衡常数___________ 。(填“增大”、“减小”或“不变”)
(3)下列措施可以提高H2的平衡转化率的是(填选项序号)___________ 。
a.选择适当的催化剂 b.增大压强 c.及时分离H2O(g) d.升高温度
(4)某温度下,c(CO2)=2mol/L,c(H2)=3mol/L,开始反应,达到平衡时CO2转化率为60%,则平衡常数K=___________ 。
(5)与(4)相同的温度下,某时刻测得c(CO2)=0.5mol/L,c(H2)=1.5mol/L,c(CO)=0.5mol/L、c(H2O)=0.5mol/L,则此时反应是否达到平衡状态_______ (填“是”或“否”)。此时,v(正)_______ v(逆)(填“ ”、“
”、“ ”或“
”或“ ”)。
”)。
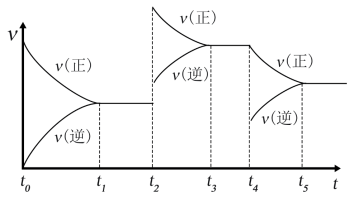
(6)该反应的反应速率(v)随时间(t)变化的关系如图所示,若t2、t4时刻只改变一个条件,下列说法正确的是(填选项序号)___________ 。
b.在t2时,采取的措施可以是升高温度
c.在t4时,采取的措施可以是增加CO2的浓度。
d.在t5时,容器内CO的体积分数是整个过程中的最大值
| t(℃) | 700 | 800 | 830 | 1000 | 1200 |
| K | 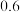 |  |  | 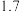 |  |
(1)该反应为
(2)该反应的化学平衡常数表达式为K=
(3)下列措施可以提高H2的平衡转化率的是(填选项序号)
a.选择适当的催化剂 b.增大压强 c.及时分离H2O(g) d.升高温度
(4)某温度下,c(CO2)=2mol/L,c(H2)=3mol/L,开始反应,达到平衡时CO2转化率为60%,则平衡常数K=
(5)与(4)相同的温度下,某时刻测得c(CO2)=0.5mol/L,c(H2)=1.5mol/L,c(CO)=0.5mol/L、c(H2O)=0.5mol/L,则此时反应是否达到平衡状态
 ”、“
”、“ ”或“
”或“ ”)。
”)。(6)该反应的反应速率(v)随时间(t)变化的关系如图所示,若t2、t4时刻只改变一个条件,下列说法正确的是(填选项序号)
b.在t2时,采取的措施可以是升高温度
c.在t4时,采取的措施可以是增加CO2的浓度。
d.在t5时,容器内CO的体积分数是整个过程中的最大值
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】Ⅰ.已知:反应aA(g)+bB(g) cC(g),某温度下,在2L的密闭容器中投入一定量的A、B,两种气体的物质的量浓度随时间变化的曲线如图所示。
cC(g),某温度下,在2L的密闭容器中投入一定量的A、B,两种气体的物质的量浓度随时间变化的曲线如图所示。
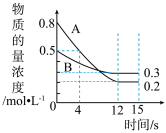
(1)经测4s时间,v(C)=0.05mol·L-1·s-1,则4s时物质C的物质的量为___________________ ,该反应的化学方程式为______________________ 。
(2)经12s时间,v(A)=___________ ,v(C)=___________ ,该反应12s时___________ 达到化学平衡(“是”或“否”)。
Ⅱ.(3)下列说法可以证明H2(g)+I2(g) 2HI(g)已达平衡状态的是
2HI(g)已达平衡状态的是________ (填序号)。
A.单位时间内生成nmolH2的同时,生成nmolHI
B.一个H—H键断裂的同时有两个H—I键断裂
C.温度和体积一定时,混合气体颜色不再变化
D.反应速率v(H2)=v(I2)= v(HI)
v(HI)
 cC(g),某温度下,在2L的密闭容器中投入一定量的A、B,两种气体的物质的量浓度随时间变化的曲线如图所示。
cC(g),某温度下,在2L的密闭容器中投入一定量的A、B,两种气体的物质的量浓度随时间变化的曲线如图所示。
(1)经测4s时间,v(C)=0.05mol·L-1·s-1,则4s时物质C的物质的量为
(2)经12s时间,v(A)=
Ⅱ.(3)下列说法可以证明H2(g)+I2(g)
 2HI(g)已达平衡状态的是
2HI(g)已达平衡状态的是A.单位时间内生成nmolH2的同时,生成nmolHI
B.一个H—H键断裂的同时有两个H—I键断裂
C.温度和体积一定时,混合气体颜色不再变化
D.反应速率v(H2)=v(I2)=
 v(HI)
v(HI)
您最近一年使用:0次



