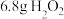实验室制备下列气体所选试剂、制备装置及收集方法均正确的是


| 选项 | 气体 | 试剂 | 制备装置 | 收集方法 |
| A |  |  固体+98%的浓 固体+98%的浓 | b | c |
| B |  |  | a | d |
| C |  | 过氧化氢溶液+ | b | e |
| D |  |  +浓盐酸 +浓盐酸 | b | c |
| A.A | B.B | C.C | D.D |
更新时间:2023-04-16 18:03:24
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】制造芯片用到高纯硅,用SiHCl3(沸点:31.85℃,SiHCl3遇水会剧烈反应,除生成H2SiO3、HCl外,还生成一种气体a)与过量H2在1100~1200℃反应制备高纯硅的装置如图所示(夹持装置和尾气处理装置略去),下列说法错误的是
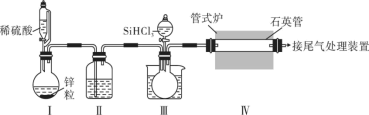

| A.实验时,先打开装有稀硫酸仪器的活塞,收集尾气验纯,再预热装置Ⅳ石英管 |
| B.装置Ⅱ、Ⅲ中依次盛装的是浓H2SO4、温度高于32℃的温水 |
| C.Ⅰ装置可用于二氧化锰固体与浓盐酸反应制备氯气 |
| D.a气体为H2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列实验过程可以达到实验目的的是
| 编号 | 实验目的 | 实验过程 |
| A | 配制 的NaOH溶液 的NaOH溶液 | 称取4.0g固体NaOH于烧杯中,加入少量蒸馏水溶解,转移至500mL容量瓶中定容 |
| B | 除去氯气中的氯化氢 | 将混合气体通过盛有饱和食盐水的洗气瓶 |
| C | 制取干燥纯净的氢气 | 向稀盐酸中加入锌粒,将生成的气体依次通过浓硫酸、NaOH溶液,然后收集 |
| D | 制备 胶体 胶体 | 将NaOH浓溶液滴加到饱和 溶液中 溶液中 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列实验方案能达到相应目的的是
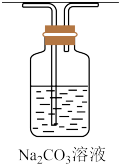 | 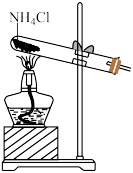 | 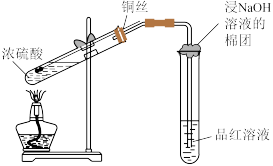 |  |
A.除 中的HCl 中的HCl | B.实验室制 | C.证明浓硫酸有强氧化性 | D.检验 溶液是否变质 溶液是否变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
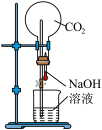
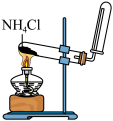
【推荐2】某兴趣小组利用下列装置进行实验,其中能达到实验目的的是
|
|
|
|
| A.喷泉实验 | B.验证压强对平衡的影响 | C.制备 | D.制取无水 固体 固体 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】以含钴废渣(主要成分CoO、 ,还含有
,还含有 、ZnO等杂质)为原料制备
、ZnO等杂质)为原料制备 的一种实验流程如下。下列与流程相关的装置和原理能达到实验目的的是
的一种实验流程如下。下列与流程相关的装置和原理能达到实验目的的是

 ,还含有
,还含有 、ZnO等杂质)为原料制备
、ZnO等杂质)为原料制备 的一种实验流程如下。下列与流程相关的装置和原理能达到实验目的的是
的一种实验流程如下。下列与流程相关的装置和原理能达到实验目的的是
A.用装置甲制备“酸浸”所需的 ,“酸浸”时 ,“酸浸”时 为还原剂 为还原剂 |
B.用装置乙配制“酸浸”所需的250mL 1  溶液 溶液 |
| C.用装置丙过滤“沉钴”所得悬浊液,为了提高“沉钴”效率可快速滴加碳酸钠溶液 |
D.用装置丁萃取振荡时,分液漏斗下口应倾斜向上,萃取的目的是除去 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列有关元素存在及应用的说法正确的是
| A.金属材料都是导体,非金属材料都是绝缘体 |
| B.工业制硫酸、硝酸的关键步骤都应用了催化氧化的方法 |
| C.硅胶吸水后不能重复再利用 |
| D.钠、铝、铁、硫、氯等元素在自然界中只有化合态存在 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】用下列实验装置和方法进行相应实验,能达到实验目的的是
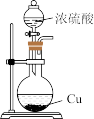 | 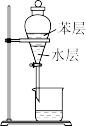 | 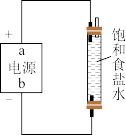 | 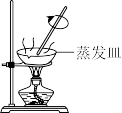 |
| 甲 | 乙 | 丙 | 丁 |
| A.用装置甲制备SO2 |
| B.用装置乙从碘水溶液中萃取碘 |
| C.装置丙用于制备少量含NaClO的消毒液 |
| D.用装置丁蒸干溶液获得(NH4)2CO3晶体 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列反应的离子方程式正确的是
| A.向 FeCl2 溶液中滴加 H2O2:H2O2+2Fe2+=2H2O+2Fe3+ |
B.NaHCO3 溶液中通入过量 SO2:HCO +SO2= HSO +SO2= HSO +CO2 +CO2 |
C.乙醇与 K2Cr2O7 酸性溶液反应:3CH3CH2OH+2Cr2O +11H2O=3CH3COOH + 4Cr(OH)3↓+4OH- +11H2O=3CH3COOH + 4Cr(OH)3↓+4OH- |
| D.氯气与热的 NaOH 溶液反应:Cl2+2OH-=Cl-+ClO-+H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】氧泡泡是一种多功能新型漂白剂,其有效成分是过碳酸钠(xNa2CO3•yH2O2)。
I.以芒硝(Na2SO4•10H2O)、H2O2等为原料制备过碳酸钠的工艺流程如图:
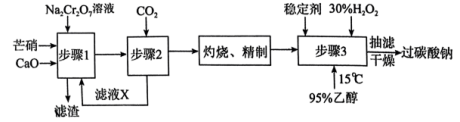
Ⅱ.测定过碳酸钠化学式的实验步骤如下(样品中杂质不参加反应):
①用电子天平称取两份质量均为mg的样品。
②将一份置于锥形瓶中,加水溶解,加催化剂使H2O2充分快速分解(催化剂不参与其它反应),然后加酚酞作指示剂,用0.0500mol•L-1H2SO4溶液滴定至终点,消耗硫酸V1mL。
③将另一份置于碘量瓶中,加入50mL蒸馏水,并立即加入6mL2.0mol•L-1H3PO4溶液,再加入过量KI固体,摇匀后于暗处放置10min,加入适量指示剂,用0.1000mol•L-1Na2S2O3标准溶液滴定至终点,消耗Na2S2O3标准溶液V2mL。(已知:2Na2S2O3+I2=Na2S4O6+2NaI)
过碳酸钠制备的流程中,下列说法错误的是
I.以芒硝(Na2SO4•10H2O)、H2O2等为原料制备过碳酸钠的工艺流程如图:

Ⅱ.测定过碳酸钠化学式的实验步骤如下(样品中杂质不参加反应):
①用电子天平称取两份质量均为mg的样品。
②将一份置于锥形瓶中,加水溶解,加催化剂使H2O2充分快速分解(催化剂不参与其它反应),然后加酚酞作指示剂,用0.0500mol•L-1H2SO4溶液滴定至终点,消耗硫酸V1mL。
③将另一份置于碘量瓶中,加入50mL蒸馏水,并立即加入6mL2.0mol•L-1H3PO4溶液,再加入过量KI固体,摇匀后于暗处放置10min,加入适量指示剂,用0.1000mol•L-1Na2S2O3标准溶液滴定至终点,消耗Na2S2O3标准溶液V2mL。(已知:2Na2S2O3+I2=Na2S4O6+2NaI)
过碳酸钠制备的流程中,下列说法错误的是
| A.步骤1中2mol芒硝参与反应时,消耗1molNa2Cr2O7 |
| B.滤渣的主要成分为CaSO4 |
C.步骤2的方程式为2Na2CrO4+2CO2+H2O Na2Cr2O7+2NaHCO3↓ Na2Cr2O7+2NaHCO3↓ |
| D.稳定剂的作用是阻止微量杂质金属离子的催化作用,减少双氧水的分解 |
您最近一年使用:0次

 )在实验室常作湿度和水分的指示剂,无水
)在实验室常作湿度和水分的指示剂,无水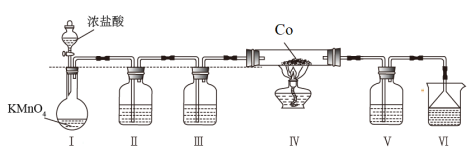
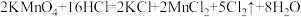


 2NH3
2NH3 的水滴后会自发形成
的水滴后会自发形成 ,揭示了世界上第一个
,揭示了世界上第一个 分子可能来自
分子可能来自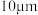 大小的水滴会产生丁达尔现象
大小的水滴会产生丁达尔现象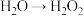 ”中氧元素化合价升高
”中氧元素化合价升高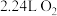 (标况下)需分解
(标况下)需分解