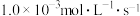与稀盐酸反应(放热反应)生成
与稀盐酸反应(放热反应)生成 的量与反应时间的关系如下图所示。下列结论正确的是
的量与反应时间的关系如下图所示。下列结论正确的是
| A.反应开始4min内温度对反应速率的影响比浓度大 |
| B.一段时间后,反应速率减小的原因是此反应是吸热反应 |
| C.反应在4~6min内平均反应速率最大 |
D.反应在2~4min内生成 的平均反应速率为 的平均反应速率为 |
更新时间:2023-04-17 13:37:03
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】某课外实验小组利用压强传感器、数据采集器和计算机等数字化实验设备,探究镁与不同浓度的盐酸的反应速率,两组实验所用试剂如下:

实验结果如图所示。结合图表分析,下列说法错误的是
| 序号 | 镁条的质量/ | 盐酸 | |
物质的量浓度/( ) ) | 体积/ | ||
| 1 | 0.01 | 1.0 | 2 |
| 2 | 0.01 | 0.5 | 2 |

实验结果如图所示。结合图表分析,下列说法错误的是
| A.曲线的斜率可以表征反应速率 |
| B.两个实验中盐酸均过量,镁条不足,理论上若时间足够长,最终反应生成的气体的量应该相同 |
| C.若改变镁条的质量,两条曲线的斜率都变大 |
| D.保持其他条件不变,将盐酸换成同浓度的稀硫酸,单位时间内压强变化值将增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】某些生物酶体系可以促进H+和e-的转移(如a、b和c),能将海洋中的 转化为N2进入大气层,反应过程如图所示。下列说法错误的是
转化为N2进入大气层,反应过程如图所示。下列说法错误的是
 转化为N2进入大气层,反应过程如图所示。下列说法错误的是
转化为N2进入大气层,反应过程如图所示。下列说法错误的是
A.过程I中 发生还原反应 发生还原反应 |
B.a和b中参与反应的 数目相等 数目相等 |
C.过程Ⅱ的反应为 |
D.过程I→Ⅲ的总反应为 |
您最近一年使用:0次
【推荐3】下列各表述与示意图一致的是( )


| A.图①表示25℃时,用0.1 mol·L-1盐酸滴定20 mL 0.1 mol·L-1KOH溶液,溶液的pH随加入酸体积的变化 |
B.图②中曲线表示反应N2(g)+3H2(g) 2NH3(g) ΔH< 0 正、逆反应的平衡常数K随温度的变化 2NH3(g) ΔH< 0 正、逆反应的平衡常数K随温度的变化 |
| C.图③表示用醋酸滴定NaOH和氨水混合溶液时,溶液的导电能力随醋酸体积变化的曲线 |
| D.图④中a、b曲线分别表示反应CH2=CH2(g)+ H2(g)→CH3CH3(g)ΔH< 0使用和未使用催化剂时,反应过程中的能量变化 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】T℃时,将15molA与10molB混合后通入容积为5L的密闭容器中,发生如下反应: ,10s时反应达到平衡,此时
,10s时反应达到平衡,此时 ,下列结论不正确的是
,下列结论不正确的是
 ,10s时反应达到平衡,此时
,10s时反应达到平衡,此时 ,下列结论不正确的是
,下列结论不正确的是| A.反应达平衡时,B的转化率为30% |
| B.该反应进行到10s时,生成了6mol的C |
C.10s内用B表示的反应速率为 |
| D.将容器的体积扩大至10L能使该反应的反应速率减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】一定温度下,将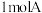 和
和 放入容积为
放入容积为 的密闭容器中,发生反应:
的密闭容器中,发生反应:
 ,
, 末达到平衡状态,测得容器内C的物质的量浓度为
末达到平衡状态,测得容器内C的物质的量浓度为 。下列叙述正确的是
。下列叙述正确的是
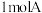 和
和 放入容积为
放入容积为 的密闭容器中,发生反应:
的密闭容器中,发生反应:
 ,
, 末达到平衡状态,测得容器内C的物质的量浓度为
末达到平衡状态,测得容器内C的物质的量浓度为 。下列叙述正确的是
。下列叙述正确的是A. 内,用A表示的平均反应速率为 内,用A表示的平均反应速率为 |
B.平衡时混合气体中B的物质的量分数为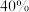 |
C.平衡后,继续向体系中加入少量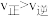 |
D.容器中初始压强和平衡时压强之比为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】100 mL 2 mol·L-1 H2SO4溶液与过量锌粉反应,一定温度下,为了减缓反应进行的速率,但又不影响生成H2的总量,可向反应物中加入适量( )
| A.硝酸钠溶液 | B.NaCl固体 | C.硫酸铵固体 | D.硫酸钾溶液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】为了研究一定量碳酸钙与足量稀盐酸反应的反应速率,一位同学通过实验测定反应中生成的CO2气体体积随反应时间变化的情况,绘制如图曲线。

下列说法不正确 的是

下列说法
| A.由图像可知,该反应是放热反应 |
B.0—t1时间段,CO2的化学反应速率v= (mL·min-1) (mL·min-1) |
| C.根据(V3—V2)<(V2—V1),推测反应速率减慢的原因可能是盐酸浓度减小 |
| D.由图像可知,0—t1的反应速率比t1—t2的反应速率快 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】少量铁粉与100mL0.01mol·L-1的稀盐酸反应,反应速率太慢,为了加快此反应速率而不改变H2的产量,可以使用如下方法中的( )
①加H2O ②加NaOH固体 ③加NaCl固体 ④加CuO固体 ⑤滴入几滴浓盐酸 ⑥升高温度(不考虑盐酸挥发) ⑦滴加几滴硫酸铜溶液
①加H2O ②加NaOH固体 ③加NaCl固体 ④加CuO固体 ⑤滴入几滴浓盐酸 ⑥升高温度(不考虑盐酸挥发) ⑦滴加几滴硫酸铜溶液
| A.①⑤⑦ | B.⑤⑥ | C.③⑦ | D.③⑥⑦ |
您最近一年使用:0次

 的四氯化碳溶液(
的四氯化碳溶液( )中发生分解反应:
)中发生分解反应: 。不同时刻测量放出的
。不同时刻测量放出的 体积,换算成
体积,换算成 为阿伏加德罗常数的值):
为阿伏加德罗常数的值):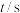

 时,转移电子的数目为
时,转移电子的数目为
 时,生成
时,生成 (标准状况)
(标准状况)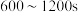 ,生成
,生成 的平均速率为
的平均速率为