化学反应中的能量变化,通常表现为热量的变化,研究化学反应中的热量变化具有重要的意义。
(1)一种化学冰袋中含有Na2SO4∙10H2O和NH4NO3,使用时将它们混合搓揉即可制冷,原因是NH4NO3溶于水吸热、_______ .
(2)某实验小组为了探究碳酸氢钠与柠檬酸反应的热效应,设计了如图所示的三套实验装置。
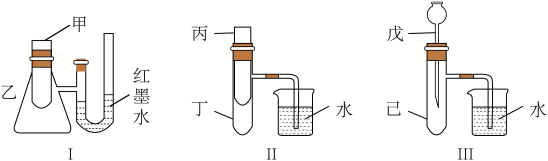
①不适合选用的装置是_______ (填装置序号)
②若观察到烧杯中产生气泡,_______ 说明反应为放热反应。(填“一定能”或“不能”)。
(3)从化学键的角度分析,化学反应的过程就是反应物的化学键的破坏和生成物的化学键的形成过程。已知:键能是指气态分子中1mol化学键解离成气态原子所吸收的能量。
已知: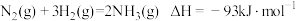 ,用电子式表达NH3中共价键的形成过程
,用电子式表达NH3中共价键的形成过程_______ ,a的数值为_______
(4)图Ⅱ表示一定条件下,在水溶液中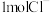 、
、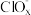 、
、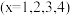 的能量相对大小。
的能量相对大小。
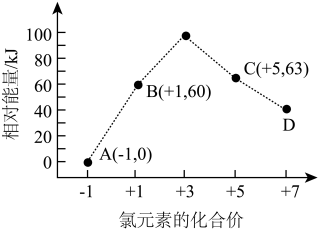
①D是_______ (填离子符号).
②B→A+C反应的热化学方程式为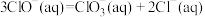

_______
(1)一种化学冰袋中含有Na2SO4∙10H2O和NH4NO3,使用时将它们混合搓揉即可制冷,原因是NH4NO3溶于水吸热、
(2)某实验小组为了探究碳酸氢钠与柠檬酸反应的热效应,设计了如图所示的三套实验装置。

①不适合选用的装置是
②若观察到烧杯中产生气泡,
(3)从化学键的角度分析,化学反应的过程就是反应物的化学键的破坏和生成物的化学键的形成过程。已知:键能是指气态分子中1mol化学键解离成气态原子所吸收的能量。
| 化学键 |  |  |  |
| 键能/ kJ∙mol-1 | 436 | a | 945 |
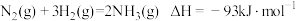 ,用电子式表达NH3中共价键的形成过程
,用电子式表达NH3中共价键的形成过程(4)图Ⅱ表示一定条件下,在水溶液中
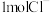 、
、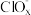 、
、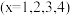 的能量相对大小。
的能量相对大小。
①D是
②B→A+C反应的热化学方程式为
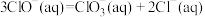

更新时间:2023-04-27 21:39:40
|
相似题推荐
【推荐1】元素周期表前四周期的A、B、C、D、E五种元素,A元素的原子最外层电子排布式为ns1;B元素的原子价电子排布式为ns2np2;C元素位于第二周期且原子中p能级与s能级电子总数相等;D元素原子的M能层的p能级中有3个未成对电子;E元素原子有五个未成对电子。
(1)写出元素名称:C___________ 、D___________ 、E___________ 。
(2)C基态原子的电子排布图为___________ 。
(3)当n=2时,B的最简单气态氢化物的电子式为___________ ,BC2分子的结构式是___________ ;当n=3时,B与C形成的化合物与氢氧化钠溶液反应的离子方程式是:___________ 。
(4)E元素原子的外围电子排布式是___________ 。
(1)写出元素名称:C
(2)C基态原子的电子排布图为
(3)当n=2时,B的最简单气态氢化物的电子式为
(4)E元素原子的外围电子排布式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】部分中学化学常见元素原子结构及性质如表所示:
(1)D元素的元素符号为______ ,C原子在周期表中的位置为__________ 。
(2)写出A单质与E的简单氢化物反应的离子方程式:_________________ 。
(3)F与E可以形成18电子的化合物Y,写出Y的电子式_________ 。用电子式表示化合物CF3的形成过程_________ 。
(4)比较C与D的氢化物稳定性大小_________ (用化学式表示)。
(5)B、C、E简单离子半径从大到小排序为__________________ (用离子符号表示)。
| 序号 | 元素 | 结构及性质 |
| ① | A | A单质是中学化学常见金属,在空气中燃烧生成淡黄色固体 |
| ② | B | B与A在同一周期,电子层数等于最外层电子数 |
| ③ | C | C是常见化肥的主要元素,单质常温下呈气态 |
| ④ | D | D单质被誉为“信息革命的催化剂”,是常用的半导体材料 |
| ⑤ | E | E是地壳中含量最多的元素 |
| ⑥ | F | F的原子半径在整个周期表中最小(稀有气体除外) |
(2)写出A单质与E的简单氢化物反应的离子方程式:
(3)F与E可以形成18电子的化合物Y,写出Y的电子式
(4)比较C与D的氢化物稳定性大小
(5)B、C、E简单离子半径从大到小排序为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】含硫化合物在生活和生产中有着重要应用,科学使用含硫化合物对人体健康及环境保护意义重大。
(1)葡萄酒中添加微量的SO2可抑制细菌生长,防止葡萄酒被__ (填“氧化”、“还原”)。
(2)氢的硫化物有多种:H2Sx(x=1,2,3,…),如H2S2,其结构与H2O2相似。请写出H2S3的结构式__ 。
(3)固体硫酸氢钾在加热熔化时,生成了焦硫酸钾(K2S2O7),反应中断裂的化学键类型为__ 。
(4)淮北某课题小组对连二亚硫酸钠(Na2S2O4)进行了如下探究。将0.050ml·L-1Na2S2O4溶液在空气中放置,其溶液的pH与时间(t)的关系如图所示(忽略溶液体积的变化)。
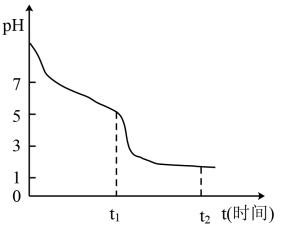
①Na2S2O4溶液显__ 性,原因是__ (用离子方程式表示)。
②t1时溶液中只有一种溶质,此时含硫元素的粒子浓度由大到小的顺序为___ 。
0-t1段发生反应的离子方程式为__ ,t1-t2段溶液的pH变小的原因是__ (用离子方程式表示)。
(1)葡萄酒中添加微量的SO2可抑制细菌生长,防止葡萄酒被
(2)氢的硫化物有多种:H2Sx(x=1,2,3,…),如H2S2,其结构与H2O2相似。请写出H2S3的结构式
(3)固体硫酸氢钾在加热熔化时,生成了焦硫酸钾(K2S2O7),反应中断裂的化学键类型为
(4)淮北某课题小组对连二亚硫酸钠(Na2S2O4)进行了如下探究。将0.050ml·L-1Na2S2O4溶液在空气中放置,其溶液的pH与时间(t)的关系如图所示(忽略溶液体积的变化)。

①Na2S2O4溶液显
②t1时溶液中只有一种溶质,此时含硫元素的粒子浓度由大到小的顺序为
0-t1段发生反应的离子方程式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】工业合成氨是人类科学技术的一项重大突破,其反应为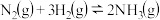 。
。
(1)已知合成氨反应为放热反应,下列图示表示的过程也为放热反应的是_______ (填序号)。
a. b.
b.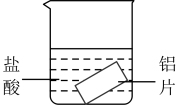 c.
c.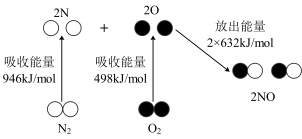
(2)合成氨反应过程可用下图模拟( 代表
代表 分子,
分子, 代表
代表 分子,
分子,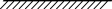 代表催化剂)。
代表催化剂)。
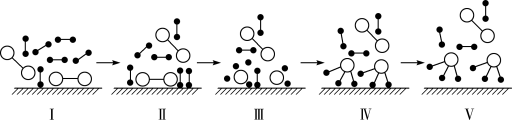
其中,状态_______ (填序号)中物质具有的总能量最高。
(3)一定条件下,向某2L恒温恒容密闭容器中通入 和
和 ,经20min反应达到平衡状态,此时
,经20min反应达到平衡状态,此时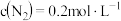 。
。
①在0~20min内,化学反应速率
_______ ; 的平衡转化率为
的平衡转化率为_______ 。
②若在15min时采取下列措施,不能增大反应速率的是_______ (填序号)。
A.恒温恒容下,再充入 B.其他条件不变,降低温度
B.其他条件不变,降低温度
C.恒温恒容下,向其中充入ArD.其他条件不变,将该反应容器的容积压缩至1L
(4) 可用于制作燃料电池,其原理如下图所示:
可用于制作燃料电池,其原理如下图所示:
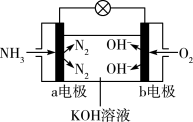
a电极的电极反应式为_______ ;理论上讲,该电池消耗的 与
与 在相同状况下的体积比为
在相同状况下的体积比为_______ 。
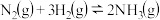 。
。(1)已知合成氨反应为放热反应,下列图示表示的过程也为放热反应的是
a.
 b.
b. c.
c.
(2)合成氨反应过程可用下图模拟(
 代表
代表 分子,
分子, 代表
代表 分子,
分子, 代表催化剂)。
代表催化剂)。
其中,状态
(3)一定条件下,向某2L恒温恒容密闭容器中通入
 和
和 ,经20min反应达到平衡状态,此时
,经20min反应达到平衡状态,此时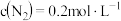 。
。①在0~20min内,化学反应速率

 的平衡转化率为
的平衡转化率为②若在15min时采取下列措施,不能增大反应速率的是
A.恒温恒容下,再充入
 B.其他条件不变,降低温度
B.其他条件不变,降低温度C.恒温恒容下,向其中充入ArD.其他条件不变,将该反应容器的容积压缩至1L
(4)
 可用于制作燃料电池,其原理如下图所示:
可用于制作燃料电池,其原理如下图所示:
a电极的电极反应式为
 与
与 在相同状况下的体积比为
在相同状况下的体积比为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】铝是一种重要的金属,在生产、生活中具有许多重要的用途,下图是工业上从铝土矿(主要成分是Al2O3,含有少量SiO2、Fe2O3等杂质)中生产铝的工艺流程:
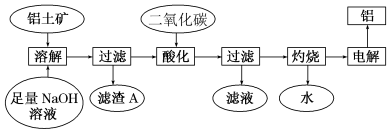
据此回答下列问题:
(1)电解制铝的化学反应中,反应物的键能之和____ 生成物的键能之和(填“大于”、“小于”或“等于”)。
(2)铝土矿中绝大部分成分都可以溶解在NaOH溶液中。请根据周期表对角线规则写出铍的氧化物与NaOH溶液反应的离子方程式:______________ 。
(3)滤渣A的主要成分是____________ 。
(4)通入过量二氧化碳所发生主要反应的化学方程式为_______________ 。
(5)某同学在实验室模拟工业生产铝,称取a g铝土矿可制得b g Al(假设每步反应进行完全),则铝土矿中Al2O3的质量分数为____________ 。

据此回答下列问题:
(1)电解制铝的化学反应中,反应物的键能之和
(2)铝土矿中绝大部分成分都可以溶解在NaOH溶液中。请根据周期表对角线规则写出铍的氧化物与NaOH溶液反应的离子方程式:
(3)滤渣A的主要成分是
(4)通入过量二氧化碳所发生主要反应的化学方程式为
(5)某同学在实验室模拟工业生产铝,称取a g铝土矿可制得b g Al(假设每步反应进行完全),则铝土矿中Al2O3的质量分数为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】含氮化合物在农业、工业、国防等领域都有着广泛的应用。如图是氮元素部分常见物质间的相互转化示意图。
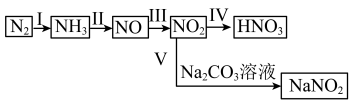
请回答下列问题:
(1)写出过程II的化学方程式:_______ 。若NO2最终完全转化为HNO3,计算1.7tNH3理论上可以得到质量分数为63%的硝酸溶液______ t。
(2)过程V是工业生产中吸收尾气NO2的一种方法,该过程中除生成NaNO2外,还产生一种气体和另一种盐,写出该反应的离子方程式:________ 。
(3)用200mL稀硝酸可以将5.6g铁粉恰好完全溶解(假设还原产物只有NO),并且溶液中的Fe2+与Fe3+的物质的量之比为3∶1,该稀硝酸的物质的量浓度为_______ mol•L-1。
(4)NO2(红棕色)和N2O4(无色)两种气体之间的转化为2NO2(g) N2O4(g)。
N2O4(g)。
①如果1molNO2(g)完全转化成N2O4(g)时放出的热量为238.5kJ,请从化学键角度描述能量变化的原因:_______ 。
②上述转化是一个典型的可逆反应。在恒温恒容密闭容器中反应,下列状况不能说明该反应达到化学平衡状态的是______ (填字母)。
A.容器内气体的颜色不再变化 B.2v正(N2O4)=v逆(NO2)
C.c(N2O4)∶c(NO2)=1:2 D.容器中N2O4的质量分数不再变化

请回答下列问题:
(1)写出过程II的化学方程式:
(2)过程V是工业生产中吸收尾气NO2的一种方法,该过程中除生成NaNO2外,还产生一种气体和另一种盐,写出该反应的离子方程式:
(3)用200mL稀硝酸可以将5.6g铁粉恰好完全溶解(假设还原产物只有NO),并且溶液中的Fe2+与Fe3+的物质的量之比为3∶1,该稀硝酸的物质的量浓度为
(4)NO2(红棕色)和N2O4(无色)两种气体之间的转化为2NO2(g)
 N2O4(g)。
N2O4(g)。①如果1molNO2(g)完全转化成N2O4(g)时放出的热量为238.5kJ,请从化学键角度描述能量变化的原因:
②上述转化是一个典型的可逆反应。在恒温恒容密闭容器中反应,下列状况不能说明该反应达到化学平衡状态的是
A.容器内气体的颜色不再变化 B.2v正(N2O4)=v逆(NO2)
C.c(N2O4)∶c(NO2)=1:2 D.容器中N2O4的质量分数不再变化
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】我国力争在2060年前实现“碳中和”,综合利用CO2具有重要的意义。300MP、200oC条件下,CO2与H2反应可制得气态甲醇(CH3OH),其反应方程式为CO2+3H2 CH3OH+H2O(g)。
CH3OH+H2O(g)。
(1)该反应的能量变化如图所示:
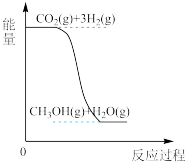
该反应是_______ 反应(填“吸热”或“放热”),判断的理由是 _______ 。
(2)为了加快该反应的速率,可以采取措施_______ (任写一种)。
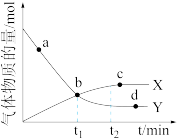
(3)在实际生产中,测得合成塔中H2及H2O(g)的物质的量随时间变化如下图所示,则图中代表 的曲线是
的曲线是_______ (填“X”或“Y”),v(正)与v(逆)相等的点为_______ (填字母)。
(4)在一定温度下,将2molCO2与6molH2气体混合于2L密闭容器中制甲醇,2min末生成0.8mol H2O(g)。
①用单位时间内 浓度的减小来表示2min内该反应的平均速率为
浓度的减小来表示2min内该反应的平均速率为_______ mol· L-1· min-1;
②2min末容器中H2的物质的量浓度_______ 。
 CH3OH+H2O(g)。
CH3OH+H2O(g)。(1)该反应的能量变化如图所示:

该反应是
(2)为了加快该反应的速率,可以采取措施
(3)在实际生产中,测得合成塔中H2及H2O(g)的物质的量随时间变化如下图所示,则图中代表
 的曲线是
的曲线是
(4)在一定温度下,将2molCO2与6molH2气体混合于2L密闭容器中制甲醇,2min末生成0.8mol H2O(g)。
①用单位时间内
 浓度的减小来表示2min内该反应的平均速率为
浓度的减小来表示2min内该反应的平均速率为②2min末容器中H2的物质的量浓度
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】江西稀土资源丰富。硫酸铵作为一种重要的化工原料,可用于稀土的提取。初始投料比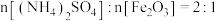 的混合物,其热分解过程如图所示:
的混合物,其热分解过程如图所示:
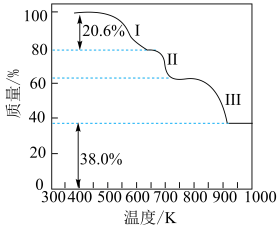
已知该过程主要分为三个阶段,其中:
阶段Ⅱ反应: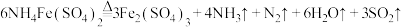
阶段Ⅲ反应: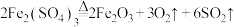
回答下列问题:
(1) 中,
中, 的空间结构为
的空间结构为_______ , 中心原子的杂化类型为
中心原子的杂化类型为______ 。
(2)阶段Ⅰ不发生氧化还原反应,对应的化学方程式为_________ ;图中阶段Ⅰ多次重复实验的实际失重均比理论值偏大,此误差属于______ (填“偶然误差”或“系统误差”)。
(3)阶段Ⅱ和Ⅲ都是吸热过程,且Ⅱ反应速率更快,下列示意图中能体现上述两反应能量变化的是______ (填标号),判断的理由是______ 。
A.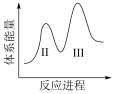 B.
B. 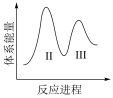 C.
C. 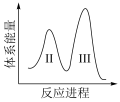 D.
D.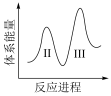
(4)该热分解过程中, 的作用为
的作用为_______ 。
(5)一定温度下,在真空刚性容器中, 的分解过程会发生下列反应:
的分解过程会发生下列反应:
主反应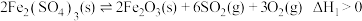
副反应
两个反应的平衡常数比值 随反应温度升高而
随反应温度升高而______ (填“增大”,“减小”或“不变”);若平衡时总压为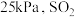 的体积分数为0.4,主反应的平衡常数
的体积分数为0.4,主反应的平衡常数
_____ 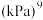 。
。
(6) 在高温下可以自发分解,原因是
在高温下可以自发分解,原因是______ 。
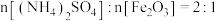 的混合物,其热分解过程如图所示:
的混合物,其热分解过程如图所示:
已知该过程主要分为三个阶段,其中:
阶段Ⅱ反应:
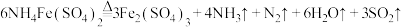
阶段Ⅲ反应:
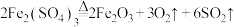
回答下列问题:
(1)
 中,
中, 的空间结构为
的空间结构为 中心原子的杂化类型为
中心原子的杂化类型为(2)阶段Ⅰ不发生氧化还原反应,对应的化学方程式为
(3)阶段Ⅱ和Ⅲ都是吸热过程,且Ⅱ反应速率更快,下列示意图中能体现上述两反应能量变化的是
A.
 B.
B.  C.
C.  D.
D.
(4)该热分解过程中,
 的作用为
的作用为(5)一定温度下,在真空刚性容器中,
 的分解过程会发生下列反应:
的分解过程会发生下列反应:主反应
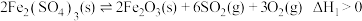
副反应

两个反应的平衡常数比值
 随反应温度升高而
随反应温度升高而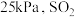 的体积分数为0.4,主反应的平衡常数
的体积分数为0.4,主反应的平衡常数
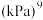 。
。(6)
 在高温下可以自发分解,原因是
在高温下可以自发分解,原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】I.某同学设计下图简易装置测定中和热。回答下列问题:
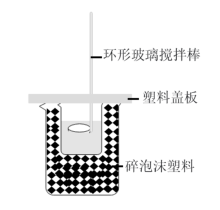
(1)该装置中缺少的仪器是___________ 。碎泡沫的作用:______
(2)50 mL 0.10 mol/L的盐酸与50 mL 0.11 mol/L的NaOH溶液混合后,测得反应放出的热量为285J,则中和热△H=___________ 。若将盐酸换成醋酸,会导致测定结果偏___________ (填小或者大)若将环形玻璃搅拌棒换为金属搅拌棒,则测得反应放出的热量将___________ (填“偏多”“偏少”或“不变”)。
II.氮是地球上含量丰富的一种元素,其单质及化合物在工农业生产、生活中有着重要作用。
(3)如图是 1 mol NO2(g)和 1 mol CO(g)反应生成 1 mol CO2(g)和 1 mol NO(g)过程中能量变化示意图。
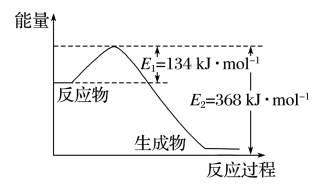
①该反应是___________ (填“吸热”或“放热”)反应。
②请写出反应的热化学方程式___________ 。
③若在该反应体系中加入催化剂对反应热___________ (填“有”或“没有”)影响。
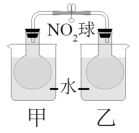
(4)已知,可逆反应2NO2(g) N2O4(g) ΔH = −56.9 kJ/mol。该反应正向是
N2O4(g) ΔH = −56.9 kJ/mol。该反应正向是___________ 反应。(填放热或吸热)在乙烧杯中投入一定量的CaO固体,此烧杯中NO2球的红棕色变深。说明CaO与水反应是___________ 反应(填吸热或者放热)

(1)该装置中缺少的仪器是
(2)50 mL 0.10 mol/L的盐酸与50 mL 0.11 mol/L的NaOH溶液混合后,测得反应放出的热量为285J,则中和热△H=
II.氮是地球上含量丰富的一种元素,其单质及化合物在工农业生产、生活中有着重要作用。
(3)如图是 1 mol NO2(g)和 1 mol CO(g)反应生成 1 mol CO2(g)和 1 mol NO(g)过程中能量变化示意图。

①该反应是
②请写出反应的热化学方程式
③若在该反应体系中加入催化剂对反应热
(4)已知,可逆反应2NO2(g)
 N2O4(g) ΔH = −56.9 kJ/mol。该反应正向是
N2O4(g) ΔH = −56.9 kJ/mol。该反应正向是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】原子序数由小到大排列的四种短周期元素X、Y、Z、W,四种元素的原子序数之和为32,在周期表中X是原子半径最小的元素,W的单质为淡黄色固体,Y、Z左右相邻,Z、W位于同主族。
(1) X元素是_______ ;W的原子结构示意图_______ 。
(2) X与W组成的化合物中存在_______ 键(填“离子”“共价”)。
(3) Y、Z形成的简单离子的半径由大到小的顺序为_______ 。
(4)工业上由X的单质与Y的单质化合生成1molA气体时放出46.2kJ的热量,写出该反应的热化学方程式_______ 。
(5)由X、Y、Z、W和Fe五种元素组成的式量为392的化合物B,1 mol B中含有6mol结晶水。对化合物B进行如下实验:
a.取B的溶液加入过量浓NaOH溶液并加热,产生白色沉淀和无色刺激性气味气体。过一段时间白色沉淀变为灰绿色,最终变为红褐色;
b.另取B的溶液,加入过量BaCl2溶液产生白色沉淀,加盐酸沉淀不溶解
① B的化学式为_______ 。
②已知1 mol·L-1 100mL B的溶液能与1 mol·L-1 20mLKMnO4溶液(硫酸酸化)恰好反应。写出反应的离子方程式_______ 。
(1) X元素是
(2) X与W组成的化合物中存在
(3) Y、Z形成的简单离子的半径由大到小的顺序为
(4)工业上由X的单质与Y的单质化合生成1molA气体时放出46.2kJ的热量,写出该反应的热化学方程式
(5)由X、Y、Z、W和Fe五种元素组成的式量为392的化合物B,1 mol B中含有6mol结晶水。对化合物B进行如下实验:
a.取B的溶液加入过量浓NaOH溶液并加热,产生白色沉淀和无色刺激性气味气体。过一段时间白色沉淀变为灰绿色,最终变为红褐色;
b.另取B的溶液,加入过量BaCl2溶液产生白色沉淀,加盐酸沉淀不溶解
① B的化学式为
②已知1 mol·L-1 100mL B的溶液能与1 mol·L-1 20mLKMnO4溶液(硫酸酸化)恰好反应。写出反应的离子方程式
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】氢气是未来最理想的能源;科学家最近研制出利用太阳能产生激光,并在二氧化光钛( )表面作用使海水分解得到复气的新技术:
)表面作用使海水分解得到复气的新技术: 。制得的氢气可用于燃料电池。试回答下列问题:
。制得的氢气可用于燃料电池。试回答下列问题:
(1)分解海水时,_______ 能转变为_______ 能,二氧化钛作_______ 。水分解时,断裂的化学键为_______ 键,分解海水的反应属于_______ 反应(填“放热”或“吸热”)。
(2)火箭推进器中盛有强还原剂液态肼( )和强氧化剂液态双氧水。当它们混合反应时,即产生大量氯气和水蒸气,并放出大量热。已知1.6g液态肼在上述反应中放出64.22kJ的热量。
)和强氧化剂液态双氧水。当它们混合反应时,即产生大量氯气和水蒸气,并放出大量热。已知1.6g液态肼在上述反应中放出64.22kJ的热量。
①反应的热化学方程式为_______ 。
②此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是_______ 。
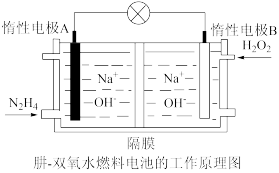
(3)肼-双氧水燃料电池由于其较高的能量密度而广受关注,其工作原理如图所示。则电池负极反应式为_______ 。
 )表面作用使海水分解得到复气的新技术:
)表面作用使海水分解得到复气的新技术: 。制得的氢气可用于燃料电池。试回答下列问题:
。制得的氢气可用于燃料电池。试回答下列问题:(1)分解海水时,
(2)火箭推进器中盛有强还原剂液态肼(
 )和强氧化剂液态双氧水。当它们混合反应时,即产生大量氯气和水蒸气,并放出大量热。已知1.6g液态肼在上述反应中放出64.22kJ的热量。
)和强氧化剂液态双氧水。当它们混合反应时,即产生大量氯气和水蒸气,并放出大量热。已知1.6g液态肼在上述反应中放出64.22kJ的热量。①反应的热化学方程式为
②此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是
(3)肼-双氧水燃料电池由于其较高的能量密度而广受关注,其工作原理如图所示。则电池负极反应式为

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】(1)在恒温、恒压的条件下,化学反应过程中吸收或释放的热量称为反应的焓变,用 表示,单位常采用
表示,单位常采用 ,在1200K、100KPa条件下,
,在1200K、100KPa条件下,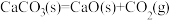
 ,若在此温度下,在一个恒容的容器中,将1mol固体碳酸钙完全分解需要吸收的热量
,若在此温度下,在一个恒容的容器中,将1mol固体碳酸钙完全分解需要吸收的热量___________ 180kJ(填“大于”、“等于”或“小于”)
(2)ⅰ.已知: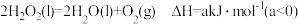
KI溶液可作为 分解反应的催化剂,催化过程按以下两步反应进行:
分解反应的催化剂,催化过程按以下两步反应进行:
Ⅰ.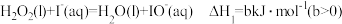
Ⅱ.___________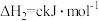
①请将上述过程补充完整___________ (提示:反应Ⅱ不是分解反应)。
②已知:相同条件下,反应Ⅰ的反应速率小于反应Ⅱ的反应速率。如图为未加催化剂时 分解反应的能量—反应历程示意图,请在图中画出加入KI溶液后该反应的能量-反应历程示意图。
分解反应的能量—反应历程示意图,请在图中画出加入KI溶液后该反应的能量-反应历程示意图。___________

ⅱ. 的水溶液呈弱酸性,其电离过程如下:
的水溶液呈弱酸性,其电离过程如下: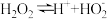 ;
;
某温度下,其电离平衡常数 ,物质的量浓度为10mol/L的
,物质的量浓度为10mol/L的 水溶液的
水溶液的
___________ 。(忽略 的二级电离及水的电离,当电离度
的二级电离及水的电离,当电离度 小于5%时,
小于5%时,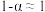 )。
)。
(3) 在水溶液中以多种水合铁离子形式存在,如
在水溶液中以多种水合铁离子形式存在,如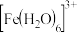 ,
,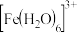 类似其他弱碱盐离子,其在水溶液中也会发生水解作用,具体如下:
类似其他弱碱盐离子,其在水溶液中也会发生水解作用,具体如下: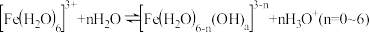 ;
;
实验室以0.50mol/L的棕黄色 溶液作为待测液,用色度计测定其透光率(透光率T是一个物理词汇,表示光线透过介质的能力,是透过透明或半透明物体的光通量与其入射光通量的百分率)。
溶液作为待测液,用色度计测定其透光率(透光率T是一个物理词汇,表示光线透过介质的能力,是透过透明或半透明物体的光通量与其入射光通量的百分率)。
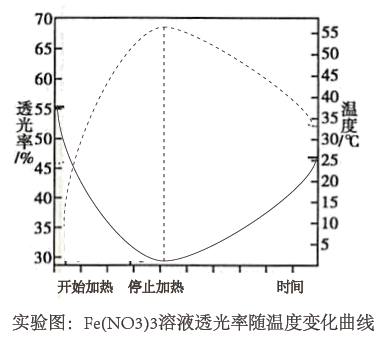
由实验分析可知,棕黄色离子是___________ (填“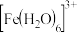 ”或“
”或“ ”)。
”)。
 表示,单位常采用
表示,单位常采用 ,在1200K、100KPa条件下,
,在1200K、100KPa条件下,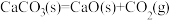
 ,若在此温度下,在一个恒容的容器中,将1mol固体碳酸钙完全分解需要吸收的热量
,若在此温度下,在一个恒容的容器中,将1mol固体碳酸钙完全分解需要吸收的热量(2)ⅰ.已知:
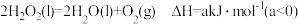
KI溶液可作为
 分解反应的催化剂,催化过程按以下两步反应进行:
分解反应的催化剂,催化过程按以下两步反应进行:Ⅰ.
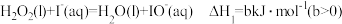
Ⅱ.___________
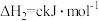
①请将上述过程补充完整
②已知:相同条件下,反应Ⅰ的反应速率小于反应Ⅱ的反应速率。如图为未加催化剂时
 分解反应的能量—反应历程示意图,请在图中画出加入KI溶液后该反应的能量-反应历程示意图。
分解反应的能量—反应历程示意图,请在图中画出加入KI溶液后该反应的能量-反应历程示意图。
ⅱ.
 的水溶液呈弱酸性,其电离过程如下:
的水溶液呈弱酸性,其电离过程如下: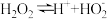 ;
;
某温度下,其电离平衡常数
 ,物质的量浓度为10mol/L的
,物质的量浓度为10mol/L的 水溶液的
水溶液的
 的二级电离及水的电离,当电离度
的二级电离及水的电离,当电离度 小于5%时,
小于5%时,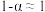 )。
)。(3)
 在水溶液中以多种水合铁离子形式存在,如
在水溶液中以多种水合铁离子形式存在,如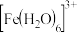 ,
,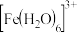 类似其他弱碱盐离子,其在水溶液中也会发生水解作用,具体如下:
类似其他弱碱盐离子,其在水溶液中也会发生水解作用,具体如下: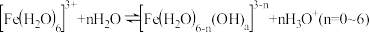 ;
;实验室以0.50mol/L的棕黄色
 溶液作为待测液,用色度计测定其透光率(透光率T是一个物理词汇,表示光线透过介质的能力,是透过透明或半透明物体的光通量与其入射光通量的百分率)。
溶液作为待测液,用色度计测定其透光率(透光率T是一个物理词汇,表示光线透过介质的能力,是透过透明或半透明物体的光通量与其入射光通量的百分率)。
由实验分析可知,棕黄色离子是
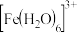 ”或“
”或“ ”)。
”)。
您最近一年使用:0次



