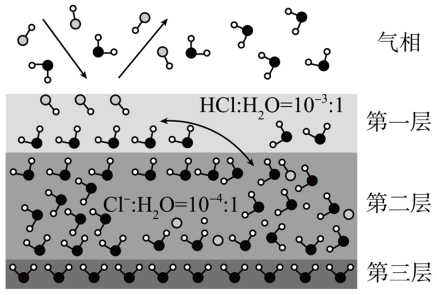
第VIA族元素的单质和化合物在生产、生活中有广泛应用。已知:分子中形成大π键的轨道必须垂直平面且相互平行,大π键可以表示为π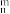 ,其中n代表大π键的原子数,m代表大π键的电子数,下列说法正确的是
,其中n代表大π键的原子数,m代表大π键的电子数,下列说法正确的是
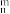 ,其中n代表大π键的原子数,m代表大π键的电子数,下列说法正确的是
,其中n代表大π键的原子数,m代表大π键的电子数,下列说法正确的是| A.在氧族气态氢化物中,H2Se的沸点最低 | B.SeO 和SeO3的空间结构相同 和SeO3的空间结构相同 |
C.SO 中的键角小于SO3中的键角 中的键角小于SO3中的键角 | D.噻吩( )含有的大π键为π )含有的大π键为π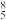 |
更新时间:2023-04-20 16:17:36
|
相似题推荐
单选题
|
困难
(0.15)
名校
【推荐1】如图是Na、Cu、Si、H、C、N等元素单质的熔点高低的顺序,其中c、d均是热和电的良导体。下列判断不正确的是
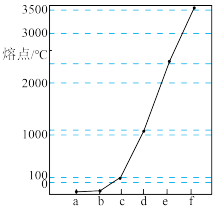

| A.图中对应的e、f单质晶体熔化时克服的是共价键 |
| B.d单质对应元素的电子排布式:1s22s22p63s23p2 |
| C.b元素形成的最高价含氧酸易与水分子之间形成氢键 |
| D.单质a、b、f对应的元素以原子个数比1∶1∶1形成的最简单分子中含2个σ键和2个π键 |
您最近一年使用:0次
单选题
|
困难
(0.15)
解题方法
【推荐2】研究者预想合成一个纯粹由氮组成的新物种—N5+N3-,若N5+离子中每个氮原子均满足8电子结构,以下有关N5+推测正确的是
| A.N5+有24个电子 | B.N5+离子中存在三对未成键的电子对 |
| C.N5+阳离子中存在两个氮氮三键 | D.N5+在水中可以稳定存在 |
您最近一年使用:0次
单选题
|
困难
(0.15)
名校
【推荐3】下列叙述正确的是
①配位键在形成时,是由成键双方各提供一个电子形成共用电子对
②C60晶体的晶胞是面心立方结构
③Ge是ⅣA族的一个主族元素,其核外电子排布式为Ge:[Ar]4s24p2,属于P区元素
④非极性分子往往是高度对称的分子,比如BF3,PCl5,H2O2,CO2这样的分子
⑤冰中存在极性共价键和氢键两种化学键的作用
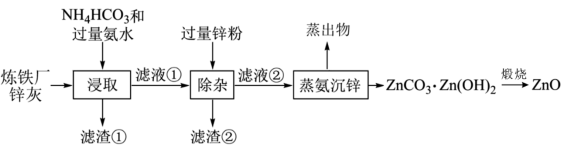
⑥Cu(OH)2是一种蓝色的沉淀,既溶于硝酸、浓硫酸,也能溶于氨水中
⑦熔融状态的HgCl2不能导电,HgCl2的稀溶液有弱的导电能力且可作手术刀的消毒液,从不同角度分类HgCl2是一种共价化合物、非电解质、盐、分子晶体
⑧氨水中大部分NH3与H2O以氢键(用“…”表示)结合成NH3·H2O分子,根据氨水的性质可知NH3·H2O的结构式为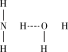
①配位键在形成时,是由成键双方各提供一个电子形成共用电子对
②C60晶体的晶胞是面心立方结构
③Ge是ⅣA族的一个主族元素,其核外电子排布式为Ge:[Ar]4s24p2,属于P区元素
④非极性分子往往是高度对称的分子,比如BF3,PCl5,H2O2,CO2这样的分子
⑤冰中存在极性共价键和氢键两种化学键的作用
⑥Cu(OH)2是一种蓝色的沉淀,既溶于硝酸、浓硫酸,也能溶于氨水中
⑦熔融状态的HgCl2不能导电,HgCl2的稀溶液有弱的导电能力且可作手术刀的消毒液,从不同角度分类HgCl2是一种共价化合物、非电解质、盐、分子晶体
⑧氨水中大部分NH3与H2O以氢键(用“…”表示)结合成NH3·H2O分子,根据氨水的性质可知NH3·H2O的结构式为
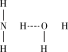
| A.②⑥ | B.②③ | C.⑤⑥ | D.③⑥ |
您最近一年使用:0次
单选题
|
困难
(0.15)
名校
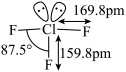
【推荐1】三氟化氯 是极强氧化剂,能发生自耦电离:
是极强氧化剂,能发生自耦电离: ,其分子结构如图所示,下列推测不合理的是
,其分子结构如图所示,下列推测不合理的是
 是极强氧化剂,能发生自耦电离:
是极强氧化剂,能发生自耦电离: ,其分子结构如图所示,下列推测不合理的是
,其分子结构如图所示,下列推测不合理的是
A. 分子的中心原子有5对价层电子对 分子的中心原子有5对价层电子对 |
B. 离子空间构型为正四面体 离子空间构型为正四面体 |
C. 与 与 反应生成 反应生成 和 和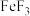 |
D.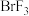 比 比 更易发生自耦电离 更易发生自耦电离 |
您最近一年使用:0次
单选题
|
困难
(0.15)
名校
【推荐1】锂离子电池中,一种电解质添加剂的阴离子结构如下图所示。Y、Z、M和R是原子序数依次增大的短周期元素。下列说法正确的是
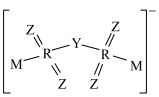
A.氧化性: | B.键角: |
| C.第一电离能:M>Z>Y | D.简单离子半径:R>Y>Z |
您最近一年使用:0次
单选题
|
困难
(0.15)
【推荐2】某储氢材料的晶胞结构如图所示,该晶体属立方晶系,晶胞棱边夹角均为 ,棱长为
,棱长为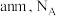 表示阿伏加德罗常数的值。下列说法错误的是
表示阿伏加德罗常数的值。下列说法错误的是

 ,棱长为
,棱长为 表示阿伏加德罗常数的值。下列说法错误的是
表示阿伏加德罗常数的值。下列说法错误的是
A. 的立体构型为三角锥形 的立体构型为三角锥形 |
B.晶胞中与 最近的 最近的 原子是8个 原子是8个 |
C.晶体中存在离子键、配位键和 键等作用力 键等作用力 |
D.晶体的密度为 |
您最近一年使用:0次
单选题
|
困难
(0.15)
名校
解题方法
【推荐1】某种阴离子结构如图所示,Q、W、X、Y、Z五种短周期元素的原子半径依次增大,基态Q原子的电子填充了3个能级,有4对成对电子,Z与其他元素不在同一周期。下列说法正确的是
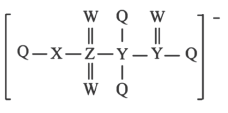
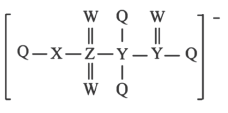
| A.Q和W形成的化合物中W为正价 | B.最简单氢化物的沸点: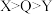 |
| C.Q、W、X的单质分子均为非极性分子 | D.同周期中第一电离能小于X的元素有4种 |
您最近一年使用:0次
单选题
|
困难
(0.15)
名校
解题方法
【推荐2】韩国首尔大学的科学家将水置于一个足够强的电场中,在20℃时,水分子瞬间凝固形成“暖冰”。下列关于“暖冰”的说法正确的是
| A.暖冰中水分子对称性由C2轴变为C∞ |
| B.在电场作用下,水分子间更易形成氢键,因而可以制得“暖冰” |
| C.暖冰中水分子的氧原子的杂化方式为sp3,氢键键能可达到250kJ/mol |
| D.水凝固形成20℃时的“暖冰”氢键键长有变化 |
您最近一年使用:0次

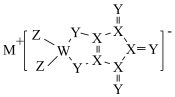
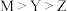
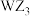 和
和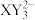 的空间结构不相同
的空间结构不相同