海洋资源的综合利用是21世纪海洋开发利用的重点发展领域之一。
I.海水提溴:“吹出法”是工业上常用的一种海水提溴技术,该技术主要流程如下:
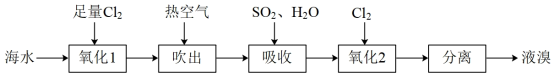
(1)吹出:热空气吹出溴是利用了___________ (填溴的一种物理性质)。
(2)吸收:吸收步骤中发生反应的化学方程式:___________ 。
(3)“吹出法”中的“吸收”及后续步骤的工艺也可采用如下流程:

写出上述步骤①中发生反应生成一种气体的离子方程式:___________ 。
II.海带提碘:从海带浸出液中提取碘的流程如下:
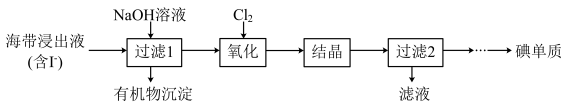
(4)实验室“过滤”操作通常使用的玻璃仪器包括烧杯、___________ 。
(5)“氧化”步骤发生反应的离子方程式为___________ 。
(6)设计简单的实验验证溴的非金属性比碘强。___________ 。(实验中须使用的试剂:溴水、KI溶液、CCl4)
I.海水提溴:“吹出法”是工业上常用的一种海水提溴技术,该技术主要流程如下:

(1)吹出:热空气吹出溴是利用了
(2)吸收:吸收步骤中发生反应的化学方程式:
(3)“吹出法”中的“吸收”及后续步骤的工艺也可采用如下流程:

写出上述步骤①中发生反应生成一种气体的离子方程式:
II.海带提碘:从海带浸出液中提取碘的流程如下:

(4)实验室“过滤”操作通常使用的玻璃仪器包括烧杯、
(5)“氧化”步骤发生反应的离子方程式为
(6)设计简单的实验验证溴的非金属性比碘强。
更新时间:2023-04-29 06:39:54
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】某同学利用以下装置探究非金属元素性质的递变规律,并验证氯气的性质。
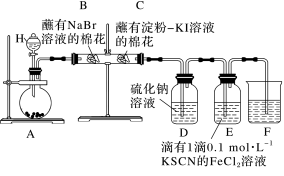
回答下列问题:
(1)仪器H的名称为_______ 。
(2)能说明氯气的氧化性强于溴的实验现象为_______ 。
(3)氯气进入D中,反应的离子方程式为_______ 。
(4)E中溶液先变为红色,后红色褪去,为探究E中溶液褪色的原因,该同学提出两种假设:
a.Fe3+被氧化;
b._______ 。
设计实验方案验证以上假设,向褪色后的溶液中滴加_______ ,若观察到_______ ,可验证假设b成立。
(5)实验结束后,在另一个蘸有淀粉-KI溶液的棉花G上滴加溴水,棉花G变蓝。通过以上实验可以得出的结论正确的是_______(填字母)。

回答下列问题:
(1)仪器H的名称为
(2)能说明氯气的氧化性强于溴的实验现象为
(3)氯气进入D中,反应的离子方程式为
(4)E中溶液先变为红色,后红色褪去,为探究E中溶液褪色的原因,该同学提出两种假设:
a.Fe3+被氧化;
b.
设计实验方案验证以上假设,向褪色后的溶液中滴加
(5)实验结束后,在另一个蘸有淀粉-KI溶液的棉花G上滴加溴水,棉花G变蓝。通过以上实验可以得出的结论正确的是_______(填字母)。
| A.氧化性:Cl2>Br2>I2 |
| B.同主族元素从上到下非金属性减弱 |
| C.同周期元素从左到右非金属性减弱 |
| D.Cl、Br、I对应含氧酸酸性逐渐减弱 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】下表列出了A-Ⅰ共9种元素在周期表中的位置:
请回答下列问题。
(1)常温下,元素F的最简单氢化物与单质A反应的化学方程式为_______ 。元素A和元素F可组成原子个数比为1:1的化合物,其电子式为_______ 。
(2)元素Ⅰ的原子半径在同周期主族元素中_______ (填“最大”或“最小”);元素F与氢元素组成的含10个电子的离子为_______ ;元素D、E对应的最简单氢化物可能形成分子间氢键的是_______ (写化学式,下同)。
(3)元素A、B、C的最高价氧化物对应的水化物具有两性的是_______ ,该物质与强碱反应的离子方程式为_______ 。
(4)下列事实不能说明G元素和H元素的非金属性强弱的是_______。
| 周期 | 族 | ||||||||
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ⅧA | ||
| 2 | D | E | F | ||||||
| 3 | A | B | C | G | H | ||||
| 4 | I | ||||||||
(1)常温下,元素F的最简单氢化物与单质A反应的化学方程式为
(2)元素Ⅰ的原子半径在同周期主族元素中
(3)元素A、B、C的最高价氧化物对应的水化物具有两性的是
(4)下列事实不能说明G元素和H元素的非金属性强弱的是_______。
| A.常温下,H单质与H2G的溶液反应,溶液变浑浊 |
| B.G和H两元素对应的简单氢化物的水溶性,后者强于前者 |
| C.G和H两元素对应的简单氢化物受热分解,前者的分解温度较低 |
| D.铁和G单质反应时,铁被氧化成+2价,而铁和H单质反应时,铁被氧化成+3价 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】下表为元素周期表的一部分:
请根据表中所列元素回答下列问题:
(1)F的原子结构示意图是_______ ,该元素单质可应用于_______ (填序号)。
①光导纤维②半导体材料③陶瓷材料
(2)表中元素N的符号为_______ ,元素M在周期表的位置为_______ 。
(3)G、K的最高价氧化物对应的水化物中,酸性较强的物质是_______ (写化学式)。
(4)E、B两元素的最高价氧化物的水化物反应的离子方程式为_______ 。
(5)对于H、I的氢化物,H的氢化物沸点较高,原因是_______ 。
(6)用电子式表示C和K形成化合物的过程:_______ ;由A、G、K三种元素可以形成一种离子化合物,此种离子化合物的电子式为_______ 。
(7)2022年2月2日北京冬奥会和冬残奥会火炬传递活动正式开始,本届冬奥会最大的特色之一就是“绿色环保”,所用火炬采用纯氢燃烧零碳排放,但是氢燃料的使用有一个“显而易见”的弊端,强光照射下火炬的火焰是“透明”的,这将严重影响火炬传递的观感,为了给火焰“上色”,团队采用加入含有B元素的盐,则“上色”后火焰的颜色为_______ 。
| A | |||||||||||||||||
| D | G | H | J | ||||||||||||||
| B | E | F | I | K | N | ||||||||||||
| C | M | L |
(1)F的原子结构示意图是
①光导纤维②半导体材料③陶瓷材料
(2)表中元素N的符号为
(3)G、K的最高价氧化物对应的水化物中,酸性较强的物质是
(4)E、B两元素的最高价氧化物的水化物反应的离子方程式为
(5)对于H、I的氢化物,H的氢化物沸点较高,原因是
(6)用电子式表示C和K形成化合物的过程:
(7)2022年2月2日北京冬奥会和冬残奥会火炬传递活动正式开始,本届冬奥会最大的特色之一就是“绿色环保”,所用火炬采用纯氢燃烧零碳排放,但是氢燃料的使用有一个“显而易见”的弊端,强光照射下火炬的火焰是“透明”的,这将严重影响火炬传递的观感,为了给火焰“上色”,团队采用加入含有B元素的盐,则“上色”后火焰的颜色为
您最近一年使用:0次
【推荐1】硫酸镍铵是重要的分析试剂和电镀材料。某矿渣的主要成分是NiFe2O4(铁酸镍)、NiO、FeO、CaO、SiO2等,图为从该矿渣中回收硫酸镍铵的工艺流程图。

已知:(NH4)2SO4在350℃以上会分解生成NH3和H2SO4;NiFe2O4在焙烧过程中生成NiSO4、Fe2(SO4)3;锡(Sn)位于第五周期IVA族;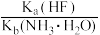 =2。
=2。
(1)焙烧前将矿渣与(NH4)2SO4混合研磨,混合研磨的目的是_______ 。常温下NH4F溶液中各离子浓度由大到小的顺序是_______ 。
(2)“浸泡”过程中由Fe2(SO4)3生成FeO(OH)的离子方程式为_______ ,“浸渣”的成分除Fe2O3、FeO(OH)外还含有_______ (填化学式)。
(3)“浸出液”中c(Ca2+)=1.0×10-3mol∙L-1,当钙率达到99%时,溶液中c(F-)=_______ mol∙L-1。[已知Ksp(CaF2)=4.0×10-11]
(4)为保证产品纯度,要检测“浸出液”的总铁量,需先将Fe3+还原为Fe2+:取一定体积的浸出液,用盐酸酸化后,再加入SnCl2,所需SnCl2的物质的量不少于“浸出液”中Fe3+的物质的量的_______ (填分数)。
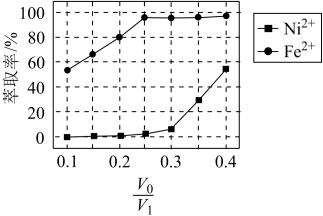
(5)本工艺中,萃取剂与溶液的体积比( )对溶液中Ni2+、Fe2+的萃取率的影响如图所示,
)对溶液中Ni2+、Fe2+的萃取率的影响如图所示, 的最佳取值是
的最佳取值是_______ 。

已知:(NH4)2SO4在350℃以上会分解生成NH3和H2SO4;NiFe2O4在焙烧过程中生成NiSO4、Fe2(SO4)3;锡(Sn)位于第五周期IVA族;
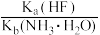 =2。
=2。(1)焙烧前将矿渣与(NH4)2SO4混合研磨,混合研磨的目的是
(2)“浸泡”过程中由Fe2(SO4)3生成FeO(OH)的离子方程式为
(3)“浸出液”中c(Ca2+)=1.0×10-3mol∙L-1,当钙率达到99%时,溶液中c(F-)=
(4)为保证产品纯度,要检测“浸出液”的总铁量,需先将Fe3+还原为Fe2+:取一定体积的浸出液,用盐酸酸化后,再加入SnCl2,所需SnCl2的物质的量不少于“浸出液”中Fe3+的物质的量的
(5)本工艺中,萃取剂与溶液的体积比(
 )对溶液中Ni2+、Fe2+的萃取率的影响如图所示,
)对溶液中Ni2+、Fe2+的萃取率的影响如图所示, 的最佳取值是
的最佳取值是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】某工厂利用废催化剂(含 及MnO2等)回收金属铜并制取锌白(
及MnO2等)回收金属铜并制取锌白( )的工艺流程如下:
)的工艺流程如下:

已知:
①
②
请回答下列问题:
(1)为了加快废催化剂酸浸的速率,可以采取的措施是______ (任写一条)。
(2)浸渣的主要成分是______ (填化学式,下同),粗铜粉中含有的杂质是______ 。
(3)“酸浸”过程中生成 ,同时还有氧气逸出,写出
,同时还有氧气逸出,写出 与浓
与浓 反应的化学方程式:
反应的化学方程式:______ 。
(4)“氧化”过程中 被氧化的离子方程式为
被氧化的离子方程式为______ 。
(5)加入氨水调节溶液 时,要使
时,要使 沉淀完全,则应调节溶液
沉淀完全,则应调节溶液 的最小值为
的最小值为______ (结果保留两位小数)(已知:当 时,认为
时,认为 沉淀完全;常温下
沉淀完全;常温下 ;
; )。
)。
(6)在加入氨水“中和、沉淀”的过程中,沉淀的析出率与溶液温度的关系如图所示:

当溶液温度高于 时,
时, 的沉淀率随着温度升高而降低的原因是
的沉淀率随着温度升高而降低的原因是______ 。
 及MnO2等)回收金属铜并制取锌白(
及MnO2等)回收金属铜并制取锌白( )的工艺流程如下:
)的工艺流程如下:
已知:
①

②

请回答下列问题:
(1)为了加快废催化剂酸浸的速率,可以采取的措施是
(2)浸渣的主要成分是
(3)“酸浸”过程中生成
 ,同时还有氧气逸出,写出
,同时还有氧气逸出,写出 与浓
与浓 反应的化学方程式:
反应的化学方程式:(4)“氧化”过程中
 被氧化的离子方程式为
被氧化的离子方程式为(5)加入氨水调节溶液
 时,要使
时,要使 沉淀完全,则应调节溶液
沉淀完全,则应调节溶液 的最小值为
的最小值为 时,认为
时,认为 沉淀完全;常温下
沉淀完全;常温下 ;
; )。
)。(6)在加入氨水“中和、沉淀”的过程中,沉淀的析出率与溶液温度的关系如图所示:

当溶液温度高于
 时,
时, 的沉淀率随着温度升高而降低的原因是
的沉淀率随着温度升高而降低的原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】铋酸钠( NaBiO3 )常用作分析试剂、氧化剂等,某同学在实验室用氯气氧化Bi(OH)2制取NaBiO3,并进行相关实验。已知NaBiO3固体不溶于冷水,能与沸水或酸溶液反应产生O2,在酸性条件下能将Mn2+氧化为 ;Bi(OH)3为白色难溶于水的固体。各实验装置如图所示:
;Bi(OH)3为白色难溶于水的固体。各实验装置如图所示:

请回答下列问题:
(1)装置的连接顺序是_____→_______→ ______→ _____(填字母)_________ 。
(2)C中装有的试剂是___________ ,若没有装置C,可能产生的影响是___________ 。
(3)反应开始时,打开K1和K2,B中Cl2发生的反应有;Cl2+2NaOH=NaClO+NaCl+H2O,______________________ (填化学方程式)。
(4)反应结束后,为从装置B中获得尽可能多的产品,需要进行的操作是___________ 、过滤、冷水洗涤、干燥。
(5)取上述NaBiO3产品w g,加入足量稀硫酸和MnSO4稀溶液使其完全反应,再用c mol·L-1的H2C2O4标准溶液滴定生成的 ,消耗V mL标准溶液。
,消耗V mL标准溶液。
①不能用c mol·L-1的H2C2O4标准溶液直接滴定NaBiO3的原因是___________ 。
②该产品的纯度为___________ (用含w 、c、V的代数式表示)。
(6)取少量B中反应后的悬浊液,加入稀硫酸,产生黄绿色气体,经检验气体中含有Cl2。该实验___________ (填“能”或“不能” )证明一定是NaBiO3氧化了Cl-,理由是___________ 。
 ;Bi(OH)3为白色难溶于水的固体。各实验装置如图所示:
;Bi(OH)3为白色难溶于水的固体。各实验装置如图所示:
请回答下列问题:
(1)装置的连接顺序是_____→_______→ ______→ _____(填字母)
(2)C中装有的试剂是
(3)反应开始时,打开K1和K2,B中Cl2发生的反应有;Cl2+2NaOH=NaClO+NaCl+H2O,
(4)反应结束后,为从装置B中获得尽可能多的产品,需要进行的操作是
(5)取上述NaBiO3产品w g,加入足量稀硫酸和MnSO4稀溶液使其完全反应,再用c mol·L-1的H2C2O4标准溶液滴定生成的
 ,消耗V mL标准溶液。
,消耗V mL标准溶液。①不能用c mol·L-1的H2C2O4标准溶液直接滴定NaBiO3的原因是
②该产品的纯度为
(6)取少量B中反应后的悬浊液,加入稀硫酸,产生黄绿色气体,经检验气体中含有Cl2。该实验
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】某化学研究性学习小组为了解从工业溴中提纯溴的方法,查阅了有关资料,Br2的沸点为59℃。微溶于水,有毒性和强腐蚀性。他们参观生产过程后,绘制了如下装置简图。
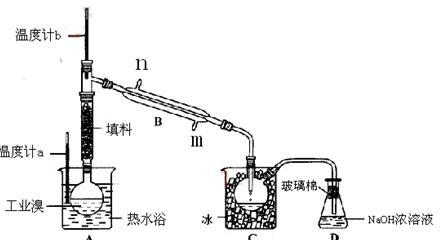
请你参与分析讨论:
①图中仪器B的名称:___ ,冷却水从_______ 进,________ 出;
②整套实验装置中仪器连接均不能用橡胶塞和橡胶管,其原因是____ 。
③实验装置气密性良好,要达到提纯溴的目的,操作中如何控制关键条件:__ 。
④C中液体产生颜色为____ ;
⑤烧杯A的作用_______________ , D中液体的作用是______________ 。

请你参与分析讨论:
①图中仪器B的名称:
②整套实验装置中仪器连接均不能用橡胶塞和橡胶管,其原因是
③实验装置气密性良好,要达到提纯溴的目的,操作中如何控制关键条件:
④C中液体产生颜色为
⑤烧杯A的作用
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】海水是宝贵的资源宝库,目前氯碱工业、海水提镁、海水提溴为人类提供了大量工业原料。下图是海水综合利用的部分流程图,据图回答问题:

(1)由海水晒制的粗盐中含有Ca2+、Mg2+、SO42-等离子,为除去这些离子,所加试剂及其先后顺序为(写化学式)______________________ 。
(2)①电解饱和食盐水的化学反应方程式为______________ 。
②制取MgCl2的过程中涉及反应:MgCl2·6H2O MgCl2+6H2O,该反应要在HCl气氛中进行,原因是
MgCl2+6H2O,该反应要在HCl气氛中进行,原因是_______________ 。
(3)苦卤中通入Cl2置换出Br2,吹出后用SO2吸收,写出用SO2吸收发生的离子方程式_________ ,由此判断Cl2、Br2、SO2的氧化性由强到弱的顺序为__________________ 。
(4)也有工艺是在吹出Br2后用碳酸钠溶液吸收,形成溴化钠和溴酸钠,同时有CO2放出。该反应的离子方程式是_____________ ;最后再用H2SO4处理得到Br2,之后加入CCl4进行Br2的萃取,最终用_____________ 方法得到单质Br2。

(1)由海水晒制的粗盐中含有Ca2+、Mg2+、SO42-等离子,为除去这些离子,所加试剂及其先后顺序为(写化学式)
(2)①电解饱和食盐水的化学反应方程式为
②制取MgCl2的过程中涉及反应:MgCl2·6H2O
 MgCl2+6H2O,该反应要在HCl气氛中进行,原因是
MgCl2+6H2O,该反应要在HCl气氛中进行,原因是(3)苦卤中通入Cl2置换出Br2,吹出后用SO2吸收,写出用SO2吸收发生的离子方程式
(4)也有工艺是在吹出Br2后用碳酸钠溶液吸收,形成溴化钠和溴酸钠,同时有CO2放出。该反应的离子方程式是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】海洋资源的利用具有非常广阔的前景,从海水中可提取多种化工原料。
Ⅰ.如图是从海水中提取镁的简单流程,回答下列问题:

(1)工业上常用于沉淀 的试剂A是
的试剂A是___________ ,操作A的名称是___________ 。
(2)由无水 制取Mg的化学方程式是
制取Mg的化学方程式是___________ 。
Ⅱ.海水中Br含量为 ,工业上常用“吹出法”从海水中提溴,工艺流程示意图如图,回答下列问题:
,工业上常用“吹出法”从海水中提溴,工艺流程示意图如图,回答下列问题:
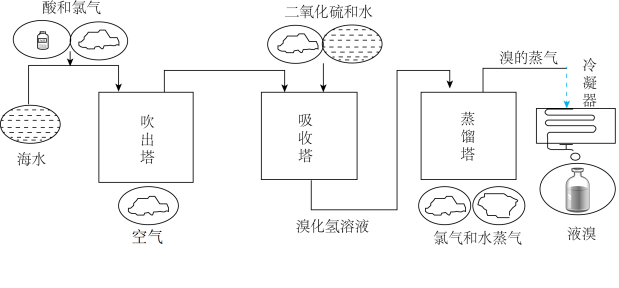
(3)鼓入热空气将生成的溴吹出,利用了 的
的___________ 性。
(4)吸收塔中 的吸收率可达95%,吸收塔中主要反应的方程式是
的吸收率可达95%,吸收塔中主要反应的方程式是 。也有工艺是在吹出
。也有工艺是在吹出 后用碳酸钠溶液吸收,生成溴化钠和溴酸钠,该反应的离子方程式是
后用碳酸钠溶液吸收,生成溴化钠和溴酸钠,该反应的离子方程式是___________ 。
Ⅲ.海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计如下实验:

(5)步骤①中灼烧海带时,应将海带放入___________ (填仪器名称)中灼烧。
(6)步骤④发生的离子反应方程式为___________ 。
(7)实验室常用碘量法测定溶液中 的含量。取200mL样品,加入
的含量。取200mL样品,加入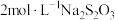 溶液,发生反应
溶液,发生反应 ,充分反应后,消耗
,充分反应后,消耗 溶液100mL。则该样品中
溶液100mL。则该样品中 的含量是
的含量是___________  。
。
Ⅰ.如图是从海水中提取镁的简单流程,回答下列问题:

(1)工业上常用于沉淀
 的试剂A是
的试剂A是(2)由无水
 制取Mg的化学方程式是
制取Mg的化学方程式是Ⅱ.海水中Br含量为
 ,工业上常用“吹出法”从海水中提溴,工艺流程示意图如图,回答下列问题:
,工业上常用“吹出法”从海水中提溴,工艺流程示意图如图,回答下列问题:
(3)鼓入热空气将生成的溴吹出,利用了
 的
的(4)吸收塔中
 的吸收率可达95%,吸收塔中主要反应的方程式是
的吸收率可达95%,吸收塔中主要反应的方程式是 。也有工艺是在吹出
。也有工艺是在吹出 后用碳酸钠溶液吸收,生成溴化钠和溴酸钠,该反应的离子方程式是
后用碳酸钠溶液吸收,生成溴化钠和溴酸钠,该反应的离子方程式是Ⅲ.海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计如下实验:

(5)步骤①中灼烧海带时,应将海带放入
(6)步骤④发生的离子反应方程式为
(7)实验室常用碘量法测定溶液中
 的含量。取200mL样品,加入
的含量。取200mL样品,加入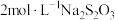 溶液,发生反应
溶液,发生反应 ,充分反应后,消耗
,充分反应后,消耗 溶液100mL。则该样品中
溶液100mL。则该样品中 的含量是
的含量是 。
。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
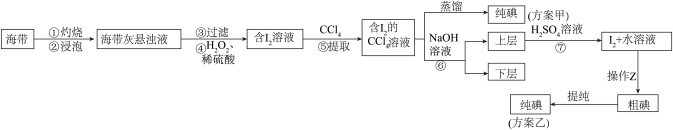
【推荐1】I.实验室从海藻中提取碘的流程如下:回答下列问题:
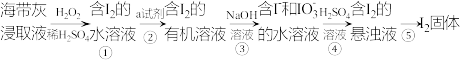
(1)实验室灼烧海带的主要仪器有酒精灯、三脚架、泥三角、玻璃棒、_________________ 。
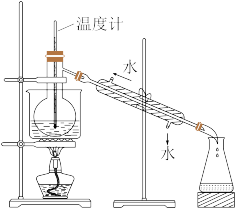
(2)从含碘的有机溶液中提取碘和回收有机溶剂还需经过蒸馏,指出右图实验装置中的错误之处:①__ ;②______ ;③_______ 。
(3)步骤④中反应的离子方程式为________ , 在此反应中,每生成38.1gI2转移_____ mol电子。
(4)上述流程中,含I2的水溶液经3步转化为含I2的悬浊液,主要目的是____________ 。
II.如图是某工厂对海水资源进行综合利用的示意图。回答下列问题:

(5)①若要验证所得无水MgCl2中不含NaCl,最简单的操作方法及步骤是______________ 。
②操作b是在通入HCl的氛围中进行,否则会生成Mg(OH)2,写出生成Mg(OH)2的化学方程式:____ 。
(6)金属镁的制备方程式为________ 。
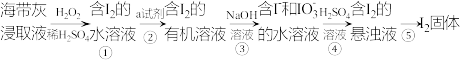
(1)实验室灼烧海带的主要仪器有酒精灯、三脚架、泥三角、玻璃棒、
(2)从含碘的有机溶液中提取碘和回收有机溶剂还需经过蒸馏,指出右图实验装置中的错误之处:①

(3)步骤④中反应的离子方程式为
(4)上述流程中,含I2的水溶液经3步转化为含I2的悬浊液,主要目的是
II.如图是某工厂对海水资源进行综合利用的示意图。回答下列问题:

(5)①若要验证所得无水MgCl2中不含NaCl,最简单的操作方法及步骤是
②操作b是在通入HCl的氛围中进行,否则会生成Mg(OH)2,写出生成Mg(OH)2的化学方程式:
(6)金属镁的制备方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】海带中含有碘元素,从海带中提取碘的实验过程如图所示。
(1)步骤①会用到下列仪器中的_____(填字母)。
(2)海带灰悬浊液含有 。步骤④的试剂选用
。步骤④的试剂选用 、稀硫酸,离子方程式是
、稀硫酸,离子方程式是______ 。
(3)检验步骤④产生了 的方法是
的方法是______ 。
(4)过程⑤⑥⑦的目的是______ 。
(5)下列说法正确的是______。
(6)方案甲中采用蒸馏分离效果不佳,原因是______ ;方案乙中操作 的名称是
的名称是______ 。

(1)步骤①会用到下列仪器中的_____(填字母)。
| A.酒精灯 | B.漏斗 | C.坩埚 | D.泥三角 |
 。步骤④的试剂选用
。步骤④的试剂选用 、稀硫酸,离子方程式是
、稀硫酸,离子方程式是(3)检验步骤④产生了
 的方法是
的方法是(4)过程⑤⑥⑦的目的是
(5)下列说法正确的是______。
| A.为提高④中反应的速率,可增大硫酸浓度或在高温条件下进行 |
B.操作⑤中 ,可用酒精、苯等代替 ,可用酒精、苯等代替 |
| C.操作⑥,得到的上层溶液为紫红色 |
D.操作 所需的玻璃仪器有烧杯、玻璃棒、漏斗 所需的玻璃仪器有烧杯、玻璃棒、漏斗 |
 的名称是
的名称是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】海带中含有丰富的碘,为了从海带中提取碘,某研究性学习小组设计并进行了如图所示的实验:
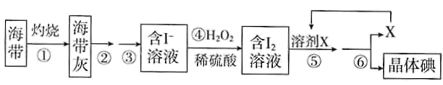
请回答下列问题:
(1)实验时灼烧海带应在________ (填仪器名称)内进行。
(2)步骤④中反应的离子方程式是____________ 。
(3)步骤⑤中选用的溶剂X可以是________ (填试剂名称)。
(4)上述流程中的实验操作包括下列选项中________ (按操作顺序选填代号)。
A.过滤 B.蒸发 C.蒸馏 D.分液
(5)请设计一个简单的实验方案,检验步骤⑤提取碘后的溶液中是否还含有单质碘_______________ 。

请回答下列问题:
(1)实验时灼烧海带应在
(2)步骤④中反应的离子方程式是
(3)步骤⑤中选用的溶剂X可以是
(4)上述流程中的实验操作包括下列选项中
A.过滤 B.蒸发 C.蒸馏 D.分液
(5)请设计一个简单的实验方案,检验步骤⑤提取碘后的溶液中是否还含有单质碘
您最近一年使用:0次



