(CN)2具有与卤素单质相似的化学性质。 在常温下能与Cu反应生成致密的氟化物薄膜,还能与熔融的
在常温下能与Cu反应生成致密的氟化物薄膜,还能与熔融的 反应生成硫酰氟(
反应生成硫酰氟( )。
)。 与浓硫酸反应可制得HF,常温下,测得氟化氢的相对分子质量约为37。下列说法不正确的是
与浓硫酸反应可制得HF,常温下,测得氟化氢的相对分子质量约为37。下列说法不正确的是
 在常温下能与Cu反应生成致密的氟化物薄膜,还能与熔融的
在常温下能与Cu反应生成致密的氟化物薄膜,还能与熔融的 反应生成硫酰氟(
反应生成硫酰氟( )。
)。 与浓硫酸反应可制得HF,常温下,测得氟化氢的相对分子质量约为37。下列说法不正确的是
与浓硫酸反应可制得HF,常温下,测得氟化氢的相对分子质量约为37。下列说法不正确的是| A.(CN)2是由极性键构成的极性分子 |
B. 、 、 中心原子的杂化方式均为 中心原子的杂化方式均为 |
| C.常温下,氟化氢可能以(HF)2子的形式存在 |
D. 与熔融 与熔融 反应时一定有氧元素化合价升高 反应时一定有氧元素化合价升高 |
2023·江苏南通·模拟预测 查看更多[2]
更新时间:2023-05-27 14:23:09
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列有关分子的结构和性质的说法正确的是
| A.H2O2和C2H2均为直线形的非极性分子 |
B. 和 和 的空间结构均为平面三角形 的空间结构均为平面三角形 |
| C.邻羟基苯甲酸沸点比对羟基苯甲酸沸点高 |
| D.H2S和NH3均是极性分子,且H2S分子的键角较小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】氨气是一种重要的化工原料,极易溶于水,合成氨反应为N2(g)+3H2(g)=2NH3(g)  =-92.4kJ•mol-1。下列说法正确的是
=-92.4kJ•mol-1。下列说法正确的是
 =-92.4kJ•mol-1。下列说法正确的是
=-92.4kJ•mol-1。下列说法正确的是A.键角:H2O>NH3>NH |
B.相同浓度的氨水和 溶液中,水的电离程度相同 溶液中,水的电离程度相同 |
C.合成氨反应的 =E(N≡N)+3E(H-H)-6E(N-H)(E表示键能) =E(N≡N)+3E(H-H)-6E(N-H)(E表示键能) |
| D.1molN2与足量H2发生合成氨反应,放出的热量为92.4kJ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】酚试纸MBTH可用来检测甲醛,涉及的反应如图所示,下列说法正确的是
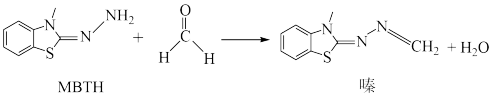
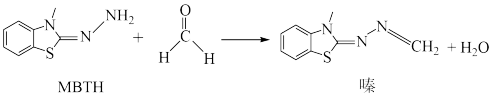
| A.MBTH中元素的电负性:C>N>H | B.“嗪”中的C原子均为 杂化 杂化 |
| C.甲醛的VSEPR模型为四面体形 | D.“嗪”中存在 键和π键 键和π键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】H与O可以形成H2O和H2O2两种化合物其中H2O2的分子结构如图所示,H+可与H2O形成H3O+。下列说法错误的是

A. 分子中两个 分子中两个 原子均采取 原子均采取 杂化轨道成键 杂化轨道成键 |
B.相同条件下, 在水中的溶解度大于在 在水中的溶解度大于在 中的溶解度 中的溶解度 |
C.液态水中的作用力由强到弱的顺序是:氢键 范德华力 范德华力 |
D. 的空间结构为三角锥形 的空间结构为三角锥形 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列各组分子均属于非极性分子的是( )
①H2S ②CO2 ③HCl ④CCl4 ⑤NH3 ⑥CO ⑦BF3 ⑧HClO
①H2S ②CO2 ③HCl ④CCl4 ⑤NH3 ⑥CO ⑦BF3 ⑧HClO
| A.①④⑧ | B.②③⑥ | C.②④⑦ | D.④⑤⑧ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法中不正确的是
| A.硫难溶于水,微溶于酒精,易溶于CS2,说明分子极性:H2O>C2H5OH>CS2 |
| B.CCl2F2无同分异构体,说明其中碳原子采取sp3杂化 |
| C.H2O的熔沸点比H2S的熔沸点高是因为H—O比H—S更稳定 |
| D.由第ⅠA族和第ⅥA族元素形成的原子个数比为1∶1、电子总数为38的化合物,是含有共价键的离子化合物 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】短周期非金属元素X、Y、Z、W的原子序数依次增大,基态X原子的未成对电子数是其所在周期中最多的,基态W原子的电子总数是其最高能级电子数的4倍,这四种元素与 元素组成的化合物的结构如图所示,下列说法错误的是
元素组成的化合物的结构如图所示,下列说法错误的是
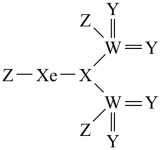
 元素组成的化合物的结构如图所示,下列说法错误的是
元素组成的化合物的结构如图所示,下列说法错误的是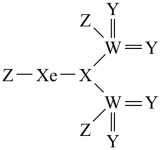
A.简单氢化物的沸点: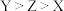 | B. 和 和 的VSEPR模型不同 的VSEPR模型不同 |
C.第一电离能: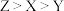 | D.同浓度时,最高价含氧酸的 : : |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】关于氢键,下列说法正确的是
| A.氢键比分子间作用力强,所以它属于化学键 |
| B.冰中存在氢键,水中不存在氢键 |
| C.分子间形成的氢键使物质的熔点和沸点升高 |
| D.H2O是一种非常稳定的化合物,这是由于氢键所致 |
您最近一年使用:0次

 为阿伏加德罗常数的值。下列说法错误的是
为阿伏加德罗常数的值。下列说法错误的是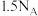

 中P的价层电子对数为
中P的价层电子对数为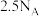
 和22.4L
和22.4L (均为标准状况)在光照下充分反应后的分子数为
(均为标准状况)在光照下充分反应后的分子数为 (金刚石)
(金刚石) 可实现人工合成金刚石。下列关于该反应的说法不正确的是
可实现人工合成金刚石。下列关于该反应的说法不正确的是
 。下列说法正确的是
。下列说法正确的是 分子间可形成氢键,沸点高于
分子间可形成氢键,沸点高于
 的电子式是
的电子式是
 晶体是离子晶体,仅含离子键
晶体是离子晶体,仅含离子键 晶体属于共价晶体
晶体属于共价晶体

