下列说法中不正确的是
| A.硫难溶于水,微溶于酒精,易溶于CS2,说明分子极性:H2O>C2H5OH>CS2 |
| B.CCl2F2无同分异构体,说明其中碳原子采取sp3杂化 |
| C.H2O的熔沸点比H2S的熔沸点高是因为H—O比H—S更稳定 |
| D.由第ⅠA族和第ⅥA族元素形成的原子个数比为1∶1、电子总数为38的化合物,是含有共价键的离子化合物 |
更新时间:2024-02-14 22:24:21
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列叙述错误的是
①共价键没有方向性和饱和性,而离子键有方向性和饱和性
②金属键的实质是金属中的“自由电子”与金属阳离子形成的一种强烈的相互作用
③配位键在形成时,是由成键双方各提供一个电子形成共用电子对
④在晶体硅中,既有非极性键,又有范德华力
⑤化合物 和
和 都存在配位键
都存在配位键
⑥NaCl、HF、 、
、 都易溶于水,但原因不完全相同
都易溶于水,但原因不完全相同
①共价键没有方向性和饱和性,而离子键有方向性和饱和性
②金属键的实质是金属中的“自由电子”与金属阳离子形成的一种强烈的相互作用
③配位键在形成时,是由成键双方各提供一个电子形成共用电子对
④在晶体硅中,既有非极性键,又有范德华力
⑤化合物
 和
和 都存在配位键
都存在配位键⑥NaCl、HF、
 、
、 都易溶于水,但原因不完全相同
都易溶于水,但原因不完全相同| A.①②④ | B.①③④ | C.①③⑤ | D.④⑤⑥ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】质子离子液体具有高质子电导率以及优异的电化学和热稳定性,某质子离子液体的结构如图所示,下列说法错误的是
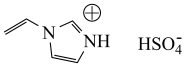

| A.上述离子液体固态时,含有极性共价键、配位键和离子键 |
B.阴离子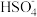 中S原子为sp3杂化 中S原子为sp3杂化 |
| C.第一电离能:S<O<N |
| D.C、N、O形成的简单氢化物的沸点均为所在主族最高的 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列化学用语正确的是
A.质量数为37的氯原子: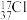 |
B.甲烷分子构型为正四面体、非极性分子,其球棍模型: |
C.反应: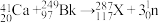 ,不属于化学变化 ,不属于化学变化 |
D.Mg和Cl形成离子键的过程: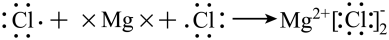 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】BF3与一定量的水形成(H2O)2•BF3,一定条件下(H2O)2•BF3可发生如图转化,下列说法正确的是
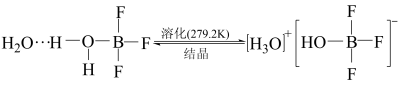
A.BF3和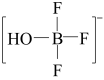 中B原子均采用sp2杂化轨道成键 中B原子均采用sp2杂化轨道成键 |
| B.(H2O)2•BF3分子中存在氢键和配位键 |
| C.(H2O)2•BF3中的所有元素都位于元素周期表中的p区 |
| D.BF3、NF3分子中的原子个数比相同,两者都是极性分子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列说法中错误的是
| A.卤化氢中,以HF沸点最高,是由于HF分子间存在氢键 |
| B.邻羟基苯甲醛的熔、沸点比对羟基苯甲醛的熔、沸点低 |
| C.H2O的沸点比HF的沸点高,是由于水中氢键键能大 |
| D.氢键X—H…Y的三个原子不一定在一条直线上 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】物质结构决定性质。下列有关物质性质的解释错误的是
| 选项 | 物质性质 | 解释 |
| A |  用作面包膨松剂 用作面包膨松剂 |  中和酸,且受热分解产生气体 中和酸,且受热分解产生气体 |
| B |  中的配位原子是C原子 中的配位原子是C原子 | C的电负性比O小 |
| C | 金刚石比晶体硅的熔点高 | C的原子半径比 小 小 |
| D |  稳定性大于 稳定性大于 |  分子间可以形成氢键 分子间可以形成氢键 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

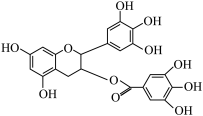
 易溶于
易溶于 ,可从
,可从 溶于氨水,是由于
溶于氨水,是由于 反应生成了可溶性配合物
反应生成了可溶性配合物
 能导电,是由于熔融状态下产生了自由移动的
能导电,是由于熔融状态下产生了自由移动的 和
和


