BF3与一定量的水形成(H2O)2•BF3,一定条件下(H2O)2•BF3可发生如图转化,下列说法正确的是
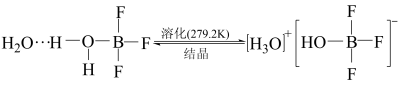
A.BF3和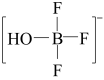 中B原子均采用sp2杂化轨道成键 中B原子均采用sp2杂化轨道成键 |
| B.(H2O)2•BF3分子中存在氢键和配位键 |
| C.(H2O)2•BF3中的所有元素都位于元素周期表中的p区 |
| D.BF3、NF3分子中的原子个数比相同,两者都是极性分子 |
更新时间:2024-02-26 18:42:23
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】EDTA(乙二胺四乙酸)结构简式如图所示,关于化合物 的说法正确的是
的说法正确的是
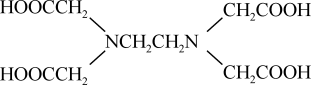
 的说法正确的是
的说法正确的是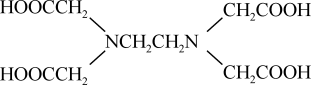
| A.1 mol EDTA中含4mol π键 |
B.EDTA中碳原子的杂化轨道类型为 、 、 、 、 |
C.EDTA组成元素的第一电离能顺序为 |
D. 中所含的化学键有离子键、共价键、配位键和氢键 中所含的化学键有离子键、共价键、配位键和氢键 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】工业上制取冰晶石(Na3AlF6)的化学方程式如下:
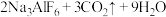 ,下列说法正确的是
,下列说法正确的是

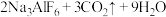 ,下列说法正确的是
,下列说法正确的是| A.Na3AlF6为离子晶体 | B. 中Al3+为配体,接受孤电子对 中Al3+为配体,接受孤电子对 |
| C.CO2中碳原子为sp2杂化 | D.熔沸点:HF>H2O |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】汽车尾气中的氮氧化物、碳氢化物与臭氧反应是造成城市光化学污染的主要原因,其中常见的反应为CH3CH=CHCH3(2—丁烯)+2O3→2CH3CHO+2O2,已知NA为阿伏加德罗常数的值,下列有关说法正确的是
| A.CH3CHO和CH3CH=CHCH3分子中采取sp2杂化和sp3杂化的碳原子数目之比均为1:1 |
| B.O2和O3均为非极性分子 |
| C.标准状况下,2.24L CH3CH2OH中所含原子数目为0.7NA |
| D.若有2mol O3参与反应,则反应中转移的电子数目为12NA |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】肼(N2H4)分子可视为NH3分子中的一个氢原子被-NH2(氨基)取代形成的。肼可用于火箭燃料,燃烧时发生的反应为N2O4(l)+2N2H4(l)=3N2(g)+4H2O(g)。下列说法正确的是
| A.上述反应为熵减反应 | B.离子 中含有配位键 中含有配位键 |
| C.0.5 mol N2中含有0.5 molπ键 | D.H2O的中心原子价层电子对数为2 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】2021年9月24日《科学》杂志发表了我国科学家的原创性重大突破,首次在实验室实现从CO2到淀粉的全合成。其合成路线如下:
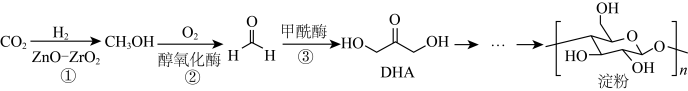
下列说法错误的是

下列说法错误的是
A.电负性: |
| B.甲醇分子中H-C-O键角大于甲醛分子中H-C-O键角 |
| C.DHA分子间存在氢键 |
D.Zn溶于氨水形成配合物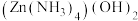 , , 的配位数为4 的配位数为4 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】X、Y、Z、W是四种原子序数依次增大的前20号主族元素,Y原子的最外层电子数为其内层电子数的2倍;Z原子的最外层电子数等于Y原子的核外电子数;W原子的半径是前20号主族元素中最大的,四种元素原子序数之和为34。下列说法错误的是
| A.X与W同主族 |
| B.最简单氢化物的稳定性:Y>Z |
| C.Y、Z的单质均有同素异形体 |
| D.Y与Z可以形成含有极性键的非极性分子 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】氮化硼(BN)是一种重要的功能陶瓷材料。以天然硼砂为起始物,经过一系列反应可以得到BF3和BN,如图所示。下列叙述正确的是
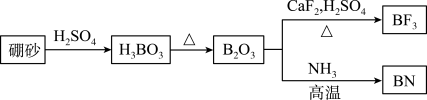
| A.NH3与BF3都是由极性键构成的极性分子 |
| B.六方氮化硼在高温高压下,可以转化为立方氮化硼,其结构与金刚石相似,立方氮化硼晶胞中含有4个氮原子、4个硼原子 |
| C.NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一,lmolNH4BF4含有配位键的数目为NA |
| D.立方氮化硼和半导体材料氮化铝的结构均类似于金刚石,立方氮化硼的熔点小于氮化铝 |
您最近半年使用:0次



