碳族元素及其化合物有十分丰富的化学性质,请回答:
(1)在有机反应中有许多活性中间体,如在异丁烯与水加成中生成的(CH3)3C+,其中C存在的杂化方式_______ ,其中C+的VSEPR模型是_______ ;在有机化合物中碳上的氢的酸性可由pK描述,K为该氢的电离平衡常数,则CCl3H与CF3H中pK较大的是_______ ,理由是_______ 。
(2)碱金属M( ,
, ,
, 等)可与石墨和
等)可与石墨和 形成化合物。
形成化合物。 与
与 作用形成的
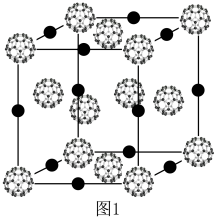
作用形成的 具有三维超导性能,图1为其晶胞,该晶体类型是
具有三维超导性能,图1为其晶胞,该晶体类型是_______ 。
(3)石墨可看成碳层的叠加,六方石墨是abab……的两层循环,三方石墨是abcabc……(a、b、c表示不同的碳层)的三层循环,图2中属于六方石墨的是_______ :石墨与钾蒸汽作用可形成石墨夹层离子化合物,图3所示的化合物的化学式是_______ 。

(4)硅也可形成的一系列氢化物,如甲硅烷能与 猛烈反应,在空气中可以自燃,请说明硅烷化学性质比相应的烷烃活泼的原因
猛烈反应,在空气中可以自燃,请说明硅烷化学性质比相应的烷烃活泼的原因_______ 。
(1)在有机反应中有许多活性中间体,如在异丁烯与水加成中生成的(CH3)3C+,其中C存在的杂化方式
(2)碱金属M(
 ,
, ,
, 等)可与石墨和
等)可与石墨和 形成化合物。
形成化合物。 与
与 作用形成的
作用形成的 具有三维超导性能,图1为其晶胞,该晶体类型是
具有三维超导性能,图1为其晶胞,该晶体类型是
(3)石墨可看成碳层的叠加,六方石墨是abab……的两层循环,三方石墨是abcabc……(a、b、c表示不同的碳层)的三层循环,图2中属于六方石墨的是

(4)硅也可形成的一系列氢化物,如甲硅烷能与
 猛烈反应,在空气中可以自燃,请说明硅烷化学性质比相应的烷烃活泼的原因
猛烈反应,在空气中可以自燃,请说明硅烷化学性质比相应的烷烃活泼的原因
更新时间:2023-06-01 14:59:54
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
【推荐1】20世纪初,哈伯和博施开发了以 和
和 为原料合成氨工艺,目前该工艺仍在广泛使用。
为原料合成氨工艺,目前该工艺仍在广泛使用。
(1)关于哈伯和博施法工业合成氨的说法正确的是___________。
(2)关于 说法正确的是___________。
说法正确的是___________。
(3)氮的氢化物 与
与 反应
反应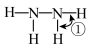

 ,比较键角①
,比较键角①___________ ②(填“>”、“<”或“=”),请说明理由___________ 。
 和
和 为原料合成氨工艺,目前该工艺仍在广泛使用。
为原料合成氨工艺,目前该工艺仍在广泛使用。(1)关于哈伯和博施法工业合成氨的说法正确的是___________。
| A.采用温度为500℃有利于反应正向进行 |
| B.尾气处理利用氨气极易溶于水的性质 |
| C.合成氨工业中利用了热交换器,实现绿色低碳化 |
D.理论上通过该反应 、 、 可以判断该反应常温下不能自发 可以判断该反应常温下不能自发 |
(2)关于
 说法正确的是___________。
说法正确的是___________。A. 遇到HCl产生白雾 遇到HCl产生白雾 | B.利用 受热分解可制得 受热分解可制得 |
C. 可用湿润的红色石蕊试纸检验 可用湿润的红色石蕊试纸检验 | D. 分子间易形成氢键,故 分子间易形成氢键,故 极易溶于水 极易溶于水 |
(3)氮的氢化物
 与
与 反应
反应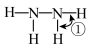

 ,比较键角①
,比较键角①
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】钙钛矿( CaTiO3)型化合物是一类可用于生产太阳能电池、传感器、固体电阻器等的功能材料。回答下列问题:
(1)元素Ca的焰色为_______ 色。
(2)下列状态的Ca中,电离最外层一个电子所需能量最大的是________ (填标号)。
A.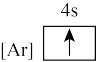 B.
B. 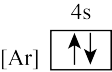 C.
C. 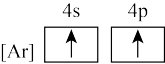 D.
D. 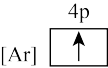
(3)TiCl4的熔、沸点分别为205K、409K,均高于CCl4,主要原因是_______ 。
(4)TiCl4溶于浓盐酸得到H2[TiCl6]溶液,再向溶液中加入NH4Cl浓溶液可析出黄色的(NH4)2[TiCl6]晶体。该晶体中微观粒子之间的作用力不含有______ 。
A.离子键 B.共价键 C.分子间作用力 D.氢键 E.配位键
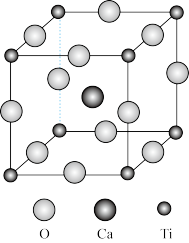
(5)CaTiO3的晶胞如图所示,边长为a nm,晶胞中Ca、Ti、O分别处于体心、顶点、棱心位置,与Ti紧邻的O形成的空间结构为_________ ,O与Ca间最短距离为_______ 。
(6)CaTiO3晶胞结构的另一种表示中,Ti处于体心位置,则Ca处于_______ 位置,O处于________ 位置。
(1)元素Ca的焰色为
(2)下列状态的Ca中,电离最外层一个电子所需能量最大的是
A.
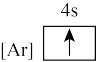 B.
B.  C.
C.  D.
D. 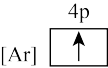
(3)TiCl4的熔、沸点分别为205K、409K,均高于CCl4,主要原因是
(4)TiCl4溶于浓盐酸得到H2[TiCl6]溶液,再向溶液中加入NH4Cl浓溶液可析出黄色的(NH4)2[TiCl6]晶体。该晶体中微观粒子之间的作用力不含有
A.离子键 B.共价键 C.分子间作用力 D.氢键 E.配位键
(5)CaTiO3的晶胞如图所示,边长为a nm,晶胞中Ca、Ti、O分别处于体心、顶点、棱心位置,与Ti紧邻的O形成的空间结构为
(6)CaTiO3晶胞结构的另一种表示中,Ti处于体心位置,则Ca处于

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】铍及其化合物的应用正日益被重视。
(l)最重要的含铍矿物是绿柱石,含2%铬(Cr)的绿柱石即为祖母绿。基态Cr原子价电子排布图为__________ 。
(2)铍与相邻主族的铝元素性质相似。下列有关铍和铝的叙述正确的有_____ (填标号)。
A.铍属于s区主族元素 B.电负性都比镁大
C.铝的第一电离能比镁小 D.氯化物的水溶液pH均大于7
(3)铍、铝晶体都是由金属原子密置层在三维空间堆积而成(最密堆积)。铍的熔点(155lK)比铝的熔点(930K)高,原因是_______________________________________________________ 。
(4)氯化铍在气态时存在BeC12分子(a)和二聚分子(BeCl2)2(b),固态时则具有如下图所示的链状结构(c)。
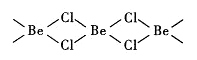
①a属于__________ (填“极性”或“非极性”)分子。
②b中Be原子的杂化方式相同,且所有原子都在同一平面上。b 的结构式为____________________ (标出配位键)。
③c中Be原子的杂化方式为__________ 。
④氯化铍晶体(c)中存在的作用力有__________ (填标号)。
A.配位键 B. σ键 C.极性键 D.非极性键 E.离子键
(5)BeO立方晶胞如下图所示。
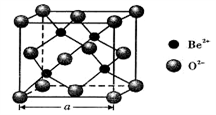
① BeO晶体中,O2-的配位数为___________ 。
② 若BeO晶体的密度为dg/cm3,则晶胞参数
a =___________________________ nm (列出计算式即可)。
(l)最重要的含铍矿物是绿柱石,含2%铬(Cr)的绿柱石即为祖母绿。基态Cr原子价电子排布图为
(2)铍与相邻主族的铝元素性质相似。下列有关铍和铝的叙述正确的有
A.铍属于s区主族元素 B.电负性都比镁大
C.铝的第一电离能比镁小 D.氯化物的水溶液pH均大于7
(3)铍、铝晶体都是由金属原子密置层在三维空间堆积而成(最密堆积)。铍的熔点(155lK)比铝的熔点(930K)高,原因是
(4)氯化铍在气态时存在BeC12分子(a)和二聚分子(BeCl2)2(b),固态时则具有如下图所示的链状结构(c)。

①a属于
②b中Be原子的杂化方式相同,且所有原子都在同一平面上。b 的结构式为
③c中Be原子的杂化方式为
④氯化铍晶体(c)中存在的作用力有
A.配位键 B. σ键 C.极性键 D.非极性键 E.离子键
(5)BeO立方晶胞如下图所示。

① BeO晶体中,O2-的配位数为
② 若BeO晶体的密度为dg/cm3,则晶胞参数
a =
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】过渡金属钛(Ti)性能优越,是继铁、铝之后应用广泛的“第三金属”,被誉为“未来钢铁”、“战略金属”。回答下列问题:
(1)下列Ti 原子电子排布式表示的状态中,电离最外层一个电子所需能量最大的是_______ (填标号)。
(2)TiCl4是氧化法制取钛的中间产物,TiCl4分子结构与TiCl4相同,二者常温下都是无色液体,则TiCl4分子的空间结构为_______ 。TiCl4的稳定性比CCl4差,极易水解,原因是_______ (从原子半径、键长和键能的角度分析)。
(3)六氟合钛酸钾(K2TiF6)可用作钛酸和金属钛的制造。六氟合钛酸钾中存在[TiF6]2-,该晶体中不存在的化学键是 _______ (填标号)。
(4)纳米TiO2是一种应用广泛的催化剂,其催化的一个实例如下:

①有机物甲中标“*”的碳原子的杂化方式为_______ ,1mol甲分子中含有_______ mol σ键。
②有机物乙中,C、N、O三种元素的第一电离能由大到小的顺序是_______ 。
③有机物乙的沸点高于有机物甲,其主要原因是_______ 。
(5)嫦娥三号卫星上的PIC元件(热敏电阻)的主要成分——钡钛矿的晶胞结构如图所示。
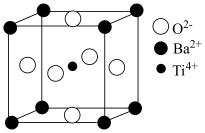
①晶体中一个Ba2+周围距离最近的O2-数目为_______ 。
②已知该晶体的密度为_______ ρg·cm-3,阿伏加德罗常数的值为NA,则该晶体中Ba2+与Ti4+之间的最短距离为 _______ pm (列出计算式)。
(1)下列Ti 原子电子排布式表示的状态中,电离最外层一个电子所需能量最大的是_______ (填标号)。
| A.[Ar]3d²4s¹4p¹ | B.[Ar]3d²4s² |
| C.[Ar]3d³4s²4p¹ | D.[Ar]3d¹4s¹4p² |
(2)TiCl4是氧化法制取钛的中间产物,TiCl4分子结构与TiCl4相同,二者常温下都是无色液体,则TiCl4分子的空间结构为
(3)六氟合钛酸钾(K2TiF6)可用作钛酸和金属钛的制造。六氟合钛酸钾中存在[TiF6]2-,该晶体中不存在的化学键是 _______ (填标号)。
| A.离子键 | B.极性键 | C.非极性键 | D.配位键 |
(4)纳米TiO2是一种应用广泛的催化剂,其催化的一个实例如下:

①有机物甲中标“*”的碳原子的杂化方式为
②有机物乙中,C、N、O三种元素的第一电离能由大到小的顺序是
③有机物乙的沸点高于有机物甲,其主要原因是
(5)嫦娥三号卫星上的PIC元件(热敏电阻)的主要成分——钡钛矿的晶胞结构如图所示。

①晶体中一个Ba2+周围距离最近的O2-数目为
②已知该晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】C、Ti的单质及其化合物在现代社会有广泛用途。
(1)基态钛原子的电子排布式为_____________________ 。
(2)CS2分子中含有σ键和π键之比为________ ;NO2+与CO2是等电子体,NO2+的电子式为______________ ,键角为__________________ 。
(3)CH3CHO沸点低于CH3CH2OH的原因是_______________________ ;CH3 CHO分子中碳原子杂化类型为__________ 。
(4)钛酸钡(BaTiO3)晶体的某种晶胞如图所示。NA为阿伏伽德罗常数值,Ba2+、O2-、Ti4+的半径分别为a cm、b cm、c cm。
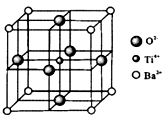
①与钡离子等距离且最近的氧离子有_____ 个;
②假设晶体中的Ti4+、Ba2+分别与O2-互相接触,则该晶体的密度表达式为________ g·cm-3。
(1)基态钛原子的电子排布式为
(2)CS2分子中含有σ键和π键之比为
(3)CH3CHO沸点低于CH3CH2OH的原因是
(4)钛酸钡(BaTiO3)晶体的某种晶胞如图所示。NA为阿伏伽德罗常数值,Ba2+、O2-、Ti4+的半径分别为a cm、b cm、c cm。

①与钡离子等距离且最近的氧离子有
②假设晶体中的Ti4+、Ba2+分别与O2-互相接触,则该晶体的密度表达式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】铁、铜和镁是生命必需的元素,也是人类使用广泛的金属,铁和铜及其重要化合物在生产中有着重要的应用。回答下列问题:
(1)某元素X与铜同周期,基态X原子是该周期基态原子中未成对电子最多的,其原子结构示意图为_______ 。
(2)Fe2+变为基态铁原子时所得的电子填充到_______ 能级。
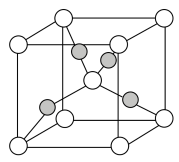
(3)新制备的Cu(OH)2可将乙醛氧化成乙酸(CH3COOH),而自身还原成Cu2O。1个乙酸分子中共平面的原子最多为_______ 个。图所示的Cu2O晶胞中,铜周围紧邻且等距的氧有_______ 个,已知其晶胞密度为bg/cm3,则该晶胞棱长为_______ pm(设NA为阿伏加德罗常数的值)。
(4)叶绿素的结构示意如图所示。
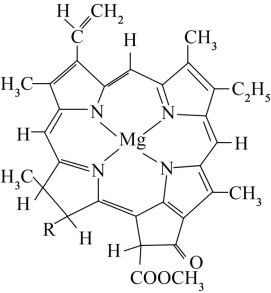
①该结构中包含的作用力有_______ (用字母填空)。
a.离子键 b.σ键 c.π键 d.分子间作用力
②其中碳原子的杂化类型为_______ ,碳、氮、氧三种元素的电负性由大到小的顺序是_______ 。元素As与N同族预测As的简单氢化物的VSEPR模型为_______ ,其键角_______ 109º28´(填“大于”、“小于”或“等于”)原因是_______ 。
(1)某元素X与铜同周期,基态X原子是该周期基态原子中未成对电子最多的,其原子结构示意图为
(2)Fe2+变为基态铁原子时所得的电子填充到
(3)新制备的Cu(OH)2可将乙醛氧化成乙酸(CH3COOH),而自身还原成Cu2O。1个乙酸分子中共平面的原子最多为

(4)叶绿素的结构示意如图所示。

①该结构中包含的作用力有
a.离子键 b.σ键 c.π键 d.分子间作用力
②其中碳原子的杂化类型为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】由P、S、Cl、Ni等元素组成的新型材料有着广泛的用途,回答下列问题。
(1)基态Cl原子核外电子占有的原子轨道数为_ 个,P、S、Cl的氢化物稳定性由强到弱顺序为___ 。
(2)已知MO与NiO的晶体结构(如图1)相同,其中Mg2+和Ni2+的离子半径分别为66pm和69pm。则熔点:MgO__ NiO(填“>”、“<”或“=”),理由是:___ 。
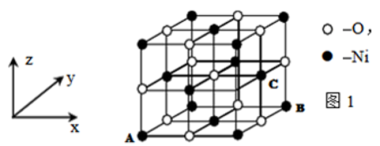
(3)若NiO晶胞中离子坐标参数A为(0,0,0),B为(1,1,0),则C离子坐标参数为_____ 。
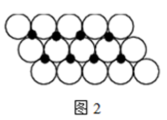
(4)一定温度下,NiO晶体可以自发地分散并形成“单分子层”,可以认为O2-作密置单层排列,Ni2+填充其中(如图2),已知O2-的半径为am,每平方米面积上分散的该晶体的质量为____ g。(用a、NA表示,相对原子质量:O-16,Ni-59)
(1)基态Cl原子核外电子占有的原子轨道数为
(2)已知MO与NiO的晶体结构(如图1)相同,其中Mg2+和Ni2+的离子半径分别为66pm和69pm。则熔点:MgO

(3)若NiO晶胞中离子坐标参数A为(0,0,0),B为(1,1,0),则C离子坐标参数为
(4)一定温度下,NiO晶体可以自发地分散并形成“单分子层”,可以认为O2-作密置单层排列,Ni2+填充其中(如图2),已知O2-的半径为am,每平方米面积上分散的该晶体的质量为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】A、B、C、D 是元素周期表中前四周期元素,其原子序数依次增大 详细信息见表:
请回答下列问题:
(1)A元素原子的价层电子排布图(价层电子的轨道表达式)为____ ,其基态原子占据的最高能级的电子云轮廓图为___ 形
(2)B的最高价含氧酸根中心原子轨道杂化类型___ ,空间构型为____ 。
(3)A元素的最简单氢化物分子和B元素最简单氢化物分子中键角大的是________ (填化学式),原因是______ 。
(4)C盐溶液中加入过量 AH3浓溶液变深蓝色,写出该反应的离子方程式__ 。深蓝色离子中结构中,配位原子为___ (填元素符号)
(5)DB 晶体的晶胞如图所示
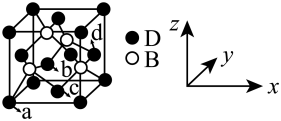
①在该晶胞中,D的配位数为_____ 。
②原子坐标参数可表示晶胞内部各原子的相对位置。如图晶胞中,原子坐标参数a为(0,0,0 ),b为( ,0,
,0, ),c为(
),c为( ,
, ,0 ) 则d的坐标参数为
,0 ) 则d的坐标参数为______ 。
| ① | A 的氧化物是导致光化学烟雾的主要物质之一 |
| ② | B的氧化物是导致酸雨的主要物质之一 |
| ③ | C能形成红色的 C2O 和黑色的 CO 两种氧化物 |
| ④ | D 的基态原子最外能层有2个电子,内层全满 |
请回答下列问题:
(1)A元素原子的价层电子排布图(价层电子的轨道表达式)为
(2)B的最高价含氧酸根中心原子轨道杂化类型
(3)A元素的最简单氢化物分子和B元素最简单氢化物分子中键角大的是
(4)C盐溶液中加入过量 AH3浓溶液变深蓝色,写出该反应的离子方程式
(5)DB 晶体的晶胞如图所示

①在该晶胞中,D的配位数为
②原子坐标参数可表示晶胞内部各原子的相对位置。如图晶胞中,原子坐标参数a为(0,0,0 ),b为(
 ,0,
,0, ),c为(
),c为( ,
, ,0 ) 则d的坐标参数为
,0 ) 则d的坐标参数为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
真题
名校
【推荐3】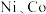 均是重要的战略性金属。从处理后的矿石硝酸浸取液(含
均是重要的战略性金属。从处理后的矿石硝酸浸取液(含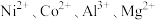 )中,利用氨浸工艺可提取
)中,利用氨浸工艺可提取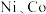 ,并获得高附加值化工产品。工艺流程如下:
,并获得高附加值化工产品。工艺流程如下:
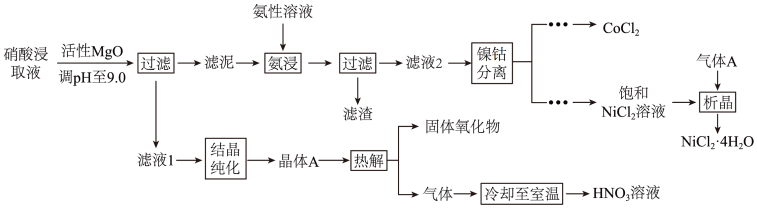
已知:氨性溶液由 、
、 和
和 配制。常温下,
配制。常温下,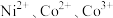 与
与 形成可溶于水的配离子:
形成可溶于水的配离子: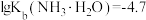 ;
; 易被空气氧化为
易被空气氧化为 ;部分氢氧化物的
;部分氢氧化物的 如下表。
如下表。
回答下列问题:
(1)活性 可与水反应,化学方程式为
可与水反应,化学方程式为___________ 。
(2)常温下, 的氨性溶液中,
的氨性溶液中,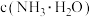
___________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(3)“氨浸”时,由 转化为
转化为 的离子方程式为
的离子方程式为___________ 。
(4) 会使滤泥中的一种胶状物质转化为疏松分布的棒状颗粒物。滤渣的X射线衍射图谱中,出现了
会使滤泥中的一种胶状物质转化为疏松分布的棒状颗粒物。滤渣的X射线衍射图谱中,出现了 的明锐衍射峰。
的明锐衍射峰。
① 属于
属于___________ (填“晶体”或“非晶体”)。
② 提高了
提高了 的浸取速率,其原因是
的浸取速率,其原因是___________ 。
(5)①“析晶”过程中通入的酸性气体A为___________ 。
②由 可制备
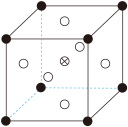
可制备 晶体,其立方晶胞如图。
晶体,其立方晶胞如图。 与O最小间距大于
与O最小间距大于 与O最小间距,x、y为整数,则
与O最小间距,x、y为整数,则 在晶胞中的位置为
在晶胞中的位置为___________ ;晶体中一个 周围与其最近的O的个数为
周围与其最近的O的个数为___________ 。
(6)①“结晶纯化”过程中,没有引入新物质。晶体A含6个结晶水,则所得 溶液中
溶液中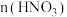 与
与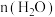 的比值,理论上最高为
的比值,理论上最高为___________ 。
②“热解”对于从矿石提取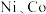 工艺的意义,在于可重复利用
工艺的意义,在于可重复利用 和
和___________ (填化学式)。
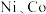 均是重要的战略性金属。从处理后的矿石硝酸浸取液(含
均是重要的战略性金属。从处理后的矿石硝酸浸取液(含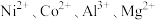 )中,利用氨浸工艺可提取
)中,利用氨浸工艺可提取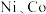 ,并获得高附加值化工产品。工艺流程如下:
,并获得高附加值化工产品。工艺流程如下:
已知:氨性溶液由
 、
、 和
和 配制。常温下,
配制。常温下,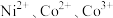 与
与 形成可溶于水的配离子:
形成可溶于水的配离子: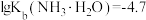 ;
; 易被空气氧化为
易被空气氧化为 ;部分氢氧化物的
;部分氢氧化物的 如下表。
如下表。| 氢氧化物 |  |  |  |  |  |
 | 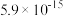 |  |  | 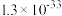 | 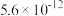 |
(1)活性
 可与水反应,化学方程式为
可与水反应,化学方程式为(2)常温下,
 的氨性溶液中,
的氨性溶液中,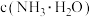
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(3)“氨浸”时,由
 转化为
转化为 的离子方程式为
的离子方程式为(4)
 会使滤泥中的一种胶状物质转化为疏松分布的棒状颗粒物。滤渣的X射线衍射图谱中,出现了
会使滤泥中的一种胶状物质转化为疏松分布的棒状颗粒物。滤渣的X射线衍射图谱中,出现了 的明锐衍射峰。
的明锐衍射峰。①
 属于
属于②
 提高了
提高了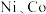 的浸取速率,其原因是
的浸取速率,其原因是(5)①“析晶”过程中通入的酸性气体A为
②由
 可制备
可制备 晶体,其立方晶胞如图。
晶体,其立方晶胞如图。 与O最小间距大于
与O最小间距大于 与O最小间距,x、y为整数,则
与O最小间距,x、y为整数,则 在晶胞中的位置为
在晶胞中的位置为 周围与其最近的O的个数为
周围与其最近的O的个数为
(6)①“结晶纯化”过程中,没有引入新物质。晶体A含6个结晶水,则所得
 溶液中
溶液中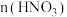 与
与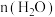 的比值,理论上最高为
的比值,理论上最高为②“热解”对于从矿石提取
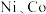 工艺的意义,在于可重复利用
工艺的意义,在于可重复利用 和
和
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】第三周期主族元素W、X、Y、Z的最高化合价与该元素的原子半径的关系如图所示。

回答下列问题:
(1)W和Z组成W2Z2晶体中所含化学键为___________ ,该晶体类型是___________ 。
(2)XY3的分子式为___________ ,该分子的立体构型是___________ ,中心原子的杂化方式是___________ 。
(3)W和Y组成晶体的晶胞如图1所示,晶胞截面如图2所示。已知:晶体密度为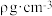 ,
,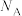 代表阿伏加德罗常数的值,Y对应的离子半径为
代表阿伏加德罗常数的值,Y对应的离子半径为 。则W的离子半径为
。则W的离子半径为___________  。
。
(4)W单质晶体的晶胞如图3所示。
①晶胞中等距离且最近的W原子有___________ 个。
②若W的半径为bnm,则该晶体密度为___________  。
。

回答下列问题:
(1)W和Z组成W2Z2晶体中所含化学键为
(2)XY3的分子式为
(3)W和Y组成晶体的晶胞如图1所示,晶胞截面如图2所示。已知:晶体密度为
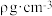 ,
,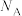 代表阿伏加德罗常数的值,Y对应的离子半径为
代表阿伏加德罗常数的值,Y对应的离子半径为 。则W的离子半径为
。则W的离子半径为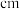 。
。
(4)W单质晶体的晶胞如图3所示。
①晶胞中等距离且最近的W原子有
②若W的半径为bnm,则该晶体密度为
 。
。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】X、Y、Z、Q、W为按原子序数由小到大排列的五种短周期元素。已知:①X与Q处于同一主族,其原子价电子排布式都为ns2np2,且X原子半径小于Q;②Y元素是地壳中含量最多的元素;W元素的电负性略小于Y元素,在W原子的价电子排布式中,p轨道上只有1个未成对电子;③Z元素的电离能数据见下表(kJ·mol-1)
请回答:
(1)XY2分子的空间构型为_______________ 。
(2)QX的晶体结构与金刚石的相似,微粒间存在的作用力是_________________ 。
(3)晶体ZW的熔点比晶体XW4明显高的原因是_____________ 。
(4)XY2在高温高压下所形成的晶胞如图所示。该晶体的类型属于____ (选填“分子”、“原子”、“离子”或“金属”)晶体,该晶体中X原子的杂化形式为_______ 。
(5)氧化物MO的电子总数与QX的相等,则M为____ (填元素符号);MO是优良的耐高温材料,其晶体结构与ZW晶体结构相似,MO的熔点比CaO的高,其原因是________ 。
| I1 | I2 | I3 | I4 | … |
| 496 | 4562 | 6912 | 9540 | … |
(1)XY2分子的空间构型为
(2)QX的晶体结构与金刚石的相似,微粒间存在的作用力是
(3)晶体ZW的熔点比晶体XW4明显高的原因是
(4)XY2在高温高压下所形成的晶胞如图所示。该晶体的类型属于

(5)氧化物MO的电子总数与QX的相等,则M为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】现有几组物质的熔点(以℃为单位)数据:
据此回答下列问题:
(1)A组属于_______ 晶体,其熔化时克服的微粒间的作用力是_______ 。
(2)B组晶体共同的物理性质是_______ (填序号)。
①有金属光泽 ②导电性 ③导热性 ④延展性
(3)C组中HF熔点反常是由于_______ 。
(4)D组晶体可能具有的性质是_______ (填序号)。
①硬度小 ②水溶液能导电 ③固体能导电 ④熔融状态能导电
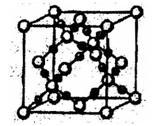
(5)加碘食盐中含有KIO3,其立体结构如图,边长为a=0.446nm,晶胞中K、I、O分别处于顶角、体心、面心位置。K与O间的最短距离为___ nm,与K紧邻的I个数为____ 。原子坐标参数表示晶胞内各原子的相对位置。如图(晶胞中,原子坐标参数A为(0,0,0);B为( ,
, ,
, );C为(0,1,1)。则D原子的坐标参数为
);C为(0,1,1)。则D原子的坐标参数为____
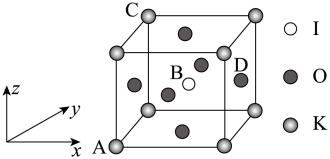
(6)ZnS在荧光体、光导体材料、涂料、颜料。等行业中应用广泛。立方ZnS晶体结构如图所示,其晶胞边长为540.0pm,密度为___ g·cm3(列式并计算),a位置S2¯离子与b位置Zn2+离子之间的距离为__ pm(列式表示)。
| A组 | B组 | C组 | D组 |
| 金刚石:3550 | Li:181 | HF:-83 | NaCl:801 |
| 硅晶体:1410 | Na:98 | HCl:-115 | KCl:776 |
| 硼晶体:2300 | K:64 | HBr:-89 | RbCl:718 |
| 二氧化硅:1723 | Rb:39 | HI:-51 | CsCl:645 |
据此回答下列问题:
(1)A组属于
(2)B组晶体共同的物理性质是
①有金属光泽 ②导电性 ③导热性 ④延展性
(3)C组中HF熔点反常是由于
(4)D组晶体可能具有的性质是
①硬度小 ②水溶液能导电 ③固体能导电 ④熔融状态能导电
(5)加碘食盐中含有KIO3,其立体结构如图,边长为a=0.446nm,晶胞中K、I、O分别处于顶角、体心、面心位置。K与O间的最短距离为
 ,
, ,
, );C为(0,1,1)。则D原子的坐标参数为
);C为(0,1,1)。则D原子的坐标参数为
(6)ZnS在荧光体、光导体材料、涂料、颜料。等行业中应用广泛。立方ZnS晶体结构如图所示,其晶胞边长为540.0pm,密度为

您最近一年使用:0次



