速率与限度是研究化学反应的重要视角,下列叙述错误的是
A.对于反应 ,其他条件不变,增加木炭的量,反应速率不变 ,其他条件不变,增加木炭的量,反应速率不变 |
| B.用锌片和稀硫酸反应制取氢气时,用粗锌比纯锌反应生成氢气的速率会加快 |
C.100 mL 2 mol·L 的盐酸跟锌片反应,加入适量的氯化钠溶液,反应速率不变 的盐酸跟锌片反应,加入适量的氯化钠溶液,反应速率不变 |
| D.在给定条件下,达到平衡时,可逆反应完成程度达到最大 |
更新时间:2023-05-06 18:30:33
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】在少量的铁片与足量的100mL 0.2mol·L—1的稀硫酸反应中,为了减缓此反应速率而不改变H2的总量,下列方法错误的是
| A.加NaCl溶液 | B.加蒸馏水 |
| C.加入少量醋酸钠固体 | D.滴入几滴硫酸铜溶液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是
| A.化学平衡正向移动,反应物的转化率一定增大 |
| B.探究温度对硫代硫酸钠与硫酸反应速率的影响时,若先将两种溶液混合并计时,再用水浴加热至设定温度,则测得的反应速率偏低 |
| C.合成氨反应需要使用催化剂,说明催化剂可以促进该平衡向生成氨的方向移动,所以也可以用勒夏特列原理解释使用催化剂的原因 |
D.在恒温恒容条件下,可逆反应PCl5(g) PCl3(g)+Cl2(g)达到平衡后,再充入PCl5(g)重新建立平衡,则PCl5(g)的转化率增大 PCl3(g)+Cl2(g)达到平衡后,再充入PCl5(g)重新建立平衡,则PCl5(g)的转化率增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】实验室用Zn与稀H2SO4反应来制取氢气,常加少量CuSO4来加快反应速率。为了研究CuSO4的量对H2生成速率的影响,某同学设计了实验方案(见下表),将表中所给的试剂按一定体积混合后,分别加入四个盛有相同大小的Zn片(过量)的反应瓶(甲、乙、丙、丁)中,收集产生的气体,并记录收集相同体积的气体所需的时间。
下列说法正确的是( )
| 实验 试剂 | 甲 | 乙 | 丙 | 丁 |
| 4 mol·L-1 H2SO4/mL | 20 | V1 | V2 | V3 |
| 饱和CuSO4溶液/mL | 0 | 2.5 | V4 | 10 |
| H2O/mL | V5 | V6 | 8 | 0 |
| 收集气体所需时间/s | t1 | t2 | t3 | t4 |
下列说法正确的是( )
| A.t1<t2<t3<t4 | B.V4=V5=10 | C.V6=7.5 | D.V1<V2<V3<20 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】控制变量法是化学实验的一种常用方法。下表是某学习小组研究等物质的量浓度的硫酸和锌反应的实验数据,下列有关叙述正确的是
| 序号 | 硫酸的体积 | 锌的质量 | 锌的状态 | 温度 | 完全溶于酸的时间 | 生成硫酸锌的质量 |
| 1 | 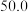 |  | 颗粒 | 25 | 70 |  |
| 2 | 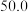 |  | 颗粒 | 35 | 35 |  |
| 3 | 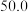 |  | 粉末 | 25 |  | 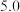 |
| 4 | 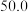 | 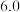 | 粉末 | 25 |  |  |
| 5 | 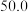 |  | 粉末 | 25 |  | 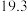 |
| 6 | 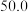 |  | 粉末 | 25 |  |  |
A. |
B. |
| C.实验1、实验2与实验3探究的是温度对化学反应速率的影响 |
| D.无法计算出硫酸的物质的量浓度 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列实验目的、实验方案以及评价正确的是( )
| 选项 | 实验目的 | 实验方案 | 评价 |
| A | 探究接触面积对化学反应速率的影响 | 相同温度下,取等质量的大理石块、大理石粉末分别投入到等体积、等浓度的盐酸中 | 该方案可行 |
| B | 证明Mg(OH)2沉淀可以转化为Fe(OH)3沉淀 | 向2 mL 1 mol·L-1 NaOH溶液中先加入3滴1 mol·L-1MgCl2溶液,再加入3滴1 mol·L-1 FeCl3溶液 | 该方案可行 |
| C | 检验蔗糖水解产物具有还原性 | 向蔗糖溶液中加入几滴稀硫酸,水浴加热几分钟,冷却后再向其中加入新制的银氨溶液,并水浴加热 | 该方案可行 |
| D | 测定铝箔中氧化铝的含量 | 取a g铝箔与足量稀盐酸充分反应,逸出的气体通过碱石灰后,测其体积为b L(已转化为标准状况下) | 该方案不可行 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】根据如图实验操作和现象所得到的结论正确的是
| A | B | C | D |
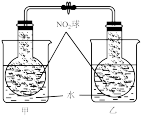 将  球浸泡在冷水和热水中 球浸泡在冷水和热水中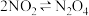  | 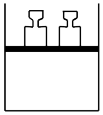  |   | 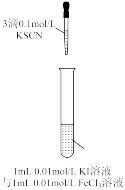 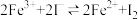 |
| 气体在热水中比在冷水中颜色浅 | 平衡体系加压后颜色先变深后变浅 | 研究浓度对化学平衡的影响 | 证明化学反应存在一定的限度 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列有关实验原理、方法和结论都正确的是
| A.已知Cu2O+2H+=Cu2++Cu+H2O,氢气还原氧化铜后所得红色固体能完全溶于稀硝酸,说明还原产物是铜 |
| B.取一定量水垢加盐酸,生成能使澄清石灰水变浑浊的气体,说明水垢的主要成分为CaCO3、MgCO3 |
| C.向5 mL 0.1 mol·L-1KI溶液中加入0.1 mol·L-1的FeCl3溶液1 mL,振荡,用苯萃取2~3次后取下层溶液滴加5滴KSCN溶液,出现血红色,说明反应2Fe3++2I-=2Fe2++I2是有一定限度的 |
| D.常温下,向饱和Na2CO3溶液中加少量BaSO4粉末,过滤,向洗净的沉淀中加稀盐酸,有气泡产生,说明常温下Ksp(BaCO3)<Ksp(BaSO4) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】NO2、O2和熔融NaNO3可制作燃料电池,其原理如图, 下列判断正确的是


| A.石墨电极Ⅱ为电池负极 |
| B.电池中NO3- 从石墨电极I向石墨电极Ⅱ作定向移动 |
| C.石墨I电极发生的电极反应为NO2+NO3- -e- =N2O5 |
| D.每消耗1 mol NO2转移电子2 mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】有科学家研究用姜黄素(姜黄中的物质)和金纳米粒子结合制造出新型纳米复合材料作为电极A的材料,得到更安全、更高效的乙醇燃料电池。下列说法不正确 的是
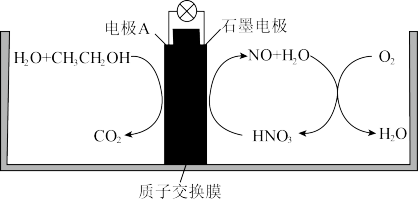
| A.石墨电极为正极,发生还原反应 |
B.电极A的电极反应: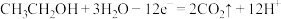 |
C.加入 可使电池持续大电流放电 可使电池持续大电流放电 |
| D.放电时,阳离子向电极A移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】一种新型酸性乙醇电池用磺酸类质子作溶剂,比甲醇电池效率高出32倍,电池反应式为:C2H5OH+3O2===2CO2+3H2O,电池构造如下图所示。下列关于该电池的说法正确的是
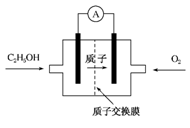

| A.放电过程中,电源内部的H+从正极区向负极区迁移 |
| B.通入乙醇的电极是正极 |
| C.该电池的正极反应为:4H++O2+4e-===2H2O |
| D.用该电池做电源,用惰性电极电解饱和NaCl溶液时,每消耗0.2 mol C2H5OH,阴极产生标准状况下气体的体积为13.44 L |
您最近一年使用:0次