如图是元素周期表的一部分。已知R的核电荷数小于36,气态氢化物沸点: 。
。
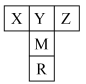
(1)Y元素在周期表中的位置为___________ ,表中五种元素电负性最大的是___________ (填元素符号)。
(2)Y的最高价氧化物熔点比M的最高价氧化物熔点低,原因是___________ , 中
中 键与
键与 键的个数比为
键的个数比为___________ 。
(3)Z的一种常见氢化物能与硫酸铜反应生成配合物。请用结构简式表示该配合物中的阳离子:___________ 。
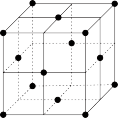
(4)如图为某金属单质的面心立方晶胞结构示意图,该晶体中配位数是___________ ;测得此晶体的密度为 ,晶胞的边长为0.405nm,则此金属原子的相对原子质量为
,晶胞的边长为0.405nm,则此金属原子的相对原子质量为___________ (结果保留整数)。
 。
。
(1)Y元素在周期表中的位置为
(2)Y的最高价氧化物熔点比M的最高价氧化物熔点低,原因是
 中
中 键与
键与 键的个数比为
键的个数比为(3)Z的一种常见氢化物能与硫酸铜反应生成配合物。请用结构简式表示该配合物中的阳离子:
(4)如图为某金属单质的面心立方晶胞结构示意图,该晶体中配位数是
 ,晶胞的边长为0.405nm,则此金属原子的相对原子质量为
,晶胞的边长为0.405nm,则此金属原子的相对原子质量为
更新时间:2023-06-08 23:42:49
|
相似题推荐
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】过渡金属在能源、环境、材料、生命科学等领域发挥着重要作用。
I.研究表明新冠病毒在铜表面存活时间最短,仅为4小时,铜被称为细菌病毒的“杀手”。
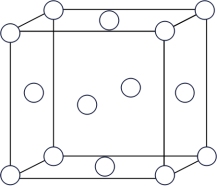
(1)铜的晶胞结构如图所示,与铜原子最近且等距离的铜原子有_______ 个。
(2)碱式硫酸铜(Cu2(OH)2SO4)是农药波尔多液的有效杀菌成分,其中非金属元素电负性由大到小的顺序是_______ ,阴离子SO 中心原子的价层电子对数目为
中心原子的价层电子对数目为_______ (列出计算式)。
II.铁是地球表面最丰富的金属之一,其合金、化合物具有广泛用途。
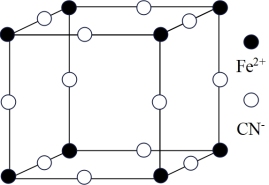
(3)普鲁士蓝俗称铁蓝,是含有铁元素的一种化合物,可以解铊中毒,结构如图所示(K+未画出),平均每两个立方体中含有一个K+,该晶体的化学式为_______ ,又知该晶体中铁元素有+2价和十3价两种,则Fe3+与Fe2+的个数比为_______ 。
III.TiO2-aNb是常见的光学活性物质。
(4)基态Ti原子的电子所占据的最高能层符号为_______ 。
(5)TiO2通过氮掺杂反应生成TiO2-aNb,表示如图。

①立方晶系TiO2晶胞参数如图甲所示,其晶体的密度为_______ g/cm3。
②图乙TiO2-aNb晶体中a=_______ 。
I.研究表明新冠病毒在铜表面存活时间最短,仅为4小时,铜被称为细菌病毒的“杀手”。
(1)铜的晶胞结构如图所示,与铜原子最近且等距离的铜原子有

(2)碱式硫酸铜(Cu2(OH)2SO4)是农药波尔多液的有效杀菌成分,其中非金属元素电负性由大到小的顺序是
 中心原子的价层电子对数目为
中心原子的价层电子对数目为II.铁是地球表面最丰富的金属之一,其合金、化合物具有广泛用途。
(3)普鲁士蓝俗称铁蓝,是含有铁元素的一种化合物,可以解铊中毒,结构如图所示(K+未画出),平均每两个立方体中含有一个K+,该晶体的化学式为

III.TiO2-aNb是常见的光学活性物质。
(4)基态Ti原子的电子所占据的最高能层符号为
(5)TiO2通过氮掺杂反应生成TiO2-aNb,表示如图。

①立方晶系TiO2晶胞参数如图甲所示,其晶体的密度为
②图乙TiO2-aNb晶体中a=
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】钙钛矿(CaTiO3)型化合物是一类可用于生产太阳能电池、传感器、固体电阻器等的功能材料,回答下列问题:
(1)基态Ti原子的核外电子排布式为______ 。
(2)Ti的四卤化物熔点如表所示,TiF4熔点明显高于其他三种卤化物,TiCl4至TiI4熔点依次升高,原因是_______ 。
(3)CaTiO3组成元素的电负性最大的为______ (用元素符号表示)。
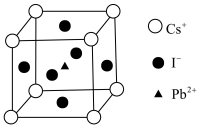
(4)某种金属卤化物无机钙钛矿的晶胞结构如图所示,晶胞的边长apm,则该物质的化学式为______ ;晶体的密度ρ=______ g•cm-3(设阿伏加德罗常数的值为NA,用含a、NA的代数式表示)。
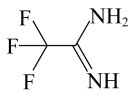
(5)我国科学家设计了一种钝化剂三氟乙脒(结构如图所示)来抑制上述金属卤化物钙钛矿晶粒表面缺陷,其中σ键与π键数目之比为______ ,两个碳原子的杂化类型分别为______ 。
(1)基态Ti原子的核外电子排布式为
(2)Ti的四卤化物熔点如表所示,TiF4熔点明显高于其他三种卤化物,TiCl4至TiI4熔点依次升高,原因是
| 化合物 | TiF4 | TiCl4 | TiBr4 | TiI4 |
| 熔点/℃ | 377 | -24.12 | 38.3 | 155 |
(4)某种金属卤化物无机钙钛矿的晶胞结构如图所示,晶胞的边长apm,则该物质的化学式为

(5)我国科学家设计了一种钝化剂三氟乙脒(结构如图所示)来抑制上述金属卤化物钙钛矿晶粒表面缺陷,其中σ键与π键数目之比为

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】二甲基亚砜(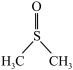 )是一种重要的非质子极性溶剂。铬和锰等过渡金属卤化物在二甲基亚砜中有一定溶解度,故可以应用在有机电化学中。回答下列问题:
)是一种重要的非质子极性溶剂。铬和锰等过渡金属卤化物在二甲基亚砜中有一定溶解度,故可以应用在有机电化学中。回答下列问题:
(1)铬和锰基态原子核外未成对电子数之比为_______ 。
(2)已知:二甲基亚砜能够与水和丙酮(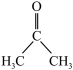 )分别以任意比互溶。
)分别以任意比互溶。
①二甲基亚砜分子中硫原子的杂化类型为_______ 。
②丙酮分子中各原子电负性由大到小的顺序为_______ 。
③二甲基亚砜易溶于水,原因可能为_______ 。
(3)CrCl3·6H2O的结构有三种,且铬的配位数均为6,等物质的量的三种物质电离出的氯离子数目之比为3:2:1,对应的颜色分别为紫色、浅绿色和蓝绿色,其中浅绿色的结构中配离子的化学式为_______ 。
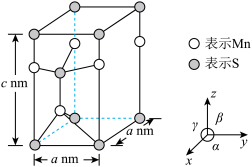
(4)已知硫化锰(MnS)晶胞如图所示,该晶胞参数α=120°,β=γ=90°。
①该晶体中,锰原子周围的硫原子数目为_______ 。
②空间利用率指的是构成晶体的原子、离子或分子在整个晶体空间中所占有的体积百分比。已知锰和硫的原子半径分别r1 nm和r2 nm,该晶体中原子的空间利用率为_______ (列出计算式即可)。
 )是一种重要的非质子极性溶剂。铬和锰等过渡金属卤化物在二甲基亚砜中有一定溶解度,故可以应用在有机电化学中。回答下列问题:
)是一种重要的非质子极性溶剂。铬和锰等过渡金属卤化物在二甲基亚砜中有一定溶解度,故可以应用在有机电化学中。回答下列问题:(1)铬和锰基态原子核外未成对电子数之比为
(2)已知:二甲基亚砜能够与水和丙酮(
 )分别以任意比互溶。
)分别以任意比互溶。①二甲基亚砜分子中硫原子的杂化类型为
②丙酮分子中各原子电负性由大到小的顺序为
③二甲基亚砜易溶于水,原因可能为
(3)CrCl3·6H2O的结构有三种,且铬的配位数均为6,等物质的量的三种物质电离出的氯离子数目之比为3:2:1,对应的颜色分别为紫色、浅绿色和蓝绿色,其中浅绿色的结构中配离子的化学式为
(4)已知硫化锰(MnS)晶胞如图所示,该晶胞参数α=120°,β=γ=90°。
①该晶体中,锰原子周围的硫原子数目为
②空间利用率指的是构成晶体的原子、离子或分子在整个晶体空间中所占有的体积百分比。已知锰和硫的原子半径分别r1 nm和r2 nm,该晶体中原子的空间利用率为

您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐1】工业上常采用Fenton氧化法去除废水中的有机物。
(1)某研究小组向废水中加入 ,以
,以 作催化剂,产生具有强氧化性的羟基自由基(
作催化剂,产生具有强氧化性的羟基自由基( )氧化降解水中的有机物(TOC)。
)氧化降解水中的有机物(TOC)。
①其他条件一定时,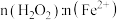 的值对TOC去除效果的影响如图所示:
的值对TOC去除效果的影响如图所示:
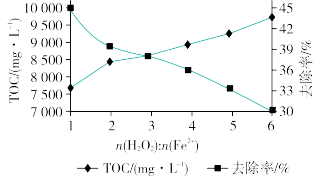
当TOC的去除率最大时,
_______ 。
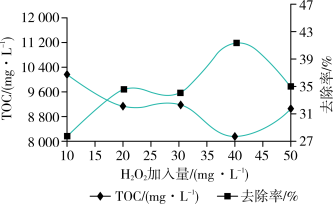
②在 ,其他条件一定时,
,其他条件一定时, 的加入量对TOC去除效果的影响如图所示,当TOC的去除效果最好时,
的加入量对TOC去除效果的影响如图所示,当TOC的去除效果最好时, 的物质的量浓度c(
的物质的量浓度c( )=
)=_______ 。当 的加入量大于40mg/L时,TOC去除率反而减小的原因是
的加入量大于40mg/L时,TOC去除率反而减小的原因是_______ 。
(2)我国学者制备了一种介孔二氧化锰负载的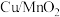 催化剂,并将其应用到苯并三唑(
催化剂,并将其应用到苯并三唑( ,BZA)的降解中,催化机理如下图:
,BZA)的降解中,催化机理如下图:
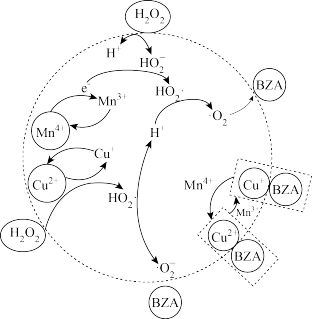
①BZA可以与 或
或 结合的原因是
结合的原因是_______ 。
②直接降解BZA的活性氧物种的化学式为_______ 。
③该过程中 分解的途径可用语言描述为
分解的途径可用语言描述为_______ 。
(1)某研究小组向废水中加入
 ,以
,以 作催化剂,产生具有强氧化性的羟基自由基(
作催化剂,产生具有强氧化性的羟基自由基( )氧化降解水中的有机物(TOC)。
)氧化降解水中的有机物(TOC)。①其他条件一定时,
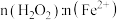 的值对TOC去除效果的影响如图所示:
的值对TOC去除效果的影响如图所示:
当TOC的去除率最大时,

②在
 ,其他条件一定时,
,其他条件一定时, 的加入量对TOC去除效果的影响如图所示,当TOC的去除效果最好时,
的加入量对TOC去除效果的影响如图所示,当TOC的去除效果最好时, 的物质的量浓度c(
的物质的量浓度c( )=
)= 的加入量大于40mg/L时,TOC去除率反而减小的原因是
的加入量大于40mg/L时,TOC去除率反而减小的原因是
(2)我国学者制备了一种介孔二氧化锰负载的
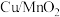 催化剂,并将其应用到苯并三唑(
催化剂,并将其应用到苯并三唑( ,BZA)的降解中,催化机理如下图:
,BZA)的降解中,催化机理如下图:
①BZA可以与
 或
或 结合的原因是
结合的原因是②直接降解BZA的活性氧物种的化学式为
③该过程中
 分解的途径可用语言描述为
分解的途径可用语言描述为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】Ⅰ.铜及其化合物在生产、生活和科研中应用广泛。请回答下列问题:
(1)下列状态的 微粒中,电离最外层一个电子所需能量最大的是___________(填字母)。
微粒中,电离最外层一个电子所需能量最大的是___________(填字母)。
Ⅱ.在 溶液中加入氨水至过量,生成
溶液中加入氨水至过量,生成 。
。
(2) 中
中 原子的杂化类型是
原子的杂化类型是___________ , 分子的立体构型是
分子的立体构型是___________ 。
(3) 能与
能与 形成
形成 ,而
,而 不能,其原因是
不能,其原因是___________ , 的键角比
的键角比 的键角
的键角___________ (填“大”或“小”)。
(4)配位原子提供孤电子对的能力是影响配体与 之间配位键强度的一个重要因素。若用某结构相似的含
之间配位键强度的一个重要因素。若用某结构相似的含 配体与
配体与 配位,所得配合物的稳定性比含
配位,所得配合物的稳定性比含 配体的低,可能的原因是
配体的低,可能的原因是___________ 。
(5) 与
与 形成长链结构的阴离子如图所示,该阴离子中
形成长链结构的阴离子如图所示,该阴离子中 键与
键与 键的数目之比为
键的数目之比为___________ 。

(6)氯化亚铜常用作催化剂、杀菌剂,其晶胞结构可看作金刚石晶胞内部的碳原子被Cl原子代替,顶点和面心的碳原子均被Cu原子代替。以晶胞参数为单位长度建立的坐标系,可以表示晶胞中各原子的位置,称作原子分数坐标。下图为沿y轴投影的氯化亚铜晶胞中所有原子的分布图。若原子1的原子分数坐标为 ( ,
, ,
, ),则原子3的原子分数坐标为
),则原子3的原子分数坐标为___________ ,若晶胞中原子1和原子2之间的距离为dnm,则该晶胞的密度为___________  (设
(设 为阿伏加德罗常数的值)
为阿伏加德罗常数的值)

(1)下列状态的
 微粒中,电离最外层一个电子所需能量最大的是___________(填字母)。
微粒中,电离最外层一个电子所需能量最大的是___________(填字母)。A.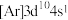 | B. |
C. | D. |
Ⅱ.在
 溶液中加入氨水至过量,生成
溶液中加入氨水至过量,生成 。
。(2)
 中
中 原子的杂化类型是
原子的杂化类型是 分子的立体构型是
分子的立体构型是(3)
 能与
能与 形成
形成 ,而
,而 不能,其原因是
不能,其原因是 的键角比
的键角比 的键角
的键角(4)配位原子提供孤电子对的能力是影响配体与
 之间配位键强度的一个重要因素。若用某结构相似的含
之间配位键强度的一个重要因素。若用某结构相似的含 配体与
配体与 配位,所得配合物的稳定性比含
配位,所得配合物的稳定性比含 配体的低,可能的原因是
配体的低,可能的原因是(5)
 与
与 形成长链结构的阴离子如图所示,该阴离子中
形成长链结构的阴离子如图所示,该阴离子中 键与
键与 键的数目之比为
键的数目之比为
(6)氯化亚铜常用作催化剂、杀菌剂,其晶胞结构可看作金刚石晶胞内部的碳原子被Cl原子代替,顶点和面心的碳原子均被Cu原子代替。以晶胞参数为单位长度建立的坐标系,可以表示晶胞中各原子的位置,称作原子分数坐标。下图为沿y轴投影的氯化亚铜晶胞中所有原子的分布图。若原子1的原子分数坐标为 (
 ,
, ,
, ),则原子3的原子分数坐标为
),则原子3的原子分数坐标为 (设
(设 为阿伏加德罗常数的值)
为阿伏加德罗常数的值)
您最近一年使用:0次
【推荐1】铌是汽车和飞机制造业特别重要的材料,具有良好的耐腐蚀、冷热加工等性能,以高钛渣(含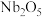 、
、 、
、 、CaO)为原料制取单质的流程如图甲所示:
、CaO)为原料制取单质的流程如图甲所示:


已知:①MIBK为甲基异丁基酮;②钽铌液中含有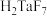 、
、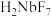 均为弱酸;③
均为弱酸;③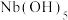 难溶于水。
难溶于水。
(1)酸溶时, 发生的反应的离子方程式为
发生的反应的离子方程式为_______ 。
(2)酸溶时,HF的浓度对铌、钽的浸出率的影响如图丙所示,则HF的最佳浓度为_______  。
。
(3)沉铌时,发生的反应的化学方程式为_______ 。
(4)电解制备铌的原理如图乙所示,阴极发生的电极反应为_______ 。
(5)铌(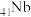 )和镍合金的用途非常广泛,Nb、Ni互化物的晶胞结构如图所示:
)和镍合金的用途非常广泛,Nb、Ni互化物的晶胞结构如图所示:

①铌元素位于周期表中的位置是_______ 。
②图中Nb原子与Ni原子的最短距离为_______ nm。
③Nb、Ni互化物晶体的密度为_______ 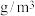 (列出计算式)。
(列出计算式)。
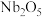 、
、 、
、 、CaO)为原料制取单质的流程如图甲所示:
、CaO)为原料制取单质的流程如图甲所示:

已知:①MIBK为甲基异丁基酮;②钽铌液中含有
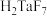 、
、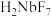 均为弱酸;③
均为弱酸;③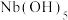 难溶于水。
难溶于水。(1)酸溶时,
 发生的反应的离子方程式为
发生的反应的离子方程式为(2)酸溶时,HF的浓度对铌、钽的浸出率的影响如图丙所示,则HF的最佳浓度为
 。
。(3)沉铌时,发生的反应的化学方程式为
(4)电解制备铌的原理如图乙所示,阴极发生的电极反应为
(5)铌(
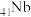 )和镍合金的用途非常广泛,Nb、Ni互化物的晶胞结构如图所示:
)和镍合金的用途非常广泛,Nb、Ni互化物的晶胞结构如图所示:
①铌元素位于周期表中的位置是
②图中Nb原子与Ni原子的最短距离为
③Nb、Ni互化物晶体的密度为
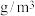 (列出计算式)。
(列出计算式)。
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐2】铜是人类最早使用的金属,在生产生活中有着重要的应用。一种以黄铜矿(主要成分为 ,含少量Fe的氧化物、
,含少量Fe的氧化物、 、Au等)为原料制备纳米Cu的工艺流程如图。
、Au等)为原料制备纳米Cu的工艺流程如图。

回答下列问题:
(1)溶浸前,要将黄铜矿粉碎过筛,目的是___________ 。
(2)溶浸后,滤渣的主要成分为Au、 、
、___________ (填化学式)。
(3)写出加入双氧水氧化时反应的离子方程式___________ 。
(4)氨化时要确保溶液的pH不小于___________ (当离子的浓度 mol·L
mol·L 时视为完全沉淀,已知常温下
时视为完全沉淀,已知常温下 ,
, )。
)。
(5)加入 还原后的滤液经处理可用于
还原后的滤液经处理可用于___________ (填用途)。
(6)保持其他条件相同,分别测得纳米Cu的产率随 和pH变化的曲线如图。
和pH变化的曲线如图。

生产时宜选用的 为
为___________ mol·L ,pH为
,pH为___________ ,pH过大,纳米Cu的产率反而下降的原因可能是___________ 。
(7)Cu的化合物种类繁多,其中与Br形成的一种化合物的晶胞结构如图所示,该晶体的化学式为___________ 。若晶胞的密度为ρg·cm ,则Cu原子与Br原子之间的最短距离为
,则Cu原子与Br原子之间的最短距离为___________ nm( 表示阿伏加德罗常数的值,用含ρ、
表示阿伏加德罗常数的值,用含ρ、 的代数式表示)。
的代数式表示)。

 ,含少量Fe的氧化物、
,含少量Fe的氧化物、 、Au等)为原料制备纳米Cu的工艺流程如图。
、Au等)为原料制备纳米Cu的工艺流程如图。
回答下列问题:
(1)溶浸前,要将黄铜矿粉碎过筛,目的是
(2)溶浸后,滤渣的主要成分为Au、
 、
、(3)写出加入双氧水氧化时反应的离子方程式
(4)氨化时要确保溶液的pH不小于
 mol·L
mol·L 时视为完全沉淀,已知常温下
时视为完全沉淀,已知常温下 ,
, )。
)。(5)加入
 还原后的滤液经处理可用于
还原后的滤液经处理可用于(6)保持其他条件相同,分别测得纳米Cu的产率随
 和pH变化的曲线如图。
和pH变化的曲线如图。
生产时宜选用的
 为
为 ,pH为
,pH为(7)Cu的化合物种类繁多,其中与Br形成的一种化合物的晶胞结构如图所示,该晶体的化学式为
 ,则Cu原子与Br原子之间的最短距离为
,则Cu原子与Br原子之间的最短距离为 表示阿伏加德罗常数的值,用含ρ、
表示阿伏加德罗常数的值,用含ρ、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐3】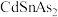 是一种高迁移率的新型热电材料,回答下列问题:
是一种高迁移率的新型热电材料,回答下列问题:
(1) 、
、 、
、 键角由大到小的顺序为
键角由大到小的顺序为___________ 。
(2)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。一种 配合物的结构如下图所示,1mol该配合物中通过螯合作用形成的配位键有
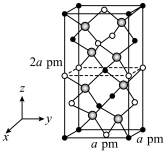
配合物的结构如下图所示,1mol该配合物中通过螯合作用形成的配位键有___________ mol,该螯合物中N的杂化方式有___________ 种。 的晶胞结构如下图所示,晶胞棱边夹角均为90°,晶胞中部分原子的分数坐标如表所示。
的晶胞结构如下图所示,晶胞棱边夹角均为90°,晶胞中部分原子的分数坐标如表所示。
___________ 个Sn,找出距离 最近的Sn
最近的Sn___________ (用分数坐标表示)。 晶体中与单个Sn键合的As有
晶体中与单个Sn键合的As有___________ 个。
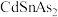 是一种高迁移率的新型热电材料,回答下列问题:
是一种高迁移率的新型热电材料,回答下列问题:(1)
 、
、 、
、 键角由大到小的顺序为
键角由大到小的顺序为(2)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。一种
 配合物的结构如下图所示,1mol该配合物中通过螯合作用形成的配位键有
配合物的结构如下图所示,1mol该配合物中通过螯合作用形成的配位键有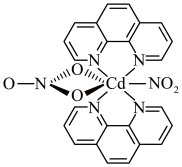
 的晶胞结构如下图所示,晶胞棱边夹角均为90°,晶胞中部分原子的分数坐标如表所示。
的晶胞结构如下图所示,晶胞棱边夹角均为90°,晶胞中部分原子的分数坐标如表所示。| 坐标原子 | X | y | Z |
| Cd | 0 | 0 | 0 |
| Sn | 0 | 0 | 0.5 |
| As | 0.25 | 0.25 | 0.125 |
 最近的Sn
最近的Sn 晶体中与单个Sn键合的As有
晶体中与单个Sn键合的As有
您最近一年使用:0次




