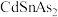 是一种高迁移率的新型热电材料,回答下列问题:
是一种高迁移率的新型热电材料,回答下列问题:(1)
 、
、 、
、 键角由大到小的顺序为
键角由大到小的顺序为(2)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。一种
 配合物的结构如下图所示,1mol该配合物中通过螯合作用形成的配位键有
配合物的结构如下图所示,1mol该配合物中通过螯合作用形成的配位键有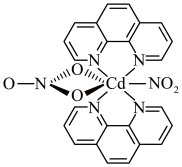
 的晶胞结构如下图所示,晶胞棱边夹角均为90°,晶胞中部分原子的分数坐标如表所示。
的晶胞结构如下图所示,晶胞棱边夹角均为90°,晶胞中部分原子的分数坐标如表所示。| 坐标原子 | X | y | Z |
| Cd | 0 | 0 | 0 |
| Sn | 0 | 0 | 0.5 |
| As | 0.25 | 0.25 | 0.125 |
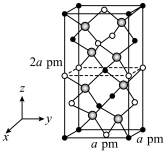
 最近的Sn
最近的Sn 晶体中与单个Sn键合的As有
晶体中与单个Sn键合的As有
更新时间:2024-04-25 13:43:22
|
相似题推荐
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】X、Y、Z、W、M、Q、R六种元素均位于前四周期,且原子序数依次增大。其相关信息如下:X的核外电子总数等于其电子层数;Y的最外层电子数是次外层的3倍;Z原子的价层电子排布为nsn-1npn-2;Q的外围电子排布为(n+1)d4n(n+2)sn; W、M、R最外层电子只有1个。回答下列问题:
(1)Q元素位于周期表第_____ 族。Q金属配合物Q(CO)n的中心原子的价电子数与配体提供的电子总数之和为18,则n=_____ 。M的一种重要化合物用于检查司机是否酒驾,该化合物的化学式______ ,如果司机酒驾检查时该物质显示的颜色变化是_____________________ 。
(2)关于R单质晶体的说法正确的是______________ 。
①晶体中的化学键具有方向性和饱和性
②晶体中不存在阴阳离子间的相互作用
③晶体导电是因为在外加电场作用下产生自由电子
④单质具有光泽是因为金属阳离子吸收并放出可见光
⑤晶体中原子的堆积方式为‥ABCABC•••‥型。
(3)离子化合物中阴阳离子半径之比是决定晶体构型的重要因素之一,配位数与离子半径之比存在如下关系:
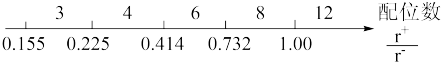
已知,在QY中Q离子的半径为70pm,Y离子的半径为140pm,分析以上信息,可以推导出该晶体结构与常见_______ 晶体(填写化学式)阴阳离子的配位数相同。与阴(阳)离子配位的这几个阳(阴)离子,在空间构成的立体形状为_______________ 。
(4)W的原子半径为r,其晶体的空间利用率______________ (用含r的表达式表示)。
(5)已知SiH4在碱的催化作用下,剧烈发生水解,反应方程式为:SiH4 +(n+2)H2O= SiO2.nH2O + 4H2,已知每1mol SiH4水解反应中转移4mol电子,则C,H,Si三种元素的电负性由大到小的顺序为___________ 。
(6)X射线衍射测定发现,I3AsF6中存在I3+离子,I3+离子的几何结构为______ ,中心原子的杂化方式为_____
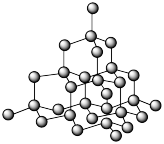
(7)已知金刚石中碳原子的连接方式如下图,则12g金刚石中含有的六元环的数目是________ 个。
(1)Q元素位于周期表第
(2)关于R单质晶体的说法正确的是
①晶体中的化学键具有方向性和饱和性
②晶体中不存在阴阳离子间的相互作用
③晶体导电是因为在外加电场作用下产生自由电子
④单质具有光泽是因为金属阳离子吸收并放出可见光
⑤晶体中原子的堆积方式为‥ABCABC•••‥型。
(3)离子化合物中阴阳离子半径之比是决定晶体构型的重要因素之一,配位数与离子半径之比存在如下关系:
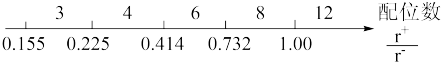
已知,在QY中Q离子的半径为70pm,Y离子的半径为140pm,分析以上信息,可以推导出该晶体结构与常见
(4)W的原子半径为r,其晶体的空间利用率
(5)已知SiH4在碱的催化作用下,剧烈发生水解,反应方程式为:SiH4 +(n+2)H2O= SiO2.nH2O + 4H2,已知每1mol SiH4水解反应中转移4mol电子,则C,H,Si三种元素的电负性由大到小的顺序为
(6)X射线衍射测定发现,I3AsF6中存在I3+离子,I3+离子的几何结构为
(7)已知金刚石中碳原子的连接方式如下图,则12g金刚石中含有的六元环的数目是

您最近半年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】A、B、C、D、E代表五种常见元素,它们的核电荷数依次增大。其中元素E的基态3d轨道上有2个电子,A的基态原子L层电子数是K层电子数的2倍, B是地壳中含量最多的元素,C是短周期中最活泼的金属元素,D与C可形成CD型离子化合物。请回答下列问题:
(1)E的基态原子价层电子排布式为_______________________________。
(2)AB2分子中,A的杂化类型为_______________________________。
(3)AB2形成的晶体的熔点________(填“大于”、“小于”或“无法判断”)CD形成的晶体的熔点,原因是_________________________。
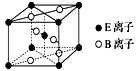
(4)E与B形成的一种橙红色晶体晶胞结构如图所示,其化学式为_______(用元素符号表示)。
(5)由C、D两元素形成的化合物组成的晶体中,阴、阳离子都具有或近似具有球型对称结构,它们都可以看做刚性圆球,并彼此“相切”。如图所示为C、D形成化合物的晶胞结构图以及晶胞的剖面图:
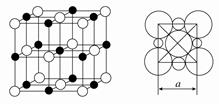
若a=5.6×10-8 cm,则该晶体的密度为________g·cm-3(精确到小数点后1位)。
(1)E的基态原子价层电子排布式为_______________________________。
(2)AB2分子中,A的杂化类型为_______________________________。
(3)AB2形成的晶体的熔点________(填“大于”、“小于”或“无法判断”)CD形成的晶体的熔点,原因是_________________________。
(4)E与B形成的一种橙红色晶体晶胞结构如图所示,其化学式为_______(用元素符号表示)。

(5)由C、D两元素形成的化合物组成的晶体中,阴、阳离子都具有或近似具有球型对称结构,它们都可以看做刚性圆球,并彼此“相切”。如图所示为C、D形成化合物的晶胞结构图以及晶胞的剖面图:

若a=5.6×10-8 cm,则该晶体的密度为________g·cm-3(精确到小数点后1位)。
您最近半年使用:0次
解答题-有机推断题
|
较难
(0.4)
名校
【推荐3】芳香烃A是一种有机合成原料,它可以通过以下合成路线制备含有酯香味物质E。
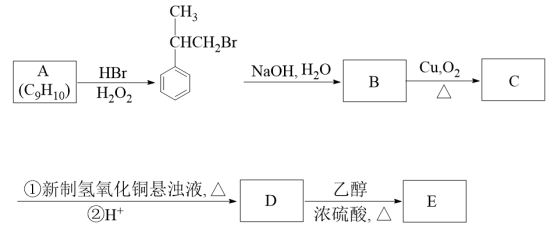
(1)已知A的核磁共振氢谱中出现五组峰,且峰面积之比为3:2:2:2:1,请结合合成路线中的信息,推测A的结构简式____ 。
(2)指出有机物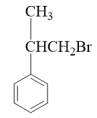 分子中碳原子的杂化方式
分子中碳原子的杂化方式___ 。
(3)B中含有的官能团名称为____ ,B→C的有机反应类型为____ 。
(4)写出D→E的化学方程式____ 。
(5)符合下列条件的D的芳香族同分异构体有____ 种,其中等效氢种类最少的同分异构体的结构简式为____ (任写一种)。
a.能发生水解反应 b.能发生银镜反应
(6)根据上述合成路线的信息,试以丙烯为原料合成丙酸(无机试剂任选)____ 。

(1)已知A的核磁共振氢谱中出现五组峰,且峰面积之比为3:2:2:2:1,请结合合成路线中的信息,推测A的结构简式
(2)指出有机物
 分子中碳原子的杂化方式
分子中碳原子的杂化方式(3)B中含有的官能团名称为
(4)写出D→E的化学方程式
(5)符合下列条件的D的芳香族同分异构体有
a.能发生水解反应 b.能发生银镜反应
(6)根据上述合成路线的信息,试以丙烯为原料合成丙酸(无机试剂任选)
您最近半年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐1】某小组探究不同阴离子与 的结合倾向并分析相关转化。
的结合倾向并分析相关转化。
资料:i. 和
和 均为白色,难溶于水。
均为白色,难溶于水。
ii. 与
与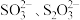 能生成
能生成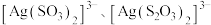
iii.与 结合倾向
结合倾向 。
。
(1)探究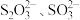 与
与 的结合倾向
的结合倾向
①由实验I推测:与 结合倾向
结合倾向
___________  (填“>”或“<”)。
(填“>”或“<”)。
②取两等份 浊液,分别滴加等浓度、等体积的
浊液,分别滴加等浓度、等体积的 和
和 溶液,前者无明显现象,后者浊液变澄清,澄清溶液中
溶液,前者无明显现象,后者浊液变澄清,澄清溶液中 价银的存在形式
价银的存在形式___________ (填化学式),推测:与 结合倾向
结合倾向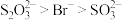 。
。
查阅资料:证实了上述推测。
(2) 的转化
的转化
①写出实验III中白色沉淀消失的离子方程式___________ 。
②查阅资料:实验IV中黑色沉淀是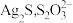 中
中 元素的化合价分别为
元素的化合价分别为 和
和 ,写出实验IV中白色沉淀变为黑色的化学方程式
,写出实验IV中白色沉淀变为黑色的化学方程式___________ 。
③ 溶液可用作定影液。向
溶液可用作定影液。向 溶液溶解
溶液溶解 之后的废定影液中,加入
之后的废定影液中,加入___________ (填试剂),可使定影液再生。
(3)资料显示: 原子与
原子与 结合比
结合比 原子更稳定。
原子更稳定。 与
与 结构相似,但与
结构相似,但与 结合倾向:
结合倾向: ,试从微粒空间结构角度解释原因
,试从微粒空间结构角度解释原因___________ 。
 的结合倾向并分析相关转化。
的结合倾向并分析相关转化。资料:i.
 和
和 均为白色,难溶于水。
均为白色,难溶于水。ii.
 与
与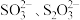 能生成
能生成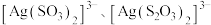
iii.与
 结合倾向
结合倾向 。
。(1)探究
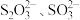 与
与 的结合倾向
的结合倾向 | 实验 | 滴管 | 试管 | 现象 |
| Ⅰ | 10滴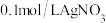 溶液 溶液 | 等浓度的 和 和 溶液 溶液 | 黄色沉淀 | |
| Ⅱ | 等浓度的 和 和 溶液 溶液 | 黄色沉淀 |
 结合倾向
结合倾向
 (填“>”或“<”)。
(填“>”或“<”)。②取两等份
 浊液,分别滴加等浓度、等体积的
浊液,分别滴加等浓度、等体积的 和
和 溶液,前者无明显现象,后者浊液变澄清,澄清溶液中
溶液,前者无明显现象,后者浊液变澄清,澄清溶液中 价银的存在形式
价银的存在形式 结合倾向
结合倾向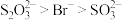 。
。查阅资料:证实了上述推测。
(2)
 的转化
的转化 | 实验 | 滴管 | 试管 | 现象 |
| Ⅲ | 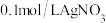 溶液 溶液 | 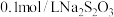 溶液 溶液 | 白色沉淀,振荡后消失 | |
| Ⅳ | 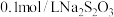 溶液 溶液 | 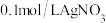 溶液 溶液 | 白色沉淀,逐渐变为灰色,最终为黑色沉淀 |
②查阅资料:实验IV中黑色沉淀是
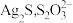 中
中 元素的化合价分别为
元素的化合价分别为 和
和 ,写出实验IV中白色沉淀变为黑色的化学方程式
,写出实验IV中白色沉淀变为黑色的化学方程式③
 溶液可用作定影液。向
溶液可用作定影液。向 溶液溶解
溶液溶解 之后的废定影液中,加入
之后的废定影液中,加入(3)资料显示:
 原子与
原子与 结合比
结合比 原子更稳定。
原子更稳定。 与
与 结构相似,但与
结构相似,但与 结合倾向:
结合倾向: ,试从微粒空间结构角度解释原因
,试从微粒空间结构角度解释原因
您最近半年使用:0次
【推荐2】化合物X由四种元素组成,某兴趣小组按如图流程进行实验。
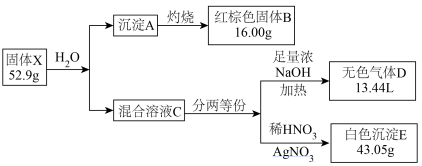
已知:化合物X遇水即分解,混合溶液C呈碱性,气体D可使湿润的红色石蕊试纸变蓝色,气体体积均在标准状况下测定。
(1)X的化学式为:___________ 。
(2)写出无色气体D的电子式:___________ 。
(3)下列关于对氯化铁的用途及性质说法正确的是___________(填字母)。
(4)新制的A略显两性,能溶于热的浓NaOH溶液中,反应的化学方程式___________ 。
(5)白色沉淀E可以溶解在D的浓溶液中,沉淀消失变为无色溶液,该反应的离子方程式为___________ 。

已知:化合物X遇水即分解,混合溶液C呈碱性,气体D可使湿润的红色石蕊试纸变蓝色,气体体积均在标准状况下测定。
(1)X的化学式为:
(2)写出无色气体D的电子式:
(3)下列关于对氯化铁的用途及性质说法正确的是___________(填字母)。
| A.实验室配制FeCl3溶液,通常将FeCl3固体先溶于较浓的盐酸中,然后再稀释至所需浓度 |
| B.用覆铜板制作印刷电路板时,可利用FeCl3溶液作为“腐蚀液”,将覆铜板上不需要的铜腐蚀 |
| C.除去FeCl2中少量FeCl3杂质,可向混合液中加足量铁粉过滤即可 |
| D.气体D与FeCl3溶液可以制备X |
(5)白色沉淀E可以溶解在D的浓溶液中,沉淀消失变为无色溶液,该反应的离子方程式为
您最近半年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】钛酸钙是最典型的钙钛矿型化合物,该类化合物具有特殊的理化性质。
(1)基态 的核外电子排布式为
的核外电子排布式为____________ 。
(2)钛酸钙的晶胞如下图所示。
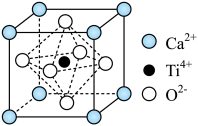
①每个 周围等距且紧邻的
周围等距且紧邻的 有
有______ 个。
②比较 和
和 的离子半径大小并说明理由
的离子半径大小并说明理由____________ 。
(3)钛酸钙的阴、阳离子均可被半径相近的其它离子替代,从而衍生出多种钙钛矿型化合物。
①已知钛酸钙晶胞中距离最近的 和
和 之间的距离为
之间的距离为 ,则钛酸钙晶体密度
,则钛酸钙晶体密度
______  (列出计算式)。
(列出计算式)。
②若忽略离子替代时的体积变化,下列钙钛矿型化合物中,密度大于钛酸钙的是______ (填字母序号)。
a. b.
b.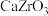 c.
c.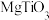
(4)通过离子替代可获得具有优异光电性能的有机钙钛矿型化合物 。其中有机阳离子
。其中有机阳离子 可由甲胺(
可由甲胺( )制得。
)制得。
① 中N的杂化方式为
中N的杂化方式为____________ 。
请从化学键的角度解释由甲胺形成 的过程:
的过程:____________ 。
(1)基态
 的核外电子排布式为
的核外电子排布式为(2)钛酸钙的晶胞如下图所示。

①每个
 周围等距且紧邻的
周围等距且紧邻的 有
有②比较
 和
和 的离子半径大小并说明理由
的离子半径大小并说明理由(3)钛酸钙的阴、阳离子均可被半径相近的其它离子替代,从而衍生出多种钙钛矿型化合物。
①已知钛酸钙晶胞中距离最近的
 和
和 之间的距离为
之间的距离为 ,则钛酸钙晶体密度
,则钛酸钙晶体密度
 (列出计算式)。
(列出计算式)。②若忽略离子替代时的体积变化,下列钙钛矿型化合物中,密度大于钛酸钙的是
a.
 b.
b.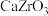 c.
c.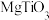
(4)通过离子替代可获得具有优异光电性能的有机钙钛矿型化合物
 。其中有机阳离子
。其中有机阳离子 可由甲胺(
可由甲胺( )制得。
)制得。①
 中N的杂化方式为
中N的杂化方式为请从化学键的角度解释由甲胺形成
 的过程:
的过程:
您最近半年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐1】教材插图具有简洁而又内涵丰富的特点。请回答以下问题:
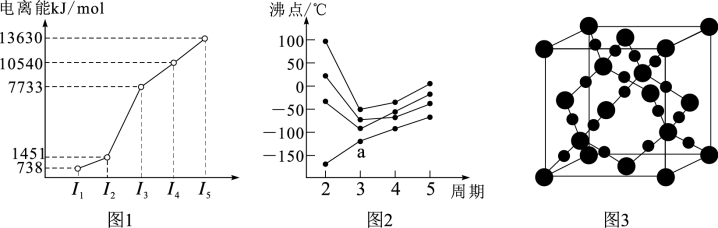
(1)第三周期的某主族元素,其第一至第五电离能数据如图1所示,则该元素原子核外有______ 种不同运动状态的电子。
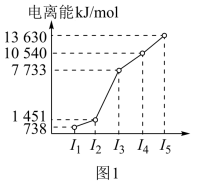
(2)如图2所示,每条折线表示周期表第ⅣA~ⅦA族中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a点代表的是______ 。
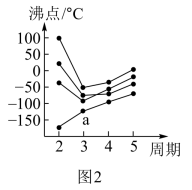
(3)CO2在高温高压下所形成的晶体其晶胞如图3所示。则该晶体的类型属于______ 晶体。
(4)第一电离能介于Al、P之间的第三周期元素有_______ 种。
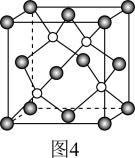
(5)图4是碳化硅的晶胞结构。若碳化硅晶胞边长为apm,阿伏加德罗常数的值为NA,则碳化硅晶体的密度为_______ g/cm3(列出计算式即可)。
(6)浓磷酸在200~300℃时脱水生成焦磷酸(化学式:H4P2O7),焦磷酸的结构式为______ 。
(1)第三周期的某主族元素,其第一至第五电离能数据如图1所示,则该元素原子核外有

(2)如图2所示,每条折线表示周期表第ⅣA~ⅦA族中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a点代表的是

(3)CO2在高温高压下所形成的晶体其晶胞如图3所示。则该晶体的类型属于

(4)第一电离能介于Al、P之间的第三周期元素有
(5)图4是碳化硅的晶胞结构。若碳化硅晶胞边长为apm,阿伏加德罗常数的值为NA,则碳化硅晶体的密度为

(6)浓磷酸在200~300℃时脱水生成焦磷酸(化学式:H4P2O7),焦磷酸的结构式为
您最近半年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】请回答以下问题:
(1)第三周期的某主族元素,其第一至第五电离能数据如图1所示,则该元素对应的原子有__ 种不同运动状态的电子。
(2)如图2所示,每条折线表示周期表ⅣA—ⅦA中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a点代表的是__ 。
(3)CO2在高温高压下所形成的晶体其晶胞如图3所示。则该晶体的类型属于___ 晶体。
(4)第一电离能介于Al、P之间的第三周期元素有___ 种。GaCl3中心原子的杂化方式为___ 。
(5)冰、干冰、碘都是分子晶体,冰的结构具有特殊性,而干冰、碘的晶体具有相似的结构特征,干冰分子中一个分子周围有___ 个紧邻分子。
(6)若[Cu(NH3)4]2+具有对称的空间构型,且当[Cu(NH3)4]2+中的两个NH3被两个Cl-取代时,能得到两种不同结构的产物,则[Cu(NH3)4]2+的空间构型为___ (填字母)。
a.平面正方形 b.正四面体形 c.三角锥形 d.V形
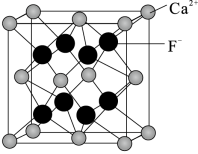
(7)F与Ca可形成离子化合物,其晶胞结构如图所示。其中Ca2+的配位数为___ ,若该晶体的密度为ag·cm-3,则该晶胞的体积是__ cm3(写出表达式即可,设NA为阿伏加德罗常数的值)。

(1)第三周期的某主族元素,其第一至第五电离能数据如图1所示,则该元素对应的原子有
(2)如图2所示,每条折线表示周期表ⅣA—ⅦA中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a点代表的是
(3)CO2在高温高压下所形成的晶体其晶胞如图3所示。则该晶体的类型属于
(4)第一电离能介于Al、P之间的第三周期元素有
(5)冰、干冰、碘都是分子晶体,冰的结构具有特殊性,而干冰、碘的晶体具有相似的结构特征,干冰分子中一个分子周围有
(6)若[Cu(NH3)4]2+具有对称的空间构型,且当[Cu(NH3)4]2+中的两个NH3被两个Cl-取代时,能得到两种不同结构的产物,则[Cu(NH3)4]2+的空间构型为
a.平面正方形 b.正四面体形 c.三角锥形 d.V形
(7)F与Ca可形成离子化合物,其晶胞结构如图所示。其中Ca2+的配位数为

您最近半年使用:0次
【推荐3】以下为一种制取铜的新工艺,原料利用率较高。
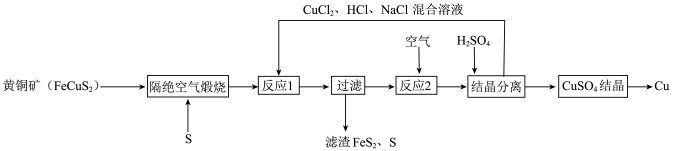
请回答下列问题:
(1)为使隔绝空气煅烧充分进行,工业可采取的措施是_______ (填写合理的一种即可)。
(2)隔绝空气煅烧后固体为 、
、 ,反应1为溶浸反应,则反应1的离子方程式为
,反应1为溶浸反应,则反应1的离子方程式为_______ (已知: )。
)。
(3)反应2发生的主要反应的离子方程式为_______ ,一定温度下,在反应2所得的溶液中加入硫酸,能析出硫酸铜晶体,其可能的原因是_______ 。
(4)滤渣中的 是黄铁矿的主要成分,其晶体结构类似
是黄铁矿的主要成分,其晶体结构类似 ,如图所示:
,如图所示:
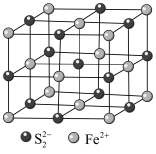
① 的电子式为
的电子式为_______ 。
②晶体结构中离 最近的
最近的 有
有_______ 个, 的电子排布式为
的电子排布式为_______ 。
③若晶胞边长为x ,则此晶体密度为
,则此晶体密度为_______  (用
(用 表示阿伏加德罗常数)。
表示阿伏加德罗常数)。

请回答下列问题:
(1)为使隔绝空气煅烧充分进行,工业可采取的措施是
(2)隔绝空气煅烧后固体为
 、
、 ,反应1为溶浸反应,则反应1的离子方程式为
,反应1为溶浸反应,则反应1的离子方程式为 )。
)。(3)反应2发生的主要反应的离子方程式为
(4)滤渣中的
 是黄铁矿的主要成分,其晶体结构类似
是黄铁矿的主要成分,其晶体结构类似 ,如图所示:
,如图所示:
①
 的电子式为
的电子式为②晶体结构中离
 最近的
最近的 有
有 的电子排布式为
的电子排布式为③若晶胞边长为x
 ,则此晶体密度为
,则此晶体密度为 (用
(用 表示阿伏加德罗常数)。
表示阿伏加德罗常数)。
您最近半年使用:0次



