绿水青山就是金山银山,减少氮的氧化物的排放是环境保护的重要内容。汽车尾气是产生氮的氧化物的主要因素。
Ⅰ.安装催化转化器对汽车尾气进行处理,可以有效减少氮的氧化物排放,减少环境污染。
(1)通过活性炭对汽车尾气进行处理,相关原理为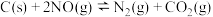 。下列情况能说明该反应达到平衡状态的是
。下列情况能说明该反应达到平衡状态的是__________ 。
A.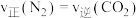
B.混合气体中N2与CO2的物质的量之比保持不变
C.单位时间内断裂NA个 同时形成NA个C=O
同时形成NA个C=O
D.恒温、恒容条件下,混合气体的压强保持不变
E.恒温、恒压条件下,混合气体的平均摩尔质量保持不变
(2)在催化转化器中,汽车尾气中的CO和NO可发生反应 ,若在容积为10L的密闭容器中进行该反应,起始时充入0.4molCO、0.2molNO,反应在不同温度下进行,反应体系总压强随时间的变化如图所示。
,若在容积为10L的密闭容器中进行该反应,起始时充入0.4molCO、0.2molNO,反应在不同温度下进行,反应体系总压强随时间的变化如图所示。

已知:pV=nRT
①实验a、b对应的温度较高的是__________ 。
②实验b从开始至平衡时的平均反应速率
_______  。
。
③实验a中NO的平衡转化率为__________ 。
Ⅱ.为减少汽车尾气的污染,在新技术的支撑下新能源汽车发展迅速。肼一空气燃料电池是一种碱性电池,无污染,能量高,有广泛的应用前景,其工作原理如图所示,
(3)回答下列问题:
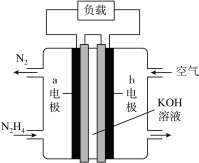
①该燃料电池中负极通入的物质是__________ ,正极发生的反应式为__________ 。
②电池工作时,b极区域碱性__________ (填“增强”或“减弱”或“不变”)。
③当电池放电转移2mol电子时,至少消耗燃料肼__________ g。
Ⅰ.安装催化转化器对汽车尾气进行处理,可以有效减少氮的氧化物排放,减少环境污染。
(1)通过活性炭对汽车尾气进行处理,相关原理为
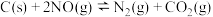 。下列情况能说明该反应达到平衡状态的是
。下列情况能说明该反应达到平衡状态的是A.
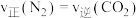
B.混合气体中N2与CO2的物质的量之比保持不变
C.单位时间内断裂NA个
 同时形成NA个C=O
同时形成NA个C=OD.恒温、恒容条件下,混合气体的压强保持不变
E.恒温、恒压条件下,混合气体的平均摩尔质量保持不变
(2)在催化转化器中,汽车尾气中的CO和NO可发生反应
 ,若在容积为10L的密闭容器中进行该反应,起始时充入0.4molCO、0.2molNO,反应在不同温度下进行,反应体系总压强随时间的变化如图所示。
,若在容积为10L的密闭容器中进行该反应,起始时充入0.4molCO、0.2molNO,反应在不同温度下进行,反应体系总压强随时间的变化如图所示。
已知:pV=nRT
①实验a、b对应的温度较高的是
②实验b从开始至平衡时的平均反应速率

 。
。③实验a中NO的平衡转化率为
Ⅱ.为减少汽车尾气的污染,在新技术的支撑下新能源汽车发展迅速。肼一空气燃料电池是一种碱性电池,无污染,能量高,有广泛的应用前景,其工作原理如图所示,
(3)回答下列问题:

①该燃料电池中负极通入的物质是
②电池工作时,b极区域碱性
③当电池放电转移2mol电子时,至少消耗燃料肼
更新时间:2023-07-01 11:19:14
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】近日IPCC发布了由来自 个国家的
个国家的 位科学家编写的《全球升温
位科学家编写的《全球升温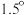 特别报告》,温室效应引发的环境问题日益严重,物种灭绝,洪灾、旱灾、粮食欠收等自然灾害发生频率不断增加,
特别报告》,温室效应引发的环境问题日益严重,物种灭绝,洪灾、旱灾、粮食欠收等自然灾害发生频率不断增加, 的减排和综合利用是解决温室及能源问题的有效途径。
的减排和综合利用是解决温室及能源问题的有效途径。
(1) 可转化成有机物实现碳循环,在体积为1L的密闭容器中,充入
可转化成有机物实现碳循环,在体积为1L的密闭容器中,充入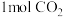 和
和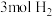 ,一定条件下反应:
,一定条件下反应: ,测得
,测得 和
和 的浓度随时间变化如图所示。
的浓度随时间变化如图所示。
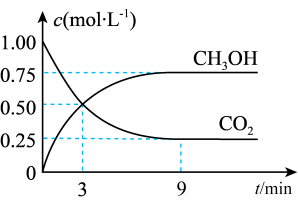
下列说法正确的是_______ (填字母)。
A.混合气体的密度不随时间的变化而变化,则说明上述反应达到平衡状态
B.平衡时 的转化率为
的转化率为
C.平衡时混合气体中 的体积分数是
的体积分数是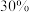
D.该条件下,第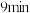 时
时 大于第
大于第 时
时 。
。
(2)工业中, 和
和 在催化剂
在催化剂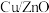 作用下可发生两个平行反应,分别生成
作用下可发生两个平行反应,分别生成 和
和 。
。
反应A:
反应B:
控制 和
和 初始投料比为
初始投料比为 时,温度对
时,温度对 平衡转化率及甲醇和CO产率的影响如图所示。
平衡转化率及甲醇和CO产率的影响如图所示。
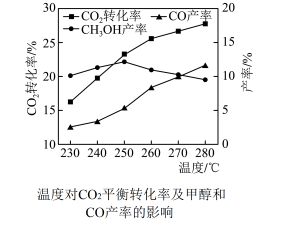
①由图可知温度升高CO的产率上升,其主要原因可能是_______ ;
②由图可知获取 最适宜的温度是
最适宜的温度是_______ ,下列措施有利于提高 转化为
转化为 的平衡转化率的有
的平衡转化率的有_______ (填字母);
A.使用催化剂
B.增大体系压强
C.增大 和
和 的初始投料比
的初始投料比
D.投料比不变和容器体积不变,增加反应物的浓度
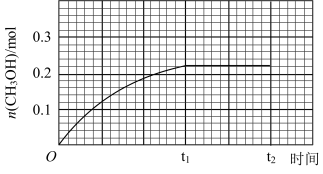
(3) 下
下 物质的量随时间的变化曲线如图所示。画出
物质的量随时间的变化曲线如图所示。画出 下
下 时刻
时刻 物质的量随时间的变化曲线示意图
物质的量随时间的变化曲线示意图_______ 。
 个国家的
个国家的 位科学家编写的《全球升温
位科学家编写的《全球升温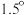 特别报告》,温室效应引发的环境问题日益严重,物种灭绝,洪灾、旱灾、粮食欠收等自然灾害发生频率不断增加,
特别报告》,温室效应引发的环境问题日益严重,物种灭绝,洪灾、旱灾、粮食欠收等自然灾害发生频率不断增加, 的减排和综合利用是解决温室及能源问题的有效途径。
的减排和综合利用是解决温室及能源问题的有效途径。(1)
 可转化成有机物实现碳循环,在体积为1L的密闭容器中,充入
可转化成有机物实现碳循环,在体积为1L的密闭容器中,充入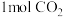 和
和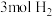 ,一定条件下反应:
,一定条件下反应: ,测得
,测得 和
和 的浓度随时间变化如图所示。
的浓度随时间变化如图所示。
下列说法正确的是
A.混合气体的密度不随时间的变化而变化,则说明上述反应达到平衡状态
B.平衡时
 的转化率为
的转化率为
C.平衡时混合气体中
 的体积分数是
的体积分数是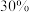
D.该条件下,第
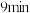 时
时 大于第
大于第 时
时 。
。(2)工业中,
 和
和 在催化剂
在催化剂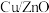 作用下可发生两个平行反应,分别生成
作用下可发生两个平行反应,分别生成 和
和 。
。反应A:

反应B:

控制
 和
和 初始投料比为
初始投料比为 时,温度对
时,温度对 平衡转化率及甲醇和CO产率的影响如图所示。
平衡转化率及甲醇和CO产率的影响如图所示。
①由图可知温度升高CO的产率上升,其主要原因可能是
②由图可知获取
 最适宜的温度是
最适宜的温度是 转化为
转化为 的平衡转化率的有
的平衡转化率的有A.使用催化剂
B.增大体系压强
C.增大
 和
和 的初始投料比
的初始投料比D.投料比不变和容器体积不变,增加反应物的浓度
(3)
 下
下 物质的量随时间的变化曲线如图所示。画出
物质的量随时间的变化曲线如图所示。画出 下
下 时刻
时刻 物质的量随时间的变化曲线示意图
物质的量随时间的变化曲线示意图
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】某兴趣小组对该反应进行了实验探究。在一定温度和催化剂的条件下,将0.1molNH3通入3L的密闭容器中进行反应(此时容器内总压为200kPa),各物质的分压随时间的变化曲线如图所示。

在该温度下,反应的标准平衡常数K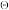 =
=___________ 。(已知:分压=总压×该组分物质的量分数,对于反应dD(g)+eE(g) gG(g)+hH(g),K
gG(g)+hH(g),K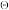 =
= ,其中p
,其中p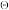 =100kPa,PG、PH、PD、PE为各组分的平衡分压)。
=100kPa,PG、PH、PD、PE为各组分的平衡分压)。

在该温度下,反应的标准平衡常数K
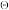 =
= gG(g)+hH(g),K
gG(g)+hH(g),K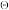 =
= ,其中p
,其中p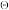 =100kPa,PG、PH、PD、PE为各组分的平衡分压)。
=100kPa,PG、PH、PD、PE为各组分的平衡分压)。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】氨和铵盐用途广泛。
(1)工业合成氨的反应是 N2+3H2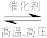 2NH3 。
2NH3 。
① 一定温度下,在某500mL的密闭容器中充入3mol H2 和 1 mol N2,3min后反应达平衡,H2的物质的量为0.75mol,求
a. H2的转化率,___________
b.平衡时NH3的体积分数___________ 。(写出计算过程)
② 对上述反应,下列说法不正确的是___________
A.正反应方向和逆反应方向均能进行的化学反应统称为可逆反应
B.当可逆反应的正反应速率和逆反应速率相等时,该反应达到化学平衡状态
C.化学反应的限度决定了反应物在该条件下的最大转化率
D.改变可逆反应的反应条件可以在一定程度上改变其化学平衡状态
(2)已知日常所用的干电池中,其电极分别为碳棒和锌皮,以糊状NH4Cl和ZnCl2作为电解质,电极反应可简化为2NH + 2e-=2NH3+H2 (还加入填充物MnO2,用于吸收H2生成水,NH3与Zn2+结合为稳定物质)。根据以上信息,日常所用的干电池的正极是
+ 2e-=2NH3+H2 (还加入填充物MnO2,用于吸收H2生成水,NH3与Zn2+结合为稳定物质)。根据以上信息,日常所用的干电池的正极是___________ ,负极是___________ 。当生成25.5克NH3时,转移___________ mol电子。
(1)工业合成氨的反应是 N2+3H2
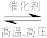 2NH3 。
2NH3 。① 一定温度下,在某500mL的密闭容器中充入3mol H2 和 1 mol N2,3min后反应达平衡,H2的物质的量为0.75mol,求
a. H2的转化率,
b.平衡时NH3的体积分数
② 对上述反应,下列说法不正确的是
A.正反应方向和逆反应方向均能进行的化学反应统称为可逆反应
B.当可逆反应的正反应速率和逆反应速率相等时,该反应达到化学平衡状态
C.化学反应的限度决定了反应物在该条件下的最大转化率
D.改变可逆反应的反应条件可以在一定程度上改变其化学平衡状态
(2)已知日常所用的干电池中,其电极分别为碳棒和锌皮,以糊状NH4Cl和ZnCl2作为电解质,电极反应可简化为2NH
 + 2e-=2NH3+H2 (还加入填充物MnO2,用于吸收H2生成水,NH3与Zn2+结合为稳定物质)。根据以上信息,日常所用的干电池的正极是
+ 2e-=2NH3+H2 (还加入填充物MnO2,用于吸收H2生成水,NH3与Zn2+结合为稳定物质)。根据以上信息,日常所用的干电池的正极是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】 的回收和利用是减少碳排放的重要途径。
的回收和利用是减少碳排放的重要途径。
(1)一定条件下, 与足量
与足量 充分反应生成水蒸气和16g甲醇蒸气时放出热量为24.5kJ。写出该反应的热化学方程式:
充分反应生成水蒸气和16g甲醇蒸气时放出热量为24.5kJ。写出该反应的热化学方程式:_______ 。
(2)我国科学家开发新型催化剂,高效电还原 制备乙烯(C2H4),装置如图。
制备乙烯(C2H4),装置如图。

通过该装置可将_______ (填“化学”或“电”,下同)能变为_______ 能。
(3)一定温度下,在某恒容密闭容器中充入 和
和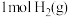 发生反应
发生反应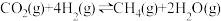 ,下列情况能说明该反应达到平衡状态的是_______(填标号)。
,下列情况能说明该反应达到平衡状态的是_______(填标号)。
(4)利用 制备合成气,发生反应为
制备合成气,发生反应为 。在2L恒容密闭容器中投入
。在2L恒容密闭容器中投入 和
和 ,发生上述反应,测得不同温度下
,发生上述反应,测得不同温度下 的转化率[反应消耗
的转化率[反应消耗 的物质的量占起始投入
的物质的量占起始投入 的物质的量的百分比]与反应时间的关系如图所示。
的物质的量的百分比]与反应时间的关系如图所示。

①T1℃下,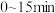 内
内 的平均反应速率为
的平均反应速率为_______  ,15min时,
,15min时, 的平衡转化率为
的平衡转化率为_______ 。
②在a、b、c三点中,正反应速率最小的是_______ 点,判断依据是_______ 。
 的回收和利用是减少碳排放的重要途径。
的回收和利用是减少碳排放的重要途径。(1)一定条件下,
 与足量
与足量 充分反应生成水蒸气和16g甲醇蒸气时放出热量为24.5kJ。写出该反应的热化学方程式:
充分反应生成水蒸气和16g甲醇蒸气时放出热量为24.5kJ。写出该反应的热化学方程式:(2)我国科学家开发新型催化剂,高效电还原
 制备乙烯(C2H4),装置如图。
制备乙烯(C2H4),装置如图。
通过该装置可将
(3)一定温度下,在某恒容密闭容器中充入
 和
和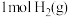 发生反应
发生反应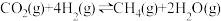 ,下列情况能说明该反应达到平衡状态的是_______(填标号)。
,下列情况能说明该反应达到平衡状态的是_______(填标号)。A. 的浓度比不随时间变化 的浓度比不随时间变化 |
| B.混合气体总压强不随时间变化 |
| C.混合气体的平均摩尔质量不随时间变化 |
D. 消耗速率等于 消耗速率等于 消耗速率的4倍 消耗速率的4倍 |
 制备合成气,发生反应为
制备合成气,发生反应为 。在2L恒容密闭容器中投入
。在2L恒容密闭容器中投入 和
和 ,发生上述反应,测得不同温度下
,发生上述反应,测得不同温度下 的转化率[反应消耗
的转化率[反应消耗 的物质的量占起始投入
的物质的量占起始投入 的物质的量的百分比]与反应时间的关系如图所示。
的物质的量的百分比]与反应时间的关系如图所示。
①T1℃下,
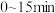 内
内 的平均反应速率为
的平均反应速率为 ,15min时,
,15min时, 的平衡转化率为
的平衡转化率为②在a、b、c三点中,正反应速率最小的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】在2 L的密闭容器中,进行如下化学反应:CO2(g)+H2(g) CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
回答下列问题:
(1)该反应为______________ (填“吸热”或“放热”)反应。
(2)能判断该反应是否达到化学平衡状态的依据是________ 。
A.容器中压强不变 B.混合气体中c(CO)不变
C.v正(H2)=v逆(H2O) D.c(CO2)=c(CO)
(3)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为________ ℃。该温度下,若向该容器中充入n(CO2)=1 mol,n(H2)=1 mol,4 min末达到平衡,CO2的转化率为_____________ ,H2的体积分数为_________ 。
 CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:| t ℃ | 700 | 800 | 830 | 1 000 | 1 200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应为
(2)能判断该反应是否达到化学平衡状态的依据是
A.容器中压强不变 B.混合气体中c(CO)不变
C.v正(H2)=v逆(H2O) D.c(CO2)=c(CO)
(3)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】已知2A2(g)+B2(g) 2C(g) ΔH=-a kJ·mol-1(a>0),在一个有催化剂的固定容积的容器中加入2 mol A2和1 mol B2,在500 ℃时充分反应达到平衡后C的浓度为w mol·L-1,放出热量b kJ。
2C(g) ΔH=-a kJ·mol-1(a>0),在一个有催化剂的固定容积的容器中加入2 mol A2和1 mol B2,在500 ℃时充分反应达到平衡后C的浓度为w mol·L-1,放出热量b kJ。
(1)a___ (填“>”“=”或“<”)b。
(2)若将反应温度升高到700 ℃,该反应的平衡常数将___ (填“增大”“减小”或“不变”)。
(3)若在原来的容器中只加入2 mol C,500 ℃时充分反应达到平衡后,吸收热量c kJ,C的浓度___ (填“>”“=”或“<”)w mol·L-1。
(4)能说明该反应已经达到平衡状态的 是
是___ 。
a.v(C)=2v(B2) b.容器内压强保持不变c.v逆(A2)=2v 正(B2)d.容器内气体的密度保持不变
正(B2)d.容器内气体的密度保持不变
(5)使该反应的反应速率增大,且平衡向正反应方向移动的操作是___ 。
a.及时分离出C气体b. 适当升高温度c.增大B2的浓度 d.选择高效的催化剂
适当升高温度c.增大B2的浓度 d.选择高效的催化剂
 2C(g) ΔH=-a kJ·mol-1(a>0),在一个有催化剂的固定容积的容器中加入2 mol A2和1 mol B2,在500 ℃时充分反应达到平衡后C的浓度为w mol·L-1,放出热量b kJ。
2C(g) ΔH=-a kJ·mol-1(a>0),在一个有催化剂的固定容积的容器中加入2 mol A2和1 mol B2,在500 ℃时充分反应达到平衡后C的浓度为w mol·L-1,放出热量b kJ。(1)a
(2)若将反应温度升高到700 ℃,该反应的平衡常数将
(3)若在原来的容器中只加入2 mol C,500 ℃时充分反应达到平衡后,吸收热量c kJ,C的浓度
(4)能说明该反应已经达到平衡状态的
 是
是a.v(C)=2v(B2) b.容器内压强保持不变c.v逆(A2)=2v
 正(B2)d.容器内气体的密度保持不变
正(B2)d.容器内气体的密度保持不变(5)使该反应的反应速率增大,且平衡向正反应方向移动的操作是
a.及时分离出C气体b.
 适当升高温度c.增大B2的浓度 d.选择高效的催化剂
适当升高温度c.增大B2的浓度 d.选择高效的催化剂
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】I.某研究性学习小组根据反应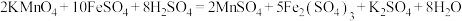 设计如图原电池,其中甲、乙两烧杯中各物质的物质的量浓度均为
设计如图原电池,其中甲、乙两烧杯中各物质的物质的量浓度均为 ,溶液的体积均为
,溶液的体积均为 ,盐桥中装有饱和
,盐桥中装有饱和 溶液。
溶液。
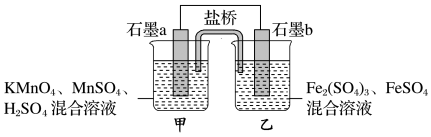
回答下列问题:
(1)此原电池的负极是石墨______ (填“a”或“b”),电池工作时,盐桥中的 移向
移向______ (填“甲”或“乙”)烧杯。
(2)正极反应式为:______ 。
II.某甲醇燃料电池的工作原理如图所示,质子交换膜(只有质子能够通过)左右两侧的溶液均为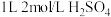 溶液。
溶液。
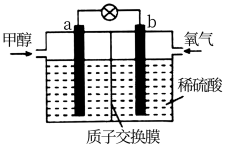
(3)当导线中有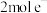 发生转移时,左右两侧溶液的质量差为
发生转移时,左右两侧溶液的质量差为______ g(假设反应物耗尽,忽略气体的溶解)。
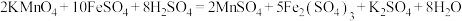 设计如图原电池,其中甲、乙两烧杯中各物质的物质的量浓度均为
设计如图原电池,其中甲、乙两烧杯中各物质的物质的量浓度均为 ,溶液的体积均为
,溶液的体积均为 ,盐桥中装有饱和
,盐桥中装有饱和 溶液。
溶液。
回答下列问题:
(1)此原电池的负极是石墨
 移向
移向(2)正极反应式为:
II.某甲醇燃料电池的工作原理如图所示,质子交换膜(只有质子能够通过)左右两侧的溶液均为
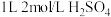 溶液。
溶液。
(3)当导线中有
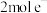 发生转移时,左右两侧溶液的质量差为
发生转移时,左右两侧溶液的质量差为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】填空。
(1)将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的。下图是通过人工光合作用,以 和
和 为原料制备
为原料制备 和
和 的原理示意图。电极b作
的原理示意图。电极b作_______ 极,表面发生的电极反应为_______ 。

(2)浓差电池中的电动势是由于电池中存在浓度差而产生的。某浓差电池的原理如下图所示,该电池从浓缩海水中提取 的同时又获得了电能。
的同时又获得了电能。
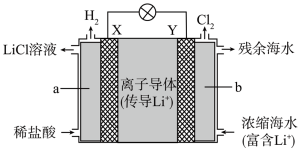
①X为_______ 极,Y极反应式为_______ 。
②Y极生成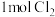 时,
时,_______ 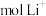 移向
移向_______ (填“X”或“Y”)极。
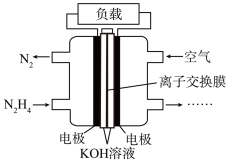
(3)一种以肼(N2H4)为液体燃料的电池装置如下图所示。该电池用空气中的氧气作氧化剂, 作电解质。负极反应式为
作电解质。负极反应式为_______ ;正极反应式为_______ 。
(1)将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的。下图是通过人工光合作用,以
 和
和 为原料制备
为原料制备 和
和 的原理示意图。电极b作
的原理示意图。电极b作
(2)浓差电池中的电动势是由于电池中存在浓度差而产生的。某浓差电池的原理如下图所示,该电池从浓缩海水中提取
 的同时又获得了电能。
的同时又获得了电能。
①X为
②Y极生成
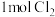 时,
时,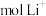 移向
移向(3)一种以肼(N2H4)为液体燃料的电池装置如下图所示。该电池用空气中的氧气作氧化剂,
 作电解质。负极反应式为
作电解质。负极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】燃料电池是一种能量转换效率高、对环境友好的化学电源,如图为一种氢氧燃料电池的结构装置。
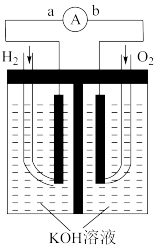
(1)电极b为该燃料电池的_______ 极(填“正”或“负”),电极方程式为_______ ;负极的电极反应式为_______ ;总反应式为_____
(2)电池工作时,溶液中的OH﹣移向_______ 极(填“a”或“b”);
(3)电池工作时,在导线中电子流动方向为_______ (用a、b表示);
(4)电池使用一段时间后,溶液的pH值_______ (填“增大”或“减小”);
(5)当电池工作一段时间后消耗标准状况下H2为6.72L时,转移电子_______ mol。

(1)电极b为该燃料电池的
(2)电池工作时,溶液中的OH﹣移向
(3)电池工作时,在导线中电子流动方向为
(4)电池使用一段时间后,溶液的pH值
(5)当电池工作一段时间后消耗标准状况下H2为6.72L时,转移电子
您最近一年使用:0次



