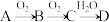铜(过量)与浓硝酸反应,制备少量NaNO3,装置如下图所示。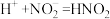 ,HNO2不稳定,易分解为硝酸和一氧化氮
,HNO2不稳定,易分解为硝酸和一氧化氮
(1)产生的红棕色气体是___________ 。
(2)一段时间后,试管中不再产生气体,静置。
①试管中溶液c(H+)___________ c( )(填“>”或“<”)。
)(填“>”或“<”)。
②滴加稀H2SO4,铜丝继续溶解,产生无色气体,反应的离子方程式是___________ 。
(3)NaOH溶液吸收NO2、NO。
①
___________
②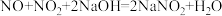
(4)向烧杯中加入稀HNO3,加热,搅拌,冷却结晶,过滤得NaNO3固体。稀HNO3的作用是 、
、___________ (用化学方程式表示)。
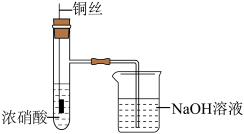
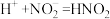 ,HNO2不稳定,易分解为硝酸和一氧化氮
,HNO2不稳定,易分解为硝酸和一氧化氮(1)产生的红棕色气体是
(2)一段时间后,试管中不再产生气体,静置。
①试管中溶液c(H+)
 )(填“>”或“<”)。
)(填“>”或“<”)。②滴加稀H2SO4,铜丝继续溶解,产生无色气体,反应的离子方程式是
(3)NaOH溶液吸收NO2、NO。
①

②
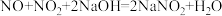
(4)向烧杯中加入稀HNO3,加热,搅拌,冷却结晶,过滤得NaNO3固体。稀HNO3的作用是
 、
、
22-23高一下·北京朝阳·期末 查看更多[3]
北京朝阳区2022-2023学年高一下学期7月期末考试化学试题北京市陈经纶中学2023-2024学年高一下学期3月月考化学试题(已下线)专题01 硫、氮及其化合物-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(北京专用)
更新时间:2023-07-13 10:02:55
|
相似题推荐
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐1】Ⅰ.将海水淡化与浓海水资源化结合起来是综合利用海水的重要途径之一,一般是先将海水淡化获得淡水,再从剩余的浓海水中通过一系列工艺流程提取其他产品。回答下问题:
(1)请列举一种海水淡化的方法:_______ 。
(2)海水提溴中将Br2从苦卤中吹出,利用了Br2的_______ 性。
Ⅱ.通过传统的海带提碘工艺提取单质碘后,其所得废水中尚残留部分的I2,可用活性炭吸附法加以回收利用。具体流程如图:
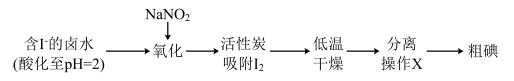
已知:i.pH=2时,NaNO2溶液只能将I-氧化为I2,同时生成NO
ii.将湿润的淀粉-KI试纸伸入盛满氯气的集气瓶中,试纸先变蓝,后褪色
(3)写出氧化含I-的卤水中发生的离子方程式:________ 。
(4)在分离操作X的装置如图所示,电加热器的作用是________ ,得到I2的位置位于该装置中________ 处(填图中选项)。

(5)已知Cl2的氧化性强于NaNO2,但该方法中却选择了价格较高的NaNO2,原因是_______ 。
(6)某工厂排出的废水,经测定含0.012mol/L的游离I2和8×10-4mol/L的H+,若改用加Na2SO3的方法除去I2,发生的化学反应为:Na2SO3+I2+H2O=Na2SO4+2HI,该反应中氧化产物与还原产物的物质的量之比为_______ ,现需处理5L该废水,则需加入0.05mol/L的Na2SO3溶液_______ L才能把I2除尽。
(1)请列举一种海水淡化的方法:
(2)海水提溴中将Br2从苦卤中吹出,利用了Br2的
Ⅱ.通过传统的海带提碘工艺提取单质碘后,其所得废水中尚残留部分的I2,可用活性炭吸附法加以回收利用。具体流程如图:

已知:i.pH=2时,NaNO2溶液只能将I-氧化为I2,同时生成NO
ii.将湿润的淀粉-KI试纸伸入盛满氯气的集气瓶中,试纸先变蓝,后褪色
(3)写出氧化含I-的卤水中发生的离子方程式:
(4)在分离操作X的装置如图所示,电加热器的作用是

(5)已知Cl2的氧化性强于NaNO2,但该方法中却选择了价格较高的NaNO2,原因是
(6)某工厂排出的废水,经测定含0.012mol/L的游离I2和8×10-4mol/L的H+,若改用加Na2SO3的方法除去I2,发生的化学反应为:Na2SO3+I2+H2O=Na2SO4+2HI,该反应中氧化产物与还原产物的物质的量之比为
您最近一年使用:0次
【推荐2】Ⅰ.氧化镁在医药、建筑等行业应用广泛。硫酸镁还原热解制备高纯氧化镁是一种新的探索。以菱镁矿(主要成分为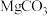 ,另含少量杂质
,另含少量杂质 和
和 等)为原料制备高纯氧化镁的实验流程如下:
等)为原料制备高纯氧化镁的实验流程如下:
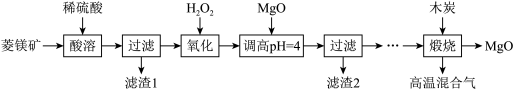
已知:① 不溶于稀硫酸和稀盐酸,②滤渣2中除了过量的MgO外,还含有
不溶于稀硫酸和稀盐酸,②滤渣2中除了过量的MgO外,还含有 。
。
(1)酸溶时,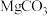 与稀硫酸反应的离子方程式为
与稀硫酸反应的离子方程式为_______ 。
(2)滤渣1的化学式为_______ 。
(3)“氧化”流程的目的把 氧化成
氧化成 ,再调节pH把
,再调节pH把 除去,写出“氧化”流程的离子方程式为
除去,写出“氧化”流程的离子方程式为_______ 。
Ⅱ.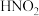 是一种弱酸,且不稳定,易分解生成NO和
是一种弱酸,且不稳定,易分解生成NO和 ;它能被常见的强氧化剂氧化:在酸性溶液中它也是一种氧化剂,如能把
;它能被常见的强氧化剂氧化:在酸性溶液中它也是一种氧化剂,如能把 氧化成
氧化成 。
。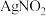 是一种难溶于水、易溶于酸的化合物,试回答下列问题:
是一种难溶于水、易溶于酸的化合物,试回答下列问题:
(4)人体正常的血红蛋白含有 ,若误食亚硝酸盐(如
,若误食亚硝酸盐(如 ),则导致血红蛋白中的
),则导致血红蛋白中的 转化为
转化为 而中毒,服用维生素C可解毒。下列叙述不正确的是_______(填字母)。
而中毒,服用维生素C可解毒。下列叙述不正确的是_______(填字母)。
(5)某同学把新制的氯水(主要成分 )加到
)加到 溶液中,观察到氯水褪色,同时生成
溶液中,观察到氯水褪色,同时生成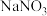 和HCl,请写出反应的离子方程式:
和HCl,请写出反应的离子方程式:_______ 。
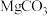 ,另含少量杂质
,另含少量杂质 和
和 等)为原料制备高纯氧化镁的实验流程如下:
等)为原料制备高纯氧化镁的实验流程如下:
已知:①
 不溶于稀硫酸和稀盐酸,②滤渣2中除了过量的MgO外,还含有
不溶于稀硫酸和稀盐酸,②滤渣2中除了过量的MgO外,还含有 。
。(1)酸溶时,
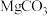 与稀硫酸反应的离子方程式为
与稀硫酸反应的离子方程式为(2)滤渣1的化学式为
(3)“氧化”流程的目的把
 氧化成
氧化成 ,再调节pH把
,再调节pH把 除去,写出“氧化”流程的离子方程式为
除去,写出“氧化”流程的离子方程式为Ⅱ.
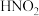 是一种弱酸,且不稳定,易分解生成NO和
是一种弱酸,且不稳定,易分解生成NO和 ;它能被常见的强氧化剂氧化:在酸性溶液中它也是一种氧化剂,如能把
;它能被常见的强氧化剂氧化:在酸性溶液中它也是一种氧化剂,如能把 氧化成
氧化成 。
。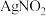 是一种难溶于水、易溶于酸的化合物,试回答下列问题:
是一种难溶于水、易溶于酸的化合物,试回答下列问题:(4)人体正常的血红蛋白含有
 ,若误食亚硝酸盐(如
,若误食亚硝酸盐(如 ),则导致血红蛋白中的
),则导致血红蛋白中的 转化为
转化为 而中毒,服用维生素C可解毒。下列叙述不正确的是_______(填字母)。
而中毒,服用维生素C可解毒。下列叙述不正确的是_______(填字母)。| A.亚硝酸盐被还原 | B.维生素C是还原剂 |
C.维生素C将 还原为 还原为 | D.亚硝酸盐是还原剂 |
 )加到
)加到 溶液中,观察到氯水褪色,同时生成
溶液中,观察到氯水褪色,同时生成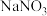 和HCl,请写出反应的离子方程式:
和HCl,请写出反应的离子方程式:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】如图是实验室研究潜水艇中供氧体系反应机理的装置图(夹持仪器略)。
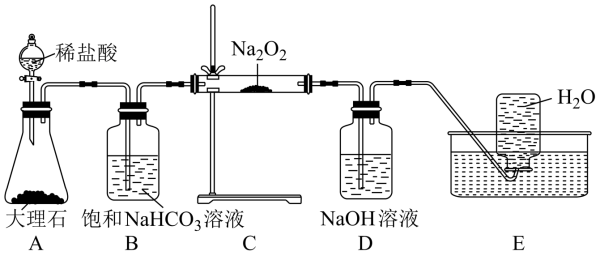
(1)A装置为 的发生装置,反应的离子方程式为
的发生装置,反应的离子方程式为_______ 。
(2)B装置的作用_______ 。
(3)C装置为 的发生装置,发生反应的化学方程式为:①
的发生装置,发生反应的化学方程式为:①_______ 、②_______ 。
(4)C装置中固体由淡黄色完全变为白色,检验固体成分的实验方案为:取少量C装置中反应后的固体溶于水,向溶液中滴入过量_______ 溶液,若有白色沉淀生成,则证明固体中含有_______ ;过滤后,向滤液中滴入几滴酚酞溶液,若_______ 且不褪色,则证明固体中含_______ 。

(1)A装置为
 的发生装置,反应的离子方程式为
的发生装置,反应的离子方程式为(2)B装置的作用
(3)C装置为
 的发生装置,发生反应的化学方程式为:①
的发生装置,发生反应的化学方程式为:①(4)C装置中固体由淡黄色完全变为白色,检验固体成分的实验方案为:取少量C装置中反应后的固体溶于水,向溶液中滴入过量
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐1】某硫化锌精矿的主要成分为ZnS(还含一定量FeS),以其为原料制备七水合硫酸锌(ZnSO4·7H2O)与铁红的工艺流程如图所示:
①焙砂的成分是ZnO和FeO
②相关金属离子形成氢氧化物沉淀的pH范围如下:
回答下列问题:
(1)“焙烧”时为了加快反应速率,可以采取的措施是_______ ,其中ZnS发生反应的化学方程式为_______ 。“净化制酸”所得的产品可用于后续的_______ 操作。
(2)“浸出”后加入H2O2发生反应的离子方程式为_______ ,调pH的目的是将Fe3+完全转化为Fe(OH)3沉淀并与Zn2+分离,为达到该目的,调节pH的范围是_______ 。
(3)“滤渣”的化学式是_______ ,由“滤液”得到ZnSO4·7H2O的操作是蒸发浓缩、_______ 、过滤洗涤。
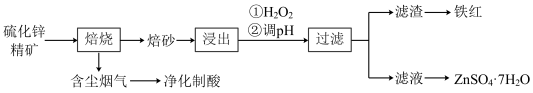
①焙砂的成分是ZnO和FeO
②相关金属离子形成氢氧化物沉淀的pH范围如下:
| 金属离子 | Fe3+ | Fe2+ | Zn2+ |
| 开始沉淀的pH | 1.5 | 6.3 | 6.2 |
| 沉淀完全的pH | 2.8 | 8.3 | 8.2 |
(1)“焙烧”时为了加快反应速率,可以采取的措施是
(2)“浸出”后加入H2O2发生反应的离子方程式为
(3)“滤渣”的化学式是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】某化学实验小组用酸性 KMnO4 溶液和草酸(H2C2O4)溶液反应,研究外界条件对反应速率的影响,实验操作及现象如下:
(1)将高锰酸钾与草酸反应的离子方程式补充完整__________ :
□MnO +□H2C2O4 + □ = □Mn2+ +□ +□H2O
+□H2C2O4 + □ = □Mn2+ +□ +□H2O
(2)由实验 I、Ⅱ可得出的结论是_____ 。
(3)关于实验Ⅱ中 80s 后溶液颜色迅速变浅的原因,该小组提出了猜想:该反应中生成的 Mn2+ 对反应有催化作用。设计实验 Ⅲ,验证猜想。
① 补全实验Ⅲ的操作:
向试管中先加入 1mL 0.01mol/L 酸性 KMnO4 溶液,_____ ,最后加入 1mL 0.1mol/L 草酸溶液。
②若猜想成立,应观察到的实验现象是________ 。
| 编号 | 实验操作 | 实验现象 |
| 向一支试管中先加入 1mL 0.01 mol/L 酸性KMnO4 溶液,再加入 1 滴 3mol/L 硫酸和 9 滴蒸馏水,最后加入1mL 0.1mol/L 草酸溶液 | 前 10min 内溶液紫色无明显变化,后颜色逐渐变浅, 30 min 后几乎变为无色 | |
Ⅱ | 向另一支试管中先加入 1mL 0.01mol/L 酸性KMnO4 溶液,再加入 10 滴 3mol/L 硫酸,最后加入 1mL 0.1mol/L 草酸溶液 | 80s 内溶液紫色无明显变化,后颜色迅速变浅,约150s 后几乎变为无色 |
□MnO
 +□H2C2O4 + □ = □Mn2+ +□ +□H2O
+□H2C2O4 + □ = □Mn2+ +□ +□H2O(2)由实验 I、Ⅱ可得出的结论是
(3)关于实验Ⅱ中 80s 后溶液颜色迅速变浅的原因,该小组提出了猜想:该反应中生成的 Mn2+ 对反应有催化作用。设计实验 Ⅲ,验证猜想。
① 补全实验Ⅲ的操作:
向试管中先加入 1mL 0.01mol/L 酸性 KMnO4 溶液,
②若猜想成立,应观察到的实验现象是
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
【推荐3】次磷酸钠(NaH2PO2)广泛应用于化学镀镍,次磷酸钠的生产与镀镍过程如下:
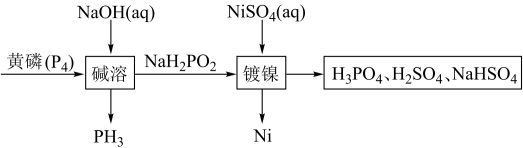
据此回答下列问题:
(1)红磷与黄磷之间的关系为___________ 。
(2)次磷酸钠中磷元素的化合价为___________ 。
(3)写出碱溶过程的化学反应方程式___________ ,该反应中氧化剂与还原剂物质的量之比为___________ 。
(4)已知次磷酸钠中的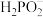 为四面体结构,请写出
为四面体结构,请写出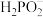 的结构式
的结构式___________ ,次磷酸钠NaH2PO2为___________ 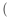 填“酸式盐”、“碱式盐”、“正盐”
填“酸式盐”、“碱式盐”、“正盐” 。
。
(5)请简述化学镀镍的反应原理___________ 。

据此回答下列问题:
(1)红磷与黄磷之间的关系为
(2)次磷酸钠中磷元素的化合价为
(3)写出碱溶过程的化学反应方程式
(4)已知次磷酸钠中的
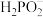 为四面体结构,请写出
为四面体结构,请写出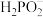 的结构式
的结构式 填“酸式盐”、“碱式盐”、“正盐”
填“酸式盐”、“碱式盐”、“正盐” 。
。(5)请简述化学镀镍的反应原理
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐1】下图甲是课本中验证铜和浓硝酸反应的装置,乙、丙是师生对演示实验改进后的装置:
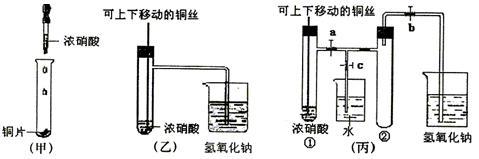
(1) 写出铜和浓硝酸反应的离子方程式________________________________ 。
(2)和甲装置相比,乙装置的优点有_________________________________________
(3)为了进一步验证NO2和水的反应,某学生设计了丙装置,做实验时先关闭弹簧夹
_______ ,再打开弹簧夹___________ ,才能使NO2气体充满②试管。
(4)当气体充满②试管后,将铜丝提起与溶液脱离,欲使烧杯中的水进入②试管应如何操
作___________________________________________________________________________ 。
(5)②试管中的NO2和水充分反应后,所得溶液物质的量浓度的最大值是_______
(气体体积按标准状况计算)。

(1) 写出铜和浓硝酸反应的离子方程式
(2)和甲装置相比,乙装置的优点有
(3)为了进一步验证NO2和水的反应,某学生设计了丙装置,做实验时先关闭弹簧夹
(4)当气体充满②试管后,将铜丝提起与溶液脱离,欲使烧杯中的水进入②试管应如何操
作
(5)②试管中的NO2和水充分反应后,所得溶液物质的量浓度的最大值是
(气体体积按标准状况计算)。
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐2】 和
和 是重要的工业产品,如图是合成氨和氨氧化制硝酸的工艺流程。
是重要的工业产品,如图是合成氨和氨氧化制硝酸的工艺流程。___________ 。
(2)氨分离器中压强约为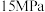 ,温度约为-20℃,分离氨时应用了氨
,温度约为-20℃,分离氨时应用了氨___________ 的性质,从氨分离器中又回到合成塔中的物质是___________ 。
(3)氧化炉中发生反应的化学方程式是___________ 。
(4)尾气中的少量 、
、 可以用
可以用 来处理,在催化剂作用下生成无污染的气体,写出
来处理,在催化剂作用下生成无污染的气体,写出 和
和 反应的化学方程式
反应的化学方程式___________ 。当有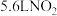 (标准状况)被还原时,转移电子的物质的量为
(标准状况)被还原时,转移电子的物质的量为___________  。
。
(5)取一定量制取的浓硝酸与铜恰好完全反应,得到硝酸铜溶液和 、
、 、
、 的混合气体,将这些气体与
的混合气体,将这些气体与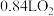 (标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸,若向所得硝酸铜溶液中加入
(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸,若向所得硝酸铜溶液中加入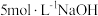 溶液至
溶液至 恰好完全沉淀,消耗
恰好完全沉淀,消耗 溶液的体积是
溶液的体积是___________  。
。
 和
和 是重要的工业产品,如图是合成氨和氨氧化制硝酸的工艺流程。
是重要的工业产品,如图是合成氨和氨氧化制硝酸的工艺流程。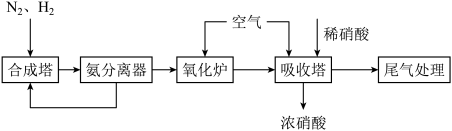
(2)氨分离器中压强约为
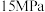 ,温度约为-20℃,分离氨时应用了氨
,温度约为-20℃,分离氨时应用了氨(3)氧化炉中发生反应的化学方程式是
(4)尾气中的少量
 、
、 可以用
可以用 来处理,在催化剂作用下生成无污染的气体,写出
来处理,在催化剂作用下生成无污染的气体,写出 和
和 反应的化学方程式
反应的化学方程式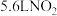 (标准状况)被还原时,转移电子的物质的量为
(标准状况)被还原时,转移电子的物质的量为 。
。(5)取一定量制取的浓硝酸与铜恰好完全反应,得到硝酸铜溶液和
 、
、 、
、 的混合气体,将这些气体与
的混合气体,将这些气体与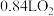 (标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸,若向所得硝酸铜溶液中加入
(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸,若向所得硝酸铜溶液中加入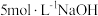 溶液至
溶液至 恰好完全沉淀,消耗
恰好完全沉淀,消耗 溶液的体积是
溶液的体积是 。
。
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐1】根据提供的情境书写指定反应的方程式。
(1)工业上用菱锰矿粉(主要成分MnCO3,杂质不与酸反应)制备MnO2的流程如下图所示:
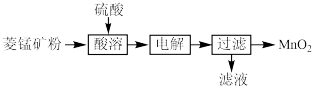
①写出“酸溶”步骤主要反应的离子方程式:____ 。
②写出“电解”步骤反应的离子反应方程式:____ 。
(2)有色金属提取工艺中会产生大量含氰(CN-)废水,对环境造成了极大的负担。在碱性条件下可用ClO-将其氧化成CO 和N2。写出反应的离子方程式:
和N2。写出反应的离子方程式:____ 。
(3)土壤中的硫元素在微生物作用下可以发生转化。
①在硫化细菌作用下,土壤中的黄铁矿(FeS2)被O2氧化为硫酸亚铁和硫酸。写出该反应的化学方程式:____ 。
②在反硫化细菌的作用下,土壤中的硫酸可以被糖类(以C6H12O6为例)还原为H2S,C6H12O6被氧化为CO2。写出该反应的化学方程式:____ 。
(1)工业上用菱锰矿粉(主要成分MnCO3,杂质不与酸反应)制备MnO2的流程如下图所示:

①写出“酸溶”步骤主要反应的离子方程式:
②写出“电解”步骤反应的离子反应方程式:
(2)有色金属提取工艺中会产生大量含氰(CN-)废水,对环境造成了极大的负担。在碱性条件下可用ClO-将其氧化成CO
 和N2。写出反应的离子方程式:
和N2。写出反应的离子方程式:(3)土壤中的硫元素在微生物作用下可以发生转化。
①在硫化细菌作用下,土壤中的黄铁矿(FeS2)被O2氧化为硫酸亚铁和硫酸。写出该反应的化学方程式:
②在反硫化细菌的作用下,土壤中的硫酸可以被糖类(以C6H12O6为例)还原为H2S,C6H12O6被氧化为CO2。写出该反应的化学方程式:
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐2】钛和钛合金被认为是21世纪的重要金属材料,广泛用于火箭、飞机制造业等。如图是工业上利用钛铁矿,其主要成分为钛酸亚铁(FeTiO3)制备金属钛的工艺流程。
资料: Ti为固体,化学性质稳定,不溶于稀硫酸、稀盐酸等。

(1)钛酸亚铁(FeTiO3)中钛元素的化合价是___________ 。
(2)反应釜中发生的反应是:2FeTiO3 + 7Cl2 + 6C 2X + 2TiCl4 + 6CO,X的化学式是
2X + 2TiCl4 + 6CO,X的化学式是___________ 。
(3)反应釜中得到TiCl4和FeCl3的混合物在沸腾炉中分离,这是利用了TiCl4与FeCl3的___________ 不同。
(4)写出合成器中反应的化学方程式___________ ,该反应___________ (填“是”或“不是”)氧化还原反应。
(5)利用上述方法制取的金属钛中可能会含有少量杂质,该杂质是金属___________ 。由金属钛的性质可知,除去这种杂质可以用___________ 。
(6)依据“绿色低碳”理念,你认为该流程中存在的不足之处是___________ 。
资料: Ti为固体,化学性质稳定,不溶于稀硫酸、稀盐酸等。

(1)钛酸亚铁(FeTiO3)中钛元素的化合价是
(2)反应釜中发生的反应是:2FeTiO3 + 7Cl2 + 6C
 2X + 2TiCl4 + 6CO,X的化学式是
2X + 2TiCl4 + 6CO,X的化学式是(3)反应釜中得到TiCl4和FeCl3的混合物在沸腾炉中分离,这是利用了TiCl4与FeCl3的
(4)写出合成器中反应的化学方程式
(5)利用上述方法制取的金属钛中可能会含有少量杂质,该杂质是金属
(6)依据“绿色低碳”理念,你认为该流程中存在的不足之处是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】三氯化硼(BCl3)用于制备光导纤维和有机硼化物等,其制备原理为B2O3+3C+3Cl2 2BCl3+3CO。某小组据此设计实验制备BCl3并测定其纯度,装置如图所示(部分夹持装置略)。
2BCl3+3CO。某小组据此设计实验制备BCl3并测定其纯度,装置如图所示(部分夹持装置略)。

已知:BCl3的相对分子质量为117.5,熔点为−107.3℃,沸点为12.5℃,极易水解产生H3BO3[或B(OH)3]和HCl。
实验(一):制备BCl3。
(1)水浴R选择_____ (填“热水浴”或“冰水浴”),盛装碱石灰的仪器是_____ (填名称)。
(2)装置F的作用是______ 。
(3)已知装置A中还原产物为Cr3+,其离子方程式为______ 。
实验(二):测定BCl3产品的纯度。
①准确称取wg产品,置于蒸馏水中,完全水解,并配成250mL溶液;
②准确量取25.00mL溶液于锥形瓶中;
③向其中加入V1mLc1 mol∙L−1AgNO3溶液(过量),然后加入3mL硝基苯(常温常压下,密度为1.205 g∙cm−3),振荡;
④向锥形瓶中滴加3滴FeCl3溶液,然后逐滴加入c2 mol∙L−1KSCN标准溶液滴定过量AgNO3溶液,消耗KSCN标准溶液的体积为V2mL。已知:Ksp(AgCl)>Ksp(AgSCN)。
(4)步骤③中加入硝基苯的目的是______ ;滴定终点的现象是______ 。
(5)该产品中BCl3的质量分数为______ %;如果其他操作都正确,仅滴定管没有用KSCN标准溶液润洗,则测得产品中BCl3的质量分数______ (填“偏高”“偏低”或“无影响”)。
 2BCl3+3CO。某小组据此设计实验制备BCl3并测定其纯度,装置如图所示(部分夹持装置略)。
2BCl3+3CO。某小组据此设计实验制备BCl3并测定其纯度,装置如图所示(部分夹持装置略)。
已知:BCl3的相对分子质量为117.5,熔点为−107.3℃,沸点为12.5℃,极易水解产生H3BO3[或B(OH)3]和HCl。
实验(一):制备BCl3。
(1)水浴R选择
(2)装置F的作用是
(3)已知装置A中还原产物为Cr3+,其离子方程式为
实验(二):测定BCl3产品的纯度。
①准确称取wg产品,置于蒸馏水中,完全水解,并配成250mL溶液;
②准确量取25.00mL溶液于锥形瓶中;
③向其中加入V1mLc1 mol∙L−1AgNO3溶液(过量),然后加入3mL硝基苯(常温常压下,密度为1.205 g∙cm−3),振荡;
④向锥形瓶中滴加3滴FeCl3溶液,然后逐滴加入c2 mol∙L−1KSCN标准溶液滴定过量AgNO3溶液,消耗KSCN标准溶液的体积为V2mL。已知:Ksp(AgCl)>Ksp(AgSCN)。
(4)步骤③中加入硝基苯的目的是
(5)该产品中BCl3的质量分数为
您最近一年使用:0次