 和
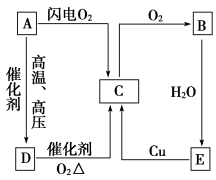
和 是重要的工业产品,如图是合成氨和氨氧化制硝酸的工艺流程。
是重要的工业产品,如图是合成氨和氨氧化制硝酸的工艺流程。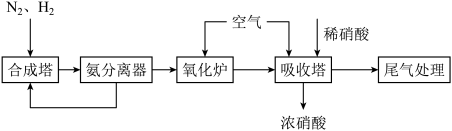
(2)氨分离器中压强约为
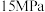 ,温度约为-20℃,分离氨时应用了氨
,温度约为-20℃,分离氨时应用了氨(3)氧化炉中发生反应的化学方程式是
(4)尾气中的少量
 、
、 可以用
可以用 来处理,在催化剂作用下生成无污染的气体,写出
来处理,在催化剂作用下生成无污染的气体,写出 和
和 反应的化学方程式
反应的化学方程式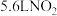 (标准状况)被还原时,转移电子的物质的量为
(标准状况)被还原时,转移电子的物质的量为 。
。(5)取一定量制取的浓硝酸与铜恰好完全反应,得到硝酸铜溶液和
 、
、 、
、 的混合气体,将这些气体与
的混合气体,将这些气体与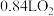 (标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸,若向所得硝酸铜溶液中加入
(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸,若向所得硝酸铜溶液中加入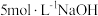 溶液至
溶液至 恰好完全沉淀,消耗
恰好完全沉淀,消耗 溶液的体积是
溶液的体积是 。
。
更新时间:2024-04-29 10:10:15
|
相似题推荐
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐1】某兴趣小组研究亚硝酸钠,查阅下列资料,试根据信息回答下列问题
(1)已知NaNO2能发生如下反应:2NaNO2 + 4HI = 2NO↑+ I2+ 2NaI + 2H2O
请用双线桥表示电子转移的方向和数目____________ 。该反应中氧化产物是_____________ (填化学式);若有2molHI被氧化,则被还原的氧化剂粒子数是________________ 。
(2)误食NaNO2会导致血红蛋白中的Fe2+转化成Fe3+而中毒,可服用维生素C解毒。下列分析正确的是_____ (填序号)
A. NaNO2被还原
B. 维生素C具有氧化性
C.还原性:Fe2+>维生素C
D. NaNO2是还原剂
(3)下列方法中,不能用来区分NaNO2和NaCl的是_________________ (填序号)
A. 在酸性条件下加入KI淀粉溶液
B. 分别滴加酸化FeSO4溶液和KSCN溶液
C.焰色反应
D. 分别滴加AgNO3溶液
(4)某同学把新制的氯水加到NaNO2溶液中,观察到氯水褪色,同时生成NaNO3和HCl,请写出反应的离子方程式_________________________________________________ 。
| 药品 | NaNO2(亚硝酸钠) |
| 性质 | 1.在酸性溶液中有较强氧化性,能将Fe2+氧化成Fe3+; 2.AgNO2是一种难溶于水、易溶于酸的盐 |
(1)已知NaNO2能发生如下反应:2NaNO2 + 4HI = 2NO↑+ I2+ 2NaI + 2H2O
请用双线桥表示电子转移的方向和数目
(2)误食NaNO2会导致血红蛋白中的Fe2+转化成Fe3+而中毒,可服用维生素C解毒。下列分析正确的是
A. NaNO2被还原
B. 维生素C具有氧化性
C.还原性:Fe2+>维生素C
D. NaNO2是还原剂
(3)下列方法中,不能用来区分NaNO2和NaCl的是
A. 在酸性条件下加入KI淀粉溶液
B. 分别滴加酸化FeSO4溶液和KSCN溶液
C.焰色反应
D. 分别滴加AgNO3溶液
(4)某同学把新制的氯水加到NaNO2溶液中,观察到氯水褪色,同时生成NaNO3和HCl,请写出反应的离子方程式
您最近一年使用:0次
【推荐2】合成氨是人类科学技术发展史上的一项重大成就。实验室利用如右图所示装置及药品制取氨气:_____________ 。
(2)下列装置中,可用于收集氨的是_________ (填标号)。______________ 。
(4)在一定条件下,将2molN2和6molH2在体积恒为5L的密闭容器中混合,发生如下反应:N2(g)+3H2(g) 2NH3(g)。2min时测得容器内N2的物质的量为1.6mol,则:
2NH3(g)。2min时测得容器内N2的物质的量为1.6mol,则:
①2min内该反应的平均反应速率v(N2)=______ mol/(L·min)
②一段时间后反应达到平衡,密闭容器中混合气体的压强比反应前减少了25%,计算此时容器中NH3的浓度为____________ mol/L。
③能说明该反应已经达到平衡状态的是____________ 。
a.气体的密度保持不变 b.NH3的含量保持不变
c.N2和H2的物质的量之比为1:3 d.N2的转化率不再发生改变
(5)工业上通常用氨转化法处理含NO、NO2等氮氧化物的尾气:已知8 mol氨恰好能将含NO和NO2共7mol的混合气体完全转化为N2,则混合气体中NO和NO2的物质的量之比为_____ 。
(2)下列装置中,可用于收集氨的是
a. 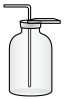 b.
b. 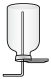 c.
c. 
(4)在一定条件下,将2molN2和6molH2在体积恒为5L的密闭容器中混合,发生如下反应:N2(g)+3H2(g)
 2NH3(g)。2min时测得容器内N2的物质的量为1.6mol,则:
2NH3(g)。2min时测得容器内N2的物质的量为1.6mol,则:①2min内该反应的平均反应速率v(N2)=
②一段时间后反应达到平衡,密闭容器中混合气体的压强比反应前减少了25%,计算此时容器中NH3的浓度为
③能说明该反应已经达到平衡状态的是
a.气体的密度保持不变 b.NH3的含量保持不变
c.N2和H2的物质的量之比为1:3 d.N2的转化率不再发生改变
(5)工业上通常用氨转化法处理含NO、NO2等氮氧化物的尾气:已知8 mol氨恰好能将含NO和NO2共7mol的混合气体完全转化为N2,则混合气体中NO和NO2的物质的量之比为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】反应物相同,通过控制不同条件,可能得到不同的产物。某兴趣小组查阅资料发现: 与碱的溶液反应生成的含氯的产物除氯化物外,还可能含有次氯酸盐或氯酸盐(杀菌消毒能力较差)。他们利用如图装置以
与碱的溶液反应生成的含氯的产物除氯化物外,还可能含有次氯酸盐或氯酸盐(杀菌消毒能力较差)。他们利用如图装置以 制备
制备 和
和 。已知:
。已知:
(1)a中盛放 的仪器名称为
的仪器名称为_______ ;若无b装置,会导致c中产生大量的副产物_______ (填化学式)。
(2)a装置中发生反应的离子方程式为_______ 。
(3)资料显示:工业上制备“84”消毒液时,采用的是从吸收塔下部通入 ,从上部喷淋循环冷却的
,从上部喷淋循环冷却的 溶液(15~20%)。
溶液(15~20%)。 需要循环冷却的目的是
需要循环冷却的目的是_______ 。
(4)该兴趣小组在 条件下,将一定量的
条件下,将一定量的 通入
通入 溶液中,
溶液中, 恰好反应,得到产物中含有
恰好反应,得到产物中含有 和
和 ,若
,若 和
和 的物质的量之比为1∶1,则生成
的物质的量之比为1∶1,则生成 的物质的量为
的物质的量为_______  。
。
 与碱的溶液反应生成的含氯的产物除氯化物外,还可能含有次氯酸盐或氯酸盐(杀菌消毒能力较差)。他们利用如图装置以
与碱的溶液反应生成的含氯的产物除氯化物外,还可能含有次氯酸盐或氯酸盐(杀菌消毒能力较差)。他们利用如图装置以 制备
制备 和
和 。已知:
。已知:

(1)a中盛放
 的仪器名称为
的仪器名称为(2)a装置中发生反应的离子方程式为
(3)资料显示:工业上制备“84”消毒液时,采用的是从吸收塔下部通入
 ,从上部喷淋循环冷却的
,从上部喷淋循环冷却的 溶液(15~20%)。
溶液(15~20%)。 需要循环冷却的目的是
需要循环冷却的目的是(4)该兴趣小组在
 条件下,将一定量的
条件下,将一定量的 通入
通入 溶液中,
溶液中, 恰好反应,得到产物中含有
恰好反应,得到产物中含有 和
和 ,若
,若 和
和 的物质的量之比为1∶1,则生成
的物质的量之比为1∶1,则生成 的物质的量为
的物质的量为 。
。
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】某化学课外兴趣小组为探究铜与浓硫酸的反应,用下图所示的装置进行实验。实验中他们取64g铜片和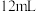
 浓硫酸放在圆底烧瓶中共热,直到反应停止,最后发现烧瓶中还有铜片剩余,该小组同学认为还有一定量的硫酸剩余。
浓硫酸放在圆底烧瓶中共热,直到反应停止,最后发现烧瓶中还有铜片剩余,该小组同学认为还有一定量的硫酸剩余。
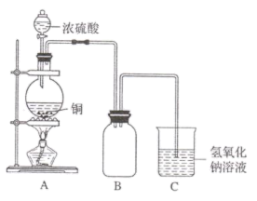
请回答下列问题:
(1)写出铜与浓硫酸反应的化学方程式:___________ 。实验中若有mg铜参加了反应,则有___________ 
 被还原,转移电子数目为
被还原,转移电子数目为___________ (设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
(2)下列试剂能证明反应停止后烧瓶中有硫酸剩余的是___________ (填字母)。
A.硫酸钠溶液B.氯化钡溶液C.银粉D.碳酸钠溶液
(3)为什么有一定量的硫酸剩余但未能使铜片完全溶解?原因是___________ 。
 浓硫酸放在圆底烧瓶中共热,直到反应停止,最后发现烧瓶中还有铜片剩余,该小组同学认为还有一定量的硫酸剩余。
浓硫酸放在圆底烧瓶中共热,直到反应停止,最后发现烧瓶中还有铜片剩余,该小组同学认为还有一定量的硫酸剩余。
请回答下列问题:
(1)写出铜与浓硫酸反应的化学方程式:

 被还原,转移电子数目为
被还原,转移电子数目为 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。(2)下列试剂能证明反应停止后烧瓶中有硫酸剩余的是
A.硫酸钠溶液B.氯化钡溶液C.银粉D.碳酸钠溶液
(3)为什么有一定量的硫酸剩余但未能使铜片完全溶解?原因是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】某兴趣小组设计出如图所示装置来制备 并探究
并探究 的性质。请回答下列问题:
的性质。请回答下列问题:

(1)装置甲中发生反应的化学方程式为_______ ,该反应体现了浓硫酸的_______ 性。
(2)装置乙中盛装品红溶液,可以观察到品红溶液褪色,证明该漂白原理是可逆的操作及现象为_______ 。
(3)装置丙中盛装酸性 溶液,可以观察到溶液褪色,发生反应的化学方程式为
溶液,可以观察到溶液褪色,发生反应的化学方程式为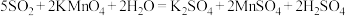 ,则其离子方程式为
,则其离子方程式为_______ 。
(4)装置丁中盛装 溶液,可以观察到
溶液,可以观察到_______ 现象,体现 的
的_______ 性。
(5)图1中装置存在明显的缺陷,改进的方法是_______ 。
(6)若用图2中装置来收集 ,气体应从
,气体应从_______ (填“A”或“B”)导管口进入。
 并探究
并探究 的性质。请回答下列问题:
的性质。请回答下列问题:
(1)装置甲中发生反应的化学方程式为
(2)装置乙中盛装品红溶液,可以观察到品红溶液褪色,证明该漂白原理是可逆的操作及现象为
(3)装置丙中盛装酸性
 溶液,可以观察到溶液褪色,发生反应的化学方程式为
溶液,可以观察到溶液褪色,发生反应的化学方程式为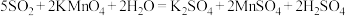 ,则其离子方程式为
,则其离子方程式为(4)装置丁中盛装
 溶液,可以观察到
溶液,可以观察到 的
的(5)图1中装置存在明显的缺陷,改进的方法是
(6)若用图2中装置来收集
 ,气体应从
,气体应从
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐3】某化学课外活动小组利用下图所示装置探究NO2能否被NH3还原(K1、K2为止水夹,夹持固定装置略去)。
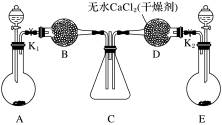
(1)A和E中制取NH3的装置为_____ ,所用试剂为___ ,装置中制取NO2的化学方程式是___________________ 。
(2)若NO2能够被NH3还原,预期观察到C装置中的现象是______________________ 。
(3)实验过程中,一段时间内未能观察到C装置中的预期现象。该小组同学从反应原理的角度分析了原因,认为可能是:
①NH3还原性较弱,不能将NO2还原;②在此条件下,NO2的转化率极低;③______________ 。
(4)此实验装置存在一个明显的缺陷是_________________________________ 。

(1)A和E中制取NH3的装置为
(2)若NO2能够被NH3还原,预期观察到C装置中的现象是
(3)实验过程中,一段时间内未能观察到C装置中的预期现象。该小组同学从反应原理的角度分析了原因,认为可能是:
①NH3还原性较弱,不能将NO2还原;②在此条件下,NO2的转化率极低;③
(4)此实验装置存在一个明显的缺陷是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】已知X、Y、Z、W是元素周期表中短周期中的四种非金属元素,它们的原子序数依次增大,X元素的原子形成的阳离子就是一个质子,Z、W在元素周期表中处于相邻的位置,它们的单质在常温下均为无色气体,Y原子的最外层电子数是内层电子数的2倍。试回答:
(1)写出下列元素的元素符号和电子排布式:
X____________________ Y___________________
Z____________________ W___________________
(2)X单质和Z单质在一定条件下反应生成化合物E,该反应的化学方程式为________________ 。E在催化剂存在的条件下可用于还原汽车尾气中的______ ,以减少对大气的污染。
(1)写出下列元素的元素符号和电子排布式:
X
Z
(2)X单质和Z单质在一定条件下反应生成化合物E,该反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】(1)写出N2的结构式___ 。下列能实现人工固氮的是___ 。
A.闪电
B.在加压降温的条件下使空气中的氮气液化
C.合成氨车间
(2)实验室通常用加热消石灰与氯化铵固体的方法来制取氨气。
写出该反应的化学方程式___ 。
实验室制取氨气的方法有多种,下面的装置和选用的试剂中错误的是__ 。
A.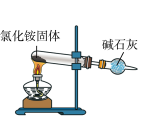 B.
B.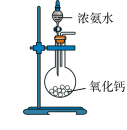 C.
C. 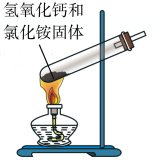 D.
D.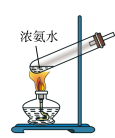
(3)氨气可使湿润的红色石蕊试纸变蓝的原因(用化学用语表示)___ 。
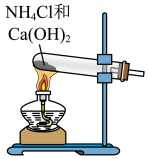
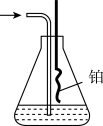
(4)用如图装置吸收一段时间氨后,再通入空气,同时将加热的铂丝插入该装置的锥形瓶内,写出该装置中氨催化氧化的化学方程式:___ 。
A.闪电
B.在加压降温的条件下使空气中的氮气液化
C.合成氨车间
(2)实验室通常用加热消石灰与氯化铵固体的方法来制取氨气。
写出该反应的化学方程式
实验室制取氨气的方法有多种,下面的装置和选用的试剂中错误的是
A.
 B.
B. C.
C.  D.
D.
(3)氨气可使湿润的红色石蕊试纸变蓝的原因(用化学用语表示)
(4)用如图装置吸收一段时间氨后,再通入空气,同时将加热的铂丝插入该装置的锥形瓶内,写出该装置中氨催化氧化的化学方程式:

您最近一年使用:0次

 的物质的量之比为
的物质的量之比为

