题型:解答题-结构与性质
难度:0.4
引用次数:686
题号:1962793
硼元素B在化学中有很重要的地位。硼的化合物在农业、医药、玻璃等方面用途很广。请回答下列问题:
(1)写出与B元素同主族的Ga元素的基态原子核外电子排布式______ 。从原子结构的角度分析,B、N、O元素的第一电离能由大到小的顺序为______ 。
(2)立方氮化硼可利用人工方法在高温高压条件下合成,属于超硬材料。同属原子晶体的氮化硼(BN)比晶体硅具有更高硬度和耐热性的原因是______ 。
(3)在BF3分子中中心原子的杂化轨道类型是______ ,SiF4微粒的空间构型是______ 。又知若有d轨道参与杂化,能大大提高中心原子成键能力。试解释为什么BF3、SiF4水解的产物中,除了相应的酸外,前者生成BF 后者却是生成SiF
后者却是生成SiF :
:______ 。
(4)科学家发现硼化镁在39K时呈超导性,在硼化镁晶体的理想模型中,镁原子和硼原子是分层排布的,一层镁一层硼相间排列。

上图是该晶体微观空间中取出的部分原子沿Z轴方向的投影,白球是镁原子投影,黑球是硼原子投影,图中的硼原子和镁原子投影在同一平面上。根据图示确定硼化镁的化学式为______ 。
(1)写出与B元素同主族的Ga元素的基态原子核外电子排布式
(2)立方氮化硼可利用人工方法在高温高压条件下合成,属于超硬材料。同属原子晶体的氮化硼(BN)比晶体硅具有更高硬度和耐热性的原因是
(3)在BF3分子中中心原子的杂化轨道类型是
 后者却是生成SiF
后者却是生成SiF :
:(4)科学家发现硼化镁在39K时呈超导性,在硼化镁晶体的理想模型中,镁原子和硼原子是分层排布的,一层镁一层硼相间排列。

上图是该晶体微观空间中取出的部分原子沿Z轴方向的投影,白球是镁原子投影,黑球是硼原子投影,图中的硼原子和镁原子投影在同一平面上。根据图示确定硼化镁的化学式为
2013·江西·一模 查看更多[3]
(已下线)2013届江西师大附中、鹰潭一中高三理综联考化学试卷(已下线)2014高考化学二轮复习限时集训 专题16物质结构与性质练习卷(已下线)2013届江西师大附中、鹰潭一中高三理综联考理综化学试卷
更新时间:2016/12/09 05:26:38
|
相似题推荐
解答题-有机推断题
|
较难
(0.4)
解题方法
【推荐1】某药物中间体H的结构简式为 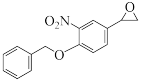 。H的一种合成路线如下:
。H的一种合成路线如下:
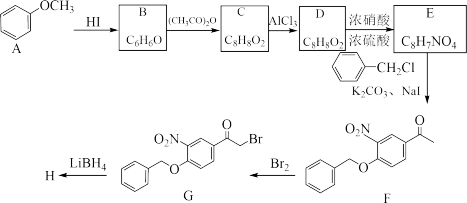
已知:C不与氯化铁溶液发生显色反应,D遇FeCl3溶液发生显色反应。
回答下列问题:
(1)A的分子式为___________ 。D中的官能团是 ___________ (填名称)。
(2)E→F 的反应类型是___________ 。
(3)写出B→C的化学方程式:___________ 。
(4)在催化剂作用下,G与足量H2反应的产物为J,1个J分子含___________ 个手性碳原子。
(5) 中B原子的杂化方式为
中B原子的杂化方式为___________ ,其空间结构为___________ 形 。
(6)芳香族化合物K是C的同分异构体,K能发生银镜反应的结构有___________ 种 ,其中在核磁共振氢谱上显示有5组峰,且峰的面积比为2: 2:2: 1: 1的结构简式为___________ (只写一种即可)。
 。H的一种合成路线如下:
。H的一种合成路线如下: 
已知:C不与氯化铁溶液发生显色反应,D遇FeCl3溶液发生显色反应。
回答下列问题:
(1)A的分子式为
(2)E→F 的反应类型是
(3)写出B→C的化学方程式:
(4)在催化剂作用下,G与足量H2反应的产物为J,1个J分子含
(5)
 中B原子的杂化方式为
中B原子的杂化方式为(6)芳香族化合物K是C的同分异构体,K能发生银镜反应的结构有
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】超分子指多个分子组合在一起形成的具有特定结构和功能的聚集体,超分子内部分子通过非共价键相结合.冠醚是大环多醚类物质的总称,能与阳离子作用,并随环大小不同对阳离子具有选择性作用,图为常见的三种冠醚结构。
已知: 与冠醚b结合能力强,使钾盐在该液体冠醚中溶解性好.
与冠醚b结合能力强,使钾盐在该液体冠醚中溶解性好.
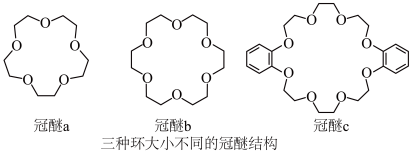
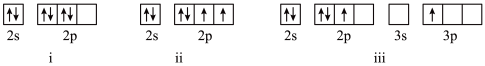
(1)下列冠醚中O原子的基态或激发态价电子中,能量由低到高排列的正确顺序为________ 。
(2) 具有强氧化性,
具有强氧化性, 在元素周期表中的位置是
在元素周期表中的位置是________ ,其水溶液对环己烯的氧化效果很差,若将环己烯溶于冠醚b再加入 ,氧化效果大幅度提升,原因是
,氧化效果大幅度提升,原因是________ 。
(3)分子A(结构如图所示)能与冠醚c形成一种分子梭结构,其中N的杂化为________ ,该分子梭可以通过加入酸或碱使冠醚c在位点1和位点2之间来回移动.加酸冠醚c移动到位点2,冠醚c与位点2之间的相互作用为________ 。
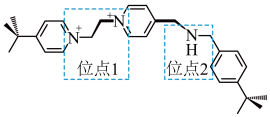
a.静电相互作用 b.离子键 c.共价键 d.氢键
(4) 与冠醚a结合能力强,
与冠醚a结合能力强, 有独特的电性、磁性和光致发光性能。
有独特的电性、磁性和光致发光性能。
① 的价电子排布式为
的价电子排布式为________ 。
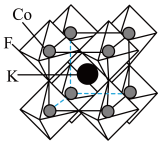
② 晶体结构如图所示,每个小正八面体的顶点均为F原子,该立方晶胞中
晶体结构如图所示,每个小正八面体的顶点均为F原子,该立方晶胞中 的配位数为
的配位数为________ ,该晶体密度为 ,则该晶胞的棱长为
,则该晶胞的棱长为________  。
。
已知:
 与冠醚b结合能力强,使钾盐在该液体冠醚中溶解性好.
与冠醚b结合能力强,使钾盐在该液体冠醚中溶解性好.
(1)下列冠醚中O原子的基态或激发态价电子中,能量由低到高排列的正确顺序为

(2)
 具有强氧化性,
具有强氧化性, 在元素周期表中的位置是
在元素周期表中的位置是 ,氧化效果大幅度提升,原因是
,氧化效果大幅度提升,原因是(3)分子A(结构如图所示)能与冠醚c形成一种分子梭结构,其中N的杂化为

a.静电相互作用 b.离子键 c.共价键 d.氢键
(4)
 与冠醚a结合能力强,
与冠醚a结合能力强, 有独特的电性、磁性和光致发光性能。
有独特的电性、磁性和光致发光性能。①
 的价电子排布式为
的价电子排布式为②
 晶体结构如图所示,每个小正八面体的顶点均为F原子,该立方晶胞中
晶体结构如图所示,每个小正八面体的顶点均为F原子,该立方晶胞中 的配位数为
的配位数为 ,则该晶胞的棱长为
,则该晶胞的棱长为 。
。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】黄铜矿是工业冶炼铜的原料,主要成分为 CuFeS2。试回答下列问题:
(1)基态硫原子核外电子有_____ 种不同运动状态,能量最高的电子所占据的原子轨道形状为_________ 。
(2)基态Cu原子的价层电子排布式为_________ ;Cu、Zn的第二电离能大小I2(Cu) _________ I2(Zn)(填“>”“<”或“=”)。
(3)SO2分子中S原子的轨道杂化类型为_________ ,分子空间构型为_________ ;与SO2互为等电子体的分子有_________ (写一种)。
(4)Cu(CH3CN)4比四氨合铜离子稳定,其配离子中心原子配位数为_________ ,配位体中σ键与π键个数之比为_________ 。
(5)请从结构角度解释H2SO3的酸性比H2SO4酸性弱的原因_________ 。
(6)铁镁合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图所示。

若该晶体储氢时,H2分子在晶胞的体心和棱的中心位置,距离最近的两个H2分子之间距离为anm。则该晶体的密度为_________ g/cm3(列出计算表达式)。
(1)基态硫原子核外电子有
(2)基态Cu原子的价层电子排布式为
(3)SO2分子中S原子的轨道杂化类型为
(4)Cu(CH3CN)4比四氨合铜离子稳定,其配离子中心原子配位数为
(5)请从结构角度解释H2SO3的酸性比H2SO4酸性弱的原因
(6)铁镁合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图所示。

若该晶体储氢时,H2分子在晶胞的体心和棱的中心位置,距离最近的两个H2分子之间距离为anm。则该晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐1】非线性光学晶体在信息、激光技术、医疗、国防等领域具有重要应用价值。我国科学家利用Cs2CO3、XO2(X=Si、Ge)和H3BO3首次合成了组成为CsXB3O7的非线性光学晶体。回答下列问题:
(1)C、O、Si三种元素电负性由大到小的顺序为____ 。
(2)基态Ge原子核外电子排布式为____ ;SiO2、GeO2具有类似的晶体结构,其中熔点较高的是___ ,原因是____ 。
(3)如图1为H3BO3晶体的片层结构,其中B的杂化方式为____ ;硼酸在热水中比在冷水中溶解度显著增大的主要原因是____ 。

(4)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。CsSiB3O7属正交晶系(长方体形),晶胞参数为apm、bpm和cpm。如图2为沿y轴投影的晶胞中所有Cs原子的分布图和原子分数坐标。据此推断该晶胞中Cs原子的数目为___ ;CsSiB3O7的摩尔质量为Mg•mol-1,设NA为阿伏加德罗常数的值,则CsSiB3O7晶体的密度为___ g•cm-3(用代数式表示)。

(1)C、O、Si三种元素电负性由大到小的顺序为
(2)基态Ge原子核外电子排布式为
(3)如图1为H3BO3晶体的片层结构,其中B的杂化方式为

(4)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。CsSiB3O7属正交晶系(长方体形),晶胞参数为apm、bpm和cpm。如图2为沿y轴投影的晶胞中所有Cs原子的分布图和原子分数坐标。据此推断该晶胞中Cs原子的数目为

您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐2】某冶炼厂电解精炼铜产生的阳极泥经分铜、分金后得到的分银渣中仍含有Pb、Sn、Bi、Sb和极少量的Au、Ag等多种富有经济价值的稀贵金属元素。选择“ 、
、 熔融盐法”对分银渣加以利用,回收Sn、Pb元素的部分工艺流程如下:
熔融盐法”对分银渣加以利用,回收Sn、Pb元素的部分工艺流程如下: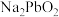 、
、 。
。
回答下列问题:
(1)将分银渣“球磨”的目的是___________ 。
(2)滤渣①中所含金属元素主要有___________ 。
(3)写出Sn在“熔炼”时反应的化学方程式:___________ 。
(4)向“含铅溶液”加入 可生成PbS,写出该反应的离子方程式:
可生成PbS,写出该反应的离子方程式:___________ ,经处理得到可以循环利用的物质是___________ (填化学式)。
(5)选取“球磨”后的分银渣,在熔炼温度700℃进行试验,熔炼时间对金属回收率的影响如图所示,“熔炼”选择的合适时间是___________ 。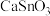 )具有介电性质,晶体属于钙钛矿结构的立方晶系,锡酸钙贮锂材料有着高能量密度、无污染、资源丰富及价格便宜等优点,是极具发展潜力的一种负极材料。
)具有介电性质,晶体属于钙钛矿结构的立方晶系,锡酸钙贮锂材料有着高能量密度、无污染、资源丰富及价格便宜等优点,是极具发展潜力的一种负极材料。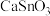 中金属离子与氧离子间的作用力为
中金属离子与氧离子间的作用力为___________ ,该晶体中每个氧离子周围与它最近且距离相等的氧离子有___________ 个。若晶胞参数为 ,则晶体密度为
,则晶体密度为___________  (设
(设 表示阿伏加德罗常数的值,列出计算式即可)。
表示阿伏加德罗常数的值,列出计算式即可)。
 、
、 熔融盐法”对分银渣加以利用,回收Sn、Pb元素的部分工艺流程如下:
熔融盐法”对分银渣加以利用,回收Sn、Pb元素的部分工艺流程如下: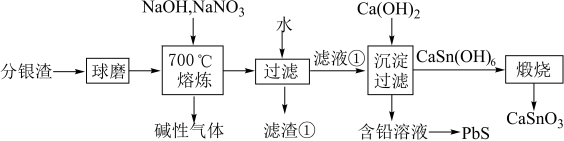
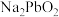 、
、 。
。回答下列问题:
(1)将分银渣“球磨”的目的是
(2)滤渣①中所含金属元素主要有
(3)写出Sn在“熔炼”时反应的化学方程式:
(4)向“含铅溶液”加入
 可生成PbS,写出该反应的离子方程式:
可生成PbS,写出该反应的离子方程式:(5)选取“球磨”后的分银渣,在熔炼温度700℃进行试验,熔炼时间对金属回收率的影响如图所示,“熔炼”选择的合适时间是

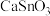 )具有介电性质,晶体属于钙钛矿结构的立方晶系,锡酸钙贮锂材料有着高能量密度、无污染、资源丰富及价格便宜等优点,是极具发展潜力的一种负极材料。
)具有介电性质,晶体属于钙钛矿结构的立方晶系,锡酸钙贮锂材料有着高能量密度、无污染、资源丰富及价格便宜等优点,是极具发展潜力的一种负极材料。 中金属离子与氧离子间的作用力为
中金属离子与氧离子间的作用力为 ,则晶体密度为
,则晶体密度为 (设
(设 表示阿伏加德罗常数的值,列出计算式即可)。
表示阿伏加德罗常数的值,列出计算式即可)。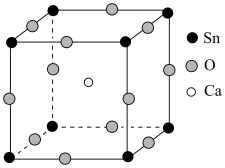
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】“嫦娥五号”首次实现了我国地外天体采样返回,它的成功发射标志看我国航天技术向前迈出了一大步,其制造材料中包含了Cu、Ti、Cr、Ni、Si、N、O等多种元素。回答下列问题:
(1)基态铬原子的价电子排布式为___________ ,基态钛原子的核外电子有___________ 种空间运动状态。
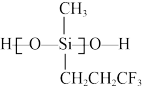
(2)硅油是一种不同聚合度链状结构的聚有机硅氧烷。它具有耐热性、电绝缘性、耐候性、疏水性、生理惰性和较小的表面张力,可用于飞船零件保护,其结构如图所示。硅油中碳原子的杂化方式为___________ 杂化,C、Si、O的第一电离能由小到大的顺序是___________ 。O—Si键的键能比C—Si键的键能___________ (填“大”或“小”)。
(3)Cu催化烯烃硝化反应过程中会产生 。键角:
。键角:
___________ (填“<”或“>”) ,其原因是
,其原因是___________ 。
(4)含有多个配位原子的配体与同一中心离子(或原子)通过鳌合配位成环而形成的配合物为螯合物。 可与某有机物形成具有较强荧光性能的配合物,其结构如图所示。
可与某有机物形成具有较强荧光性能的配合物,其结构如图所示。
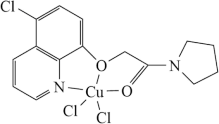
①溶液中的水存在 、
、 等微粒形式,
等微粒形式, 可看作是
可看作是 与
与 通过氢键形成的离子,写出
通过氢键形成的离子,写出 的结构式:
的结构式:___________ 。
②1 mol该配合物中通过鳌合作用形成的配位键有___________ mol。
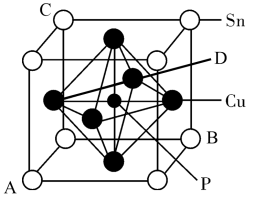
(5)磷青铜晶体的晶胞结构如图所示。原子分数坐标可表示晶胞内部各原子的相对位置,图中各原子分数坐标:A为(0,0,0)、B为(1,1,0)、C为(0,1,1),则D原子的分数坐标为___________ 。晶体中P原子位于由Cu原子形成的___________ 空隙中,该晶体中两个距离最近的Cu原子的核间距为a nm,则晶体密度为___________  (列出计算式,设
(列出计算式,设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
(1)基态铬原子的价电子排布式为
(2)硅油是一种不同聚合度链状结构的聚有机硅氧烷。它具有耐热性、电绝缘性、耐候性、疏水性、生理惰性和较小的表面张力,可用于飞船零件保护,其结构如图所示。硅油中碳原子的杂化方式为

(3)Cu催化烯烃硝化反应过程中会产生
 。键角:
。键角:
 ,其原因是
,其原因是(4)含有多个配位原子的配体与同一中心离子(或原子)通过鳌合配位成环而形成的配合物为螯合物。
 可与某有机物形成具有较强荧光性能的配合物,其结构如图所示。
可与某有机物形成具有较强荧光性能的配合物,其结构如图所示。
①溶液中的水存在
 、
、 等微粒形式,
等微粒形式, 可看作是
可看作是 与
与 通过氢键形成的离子,写出
通过氢键形成的离子,写出 的结构式:
的结构式:②1 mol该配合物中通过鳌合作用形成的配位键有
(5)磷青铜晶体的晶胞结构如图所示。原子分数坐标可表示晶胞内部各原子的相对位置,图中各原子分数坐标:A为(0,0,0)、B为(1,1,0)、C为(0,1,1),则D原子的分数坐标为
 (列出计算式,设
(列出计算式,设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
您最近一年使用:0次



