实验室利用甲苯( ,
,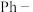 代表苯基)为原料制备苯甲酸
代表苯基)为原料制备苯甲酸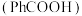 。
。
Ⅰ.制备原理:
氧化:
酸化:
Ⅱ.实验流程及步骤:
(1)苯甲酸相对分子质量:122
(2)苯甲酸在水中的溶解度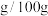 水:0.34(25℃)、0.85(50℃)、2.2(75℃)。
水:0.34(25℃)、0.85(50℃)、2.2(75℃)。
请回答:
(1)步骤③的操作名称是_____ 。步骤④热水洗涤的目的是_____ 。
(2)有关实验流程Ⅱ步骤,下列说法正确的是_____。
(3)步骤②中,除去多余 反应的离子方程式为
反应的离子方程式为_____ 。
(4)用碱滴定法测纯度:称取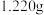 产品,配成
产品,配成 乙醇溶液,取
乙醇溶液,取 溶液于锥形瓶中,滴加2~3滴酚酞试液,然后用
溶液于锥形瓶中,滴加2~3滴酚酞试液,然后用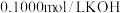 溶液滴定,重复操作三次,到达滴定终点时消耗
溶液滴定,重复操作三次,到达滴定终点时消耗 溶液分别为
溶液分别为 ,
,
 。
。
①下列说法正确的是_____ 。
B.将溶液装入滴定管时,应借助烧杯或漏斗等玻璃仪器转移
C.润洗滴定管时,待液体润湿全部滴定管内壁后,应将液体从滴定管上口倒入预置的烧杯中
D.接近终点时,需用蒸馏水冲洗锥形瓶壁和滴定管尖端悬挂的液滴
E.若滴定前滴定管尖嘴部分气泡未赶走,滴定后气泡消失,则测定结果偏高
②产品苯甲酸的纯度为_____ 。
 ,
,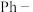 代表苯基)为原料制备苯甲酸
代表苯基)为原料制备苯甲酸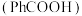 。
。Ⅰ.制备原理:
氧化:

酸化:

Ⅱ.实验流程及步骤:


(1)苯甲酸相对分子质量:122
(2)苯甲酸在水中的溶解度
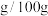 水:0.34(25℃)、0.85(50℃)、2.2(75℃)。
水:0.34(25℃)、0.85(50℃)、2.2(75℃)。请回答:
(1)步骤③的操作名称是
(2)有关实验流程Ⅱ步骤,下列说法正确的是_____。
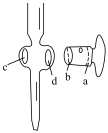
| A.图甲装置中,冷凝管进水口为1 |
| B.图甲球形冷凝管的内芯管为球泡状,冷却面积大,可用于蒸馏实验 |
| C.图甲控制反应温度,以蒸气上升至内芯管下端为宜 |
| D.步骤⑧粗苯甲酸晶体的提纯可采用重结晶的方法 |
 反应的离子方程式为
反应的离子方程式为(4)用碱滴定法测纯度:称取
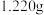 产品,配成
产品,配成 乙醇溶液,取
乙醇溶液,取 溶液于锥形瓶中,滴加2~3滴酚酞试液,然后用
溶液于锥形瓶中,滴加2~3滴酚酞试液,然后用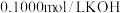 溶液滴定,重复操作三次,到达滴定终点时消耗
溶液滴定,重复操作三次,到达滴定终点时消耗 溶液分别为
溶液分别为 ,
,
 。
。①下列说法正确的是
B.将溶液装入滴定管时,应借助烧杯或漏斗等玻璃仪器转移
C.润洗滴定管时,待液体润湿全部滴定管内壁后,应将液体从滴定管上口倒入预置的烧杯中
D.接近终点时,需用蒸馏水冲洗锥形瓶壁和滴定管尖端悬挂的液滴
E.若滴定前滴定管尖嘴部分气泡未赶走,滴定后气泡消失,则测定结果偏高
②产品苯甲酸的纯度为
更新时间:2023-08-21 08:40:51
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】乙二酸(HOOC—COOH)俗名草酸,是一种有还原性的有机弱酸,在化学上有广泛应用。
(1)小刚在做“研究温度对化学反应速率的影响”实验时,他往A、B两支试管中均加入4 mL 0.01 mol·L-1的酸性KMnO4溶液和2 mL 0.1 mol·L-1 H2C2O4(乙二酸)溶液,振荡,A试管置于热水中,B试管置于冷水中,记录溶液褪色所需的时间。褪色所需时间tA________ tB(填“>”“=”或“<”)。写出该反应的离子方程式:_______________________ 。
(2)实验室有一瓶混有泥沙的乙二酸样品,小刚利用上述反应的原理来测定其含量,具体操作为:
①配制250 mL溶液:准确称量5.000 g乙二酸样品,配成250 mL溶液。配制溶液需要的计量仪器有__________________________________________________ 。
②滴定:准确量取25.00 mL所配溶液于锥形瓶中,加少量酸酸化,将0.100 0 mol·L-1 KMnO4标准溶液装入______ (填“酸式”或“碱式”)滴定管,进行滴定操作。在滴定过程中发现,刚滴下少量KMnO4标准溶液时,溶液紫红色并没有马上褪去。将锥形瓶摇动一段时间后,紫红色才慢慢消失;再继续滴加时,紫红色就很快褪去,可能的原因是______________________ ;判断滴定达到终点的现象是_______________________________________ 。
③计算:重复上述操作2次,记录实验数据如下表。则消耗KMnO4标准溶液的平均体积为________ mL,此样品的纯度为____________ 。
④误差分析:下列操作会导致测定结果偏高的是________ 。
A.未用KMnO4标准溶液润洗滴定管
B.滴定前锥形瓶内有少量水
C.滴定前滴定管尖嘴部分有气泡,滴定后气泡消失
D.观察读数时,滴定前仰视,滴定后俯视
(1)小刚在做“研究温度对化学反应速率的影响”实验时,他往A、B两支试管中均加入4 mL 0.01 mol·L-1的酸性KMnO4溶液和2 mL 0.1 mol·L-1 H2C2O4(乙二酸)溶液,振荡,A试管置于热水中,B试管置于冷水中,记录溶液褪色所需的时间。褪色所需时间tA
(2)实验室有一瓶混有泥沙的乙二酸样品,小刚利用上述反应的原理来测定其含量,具体操作为:
①配制250 mL溶液:准确称量5.000 g乙二酸样品,配成250 mL溶液。配制溶液需要的计量仪器有
②滴定:准确量取25.00 mL所配溶液于锥形瓶中,加少量酸酸化,将0.100 0 mol·L-1 KMnO4标准溶液装入
③计算:重复上述操作2次,记录实验数据如下表。则消耗KMnO4标准溶液的平均体积为
| 序号 | 滴定前读数 | 滴定后读数 |
| 1 | 0.00 | 20.01 |
| 2 | 1.00 | 20.99 |
| 3 | 0.00 | 21.10 |
④误差分析:下列操作会导致测定结果偏高的是
A.未用KMnO4标准溶液润洗滴定管
B.滴定前锥形瓶内有少量水
C.滴定前滴定管尖嘴部分有气泡,滴定后气泡消失
D.观察读数时,滴定前仰视,滴定后俯视
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】某同学探究Cu与NO的反应,查阅资料:①Cu与NO反应可生成CuO和N2,②酸性条件下,NO或NO2–都能与MnO4–反应生成NO3–和Mn2+
(1)实验室利用Cu和稀HNO3制备NO,写出反应的化学方程式_____________ 。
(2)选用如图所示装置完成Cu与NO的实验。(夹持装置略) 实验开始前,向装置中通入一段时间的N2。回答下列问题:

①使用铜丝的优点是_____________________ 装置E的作用为_______________ 。
②装置C中盛放的药品可能是_________ ;
③装置D中的现象是_______________ ;装置F中反应的离子方程式是_______________ 。
(3)测定NaNO2和NaNO3 混合溶液中NaNO2的浓度。 取25.00mL混合溶液于锥形瓶中,用0.1000mol·L-1酸性KMnO4溶液进行滴定,实验所得数据如下表所示:
①第一次实验数据出现异常,造成这种异常的原因可能是_________ (填字母代号)。
a.锥形瓶洗净后未干燥
b.酸式滴定管用蒸馏水洗净后未用标准液润洗
c.滴定终点时仰视读数
d.酸性KMnO4溶液中含有其他氧化性试剂
e.锥形瓶洗净后用待测液润洗
②酸性KMnO4溶液滴定亚硝酸钠溶液的离子方程式为___________________ 。
③NaNO2 的物质的量浓度为__________
(1)实验室利用Cu和稀HNO3制备NO,写出反应的化学方程式
(2)选用如图所示装置完成Cu与NO的实验。(夹持装置略) 实验开始前,向装置中通入一段时间的N2。回答下列问题:

①使用铜丝的优点是
②装置C中盛放的药品可能是
③装置D中的现象是
(3)测定NaNO2和NaNO3 混合溶液中NaNO2的浓度。 取25.00mL混合溶液于锥形瓶中,用0.1000mol·L-1酸性KMnO4溶液进行滴定,实验所得数据如下表所示:
| 滴定次数 | 1 | 2 | 3 | 4 |
| 消耗KMnO4溶液体积/mL | 20.90 | 20.12 | 20.00 | 19.88 |
①第一次实验数据出现异常,造成这种异常的原因可能是
a.锥形瓶洗净后未干燥
b.酸式滴定管用蒸馏水洗净后未用标准液润洗
c.滴定终点时仰视读数
d.酸性KMnO4溶液中含有其他氧化性试剂
e.锥形瓶洗净后用待测液润洗
②酸性KMnO4溶液滴定亚硝酸钠溶液的离子方程式为
③NaNO2 的物质的量浓度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】为测定某品牌洗厕精的酸(盐酸)含量,某学生欲用已知物质的量浓度的NaOH溶液来测定该洗厕精(盐酸)的物质的量浓度时,选择酚酞作指示剂。请填写下列空白:
(1)碱式滴定管的使用方法,正确步骤的先后顺序为____ (填字母)。
A.用NaOH溶液润洗仪器并加入NaOH溶液
B.放出NaOH溶液进行滴定
C.调节起始读数
D.查漏,再水洗2~3遍
(2)用标准的NaOH溶液滴定待测的盐酸时,左手控制碱式滴定管的玻璃球,右手摇动锥形瓶,眼睛应注视____ 。
(3)排除碱式滴定管中气泡的方法应采用操作___ (填图编号),轻轻挤压玻璃球使尖嘴部分充满碱液。

(4)滴定达到终点的标志是______ 。
(5)某学生根据三次实验分别记录有关数据如下表:
请选用其中合理的数据计算三次滴定用去NaOH的体积的平均值为__ ;该洗厕精中酸(盐酸)的物质的量浓度:c(HCl)=__ 。
(6)分析下列操作对所测洗厕精的酸(盐酸)的浓度的影响:
A.若取待测液时,开始仰视读数,后俯视读数,则___ (填“偏大”、“偏小”或“无影响”);
B.若碱式滴定管在滴定前有气泡,滴定后气泡消失,则____ (填“偏大”、“偏小”或“无影响”)。
(1)碱式滴定管的使用方法,正确步骤的先后顺序为
A.用NaOH溶液润洗仪器并加入NaOH溶液
B.放出NaOH溶液进行滴定
C.调节起始读数
D.查漏,再水洗2~3遍
(2)用标准的NaOH溶液滴定待测的盐酸时,左手控制碱式滴定管的玻璃球,右手摇动锥形瓶,眼睛应注视
(3)排除碱式滴定管中气泡的方法应采用操作

(4)滴定达到终点的标志是
(5)某学生根据三次实验分别记录有关数据如下表:
| 滴定次数 | 待测盐酸的体积 / mL | 0.100mol/L NaOH 溶液的体积/ mL | |
| 滴定前刻度 | 滴定后刻度 | ||
| 第一次 | 25.00 | 2.00 | 28.15 |
| 第二次 | 25.00 | 1.50 | 27.75 |
| 第三次 | 25.00 | 0.20 | 26.55 |
(6)分析下列操作对所测洗厕精的酸(盐酸)的浓度的影响:
A.若取待测液时,开始仰视读数,后俯视读数,则
B.若碱式滴定管在滴定前有气泡,滴定后气泡消失,则
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】根据下面各物质之间的转化关系,回答下列问题:
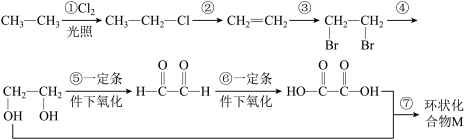
(1)写出反应类型:反应②_______ ,反应③_______ ,反应⑦_______ 。
(2)已知化合物M的化学式为C4H4O4,写出其结构简式_______ 。
(3)写出反应②的化学方程式(有机物用结构简式表示,注明反应条件,下同)_______ 。
(4)写出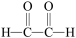 和新制的氢氧化铜悬浊液(NaOH碱性环境)按物质的量之比为1:4反应的化学方程式
和新制的氢氧化铜悬浊液(NaOH碱性环境)按物质的量之比为1:4反应的化学方程式_______ 。

(1)写出反应类型:反应②
(2)已知化合物M的化学式为C4H4O4,写出其结构简式
(3)写出反应②的化学方程式(有机物用结构简式表示,注明反应条件,下同)
(4)写出
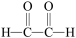 和新制的氢氧化铜悬浊液(NaOH碱性环境)按物质的量之比为1:4反应的化学方程式
和新制的氢氧化铜悬浊液(NaOH碱性环境)按物质的量之比为1:4反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】已知A是化学实验室中最常见的有机物,它易溶于水并有特殊香味;B是石油化学工业重要的基本原料,相对分子质量为28,有关物质的转化关系如图所示(部分反应条件、产物省略)。

回答下列问题:
(1)工业上,由石油获得B的方法称为___ 。
(2)A中含有的官能团的名称为___ ;H的化学名称为___ 。
(3)B到A的反应类型为___ ;A到E的反应类型为___ 。
(4)C的分子式为___ ;F的结构简式为___ 。
(5)由A生成G的化学方程式为___ 。
(6)A与D反应生成E的化学方程式为___ 。

回答下列问题:
(1)工业上,由石油获得B的方法称为
(2)A中含有的官能团的名称为
(3)B到A的反应类型为
(4)C的分子式为
(5)由A生成G的化学方程式为
(6)A与D反应生成E的化学方程式为
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
【推荐3】【化学——选修5 有机化学基础】化合物H是重要的有机化合物,可由E和F在一定条件下合成:(有些反应条件省略如:加热等)
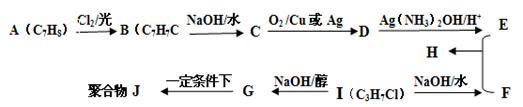
已知以下信息:
① A属于芳香烃,H属于酯类化合物。
② I的核磁共振氢谱为二组峰,且峰的面积比为6:1。
回答下列问题:
(1)B的结构简式____________ ,C的官能团名称_____________ 。
(2)B C ; G
C ; G J两步的反应类型
J两步的反应类型 _______________ ,_______________ 。
(3)①E+F H的化学方程式
H的化学方程式________________________________ 。
②I G 的化学方程式
G 的化学方程式_________________________________ 。
(4)H的同系物K比H相对分子质量小28,K的同分异构体中能同时满足如下条件:
①属于芳香族化合物
②能和饱和NaHCO3溶液反应放出CO2,共有______ 种(不考虑立体异构)。
K的一个同分异构体能发生银镜反应,也能使FeCl3溶液显紫色,苯环上有两个支链,苯环上的氢的核磁共振氢谱为二组峰,且峰面积比为1:1,写出K的这种同分异构体的结构简式________________ 。

已知以下信息:
① A属于芳香烃,H属于酯类化合物。
② I的核磁共振氢谱为二组峰,且峰的面积比为6:1。
回答下列问题:
(1)B的结构简式
(2)B
 C ; G
C ; G J两步的反应类型
J两步的反应类型 (3)①E+F
 H的化学方程式
H的化学方程式②I
 G 的化学方程式
G 的化学方程式(4)H的同系物K比H相对分子质量小28,K的同分异构体中能同时满足如下条件:
①属于芳香族化合物
②能和饱和NaHCO3溶液反应放出CO2,共有
K的一个同分异构体能发生银镜反应,也能使FeCl3溶液显紫色,苯环上有两个支链,苯环上的氢的核磁共振氢谱为二组峰,且峰面积比为1:1,写出K的这种同分异构体的结构简式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】联苄(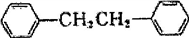 )是一种重要的有机合成中间体,实验室可用苯和1,2—二氯乙烷(ClCH2CH2Cl)为原料,在无水AlCl3催化下加热制得,其制取步骤为:
)是一种重要的有机合成中间体,实验室可用苯和1,2—二氯乙烷(ClCH2CH2Cl)为原料,在无水AlCl3催化下加热制得,其制取步骤为:
Ⅰ.催化剂的制备
下图是实验室制取取少量无水AlCl3的相关实验装置的试剂:

(1)仪器K名称________ ,将上述仪器连接成一套制备并保存无水ALCl3的装置,各管口标号连接顺序为:c接________ ,________接________,________接________,________接h.
(2)装置c的作用________ ,装置E除防止空气中水蒸气进入D中使所制无水AlCl3不纯外还有的作用是________ ,装置B中所发生的化学反应方程式为________ .
Ⅱ.联苄的制备
联苄的制取原理为:
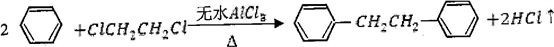
反应最佳条件为n(苯)︰n(1,2—二氯乙烷)=10︰1,反应温度在60—65℃之间.实验室制取联苄的装置如下图所示(加热和加持仪器略去):

实验步骤:
在三口烧瓶中加入120.0mL苯和适量无水AlCl3,由滴液漏斗滴加10.7mol,2—二氯乙烷,控制反应温度在65℃,反应约60min.将反应后的混合物依次用稀盐酸、2%Na2CO3溶液和H2O洗涤分离,在所得产物中加入少量无水MgSO4固体,静止、过滤,先常压蒸馏,再减压蒸馏收集170~172℃的馏分,得联苄18.2g.
相关物理常数和物理性质如下表
(3)仪器a的名称为________ .
(4)控制反应温度在65℃的方法是________ ,吸收尾气的烧杯中漏斗倒置的目的是________ ;无水硫酸镁的作用________
(5)该实验的产率约为________ %(填整数).
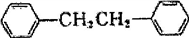 )是一种重要的有机合成中间体,实验室可用苯和1,2—二氯乙烷(ClCH2CH2Cl)为原料,在无水AlCl3催化下加热制得,其制取步骤为:
)是一种重要的有机合成中间体,实验室可用苯和1,2—二氯乙烷(ClCH2CH2Cl)为原料,在无水AlCl3催化下加热制得,其制取步骤为:Ⅰ.催化剂的制备
下图是实验室制取取少量无水AlCl3的相关实验装置的试剂:

(1)仪器K名称
(2)装置c的作用
Ⅱ.联苄的制备
联苄的制取原理为:
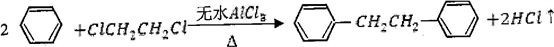
反应最佳条件为n(苯)︰n(1,2—二氯乙烷)=10︰1,反应温度在60—65℃之间.实验室制取联苄的装置如下图所示(加热和加持仪器略去):

实验步骤:
在三口烧瓶中加入120.0mL苯和适量无水AlCl3,由滴液漏斗滴加10.7mol,2—二氯乙烷,控制反应温度在65℃,反应约60min.将反应后的混合物依次用稀盐酸、2%Na2CO3溶液和H2O洗涤分离,在所得产物中加入少量无水MgSO4固体,静止、过滤,先常压蒸馏,再减压蒸馏收集170~172℃的馏分,得联苄18.2g.
相关物理常数和物理性质如下表
名称 | 相对分子质量 | 密度g·cm-3 | 熔点 ℃ | 沸点℃ | 溶解性 |
苯 | 78 | 0.88 | 5.5 | 80.1 | 难溶水,易溶乙醇 |
1,2—二氯乙烷 | 99 | 1.27 | -35.3 | 83.5 | 难溶水,可溶苯 |
无水氯化铝 | 133.5 | 2.44 | 190 | 178(升华) | 遇水水解,微溶苯 |
联苄 | 182 | 0.98 | 52 | 284 | 难溶水,易溶苯 |
(4)控制反应温度在65℃的方法是
(5)该实验的产率约为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
真题
【推荐2】本题包括A、B两小题,分别对应于“物质结构与性质”和“实验化学”两个选修模块的内容。请选定其中一题,并在相应的答题区域内作答。若两题都做,则按A题评分。
A.乙炔是有机合成工业的一种原料。工业上曾用 与水反应生成乙炔。
与水反应生成乙炔。
(1) 中
中 与
与 互为等电子体,
互为等电子体, 的电子式可表示为
的电子式可表示为_______ ;1mol 中含有的
中含有的 键数目为
键数目为___________ 。
(2)将乙炔通入 溶液生成
溶液生成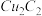 红棕色沉淀。
红棕色沉淀。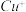 基态核外电子排布式为
基态核外电子排布式为_________________________ 。
(3)乙炔与氢氰酸反应可得丙烯腈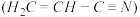 。丙烯腈分子中碳原子轨道杂化类型是
。丙烯腈分子中碳原子轨道杂化类型是________________ ;分子中处于同一直线上的原子数目最多为__________________ 。
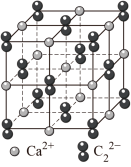
(4) 晶体的晶胞结构与
晶体的晶胞结构与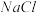 晶体相似(如图所示),但
晶体相似(如图所示),但 晶体中含有的中哑铃形
晶体中含有的中哑铃形 的存在,使晶胞沿一个方向拉长。
的存在,使晶胞沿一个方向拉长。 晶体中1个
晶体中1个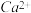 周围距离最近的
周围距离最近的 数目为
数目为______________ 。
B.对硝基甲苯是医药、染料等工业的一种重要有机中间体,它常以浓硝酸为硝化剂,浓硫酸为催化剂,通过甲苯的硝化反应制备。

一种新的制备对硝基甲苯的实验方法是:以发烟硝酸为硝化剂,固体NaHSO4为催化剂(可循环使用),在 溶液中,加入乙酸酐(有脱水作用),45℃反应1h 。反应结束后,过滤,滤液分别用5% NaHCO3,溶液、水洗至中性,再经分离提纯得到对硝基甲苯。
溶液中,加入乙酸酐(有脱水作用),45℃反应1h 。反应结束后,过滤,滤液分别用5% NaHCO3,溶液、水洗至中性,再经分离提纯得到对硝基甲苯。
(l)上述实验中过滤的目的是_________________ 。
(2) 滤液在分液漏斗中洗涤静置后,有机层处于_______ 层(填“上”或'下”);放液时,若发现液体流不下来,其可能原因除分液漏斗活塞堵塞外,还有_____________ 。
(3) 下列给出了催化剂种类及用量对甲苯硝化反应影响的实验结果。
①NaHSO4催化制备对硝基甲苯时,催化剂与甲苯的最佳物质的量之比为______________ 。
②由甲苯硝化得到的各种产物的含量可知,甲苯硝化反应的特点是____________________ 。
③与浓硫酸催化甲苯硝化相比,NaHSO4催化甲苯硝化的优点有_________ 、_________ 。
A.乙炔是有机合成工业的一种原料。工业上曾用
 与水反应生成乙炔。
与水反应生成乙炔。(1)
 中
中 与
与 互为等电子体,
互为等电子体, 的电子式可表示为
的电子式可表示为 中含有的
中含有的 键数目为
键数目为(2)将乙炔通入
 溶液生成
溶液生成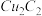 红棕色沉淀。
红棕色沉淀。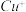 基态核外电子排布式为
基态核外电子排布式为(3)乙炔与氢氰酸反应可得丙烯腈
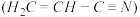 。丙烯腈分子中碳原子轨道杂化类型是
。丙烯腈分子中碳原子轨道杂化类型是(4)
 晶体的晶胞结构与
晶体的晶胞结构与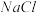 晶体相似(如图所示),但
晶体相似(如图所示),但 晶体中含有的中哑铃形
晶体中含有的中哑铃形 的存在,使晶胞沿一个方向拉长。
的存在,使晶胞沿一个方向拉长。 晶体中1个
晶体中1个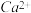 周围距离最近的
周围距离最近的 数目为
数目为
B.对硝基甲苯是医药、染料等工业的一种重要有机中间体,它常以浓硝酸为硝化剂,浓硫酸为催化剂,通过甲苯的硝化反应制备。

一种新的制备对硝基甲苯的实验方法是:以发烟硝酸为硝化剂,固体NaHSO4为催化剂(可循环使用),在
 溶液中,加入乙酸酐(有脱水作用),45℃反应1h 。反应结束后,过滤,滤液分别用5% NaHCO3,溶液、水洗至中性,再经分离提纯得到对硝基甲苯。
溶液中,加入乙酸酐(有脱水作用),45℃反应1h 。反应结束后,过滤,滤液分别用5% NaHCO3,溶液、水洗至中性,再经分离提纯得到对硝基甲苯。(l)上述实验中过滤的目的是
(2) 滤液在分液漏斗中洗涤静置后,有机层处于
(3) 下列给出了催化剂种类及用量对甲苯硝化反应影响的实验结果。
| 催化剂 | 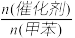 | 硝化产物中各种异构体质量分数(%) | 总产率(%) | ||
| 对硝基甲苯 | 邻硝基甲苯 | 间硝基甲苯 | |||
| 浓H2SO4 | 1.0 | 35.6 | 60.2 | 4.2 | 98.0 |
| 1.2 | 36.5 | 59.5 | 4.0 | 99.8 | |
| NaHSO4 | 0.15 | 44.6 | 55.1 | 0.3 | 98.9 |
| 0.25 | 46.3 | 52.8 | 0.9 | 99.9 | |
| 0.32 | 47.9 | 51.8 | 0.3 | 99.9 | |
| 0.36 | 45.2 | 54.2 | 0.6 | 99.9 | |
②由甲苯硝化得到的各种产物的含量可知,甲苯硝化反应的特点是
③与浓硫酸催化甲苯硝化相比,NaHSO4催化甲苯硝化的优点有
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】1, 2-二溴乙烷的制备原理是CH3CH2OH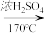 CH2=CH2↑+H2O;CH2=CH2+Br2→BrCH2—CH2Br。某课题小组用下图所示的装置制备1, 2-二溴乙烷。
CH2=CH2↑+H2O;CH2=CH2+Br2→BrCH2—CH2Br。某课题小组用下图所示的装置制备1, 2-二溴乙烷。

回答下列问题:
(1)组装仪器后进行该实验前必须进行的操作是___________ 。
(2)装置B的作用是____________ 。
(3)三颈瓶内加入一定量的乙醇-浓硫酸混合液和少量粗砂,加入粗砂的目的是_____ ,仪器F的名称是________ 。
(4)装置C内发生的主要反应的离子方程式为_________ 。
(5)加热三颈烧瓶前,先将C与D连接处断开,再将三颈烧瓶在石棉网上加热,待温度升到约120℃时,连接C与D,并迅速将A反应温度升温至160~180℃,从F中慢慢滴加乙醇-浓硫酸混合液,保持乙烯气体均匀地通入装有3.20mL液溴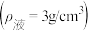 和3mL水的D中试管,直至反应结束。
和3mL水的D中试管,直至反应结束。
①将C与D连接处断开的原因是_____________________ 。
②判断反应结束的现象是____________________
(6)将粗品移入分液漏斗,分别用a. 水洗涤,b. 氢氧化钠溶液洗涤,c. 过滤,d. 用无水氯化钙干燥,e. 蒸馏收集129~133℃馏分,最后得到7.896g 1, 2-二溴乙烷。
①粗品提纯的步骤是______ (填序号),②1, 2-二溴乙烷的产率为________ 。
(7)下列操作中,不会导致产物产率降低的是______ (填正确答案的标号)
a. 乙烯通过溴水时速率太快 b. 装置C中的NaOH溶液用水代替
c. 去掉装置D烧杯中的水 d.实验时没有E装置 e. D中的试管里不加水
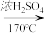 CH2=CH2↑+H2O;CH2=CH2+Br2→BrCH2—CH2Br。某课题小组用下图所示的装置制备1, 2-二溴乙烷。
CH2=CH2↑+H2O;CH2=CH2+Br2→BrCH2—CH2Br。某课题小组用下图所示的装置制备1, 2-二溴乙烷。
回答下列问题:
(1)组装仪器后进行该实验前必须进行的操作是
(2)装置B的作用是
(3)三颈瓶内加入一定量的乙醇-浓硫酸混合液和少量粗砂,加入粗砂的目的是
(4)装置C内发生的主要反应的离子方程式为
(5)加热三颈烧瓶前,先将C与D连接处断开,再将三颈烧瓶在石棉网上加热,待温度升到约120℃时,连接C与D,并迅速将A反应温度升温至160~180℃,从F中慢慢滴加乙醇-浓硫酸混合液,保持乙烯气体均匀地通入装有3.20mL液溴
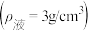 和3mL水的D中试管,直至反应结束。
和3mL水的D中试管,直至反应结束。①将C与D连接处断开的原因是
②判断反应结束的现象是
(6)将粗品移入分液漏斗,分别用a. 水洗涤,b. 氢氧化钠溶液洗涤,c. 过滤,d. 用无水氯化钙干燥,e. 蒸馏收集129~133℃馏分,最后得到7.896g 1, 2-二溴乙烷。
①粗品提纯的步骤是
(7)下列操作中,不会导致产物产率降低的是
a. 乙烯通过溴水时速率太快 b. 装置C中的NaOH溶液用水代替
c. 去掉装置D烧杯中的水 d.实验时没有E装置 e. D中的试管里不加水
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】氧化法是测定葡萄酒中SO2含量的常用方法,其原理是在低温条件下,用过量的过氧化氢溶液氧化从样品中挥发出的SO2,再用碱标准溶液滴定生成的酸。
按图组装好装置,检查装置气密性,由c向A中注入20.00mL葡萄酒,10mL25%磷酸溶液,C、D中分别注入20.00mL,5.00mL稀H2O2溶液。回答下列问题:

(1)装置B的名称是___________ ,冷凝水从___________ (填“a”或“b”)口进入。
(2)C中发生反应的化学方程式为___________ ,使用D的目的是___________________ 。
(3)真空泵抽气速率不宜过快,原因是______________________ 。
(4)抽气十分钟后,合并C、D中的溶液,加入指示剂,用浓度为c(单位为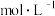 )的NaOH标准溶液滴定,消耗
)的NaOH标准溶液滴定,消耗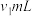 ;另取装置,向A中注入20.00mL蒸馏水,按同样的方法做空白实验,消耗NaOH溶液
;另取装置,向A中注入20.00mL蒸馏水,按同样的方法做空白实验,消耗NaOH溶液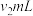 ,则该葡萄酒中SO2的含量为
,则该葡萄酒中SO2的含量为___________ mg/L.(用c、 、
、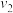 表示)
表示)
(5)葡萄酒中含有的SO2的作用是______________________ 。(答一点)
按图组装好装置,检查装置气密性,由c向A中注入20.00mL葡萄酒,10mL25%磷酸溶液,C、D中分别注入20.00mL,5.00mL稀H2O2溶液。回答下列问题:

(1)装置B的名称是
(2)C中发生反应的化学方程式为
(3)真空泵抽气速率不宜过快,原因是
(4)抽气十分钟后,合并C、D中的溶液,加入指示剂,用浓度为c(单位为
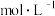 )的NaOH标准溶液滴定,消耗
)的NaOH标准溶液滴定,消耗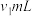 ;另取装置,向A中注入20.00mL蒸馏水,按同样的方法做空白实验,消耗NaOH溶液
;另取装置,向A中注入20.00mL蒸馏水,按同样的方法做空白实验,消耗NaOH溶液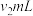 ,则该葡萄酒中SO2的含量为
,则该葡萄酒中SO2的含量为 、
、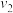 表示)
表示)(5)葡萄酒中含有的SO2的作用是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】含钛高炉渣的主要化学成分为 、
、 、
、 、
、 、
、 、
、 、
、 和金属
和金属 等,对其综合利用具有重要的经济价值和社会效益。
等,对其综合利用具有重要的经济价值和社会效益。
Ⅰ、一种含钛高炉渣提钛工艺流程如下图所示。

已知:① 不溶于水、稀酸和碱溶液;②
不溶于水、稀酸和碱溶液;② 能与强酸、强碱反应。
能与强酸、强碱反应。
(1)盐酸酸浸过程中 发生反应的离子方程式为
发生反应的离子方程式为___________ 。
(2)“磁选”的目的是___________ 。
(3)下列说法正确的是___________ (填字母序号)。
a、滤渣1的主要成分为 、
、
b、若将流程A部分与流程B部分互换顺序,最终得到的滤渣成分相同
c、若将流程A部分与流程B部分互换顺序,理论上氢氧化钠用量不变
Ⅱ、含钛高炉渣中金属 含量的测定:
含量的测定:
ⅰ、配制金属 浸取液:取一定量的亚硫酸钠和邻菲岁啉(抑制
浸取液:取一定量的亚硫酸钠和邻菲岁啉(抑制 水解)溶于水,加入乙酸和乙酸铵混合溶液调
水解)溶于水,加入乙酸和乙酸铵混合溶液调 ,此时铁的化合物不溶解。
,此时铁的化合物不溶解。
ⅱ、取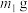 粉碎后的含钛高炉渣,加入足量金属
粉碎后的含钛高炉渣,加入足量金属 浸取液,室温下浸取
浸取液,室温下浸取 。
。
ⅲ、过滤,将滤液及洗涤液全部转移至盛有过量 溶液的烧杯中,加入稀硫酸充分反应。
溶液的烧杯中,加入稀硫酸充分反应。
ⅳ、将反应后的溶液煮沸至冒大气泡并继续微沸 。
。
ⅴ、冷却,用浓度为 的抗坏血酸
的抗坏血酸 标准液滴定,消耗抗坏血酸标准液
标准液滴定,消耗抗坏血酸标准液 。
。
已知:①酸性条件下,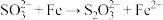 (未配平)
(未配平)
② (抗坏血酸)
(抗坏血酸) (脱氢抗坏血酸)
(脱氢抗坏血酸)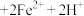
(4)步骤ⅱ中浸取铁时发生反应的离子方程式为___________ 。
(5)步骤ⅲ中加入过量 溶液的主要作用是
溶液的主要作用是___________ (用离子方程式表示)。
(6)该含钛高炉渣中金属 的质量分数=
的质量分数=___________ (用代数式表示)。
(7)下列两种情况均会对“金属 的质量分数”测定结果造成偏差,任选其中一种情况分析并说明判断理由。
的质量分数”测定结果造成偏差,任选其中一种情况分析并说明判断理由。
情况一:配制金属 浸取液时,溶液
浸取液时,溶液 等于2
等于2
情况二:未进行步骤ⅳ,直接用抗坏血酸标准液滴定
①情况___________ 的测定结果___________ (填“偏高”或“偏低”)。
②理由是___________ 。
 、
、 、
、 、
、 、
、 、
、 、
、 和金属
和金属 等,对其综合利用具有重要的经济价值和社会效益。
等,对其综合利用具有重要的经济价值和社会效益。Ⅰ、一种含钛高炉渣提钛工艺流程如下图所示。

已知:①
 不溶于水、稀酸和碱溶液;②
不溶于水、稀酸和碱溶液;② 能与强酸、强碱反应。
能与强酸、强碱反应。(1)盐酸酸浸过程中
 发生反应的离子方程式为
发生反应的离子方程式为(2)“磁选”的目的是
(3)下列说法正确的是
a、滤渣1的主要成分为
 、
、
b、若将流程A部分与流程B部分互换顺序,最终得到的滤渣成分相同
c、若将流程A部分与流程B部分互换顺序,理论上氢氧化钠用量不变
Ⅱ、含钛高炉渣中金属
 含量的测定:
含量的测定:ⅰ、配制金属
 浸取液:取一定量的亚硫酸钠和邻菲岁啉(抑制
浸取液:取一定量的亚硫酸钠和邻菲岁啉(抑制 水解)溶于水,加入乙酸和乙酸铵混合溶液调
水解)溶于水,加入乙酸和乙酸铵混合溶液调 ,此时铁的化合物不溶解。
,此时铁的化合物不溶解。ⅱ、取
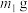 粉碎后的含钛高炉渣,加入足量金属
粉碎后的含钛高炉渣,加入足量金属 浸取液,室温下浸取
浸取液,室温下浸取 。
。ⅲ、过滤,将滤液及洗涤液全部转移至盛有过量
 溶液的烧杯中,加入稀硫酸充分反应。
溶液的烧杯中,加入稀硫酸充分反应。ⅳ、将反应后的溶液煮沸至冒大气泡并继续微沸
 。
。ⅴ、冷却,用浓度为
 的抗坏血酸
的抗坏血酸 标准液滴定,消耗抗坏血酸标准液
标准液滴定,消耗抗坏血酸标准液 。
。已知:①酸性条件下,
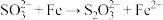 (未配平)
(未配平)②
 (抗坏血酸)
(抗坏血酸) (脱氢抗坏血酸)
(脱氢抗坏血酸)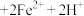
(4)步骤ⅱ中浸取铁时发生反应的离子方程式为
(5)步骤ⅲ中加入过量
 溶液的主要作用是
溶液的主要作用是(6)该含钛高炉渣中金属
 的质量分数=
的质量分数=(7)下列两种情况均会对“金属
 的质量分数”测定结果造成偏差,任选其中一种情况分析并说明判断理由。
的质量分数”测定结果造成偏差,任选其中一种情况分析并说明判断理由。情况一:配制金属
 浸取液时,溶液
浸取液时,溶液 等于2
等于2情况二:未进行步骤ⅳ,直接用抗坏血酸标准液滴定
①情况
②理由是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
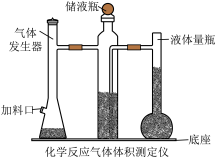
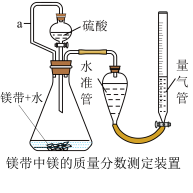
【推荐3】利用镁和稀硫酸反应,不仅可以测定1mol氢气的体积,装置如下左图,也可以测定镁带中镁的质量分数(杂质与酸反应不产生气体),装置如图。
(1)用离子方程式表示测定实验的反应原理____________________________________ 。
(2)硫酸必须过量的目的是__________________________________________________ 。
(3)用“化学反应气体体积测定仪”测定1mol氢气的体积时,要三次用到注射器,其中两次是抽气调压,还有一次是___________________________________________ 。
(4)a(g)镁和足量稀硫酸反应,镁完全反应后,测得氢气在常温时的体积为V(L),则常温下l mol氢气的体积为_________________ L。
(5)某学生在测定1molH2体积时,镁中混有少量铝,测定结果将_______________ (填:偏大、偏小或没有变化)。
(6)若用“化学反应气体体积测定仪”也可以测定1mol二氧化碳气体的体积,那么储液瓶中应盛放________________________ 溶液。
(7)在“镁带中镁的质量分数测定装置”中,导管a的作用是______________________ 。
(8)“镁带中镁的质量分数测定”中,读取量气管的读数时,要使装置内外压强保持一致,具体操作为_________________________________________________________ 。
(9)在“镁带中镁的质量分数测定”中,如果实验的测定结果偏高,可能的原因是____________ (选填编号)。
a.装置漏气 b.未冷却至室温即读数
c.镁带中含有氧化镁 d.末读数时量气管的液面低于水准管


(1)用离子方程式表示测定实验的反应原理
(2)硫酸必须过量的目的是
(3)用“化学反应气体体积测定仪”测定1mol氢气的体积时,要三次用到注射器,其中两次是抽气调压,还有一次是
(4)a(g)镁和足量稀硫酸反应,镁完全反应后,测得氢气在常温时的体积为V(L),则常温下l mol氢气的体积为
(5)某学生在测定1molH2体积时,镁中混有少量铝,测定结果将
(6)若用“化学反应气体体积测定仪”也可以测定1mol二氧化碳气体的体积,那么储液瓶中应盛放
(7)在“镁带中镁的质量分数测定装置”中,导管a的作用是
(8)“镁带中镁的质量分数测定”中,读取量气管的读数时,要使装置内外压强保持一致,具体操作为
(9)在“镁带中镁的质量分数测定”中,如果实验的测定结果偏高,可能的原因是
a.装置漏气 b.未冷却至室温即读数
c.镁带中含有氧化镁 d.末读数时量气管的液面低于水准管
您最近一年使用:0次



