将氧化铁还原为铁的技术在人类文明的进步中占有十分重要的地位。炼铁高炉中发生的关键反应如下:
C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ/mol
CO2(g)+C(s)=2CO(g) ΔH=+172.46 kJ/mol
Fe2O3+CO→Fe+CO2
若已知:2Fe(s)+ O2(g)=Fe2O3(s) ΔH=-824.21 kJ/mol
O2(g)=Fe2O3(s) ΔH=-824.21 kJ/mol
根据上面三个热化学方程式,回答下列问题:
(1)CO的摩尔燃烧焓为_______ ;写出其热化学方程式:_______ 。
(2)高炉内Fe2O3被CO还原为Fe的热化学方程式为_______ 。
(3)炼制1吨含铁96%的生铁所需焦炭的理论用量是_______ 吨,实际生产中所需焦炭远高于理论用量,其原因是_______ 。
C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ/mol
CO2(g)+C(s)=2CO(g) ΔH=+172.46 kJ/mol
Fe2O3+CO→Fe+CO2
若已知:2Fe(s)+
 O2(g)=Fe2O3(s) ΔH=-824.21 kJ/mol
O2(g)=Fe2O3(s) ΔH=-824.21 kJ/mol根据上面三个热化学方程式,回答下列问题:
(1)CO的摩尔燃烧焓为
(2)高炉内Fe2O3被CO还原为Fe的热化学方程式为
(3)炼制1吨含铁96%的生铁所需焦炭的理论用量是
23-24高二上·全国·课时练习 查看更多[2]
更新时间:2023-08-27 10:46:22
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】已知亚磷酸 是具有强还原性的二元弱酸,可被银离子氧化为磷酸。
是具有强还原性的二元弱酸,可被银离子氧化为磷酸。
 亚磷酸与银离子反应的离子方程式为
亚磷酸与银离子反应的离子方程式为______ 。
 向亚磷酸溶液中滴加氢氧化钠溶液至中性,写出所得溶液中电荷守恒方程式
向亚磷酸溶液中滴加氢氧化钠溶液至中性,写出所得溶液中电荷守恒方程式______ 。
 某温度下,
某温度下, 的亚磷酸溶液的pH为
的亚磷酸溶液的pH为 ,即c(H+)=3.9×10-2,则该温度下亚磷酸的一级电离平衡常数
,即c(H+)=3.9×10-2,则该温度下亚磷酸的一级电离平衡常数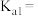
______ 。 亚磷酸第二级电离忽略不计,结果保留两位有效数字
亚磷酸第二级电离忽略不计,结果保留两位有效数字
 是具有强还原性的二元弱酸,可被银离子氧化为磷酸。
是具有强还原性的二元弱酸,可被银离子氧化为磷酸。 亚磷酸与银离子反应的离子方程式为
亚磷酸与银离子反应的离子方程式为 向亚磷酸溶液中滴加氢氧化钠溶液至中性,写出所得溶液中电荷守恒方程式
向亚磷酸溶液中滴加氢氧化钠溶液至中性,写出所得溶液中电荷守恒方程式 某温度下,
某温度下, 的亚磷酸溶液的pH为
的亚磷酸溶液的pH为 ,即c(H+)=3.9×10-2,则该温度下亚磷酸的一级电离平衡常数
,即c(H+)=3.9×10-2,则该温度下亚磷酸的一级电离平衡常数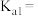
 亚磷酸第二级电离忽略不计,结果保留两位有效数字
亚磷酸第二级电离忽略不计,结果保留两位有效数字
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】医学上常用酸性高锰酸钾溶液和草酸溶液的反应用于测定血钙的含量回答下列问题:
(1)配平以下离子方程式,并用单线桥表示电子转移的方向和数目:
______ +_____MnO4-+_____H2C2O4=_____CO2↑+_____Mn2++____。
(2)该反应中的还原剂是______ 。
(3)反应转移了0.4mol电子,则消耗KMnO4的物质的量为______ mol。
(4)将一定质量的镁、铝合金投入100 mL一定物质的量浓度的HCl中,合金全部溶解,向所得溶液中滴加5 mol·L-1NaOH溶液到过量,生成沉淀的质量与加入的NaOH溶液体积关系如下图。
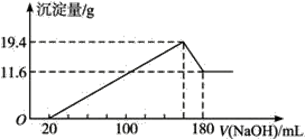
①原合金中铝的质量分数是___________ 。
②盐酸的物质的量浓度是_____________ 。
(1)配平以下离子方程式,并用单线桥表示电子转移的方向和数目:
(2)该反应中的还原剂是
(3)反应转移了0.4mol电子,则消耗KMnO4的物质的量为
(4)将一定质量的镁、铝合金投入100 mL一定物质的量浓度的HCl中,合金全部溶解,向所得溶液中滴加5 mol·L-1NaOH溶液到过量,生成沉淀的质量与加入的NaOH溶液体积关系如下图。

①原合金中铝的质量分数是
②盐酸的物质的量浓度是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】现在反应NH3+Cl2=NH4Cl+N2(未配平),完成下列问题:
(1)配平该方程式___________ 。
(2)氧化剂___________ ,还原产物___________
(3)氧化剂与还原剂的分子个数之比:___________
(4)写出配平好的方程式,用单线桥法表示该反应的电子转移情况___________
(5)写出配平好的方程式,用双线桥法表示该反应的电子转移情况___________
(6)当有8个NH3参加反应时,转移的电子数目为___________ 个
(1)配平该方程式
(2)氧化剂
(3)氧化剂与还原剂的分子个数之比:
(4)写出配平好的方程式,用单线桥法表示该反应的电子转移情况
(5)写出配平好的方程式,用双线桥法表示该反应的电子转移情况
(6)当有8个NH3参加反应时,转移的电子数目为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
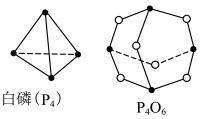
【推荐1】(1)化学反应可视为旧键断裂和新键形成的过程,化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)的能量,已知白磷和P4O6的分子结构如图所示,现提供以下化学键的键能:P-P:198kJ·mol-1,P-O:360 kJ·mol-1,O=O:498kJ·mol-1,则反应P4(白磷)与O2反应生成P4O6的热化学反应方程式为____ 。
(2)肼(N2H4)可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气。已知:
①N2(g)+2O2(g)═N2O4(l) △H1═-19.5kJ/mol
②N2H4(l)+O2(g)═N2(g)+2H2O(g) △H2═-534.2kJ/mol
写出肼和N2O4反应的热化学方程式_____ 。
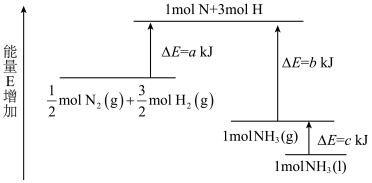
(3)化学反应N2+3H2 2NH3的能量变化如图所示,该反应生成NH3(l)的热化学方程式是
2NH3的能量变化如图所示,该反应生成NH3(l)的热化学方程式是_____ 。

(2)肼(N2H4)可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气。已知:
①N2(g)+2O2(g)═N2O4(l) △H1═-19.5kJ/mol
②N2H4(l)+O2(g)═N2(g)+2H2O(g) △H2═-534.2kJ/mol
写出肼和N2O4反应的热化学方程式
(3)化学反应N2+3H2
 2NH3的能量变化如图所示,该反应生成NH3(l)的热化学方程式是
2NH3的能量变化如图所示,该反应生成NH3(l)的热化学方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】为解决能源短缺问题,工业生产中应合理利用化学能。
(1)实验室用50mL 0.5mol/L的盐酸和50mL 0.55mol/L的NaOH(密度均为1g/cm3)测定中和热。反应前两溶液的温度均为25.2℃,混合后混合溶液的最高温度为28.2℃,反应溶液的比热容为C=4.18J/(g·℃),请写出该反应的热化学方程式_______ 。
(2)25℃,1.01×105Pa时,实验测得,4g氢气在O2中完全燃烧生成液态水放出572kJ的热量,则H2的燃烧热 的热化学方程式为_______ 。
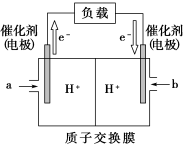
(3)下图是某笔记本电脑使用的甲醇燃料电池的结构示意图。放电时甲醇应从_______ 处通入(填“a”或“b”),电池内部H+向_______ (填“左”或“右”)移动。写出电池负极的电极反应式_______ 。
(4)从化学键的角度分析,化学反应的过程就是反应物的化学键的破坏和生成物的化学键的形成过程。
已知:N2(g)+3H2(g)=2NH3(g) ΔH=-93kJ·mol-1.试根据表中所列键能数据计算a的数值_______ 。
(5)已知:C(s,石墨)+O2(g)=CO2(g) ΔH1=-393.5kJ·mol-1①
2H2(g)+O2(g)=2H2O(l) ΔH2=-571.6kJ·mol-1②
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ΔH3=-2599kJ·mol-1③
根据盖斯定律,计算反应2C(s,石墨)+H2(g)=C2H2(g)的ΔH=_______ 。
(1)实验室用50mL 0.5mol/L的盐酸和50mL 0.55mol/L的NaOH(密度均为1g/cm3)测定中和热。反应前两溶液的温度均为25.2℃,混合后混合溶液的最高温度为28.2℃,反应溶液的比热容为C=4.18J/(g·℃),请写出该反应的热化学方程式
(2)25℃,1.01×105Pa时,实验测得,4g氢气在O2中完全燃烧生成液态水放出572kJ的热量,则H2的
(3)下图是某笔记本电脑使用的甲醇燃料电池的结构示意图。放电时甲醇应从

(4)从化学键的角度分析,化学反应的过程就是反应物的化学键的破坏和生成物的化学键的形成过程。
| 化学键 | H—H | N—H | N≡N |
| 键能/kJ·mol-1 | 436 | a | 945 |
已知:N2(g)+3H2(g)=2NH3(g) ΔH=-93kJ·mol-1.试根据表中所列键能数据计算a的数值
(5)已知:C(s,石墨)+O2(g)=CO2(g) ΔH1=-393.5kJ·mol-1①
2H2(g)+O2(g)=2H2O(l) ΔH2=-571.6kJ·mol-1②
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ΔH3=-2599kJ·mol-1③
根据盖斯定律,计算反应2C(s,石墨)+H2(g)=C2H2(g)的ΔH=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】能源问题是人类社会面临的重大课题,甲醇是未来重要的绿色能源之一。
(1)已知H2(g)、CO(g)和CH3OH(l )的燃烧热△H分别为285.8 kJ·mol1、283.0 kJ·mol1和726.5kJ·mol1。请回答下列问题:
①写出表示H2燃烧热的热化学反应方程式__________________________ 。
②甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为_______________________ 。
(2)以CH4和H2O为原料,通过下列反应来制备甲醇。
Ⅰ.CH4(g)+H2O(g)= CO(g)+3H2(g) ΔH=+206.0 kJ/mol
Ⅱ.CO(g)+2H2(g)= CH3OH(g) ΔH=-129.0 kJ/mol
①将1.0 mol CH4和2.0 mol H2O(g)通入容积为10 L的反应容器,在一定条件下发生反应Ⅰ,测得在一定的压强下CH4的转化率与温度的关系如图。在100 ℃时达到平衡所需的时间为5 min,则用H2表示该反应的平均反应速率为___________ 。100 ℃时反应Ⅰ的平衡常数为_______ 。在温度和容积不变的情况下,再向平衡体系中充入1.0 mol CH4和2.0 mol H2O(g),达到平衡时CO转化率_________ 。(填“增大”“不变”或“减小”)

②工业上利用甲醇制备氢气的常用方法有甲醇蒸气重整法。该法中的一个主要反应为CH3OH(g)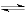 CO(g)+2H2(g),此反应高温下能自发进行的原因是:
CO(g)+2H2(g),此反应高温下能自发进行的原因是:________________ 。
(1)已知H2(g)、CO(g)和CH3OH(l )的燃烧热△H分别为285.8 kJ·mol1、283.0 kJ·mol1和726.5kJ·mol1。请回答下列问题:
①写出表示H2燃烧热的热化学反应方程式
②甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为
(2)以CH4和H2O为原料,通过下列反应来制备甲醇。
Ⅰ.CH4(g)+H2O(g)= CO(g)+3H2(g) ΔH=+206.0 kJ/mol
Ⅱ.CO(g)+2H2(g)= CH3OH(g) ΔH=-129.0 kJ/mol
①将1.0 mol CH4和2.0 mol H2O(g)通入容积为10 L的反应容器,在一定条件下发生反应Ⅰ,测得在一定的压强下CH4的转化率与温度的关系如图。在100 ℃时达到平衡所需的时间为5 min,则用H2表示该反应的平均反应速率为

②工业上利用甲醇制备氢气的常用方法有甲醇蒸气重整法。该法中的一个主要反应为CH3OH(g)
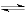 CO(g)+2H2(g),此反应高温下能自发进行的原因是:
CO(g)+2H2(g),此反应高温下能自发进行的原因是:
您最近一年使用:0次



